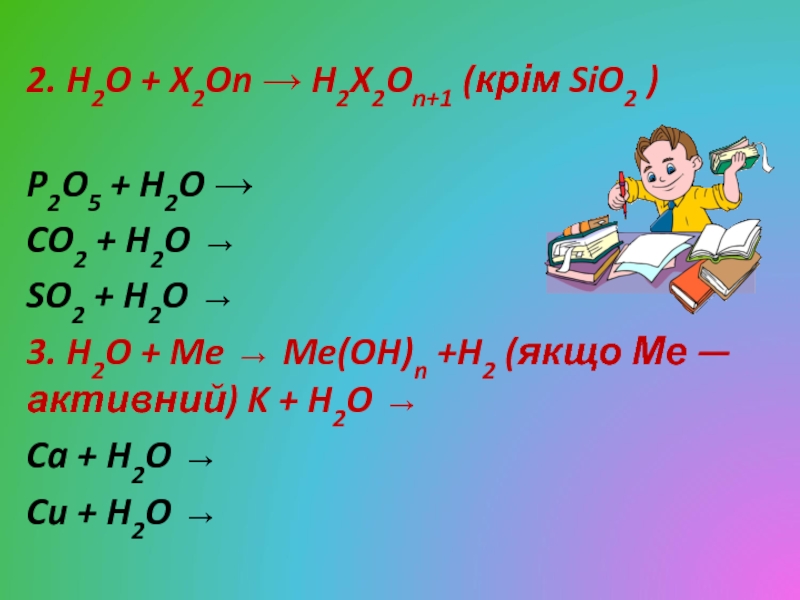Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Розчин та його компоненти : розчинник, розчинена речовина. Вода як розчинник
Содержание
- 1. Розчин та його компоненти : розчинник, розчинена речовина. Вода як розчинник
- 2. Відповісти на питанняНа які дві групи поділяються
- 3. Розчини — це багатокомпонентні системи. Один із
- 4. Вода — універсальний розчинник усіх речовин на Землі. Наведіть приклади водних розчинівНаведіть приклади неводних розчинів
- 5. За реакцією з водою всі речовини поділяються на три групи: розчинні;малорозчинні;практично нерозчинні.
- 6. — Як можна пояснити таку особливість молекул води?
- 7. Тип зв’язку — ковалентний полярний, кут
- 8. — Ґратка молекулярна? Чому ж за нормальних
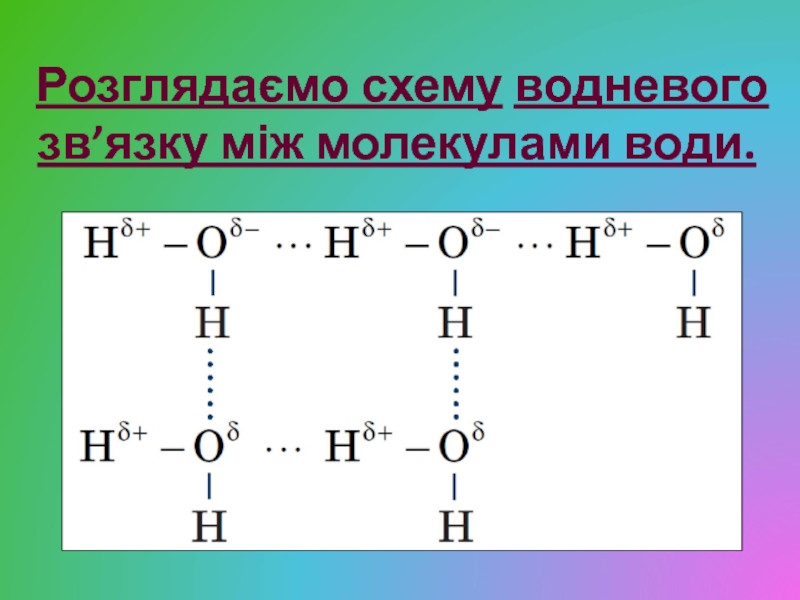
- 9. Розглядаємо схему водневого зв’язку між молекулами води.
- 10. Заповнюємо опорну схемуМолекулярна формула: ________Структурна формула: ________M(H2O) _______________________
- 11. Поширення в природіВ організмі людини: ___________На Землі: _____________________У Космосі: ____________________
- 12. Фізичні властивостіЗа атмосферного тиску 1 атм:Ткип = 100°С,Тплав = 0°С,ρ = 1 г/см3.Агрегатні стани:
- 13. Хімічні властивості1. H2O + Me2On → Me(OH)n
- 14. 2. H2O + X2On → H2X2On+1 (крім
- 15. Завдання 1 Обчисліть масу води, що утворюється внаслідок
- 16. Домашнє завдання Опрацювати матеріал параграфа, відповісти на
- 17. Скачать презентанцию
Відповісти на питанняНа які дві групи поділяються дисперсні системи?Які розчини називаються колоїдними?Які розчини називаються істинними?З яких компонентів складається розчин?Чи можна стверджувати, що розчини мають постійний склад? Чому?
Слайды и текст этой презентации
Слайд 1Розчин та його компоненти: розчинник, розчинена речовина. Вода як розчинник.
Будова молекули води, поняття про водневий зв’язок
Слайд 2Відповісти на питання
На які дві групи поділяються дисперсні системи?
Які розчини
називаються колоїдними?
Які розчини називаються істинними?
З яких компонентів складається розчин?
Чи можна
стверджувати, що розчини мають постійний склад? Чому?
Слайд 3Розчини — це багатокомпонентні системи. Один із компонентів називається розчинником.
Зазвичай це речовина, що перебуває в тому ж агрегатному стані,
що й розчин. Слайд 4Вода — універсальний розчинник усіх речовин на Землі.
Наведіть приклади
водних розчинів
Наведіть приклади неводних розчинів
Слайд 5За реакцією з водою всі речовини поділяються на три групи:
розчинні;
малорозчинні;
практично нерозчинні.
Слайд 7Тип зв’язку — ковалентний полярний, кут зв’язку — 104,5°. Тип
кристалічної ґратки — молекулярний.
Слайд 8— Ґратка молекулярна? Чому ж за нормальних умов вода —
рідина?
Молекула води полярна — диполь. Між молекулами води виникає взаємне
притягання за температури менш ніж 100°С. Такий зв’язок називається водневим.Слайд 10Заповнюємо опорну схему
Молекулярна формула: ________
Структурна формула: ________
M(H2O) _______________________
Слайд 11Поширення в природі
В організмі людини: ___________
На Землі: _____________________
У Космосі: ____________________
Слайд 12Фізичні властивості
За атмосферного тиску 1 атм:
Ткип = 100°С,
Тплав = 0°С,
ρ
= 1 г/см3.
Агрегатні стани:
Слайд 13Хімічні властивості
1. H2O + Me2On → Me(OH)n (якщо Ме —
активний, а основа — розчинна або малорозчинна)
Na2O + H2O →
CaO
+ H2O →CuO + H2O →
Слайд 142. H2O + X2On → H2X2On+1 (крім SiO2 )
P2O5 +
H2O →
CO2 + H2O →
SO2 + H2O →
3. H2O +
Me → Me(OH)n +H2 (якщо Ме — активний) K + H2O →Ca + H2O →
Cu + H2O →