Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Самостоятельная работа
Содержание
- 1. Самостоятельная работа
- 2. Продолжение лекции 2 МОНРЕАЛЬСКИЙ ПРОТОКОЛМонреа́льский протоко́л по
- 3. МОНРЕАЛЬСКИЙ ПРОТОКОЛПротокол был подготовлен к подписанию 16
- 4. Монреальский протокол предусматривает для каждой группы галогенированных
- 5. По состоянию на декабрь 2009 года
- 6. В ООН 16 сентября отмечается Международный день
- 7. Влияние вулканов на озоновый слойВ Антарктиде находится
- 8. Эребус – один из немногих вулканов, представляющий
- 9. Весной над Антарктидой одновременно с сильным понижением
- 10. Лондонская пожарная служба неоднократно сообщала, что 90%
- 11. Последняя крупная катастрофа, причины которой подготовлены Монреальским
- 12. Монреальский протокол (МП), подписанный всеми государствами мира,
- 13. Существенное сокращение антарктической стратосферной озоновой дыры в
- 14. Лекция 3Физико-химические процессы в тропосфере
- 15. Тропосфера Тропосфера – нижний, непосредственно соприкасающийся с
- 16. Процессы окисления примесей в тропосфере Протекают по
- 17. Концентрация примесей в тропосфере
- 18. Образование гидроксильного радикала в тропосфереO(1D)+Н2О = 2ОН O(1D)+СН4
- 19. Главные пути стока ОН - радикала СО
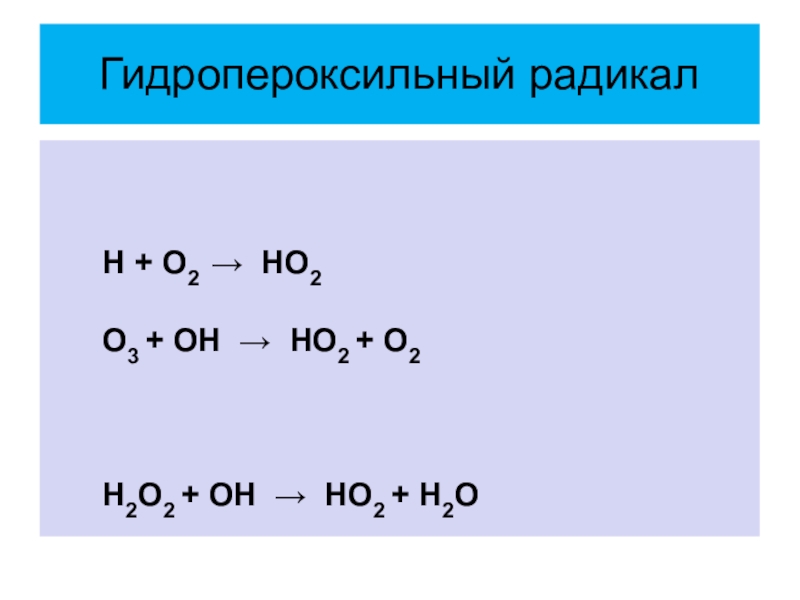
- 20. Гидропероксильный радикал Н +
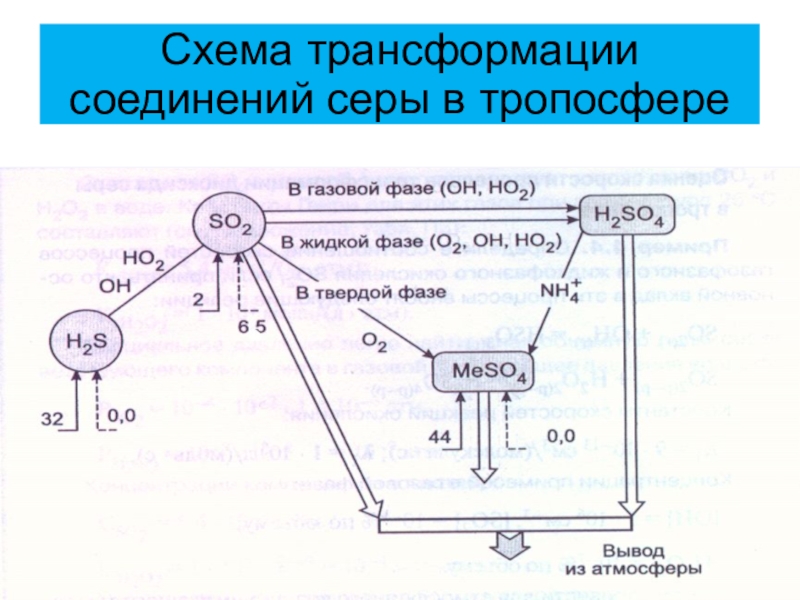
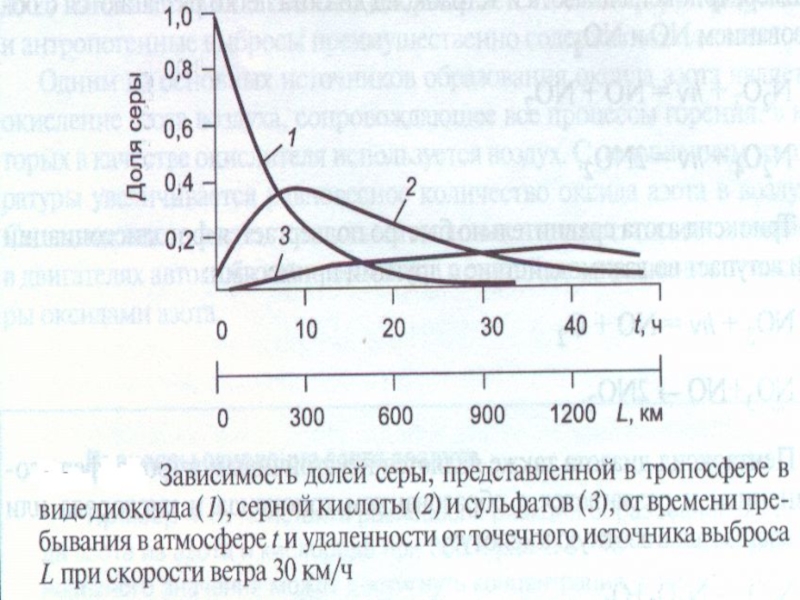
- 21. Схема трансформации соединений серы в тропосфере
- 22. Основные поступления неорганических соединений серы в тропосферу
- 23. Из природных источников поступлений неорганических соединений серы
- 24. Биологические источники неорганических соединений серы выделяют преимущественно
- 25. Имеющиеся в литературе сведения позволяют лишь грубо
- 26. Принимая во внимание скорость поступления сероводорода
- 27. Полученный в результате диоксид серы, как и
- 28. Реакция окисления SO2 атомарным кислородом не играет
- 29. Триоксид серы - серный ангидрид легко взаимодействует с частицами атмосферной влаги и образует растворы серной кислоты
- 30. Реагируя с аммиаком или ионами металлов, присутствующими
- 31. Оксиды железа, алюминия, хрома и других металлов,
- 32. Необходимо отметить, однако, что данное значение получено
- 33. Третий путь окисления диоксида серы в тропосфере
- 34. В качестве окислителя в природных условиях часто
- 35. Помимо процессов химической трансформации диоксида серы в
- 36. Слайд 36
- 37. В первый момент после выброса диоксида серы
- 38. Полученные результаты наглядно демонстрируют опасность загрязнения атмосферы
- 39. В случае выпадения дождевых осадков над этой
- 40. Скачать презентанцию
Продолжение лекции 2 МОНРЕАЛЬСКИЙ ПРОТОКОЛМонреа́льский протоко́л по вещества́м, разруша́ющим озо́новый слой (англ. The Montreal Protocol on Substances That Deplete the Ozone Layer) — международный протокол к Венской конвенции об охране озонового слоя 1985
Слайды и текст этой презентации
Слайд 1Самостоятельная работа
Вопрос 1.
На каких фактах основывается современное научное представление о
возникновении
Слайд 2Продолжение лекции 2
МОНРЕАЛЬСКИЙ ПРОТОКОЛ
Монреа́льский протоко́л по вещества́м, разруша́ющим озо́новый слой
(англ. The Montreal Protocol on Substances That Deplete the Ozone Layer) —
международный протокол к Венской конвенции об охране озонового слоя 1985 года, разработанный с целью защиты озонового слоя с помощью снятия с производства некоторых химических веществ, которые разрушают озоновый слой.Слайд 3МОНРЕАЛЬСКИЙ ПРОТОКОЛ
Протокол был подготовлен к подписанию 16 сентября 1987 года
и вступил в силу 1 января 1989 года.
После этого
последовала первая встреча в Хельсинки в мае 1989 года.С тех пор протокол подвергался пересмотру семь раз: в 1990 (Лондон), 1991 (Найроби),
1992 (Копенгаген), 1993 (Бангкок), 1995 (Вена),
1997 (Монреаль) и 1999 (Пекин).
Слайд 4
Монреальский протокол предусматривает для каждой группы галогенированных углеводородов определённый срок,
в течение которого она должна быть снята с производства и
исключена из использования.Слайд 5
По состоянию на декабрь 2009 года 196
государств-членов ООН ратифицировали
первоначальную
версию Монреальского
протокола.
Генеральный секретарь ООН (1997—2006) - Кофи Аннан сказал,
что «возможно, единственным очень успешным международным соглашением можно считать Монреальский протокол».Слайд 6В ООН 16 сентября отмечается Международный день охраны озонового слоя.
Он был установлен в 1994 году в память о подписании
Монреальского протокола по веществам, разрушающим озоновый слой.Слайд 7Влияние вулканов на озоновый слой
В Антарктиде находится постояннодействующий вулкан Эребус
(77,5° ю.ш., 167,2° в.д.; высота – 3794 м.),
входящий в список
самых активных вулканов на Земле. В его главном кратере находится лавовое озеро, не застывающее из-за непрерывных конвективных процессов подъема и перемешивания магмы, которая циркулирует от камеры, расположенной глубоко в вулкане.
Слайд 8Эребус – один из немногих вулканов, представляющий собой систему открытого
жерла, объясняющую устойчивость и разнообразие активности вулкана: частую смену между
пассивной и активной дегазацией и взрывными извержениями.Рядом с лавовым озером, в главном кратере находится жерло активной дегазации (пепловое жерло), из которого периодически выбрасывается столб вулканических газов.
Слайд 9Весной над Антарктидой одновременно с сильным понижением стратосферного озона наблюдается
рост концентрации монооксида хлора ClO.
По максимальным значениям концентрации ClO
в стратосфере над станцией McMurdo в сентябре 1992 г. с учетом площади озоновой дыры рассчитана масса хлороводорода HCl, необходимого для ее образования. Масса HCl составила 9,3 кт. Наиболее вероятным источником такого количества HCl в Антарктиде является вулкан Эребус.
Слайд 10Лондонская пожарная служба неоднократно сообщала, что 90% пожаров с летальным
исходом связано именно с взрывами холодильников и вдыханием черного токсичного
дыма, образующегося при горении теплоизоляционных материалов холодильников. Таких пожаров в Лондоне происходит приблизительно 300 в год, то есть практически почти каждый день происходит пожар из-за возгорания холодильника.Подробности: https://regnum.ru/news/polit/2302128.html Любое использование материалов допускается только при наличии гиперссылки на ИА REGNUM.
Слайд 11Последняя крупная катастрофа, причины которой подготовлены Монреальским и Киотским протоколами,
— пожар 24-этажного жилого дома Grenfell Tower постройки 1970-х годов
в Лондоне, случившийся 14 июня 2017 года. В результате трагедии погибло не менее 100 человекПодробности: https://regnum.ru/news/polit/2302128.html Любое использование материалов допускается только при наличии гиперссылки на ИА REGNUM.
Слайд 12Монреальский протокол (МП), подписанный всеми государствами мира, регулирует производство, использование
и оборот более 100 химических веществ, подозреваемых в разрушении озонового
слоя. Большая часть из них изъята из использования. Таким образом, совершен технологический переворот в мировой химической промышленности, отбросивший многие ее отрасли на годы назад.Подробности: https://regnum.ru/news/polit/2302128.html Любое использование материалов допускается только при наличии гиперссылки на ИА REGNUM.
Слайд 13Существенное сокращение антарктической стратосферной озоновой дыры в 2010 году и
в течение ряда предыдущих лет — результат чрезвычайного метеорологического явления,
иногда свойственного полярной зиме.Учёные называют это внезапным стратосферным потеплением (sudden stratospheric warming, SSW).
Слайд 15Тропосфера
Тропосфера – нижний, непосредственно соприкасающийся с земной поверхностью, слой атмосферы.
Именно воздухом тропосферы дышат живые организмы, влага, конденсирующаяся в тропосфере
и выпадающая с атмосферными осадками, обеспечивает человека питьевой водой.Слайд 16Процессы окисления примесей в тропосфере
Протекают по различным направлениям:
1) Окисление
непосредственно в газовой фазе;
2) Окислению предшествует абсорбция частицами воды, и
в дальнейшем процесс окисления протекает в растворе;3) Окислению предшествует адсорбция примесей на поверхности твердых частиц, взвешенных в воздухе.
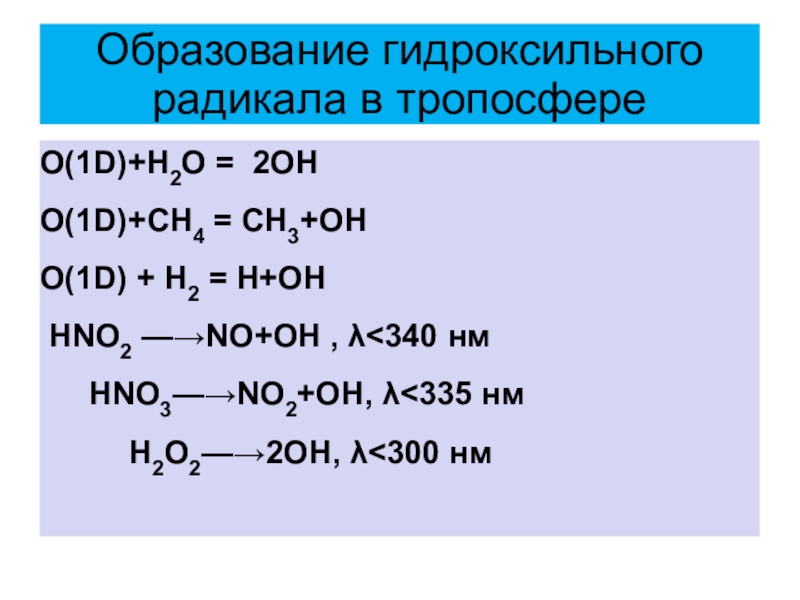
Слайд 18Образование гидроксильного радикала в тропосфере
O(1D)+Н2О = 2ОН
O(1D)+СН4 = СН3+ОН
O(1D) +
Н2 = Н+ОН
НNO2 —→NO+ОН , λ
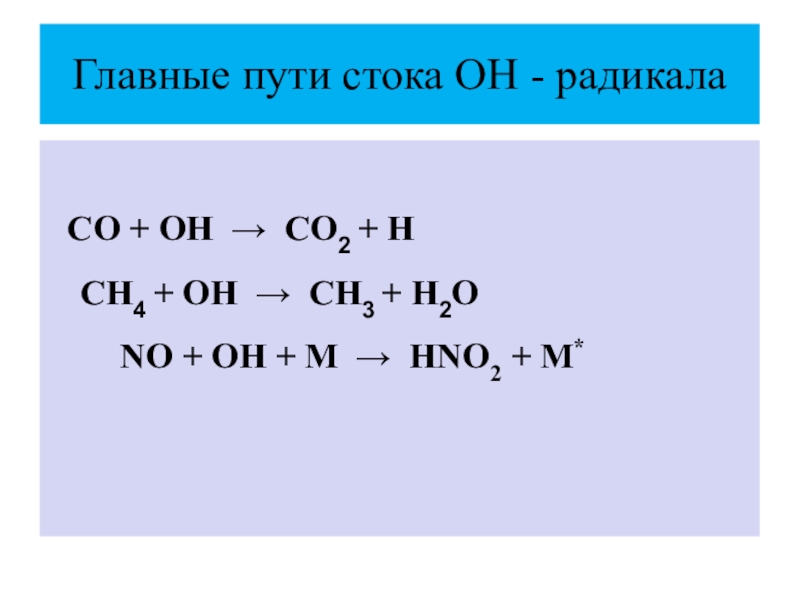
λ<335 нм Н2O2—→2ОН, λ<300 нм Слайд 19Главные пути стока ОН - радикала
СО + ОН →
СО2 + Н СН4 + ОН → СН3 + Н2О NO
+ OH + M → НNO2 + М*Слайд 22Основные поступления неорганических соединений серы в тропосферу связаны с антропогенными
источниками.
На их долю приходится примерно 65% от всех поступлений
неорганических соединений серы в атмосферу. Около 95% из этого количества составляет диоксид серы.Слайд 23Из природных источников поступлений неорганических соединений серы следует выделить волновую
деятельность в океанах, приводящую к образованию аэрозолей.
Общее количество серы,
содержащейся в аэрозолях в виде сульфатов магния и кальция, оценивается в 44 млн. т. в год, что составляет примерно 30% от ее поступления в атмосферу в виде неорганических соединений.Слайд 24Биологические источники неорганических соединений серы выделяют преимущественно сероводород, с которым
в атмосферу поступает, по различным оценкам, от 23 до 49%
от всех неорганических соединений серы.Масштабы поступления сероводорода в атмосферу и процессы его трансформации в атмосфере изучены еще недостаточно подробно.
Слайд 25Имеющиеся в литературе сведения позволяют лишь грубо оценить его содержание
в тропосфере. Так над океанами концентрация H2S колебалась от 0.0076
до 0.076 мкг*м-3, а над континентами от 0,05 до 0.1 мкг*м-3.Сероводород последовательно, в ряде стадий окисляется до SO2.
Слайд 26 Принимая во внимание скорость поступления сероводорода в атмосферу и
его содержание в тропосфере, время его жизни в атмосфере можно
оценить в несколько часов.Слайд 27Полученный в результате диоксид серы, как и SO2, поступающий из
других источников, окисляется далее.
Механизм этого процесса изучен более подробно.
Слайд 28Реакция окисления SO2 атомарным кислородом не играет существенной роли для
процессов трансформации соединений серы в тропосфере. Ведущую роль в этих
процессах играют свободные радикалы. Протекающие при этом процессы можно представить следующими уравнениями реакций: SO2 + ОН + М = HSO3 + M*HSO3 + HO2 = SO3 + 2OH
SO2 + HO2 = SO3 + OH
SO2 + CH3O2 = SO3 + CH3O
Слайд 29Триоксид серы - серный ангидрид легко взаимодействует с частицами атмосферной
влаги и образует растворы серной кислоты
Слайд 30Реагируя с аммиаком или ионами металлов, присутствующими в частицах атмосферной
влаги, SO3 частично переходят в соответствующие сульфаты.
В основном это
сульфаты аммония, натрия, кальция.Образование сульфатов происходит и в процессе окисления сульфитов на поверхности твердых частиц, присутствующих в воздухе.
Слайд 31Оксиды железа, алюминия, хрома и других металлов, которые также могут
присутствовать в воздухе, резко ускоряют процесс окисления диоксида серы. Как
показали лабораторные эксперименты, в присутствии, например, частиц Fe2O3, скорость процесса трансформации SO2 составляет примерно 100%•ч-1 .Слайд 32Необходимо отметить, однако, что данное значение получено для воздуха, в
котором содержание оксидов железа в 100 - 200 раз превышало
фоновые концентрации. Поэтому данный процесс трансформации диоксида серы играет основную роль лишь в сильно запыленном воздухе, содержащем значительные количества оксидов металлов.Слайд 33Третий путь окисления диоксида серы в тропосфере связан с предварительной
абсорбцией SO2 каплями атмосферной влаги.
В дождливую погоду и при
высокой влажности атмосферы этот путь окисления может стать основным в процессе трансформации диоксида серы. Слайд 34В качестве окислителя в природных условиях часто выступает пероксид водорода.
При высоких значениях рН, когда в растворе в основном находятся
ионы SO3- скорость окисления заметно возрастает.Конечным продуктом окисления, как и в случае окисления в газовой фазе, является серная кислота, которая в дальнейшем может перейти в сульфаты.
Слайд 35Помимо процессов химической трансформации диоксида серы в серную кислоту и
сульфаты, сток - вывод из атмосферы этих соединений происходит в
результате процессов:- мокрого осаждения, с атмосферными осадками;
- сухого осаждения - при контакте с поверхностью почвы, поверхностного водоема или растительностью.
Слайд 37В первый момент после выброса диоксида серы в атмосфере отсутствуют
серная кислота и сульфаты. Со временем доля SO2 уменьшается, доля
серной кислоты увеличивается, проходит через максимум спустя 10 –15 часов после выброса, количество сульфатов в атмосфере будет постепенно увеличиваться в течение 40 –50 часов, затем медленно начнет уменьшаться.Слайд 38Полученные результаты наглядно демонстрируют опасность загрязнения атмосферы соединениями серы, связанную
с возможностью трансграничного переноса примесей (перенос примесей на большие расстояния,
свыше 100 км).Так, предположим, что над источником выбросов соединений серы дует ветер, имеющий скорость порядка 30 км/ч. В этом случае, спустя 10 часов с момента выброса примеси будут удалены на расстояние 300 км от источника выброса.
В этом воздухе доля диоксида серы уменьшится примерно в 5 раз, и основное количество соединений серы будет представлено серной кислотой.
Слайд 39В случае выпадения дождевых осадков над этой территорией практически все
соединения серы будут выведены из атмосферы в виде кислотного дождя.
Необходимо отметить, что, несмотря на наметившееся в последние годы сокращение общего количества диоксида серы, выбрасываемого в атмосферу,серная кислота остается основным компонентом, приводящим к закислению атмосферных осадков.