Вернадский В. И.
Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Соединения кремния
Содержание
- 1. Соединения кремния
- 2. Кремний вырисовывается в мироздании как элемент, обладающий
- 3. Соединения кремния
- 4. Сравните оксид углерода CO2 и оксид кремния
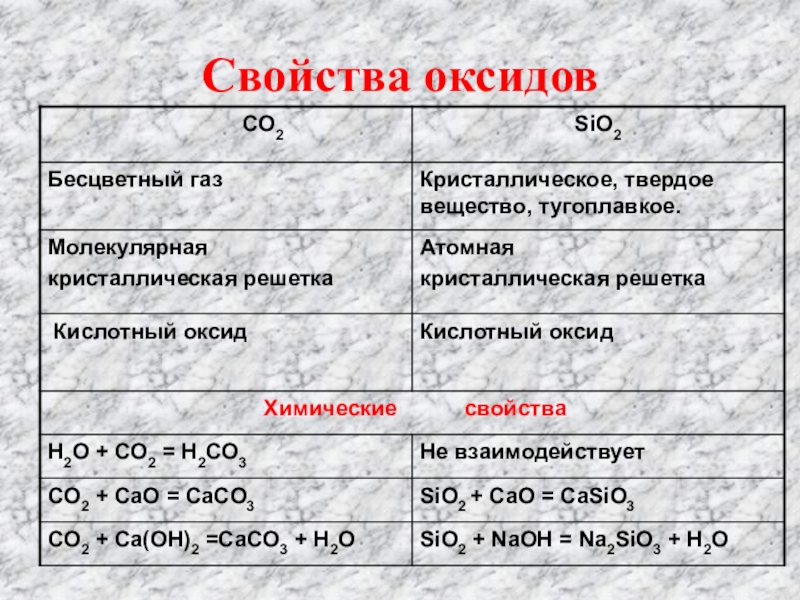
- 5. Свойства оксидов
- 6. Химические свойства оксида кремнияСоставить уравнения реакции1.Взаимодействие оксида
- 7. Оксид кремния(IV)- кислотный оксидХимические свойства оксида кремнияСоставить
- 8. Оксид кремния(IV)- кислотный оксидХимические свойства оксида
- 9. Оксид кремния(IV)- кислотный оксидХимические свойства оксида кремнияСоставить
- 10. nSiO2 ∙ mH2O поликремниевые кислотыH2SiO3 – кремниевая
- 11. Слайд 11
- 12. Применение соединений кремния СтеклоОконное стекло Na2CO3 +
- 13. Керамика Применение соединений кремнияИз керамики изготавливают
- 14. Керамика - общее название многочисленных материалов, полученных
- 15. №1. Закончите уравнения практически осуществимых реакций:
- 16. №2. Составьте молекулярные и, где это возможно,
- 17. Параграф 35, стр. 252-258, стр. 258 зад. 1Домашнее задание
- 18. Скачать презентанцию
Кремний вырисовывается в мироздании как элемент, обладающий исключительным значением.
Слайды и текст этой презентации
Слайд 1Соединения кремния
Розовый аметист
Агат
Ваза из оникса
(разновидности
агата)
Халцедон
Аметист лиловый
Яшма
Сердолик
Слайд 2Кремний вырисовывается в мироздании как элемент, обладающий исключительным значением.
Вернадский В. И.
Слайд 4Сравните оксид углерода CO2 и оксид кремния SiO2
CO2
SiO2
А.Газ, в воде
растворяется
Б.Твердое вещество,
в воде не растворяется
В.Молекулярная кристаллическая
решетка
Г.Атомная кристаллическая решетка
SiO2 - оксид кремния(IV)
Слайд 6Химические свойства оксида кремния
Составить уравнения реакции
1.Взаимодействие оксида кремния с щелочами(KOH)
Оксид кремния(IV)- кислотный оксид
2KOH + SiO2 = K2SiO3 + H2O
Слайд 7Оксид кремния(IV)- кислотный оксид
Химические свойства оксида кремния
Составить уравнения реакции
2.Взаимодействие оксида
кремния с основными оксидами(CaO)
CaO + SiO2 = CaSiO3
Слайд 8 Оксид кремния(IV)- кислотный оксид
Химические свойства оксида кремния
Составить уравнения реакции
3.Взаимодействие
оксида кремния с водой
SiO2 + H2O =
Слайд 9Оксид кремния(IV)- кислотный оксид
Химические свойства оксида кремния
Составить уравнения реакции
4.Взаимодействие оксида
кремния с металлами(Mg)
SiO2 + 2Mg = 2MgO + Si
Слайд 10nSiO2 ∙ mH2O поликремниевые кислоты
H2SiO3 – кремниевая кислота. Слабая, непрочная,
в воде малорастворима (образует коллоидный раствор), нет кислого вкуса.
При нагревании
разлагается H2SiO3 → H2O + SiO2Со щелочами H2SiO3 +2NaOH → 2H2O + Na2SiO3
3. C оксидами металлов H2SiO3 + CaO = CaSiO3+H2O
4.C солями H2SiO3 + MgCl2=MgSiO3+HCL
Na2SiO3 и K2SiO3 – жидкое стекло
Получение: Na2SiO3 + 2HCl → 2NaCl + H2SiO3
Студенистый осадок
Свойства:
Кремниевая кислота. Силикаты.
Слайд 11 Силикаты На силикаты приходится более 1/4 массы всей земной коры.
К ним относится около 500 минералов, в т.ч.
важнейшие породообразующие: полевые шпаты, слюды, пироксены и др. силикаты – это и песок, и глина, и кирпич, и стекло, и цемент, и эмаль, и тальк, и асбест, и изумруд, и топаз.Слайд 12Применение соединений кремния
Стекло
Оконное стекло
Na2CO3 + CaCO3 + 6SiO2
=
Na2O .CaO .6SiO2
Хрусталь
K2O . PbO . 6SiO2
Слайд 13 Керамика
Применение соединений кремния
Из керамики изготавливают изоляторы для высоковольтных
ЛЭП и другие изделия, используемые в технике, строительстве, быту и т.п.
Слайд 14Керамика - общее название многочисленных материалов, полученных при спекании глин
с различными минеральными добавками. Значит, и кирпич - керамика, и
кафель, и осколки древнегреческой амфоры - тоже керамика.Слайд 15№1. Закончите уравнения практически осуществимых реакций:
1) SiO2 +
MgO → 2) CaSiO3 + CO2 →
3) CaSiO3 + HNО3 → 4) Na2SiO3+Ba(NO3)2 → 5) SiO2 +KOH → 6) K2SiO3 + MgCl2 →Задание