Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Современные возможности терапии дифференцированного рака щитовидной железы
Содержание
- 1. Современные возможности терапии дифференцированного рака щитовидной железы
- 2. Заболеваемость и смертность от онкологических новообразований в
- 3. Заболеваемость раком щитовидной железы в мире (в зависимости от пола)Значения (тыс)GLOBOCAN 2008 Fast Stats. http://globocan.iarc.fr/factsheet.asp.
- 4. В США заболеваемость раком щитовидной железы с
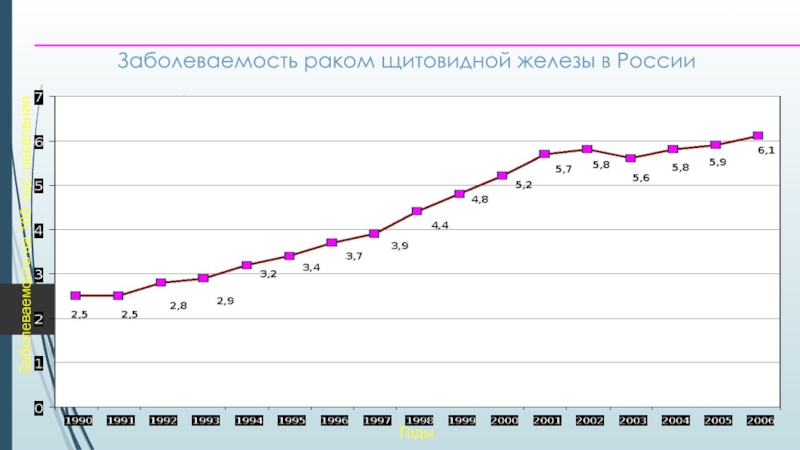
- 5. Заболеваемость раком щитовидной железы в России ГодыЗаболеваемость на 100 тыс. населения
- 6. Динамика смертности от злокачественных новообразований но нозологическим группам в Курской области
- 7. Факторы риска рака развития щитовидной железы1. American
- 8. Рак щитовидной железы: Гистологическая классификацияПРЩЖ80%-90%6,7ФРЩЖ5%-10%3,7АРЩЖ1%-2%4,7МРЩЖ2%-4%5,7,8Гюртле3%-4%1. Regalbuto
- 9. Распределение пациентов на группы рискаГруппа низкого риска
- 10. Оценка риска рецидивирования:ATA, American Thyroid Association; RAI,
- 11. Подходы к терапии дифференцированного РЩЖ ХирургияI131ИТК
- 12. Алгоритм лечения ДРЩЖСистемная терапияЛокальные методыХирургияЛучевая терапияРЧАГормоносупрессивная терапияРадиойодтерапия
- 13. Хирургическое лечение РЩЖГемитиреоидэктомия с удалением перешейкаТиреоидэктомия
- 14. Слайд 14
- 15. Изображения лимфатической сети ЩЖ с помощью рентгено-, хромолимфографии и коррозивной методик
- 16. Гемитиреоидэктомия с перешейком может быть выполнена при
- 17. Слайд 17
- 18. ДРЩЖ: роль уровня ТГ в установлении прогрессирования
- 19. Применение радиоактивного йода при РЩЖСканирование всего тела1ДРЩЖ
- 20. Выживаемость и ответ на лечениеГруппа 1: исходное накопления 131I и ПОВозраст
- 21. Критерии радиойодрезистентности ДРЩЖ Наличие по крайней мере
- 22. Обоснование применения ИТКИТК воздействуют на проангиогенные и
- 23. Системная терапия радиойод-рефрактерного ДРЩЖ Schlumberger M
- 24. Рандомизированное двойное слепое плацебо-контролируемое исследование сорафениба у
- 25. Международное, мультицентровое, рандомизированное, двойное-слепое исследование III фазыwww.clinicaltrials.gov.
- 26. www.clinicaltrials.gov. ClinicalTrials.gov identifier # NCT00984282. Brose
- 27. ДИ – доверительный интервал; ОР относительный рискBrose
- 28. Brose M, et al. Presented at ASCO
- 29. Наиболее частые нежелательные явленияBrose M, et al.
- 30. Выводы: DECISIONDECISION – первое положительное исследование III
- 31. Исследование 303 (SELECT): многоцентровое, рандомизированное, двойное слепое,
- 32. Обоснование исследованияУ пациентов с РЙР-ДРЩЖ уровень 10-летней
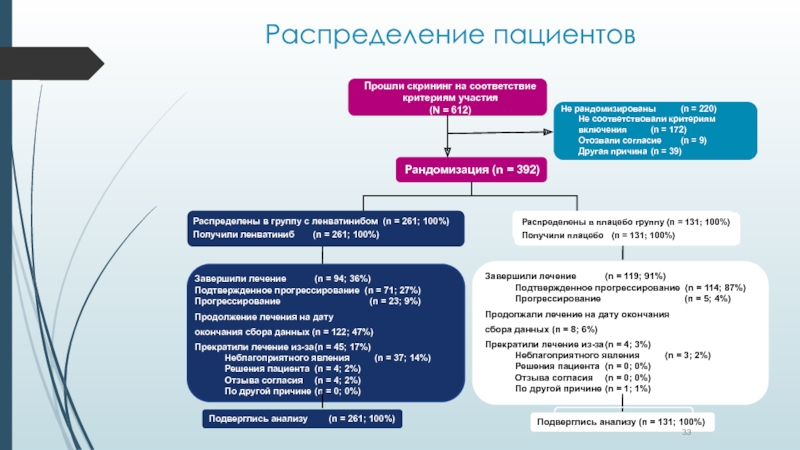
- 33. Распределение пациентов
- 34. Исследование 303 (SELECT): схема исследованияПациенты с ДРЩЖ
- 35. Первичная конечная точка: Оценка ВБП с
- 36. Частота объективного ответа: независимая оценкаМедиана времени до
- 37. Максимальное процентное изменение размера изучаемого очага относительно
- 38. Наиболее часто регистрировавшиеся связанные с лечением неблагоприятные явленияSchlumberger M et al. NEJM 2015; 372: 621-30.
- 39. Обзор нежелательных явленийSchlumberger M et al. NEJM
- 40. Исследование SELECT: выводыУ пациентов с РЙР-ДРЩЖ ленватиниб
- 41. Обновленный анализ данных исследования «SELECT» дата среза данных: 31 Августа 2015г.
- 42. Оценка Выживаемости без прогрессирования ДИ, доверительный интервал;
- 43. Оценка Выживаемости без прогрессирования в подгруппах
- 44. Суммарные данные по частоте ответов опухоли по
- 45. Медиана ДОО в группе ленватиниба в исследовании
- 46. Системная терапия радиойод-рефрактерного ДРЩЖ Schlumberger M et
- 47. Клинические рекомендации NCCN v. 1.2017: Рак щитовидной
- 48. СПАСИБО ЗА ВНИМАНИЕ!
- 49. Скачать презентанцию
Слайды и текст этой презентации
Слайд 1Современные возможности терапии дифференцированного рака щитовидной железы рефрактерного к терапии
радиоактивным йодом
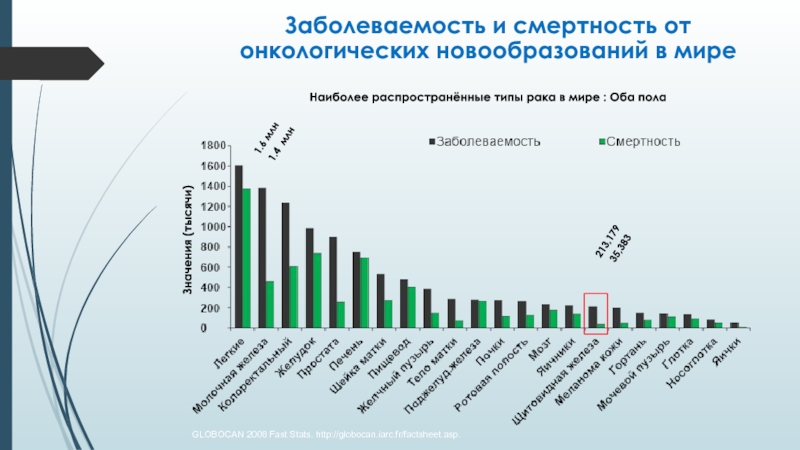
Слайд 2Заболеваемость и смертность от онкологических новообразований в мире
GLOBOCAN 2008
Fast Stats. http://globocan.iarc.fr/factsheet.asp.
Значения (тысячи)
Наиболее распространённые типы рака в мире :
Оба пола1.4 млн
1.6 млн
213,179
35,383
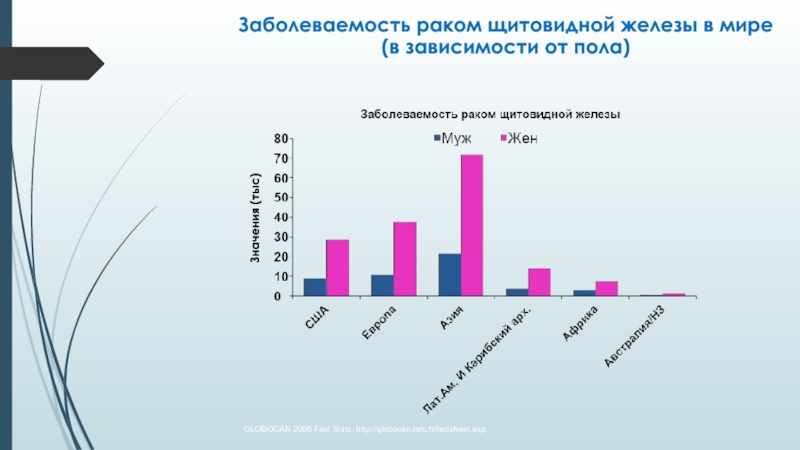
Слайд 3Заболеваемость раком щитовидной железы в мире (в зависимости от пола)
Значения
(тыс)
GLOBOCAN 2008 Fast Stats. http://globocan.iarc.fr/factsheet.asp.
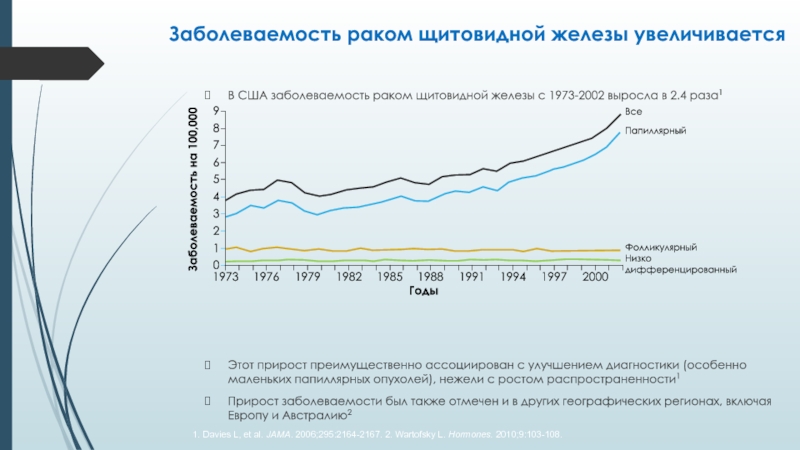
Слайд 4В США заболеваемость раком щитовидной железы с 1973-2002 выросла в
2.4 раза1
Этот прирост преимущественно ассоциирован с улучшением диагностики (особенно маленьких
папиллярных опухолей), нежели с ростом распространенности1Прирост заболеваемости был также отмечен и в других географических регионах, включая Европу и Австралию2
Заболеваемость раком щитовидной железы увеличивается
1. Davies L, et al. JAMA. 2006;295:2164-2167. 2. Wartofsky L. Hormones. 2010;9:103-108.
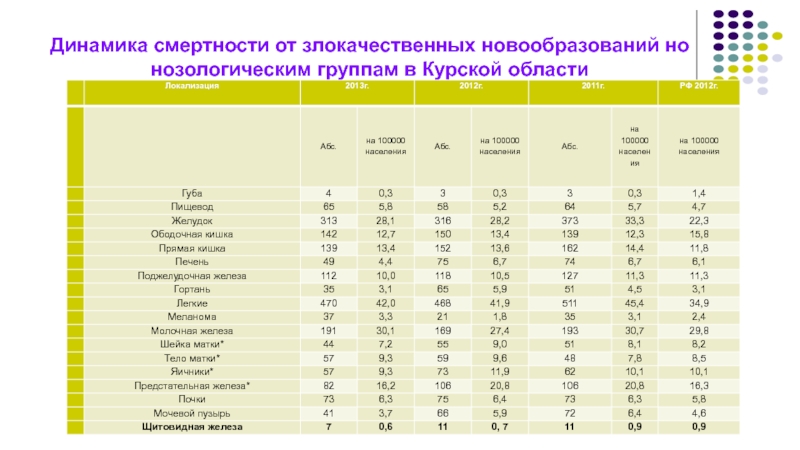
Слайд 6Динамика смертности от злокачественных новообразований но нозологическим группам в Курской
области
Слайд 7Факторы риска рака развития щитовидной железы
1. American Cancer Society. Thyroid
cancer. http://www.cancer.org/cancer/thyroidcancer/detailedguide/thyroid-cancer-risk-factors.
2. Wartofsky L. Hormones (Athens). 2010;9:103-108.
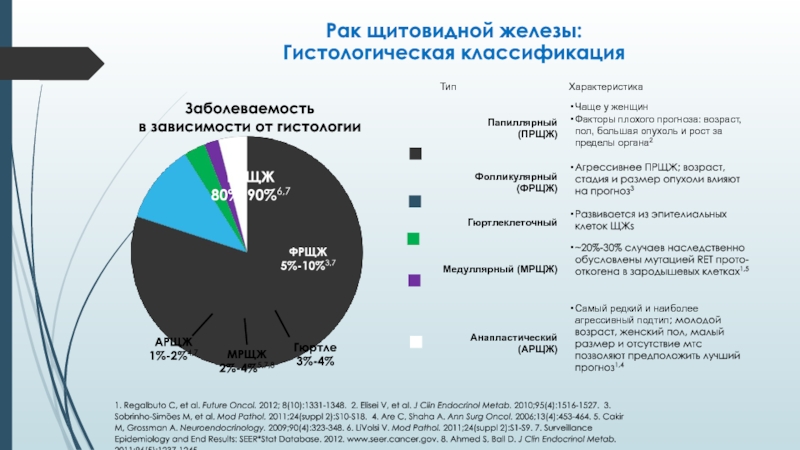
Слайд 8Рак щитовидной железы:
Гистологическая классификация
ПРЩЖ
80%-90%6,7
ФРЩЖ
5%-10%3,7
АРЩЖ
1%-2%4,7
МРЩЖ
2%-4%5,7,8
Гюртле
3%-4%
1. Regalbuto C, et al. Future
Oncol. 2012; 8(10):1331-1348. 2. Elisei V, et al. J Clin
Endocrinol Metab. 2010;95(4):1516-1527. 3. Sobrinho-Simões M, et al. Mod Pathol. 2011;24(suppl 2):S10-S18. 4. Are C, Shaha A. Ann Surg Oncol. 2006;13(4):453-464. 5. Cakir M, Grossman A. Neuroendocrinology. 2009;90(4):323-348. 6. LiVolsi V. Mod Pathol. 2011;24(suppl 2):S1-S9. 7. Surveillance Epidemiology and End Results: SEER*Stat Database. 2012. www.seer.cancer.gov. 8. Ahmed S, Ball D. J Clin Endocrinol Metab. 2011;96(5):1237-1245.Заболеваемость
в зависимости от гистологии
Слайд 9Распределение пациентов на группы риска
Группа низкого риска — пациенты с
солитарной опухолью Т1N0M0 (размером менее 2 см, без признаков экстратиреоидного
распространения)Группа промежуточного риска — пациенты с опухолью Т2N0M0 или первично-множественным РЩЖ T1N0M0
Группа высокого риска — пациенты с любой опухолью Т3, Т4, N1 или М1, персистенцией РЩЖ, а также пациенты после паллиативных операций
Слайд 10Оценка риска рецидивирования:
ATA, American Thyroid Association; RAI, radioactive iodine; RxWBS,
posttreatment whole-body RAI scan.
Tuttle R, et al. J Surg Oncol.
2008;97:712-716. 2. Cooper D, et al. Thyroid. 2009;19:1167-1214.Риск рецидива и риск смерти при раке щитовидной железы не всегда сочетаются между собой
Слайд 12Алгоритм лечения ДРЩЖ
Системная терапия
Локальные методы
Хирургия
Лучевая терапия
РЧА
Гормоносупрессивная терапия
Радиойодтерапия
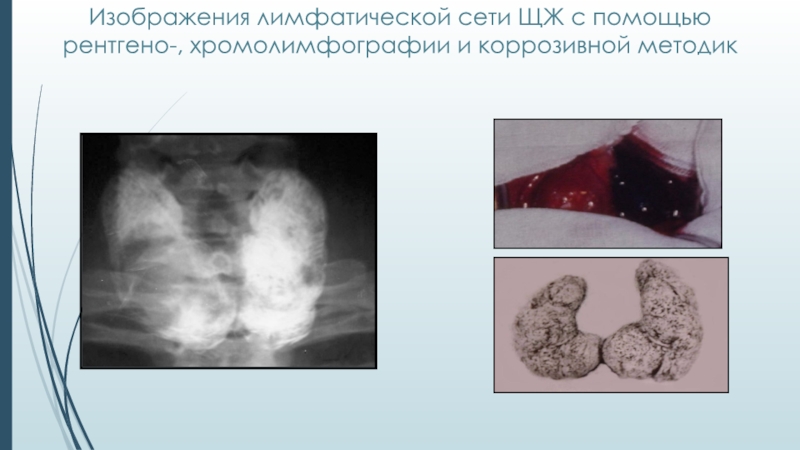
Слайд 15Изображения лимфатической сети ЩЖ с помощью рентгено-, хромолимфографии и коррозивной
методик
Слайд 16Гемитиреоидэктомия с перешейком может быть выполнена при папиллярном раке Т1
до (опухоль до 2 см, ограниченная тканью железы), при информировании
больного о всех преимуществах и недостатках данной операцииСлайд 18ДРЩЖ: роль уровня ТГ в установлении прогрессирования заболевания
Уровень ТГ является
наиболее часто используемым маркером прогрессирования заболевания и ответа на терапию
при ДРЩЖ.1,2гликопротеин с молекулярной массой 670 кДа; секретируется фолликулярными клетками щитовидной железы.
Уровень ТГ в сыворотке – высокоспецифичный и чувствительный маркер для выявления персистирующего или рецидивирующего рака ЩЖ, а также для клинического наблюдения.
После тиреоидэктомии и абляции радиоактивным йодом1
Наличие любого определяемого уровня ТГ указывает на остаточное заболевание; рекомендуется2,3:
Подавление секреции до <0,1 мЕ/л у пациентов из группы высокого и промежуточного риска
Подавление секреции до 0,1-0,5 мЕ/л у пациентов из группы низкого риска
Важные принципы послеоперационного ведении пациентов с ДРЩЖ
Циркулирующие антитела к ТГ1
Присутствуют у 10% здоровых людей и часто обнаруживаются у пациентов с раком щитовидной железы (20%)
Присутствие может быть причиной трудностей при определении уровня ТГ сыворотки
Практически во всех случаях (>95%) папиллярного или фолликулярного рака ЩЖ наблюдается секреция ТГ, даже при метастатическом процессе
1. Whitley RJ, Ain KB. Clin Lab Med. 2004;24(1):29-47.
2. McLeod DS. Clin Biochem Rev. 2010;31(1):9-19.
3. Cooper DS et al. Thyroid. 2009,19(11):1167-1214.
Слайд 19Применение радиоактивного йода при РЩЖ
Сканирование всего тела1
ДРЩЖ накапливает РЙ в
большей степени, чем другие ткани1
После полной тиреоидэктомии, очаги, накапливающие
РЙ считаются метастазамиПеред исследованием заместительная терапия тироксином приостанавливается с целью повышения уровня ТТГ1
Это также достигается путем введения рекомбинантного ТТГ(рТТГ) без прекращения заместительной терапии гормонами ЩЖ
Диета с низким содержанием йода
Доза 131I ≤1-5 мКи1
Предпочтительным является использование низких доз (1-2 мКи) для предотвращения “оглушения” остаточной ткани ЩЖ/опухоли
1. Ahn B-C, 2011: http://cdn.intechopen.com/pdfs/25565/InTech-Physiologic_and_false_positive_pathologic_uptakes_on_radioiodine_whole_body_scan.pdf.
2. Pacini F et al. ESMO Guidelines Working Group. Ann Oncol. 2012;23(suppl 7):vii110-vii119.
3. NCCN. Thyroid Carcinoma (version 1.2013). http://www.nccn.org/professionals/physician_gls/pdf/thyroid.pdf.
4. Schlumberger M, Sherman SI. Eur J Endocrinol. 2012;166(1):5-11.
Аблятивная терапия2,3
Цель – ликвидация резидуальной ткани опухоли2
Аблятивная терапия РЙ2
Показана пациентам из группы высокого, но не низкого риска
Показана всем пациентам с метастазированием, поражением лимфоузлов или размером опухоли >2 см
Требуется стимуляция ТТГ без прекращения заместительной терапии левотироксином (T4)
Успешная абляция может быть достигнута при применении низких доз 131I (30-50 мКи)2
У некоторых пациентов с отдаленными метастазами может быть необходимым использование более высоких активностей (до 200 мКи)3
Консервативное лечение радиоактивным 131I3
Показано в случаях обнаружения нерезектабельной опухоли при осмотре, рентгенологическом обследовании, или обнаружении повышенного уровня ТГ3
Пальпируемая опухоль в области шеи должна быть резецирована до начала терапии РЙ3
Опухоль должна накапливать 131I3
У пациентов с РЙ-накапливающими остаточными опухолями (подозреваемыми или подтвержденными)3
Рекомендуется терапия РЙ в дозе (100-200 мКи)3; макс. до 600 мКи4
После терапии необходимо обследование с применением визуализирующих методов
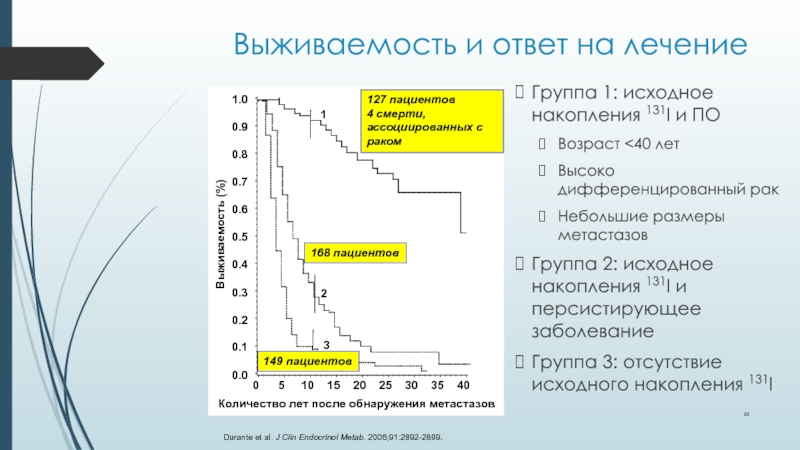
Слайд 20Выживаемость и ответ на лечение
Группа 1: исходное накопления 131I и
ПО
Возраст
2: исходное накопления 131I и персистирующее заболевание Группа 3: отсутствие исходного накопления 131I
Durante et al. J Clin Endocrinol Metab. 2006;91:2892-2899.
Слайд 21Критерии радиойодрезистентности ДРЩЖ
Наличие по крайней мере одного очага, не накапливающего
радиоактивный йод
или
Прогрессирование опухолевого процесса в течение года после лечения
радиоактивным йодом в терапевтической активности (3,7 ГБк и более), или
Отсутствие регрессии опухоли при суммарной лечебной активности более 22 ГБк (600 мКи)
Тема резистентности к РЙТ особо актуализировалась в последние 20- 30 лет
Слайд 22Обоснование применения ИТК
ИТК воздействуют на проангиогенные и онкогенные сигнальные пути
как в эндотелиальных клетках (перицитах), так и в опухолевых клетках1-8
Для
эндотелиальных клеток самыми важными проангиогенными мембранно-связанными факторами роста являются VEGF, FGF и PDGF.1-3Для опухолевых клеток, несмотря на то что VEGF, FGF и PDGF регулируют важные онкогенные сигнальные пути, RET и аберрантные сигналы от нижестоящих эффекторов, таких как RAS и BRAF, вероятно также участвуют в механизме опухолевой пролиферации.2-8
1. Folkman J. Semin Oncol. 2002;29(6 suppl 16):15-18; 2. Turner N, Grose R. Nat Rev Cancer. 2010;10(2):116-129; 3. Andrae J et al. Genes Dev. 2008;22(10):1276-1312; 4. Ferrara N. Endocr Rev. 2004;25(4):581-611; 5. Wells SA Jr, Santoro M. Clin Cancer Res. 2009;15(23):7119-7123; 6.Hanahan D, Weinberg RA. Cell. 2000;100(1):57-70; 7. Ricarte-Filho JC et al. Cancer Res. 2009;69(11):4885-4893; 8. Nikiforova MN et al. J Clin Endocrinol Metab. 2003;88(11):5399-5404.
Слайд 23Системная терапия
радиойод-рефрактерного ДРЩЖ
Schlumberger M et al. NEJM 2015;
Brose M. et al. Lancet 2014
Sorafenib in radioactive iodine-refractory localy
advanced or metastatic differentiated thyroid cancer: a randomized double-blind phase 3 trial (DECISION)Brose M. et al. 2014
или
Lenvatinib versus Placebo in Radioiodine-Refractory Thyroid Cancer. Phase 3 Study of (E7080) Lenvatinib in Differentiated Cancer of the Thyroid (SELECT)
Schlumberger M. et al. 2015
Слайд 24Рандомизированное двойное слепое плацебо-контролируемое исследование сорафениба у пациентов с местно-распространенным
или метастатическим I131-рефрактерным дифференцированным раком щитовидной железы
DECISION
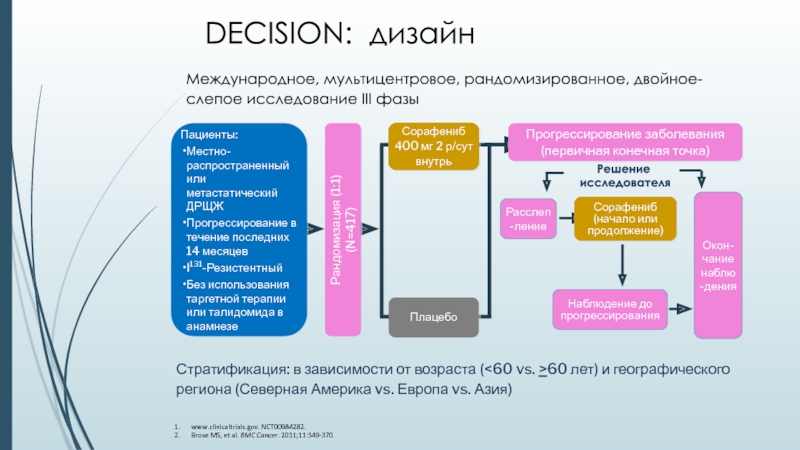
Слайд 25Международное, мультицентровое, рандомизированное, двойное-слепое исследование III фазы
www.clinicaltrials.gov. NCT00984282.
Brose MS,
et al. BMC Cancer. 2011;11:349-370.
Стратификация: в зависимости от возраста (
vs. >60 лет) и географического региона (Северная Америка vs. Европа vs. Азия)DECISION: дизайн
Слайд 26www.clinicaltrials.gov. ClinicalTrials.gov identifier # NCT00984282.
Brose M, et al.
BMC Cancer. 2011;11:349.
Первичная конечная точка
Выживаемость без прогрессирования (PFS)
Вторичные конечные
точкиОбщая выживаемость (OS)
Время до прогрессирования (TTP)
Частота контроля заболевания (стабилизация + частичный ответ + полный ответ)
DECISION:
Конечные точки исследования
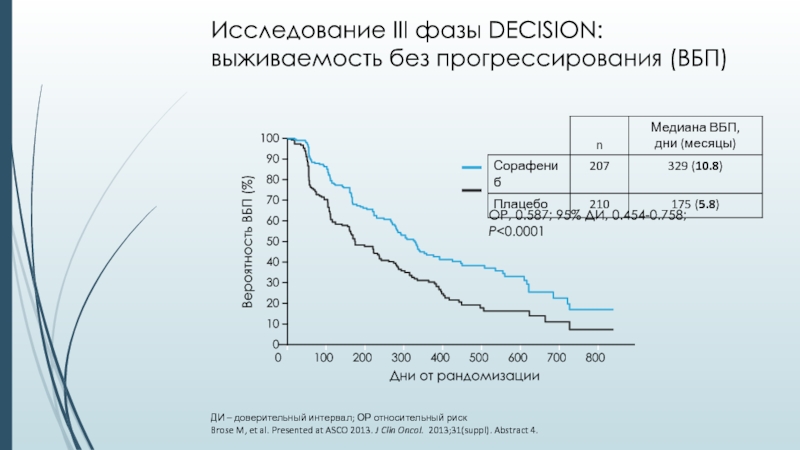
Слайд 27ДИ – доверительный интервал; ОР относительный риск
Brose M, et al.
Presented at ASCO 2013. J Clin Oncol. 2013;31(suppl). Abstract 4.
Исследование
III фазы DECISION: выживаемость без прогрессирования (ВБП)Слайд 28Brose M, et al. Presented at ASCO 2013. J Clin
Oncol. 2013;31(suppl). Abstract 4.
Вторичные точки эффективности в исследовании DECISION
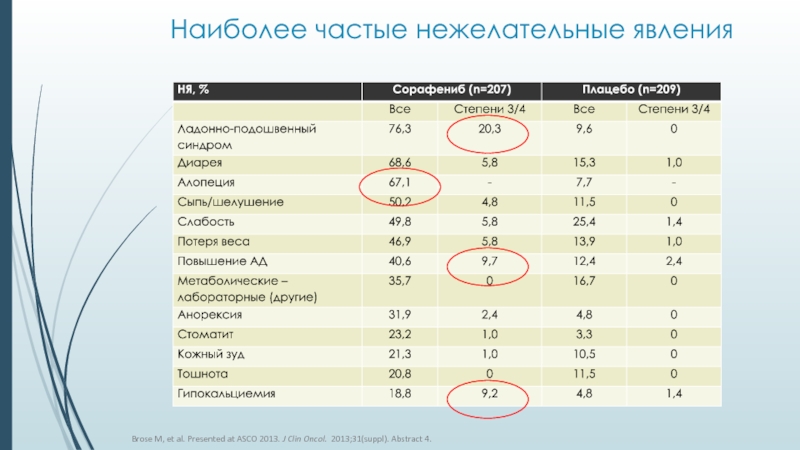
Слайд 29Наиболее частые нежелательные явления
Brose M, et al. Presented at ASCO
2013. J Clin Oncol. 2013;31(suppl). Abstract 4.
Слайд 30Выводы: DECISION
DECISION – первое положительное исследование III фазы таргетной терапии
при радиойодрефрактерном дифференцированном раке щитовидной железы
Выживаемость без прогрессирования в группе
сорафениба оказалась на 70% выше по сравнению с плацебоМедиана ВБП в группе сорафениба была на 5 месяцев больше по сравнению с плацебо
10,8 месяца по сравнению с 5,8 месяца (ОР: 0,587, 95% ДИ: 0,454-0,758, р <0,0001)
Побочные эффекты соответствовали известному профилю безопасности сорафениба
Наиболее частыми НЯ были ладонно-подошвенный синдром, диарея, алопеция, сыпь / шелушение, слабость и артериальная гипертензия
Слайд 31Исследование 303 (SELECT): многоцентровое, рандомизированное, двойное слепое, плацебо-контролируемое ИССЛЕДОВАНИЕ применения
ленватиниба у пациентов с рефрактерным к ЛЕЧЕНИЮ 131I дифференцированным раком
щитовидной железыSchlumberger M, Tahara M, Wirth LJ, et al Lenvatinib versus placebo in radioiodine-refractory thyroid cancer.
N Engl J Med. 2015 Feb 12;372(7):621-30
Слайд 32Обоснование исследования
У пациентов с РЙР-ДРЩЖ уровень 10-летней выживаемости со времени
обнаружения метастазов составлял 10% 1-3
До недавнего времени варианты лечения этих
пациентов были ограничены.Сигнальная сеть VEGF участвует в процессе ангиогенеза в опухоли и связана с агрессивностью и способностью к метастазированию рака щитовидной железы4-7
Однако в патогенезе рака щитовидной железы участвуют другие стимулирующие молекулярные факторы опухолевого роста и поддержания не обусловленного VEGF ангиогенеза 6,7
Ленватиниб, пероральный ингибитор разнообразных тирозинкиназ (VEGFR1-3, FGFR1-4, PDGFRα, RET и KIT), продемонстрировал эффективность в исследовании II фазы у пациентов с РРЙ-ДРЩЖ8,9
Исследование Фазы 3 (Study of (E7080) LEnvatinib in Differentiated Cancer of the Thyroid (SELECT)) проводилось для оценки выживаемости без прогрессирования у пациентов с РРЙ-ДРЩЖ, получавших лечение ленватинибом в сравнении с плацебо
РРЙ-ДРЩЖ, резистентный к лечению радиоактивным йодом дифференцированный рак щитовидной железы.
1. Busaidy N, Cabanillas M. J Thyroid Res. 2012;2012:618985
2. Durante C et al. J Clin Endocrinol Metab. 2006;91:2892
3. Schlumberger M et al. Lancet Diabetes Endocrinol. 2014 (ePub)
4. Berger G, Hanahan D. Nat Rev Cancer 2008;8:592
5. Ebos J et al. Clin Cancer Res. 15:5020
6. Rivera M et al. Modern Pathol. 2010;23:1191
7. Volante M et al. J Clin Endocrinol Metab. 2009;94:473
8. Sherman S et al. J Clin Oncol. 2011;29S:5503
9. Cabanillas M et al. Clin Cancer Res. Manuscript submitted
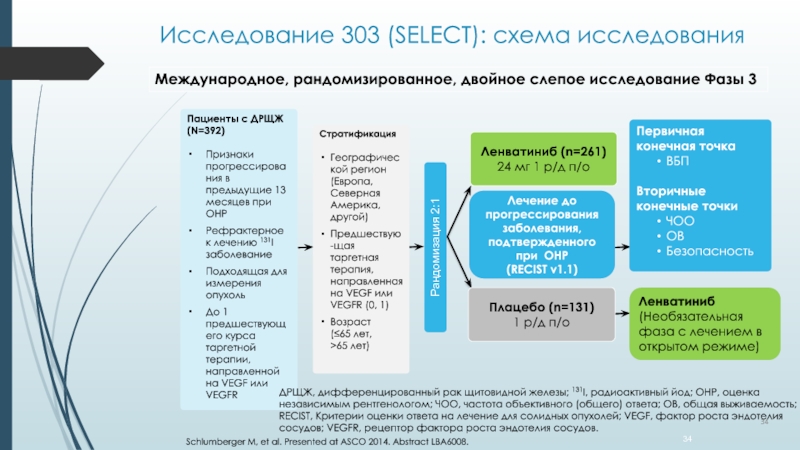
Слайд 34Исследование 303 (SELECT): схема исследования
Пациенты с ДРЩЖ
(N=392)
Признаки прогрессирования в
предыдущие 13 месяцев при ОНР
Рефрактерное к лечению 131I заболевание
Подходящая
для измерения опухольДо 1 предшествующего курса таргетной терапии, направленной на VEGF или VEGFR
Ленватиниб (n=261)
24 мг 1 р/д п/о
Стратификация
Географической регион
(Европа, Северная Америка, другой)
Предшествую-щая таргетная терапия, направленная на VEGF или VEGFR (0, 1)
Возраст
(≤65 лет,
>65 лет)
Лечение до прогрессирования заболевания, подтвержденного при ОНР
(RECIST v1.1)
Ленватиниб
(Необязательная фаза с лечением в открытом режиме)
Рандомизация 2:1
Международное, рандомизированное, двойное слепое исследование Фазы 3
ДРЩЖ, дифференцированный рак щитовидной железы; 131I, радиоактивный йод; ОНР, оценка независимым рентгенологом; ЧОО, частота объективного (общего) ответа; ОВ, общая выживаемость; RECIST, Критерии оценки ответа на лечение для солидных опухолей; VEGF, фактор роста эндотелия сосудов; VEGFR, рецептор фактора роста эндотелия сосудов.
Первичная конечная точка
ВБП
Вторичные конечные точки
ЧОО
ОВ
Безопасность
Schlumberger M, et al. Presented at ASCO 2014. Abstract LBA6008.
Плацебо (n=131)
1 р/д п/о
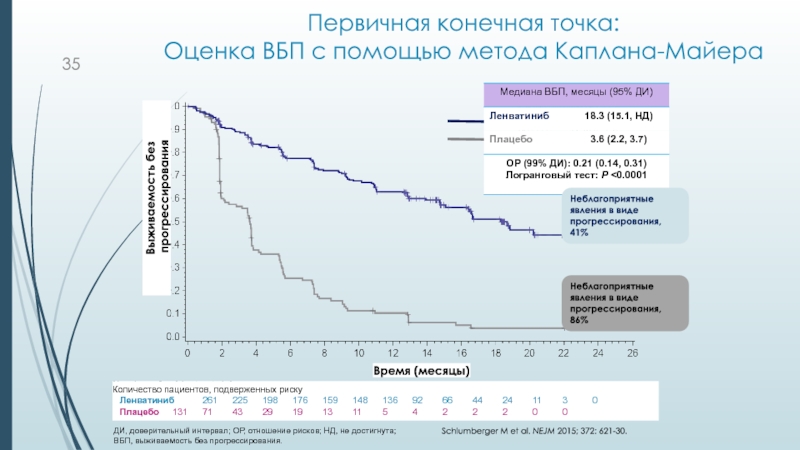
Слайд 35Первичная конечная точка:
Оценка ВБП с помощью метода Каплана-Майера
ДИ, доверительный
интервал; ОР, отношение рисков; НД, не достигнута; ВБП, выживаемость без
прогрессирования.Неблагоприятные явления в виде прогрессирования, 41%
Неблагоприятные явления в виде прогрессирования, 86%
Количество пациентов, подверженных риску
Ленватиниб 261 225 198 176 159 148 136 92 66 44 24 11 3 0
Плацебо 131 71 43 29 19 13 11 5 4 2 2 2 0 0
Время (месяцы)
Выживаемость без
прогрессирования
Schlumberger M et al. NEJM 2015; 372: 621-30.
Слайд 36Частота объективного ответа: независимая оценка
Медиана времени до ответа на ленватиниб:
2.0 месяца (диапазон, 1.9–3.5 месяцев) Медиана продолжительности ответа на ленватиниб: НД
(95% ДИ, 16.8–НД)
ПР, полный регресс; ПЗ, прогрессирование заболевания, ЧР, частичный регресс; СЗ, cтабилизация заболевания
Schlumberger M et al. NEJM 2015; 372: 621-30.
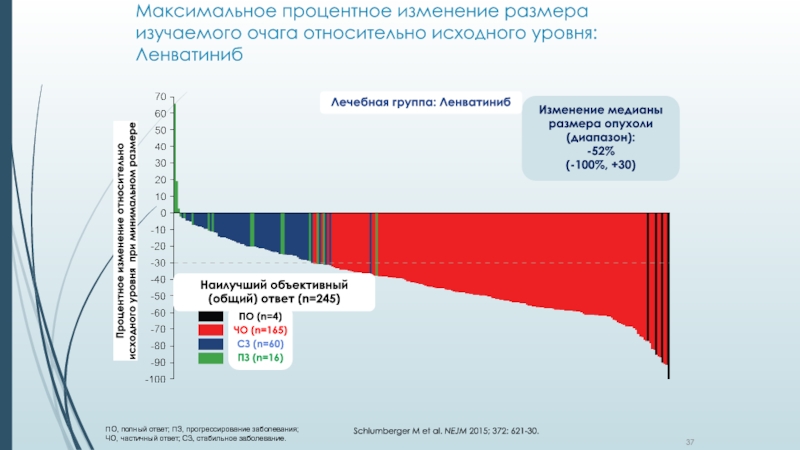
Слайд 37Максимальное процентное изменение размера изучаемого очага относительно исходного уровня: Ленватиниб
ПО,
полный ответ; ПЗ, прогрессирование заболевания; ЧО, частичный ответ; СЗ, cтабильное
заболевание.Изменение медианы размера опухоли (диапазон):
-52%
(-100%, +30)
Лечебная группа: Ленватиниб
Наилучший объективный (общий) ответ (n=245)
ПО (n=4)
ЧО (n=165)
СЗ (n=60)
ПЗ (n=16)
Процентное изменение относительно исходного уровня при минимальном размере
Schlumberger M et al. NEJM 2015; 372: 621-30.
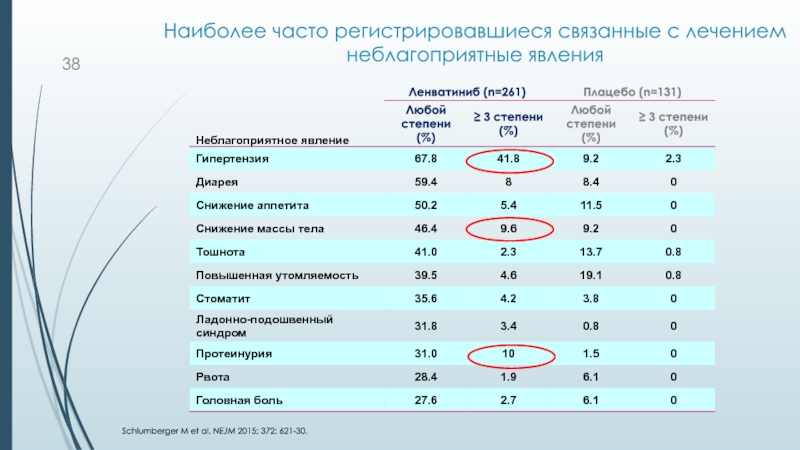
Слайд 38Наиболее часто регистрировавшиеся связанные с лечением неблагоприятные явления
Schlumberger M et
al. NEJM 2015; 372: 621-30.
Слайд 39Обзор нежелательных явлений
Schlumberger M et al. NEJM 2015; 372: 621-30.;
НЯ, неблагоприятные явления.
6/20 летальных исходов, вызванных лечением ленватинибом, были признаны
исследователем связанными с лечением:Тромбоэмболия легочной артерии (n=1)
Геморрагический инсульт (n=1)
Ухудшение общего состояния здоровья (n=4)
Слайд 40Исследование SELECT: выводы
У пациентов с РЙР-ДРЩЖ ленватиниб существенно увеличивал медиану
ВБП на 14.7 месяцев в сравнении с плацебо:
Медиана ВБП при
лечении Ленватинибом: 18.3 месяцев (95% ДИ: 15.1-НД)Медиана ВБП при назначении плацебо: 3.6 месяцев (95% ДИ: 2.2-3.7)
ОР 0.21 (99% ДИ: 0.14-0.31)
Частота ответа при использовании ленватиниба и плацебо, соответственно:
Объективный (общий) ответ: 64.8% в сравнении с 1.5%
Полный регресс: 1.5% в сравнении с 0%
Частичный регресс: 63.2% в сравнении с 1.5%
Медиана времени до объективного ответа в группе с ленватинибом составляла 2.0 месяца (диапазон 1.9–3.5 месяцев)
Медиана продолжительности ответа при назначении ленватиниба достигнута не была
У 75% респондентов частота объективного ответа составляла >9.4 месяцев
Несмотря на существенную токсичность, ее удается контролировать с помощью изменения дозы и стандартной сопутствующей/симптоматической терапии
Schlumberger M, Tahara M, Wirth LJ, et al. A phase 3, multicenter, double-blind, placebo-controlled trial of lenvatinib (E7080) in patients with 131I-refractory differentiated thyroid cancer (SELECT).
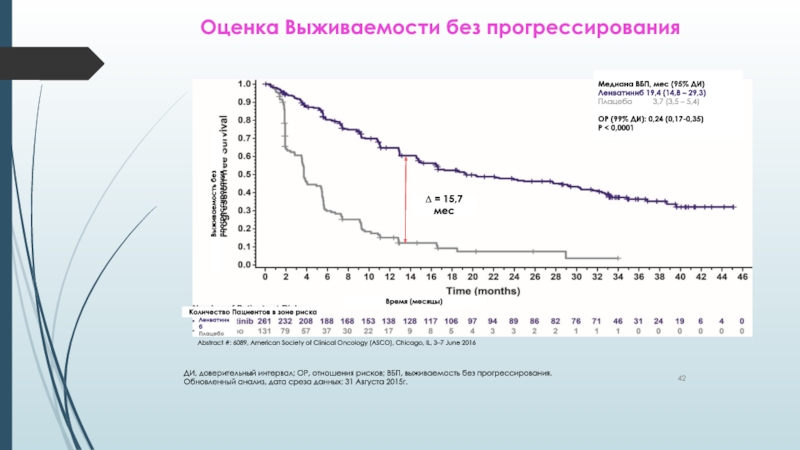
Слайд 42Оценка Выживаемости без прогрессирования
ДИ, доверительный интервал; ОР, отношения рисков;
ВБП, выживаемость без прогрессирования.
Обновленный анализ, дата среза данных: 31 Августа
2015г.Медиана ВБП, мес (95% ДИ)
Ленватиниб 19,4 (14,8 – 29,3)
Плацебо 3,7 (3,5 – 5,4)
ОР (99% ДИ): 0,24 (0,17-0,35)
P < 0,0001
Ленватиниб
Плацебо
Количество Пациентов в зоне риска
Время (месяцы)
Выживаемость без прогрессирования
∆ = 15,7 мес
Abstract #: 6089, American Society of Clinical Oncology (ASCO), Chicago, IL, 3–7 June 2016
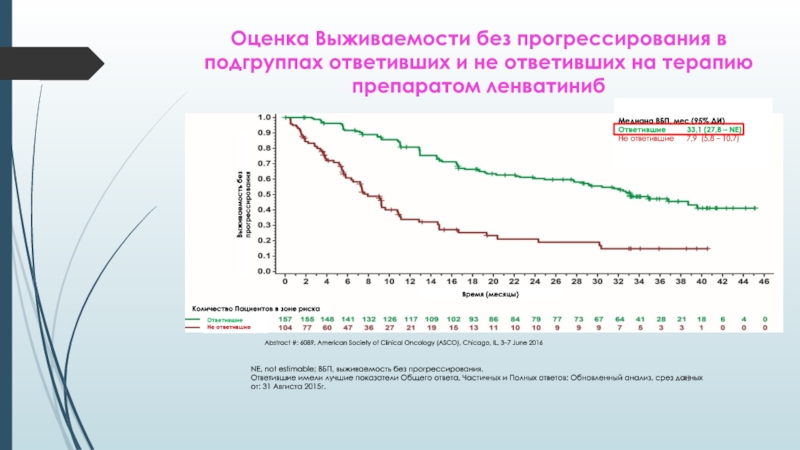
Слайд 43Оценка Выживаемости без прогрессирования в подгруппах ответивших и не ответивших
на терапию препаратом ленватиниб
NE, not estimable; ВБП, выживаемость без прогрессирования.
Ответившие
имели лучшие показатели Общего ответа, Частичных и Полных ответов; Обновленный анализ, срез данных от: 31 Авгиста 2015г.Медиана ВБП, мес (95% ДИ)
Ответившие 33,1 (27,8 – NE)
Не ответившие 7,9 (5,8 – 10,7)
Время (месяцы)
Количество Пациентов в зоне риска
Ответившие
Не ответившие
Выживаемость без прогрессирования
Abstract #: 6089, American Society of Clinical Oncology (ASCO), Chicago, IL, 3–7 June 2016
Слайд 44Суммарные данные по частоте ответов опухоли по оценке исследователей.
*По
оценке исследователей, ДИ, Доверительный интервал; ПО, полный ответ; NE, not
evaluable; ЧО, частичный ответ; СЗ, Стабилизация заболевания.Длительная стабилизация определялась, как стабилизация длившаяся более 23 недель.
Обновленный анализ, срез данных от: 31 Авгиста 2015г.
Abstract #: 6089, American Society of Clinical Oncology (ASCO), Chicago, IL, 3–7 June 2016
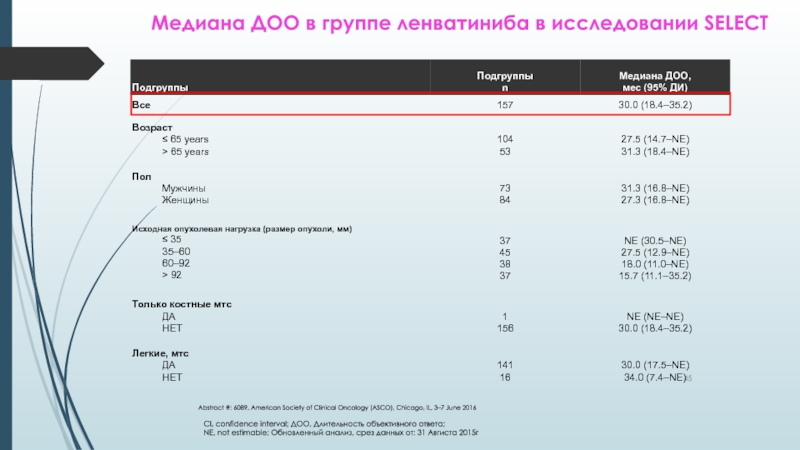
Слайд 45Медиана ДОО в группе ленватиниба в исследовании SELECT
CI, confidence interval;
ДОО, Длительность объективного ответа;
NE, not estimable; Обновленный анализ, срез данных
от: 31 Авгиста 2015гAbstract #: 6089, American Society of Clinical Oncology (ASCO), Chicago, IL, 3–7 June 2016
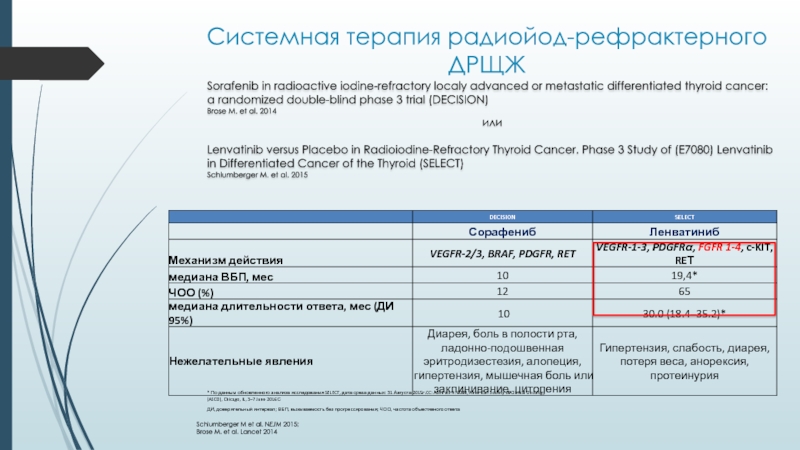
Слайд 46Системная терапия радиойод-рефрактерного ДРЩЖ
Schlumberger M et al. NEJM 2015;
Brose M. et al. Lancet 2014
Sorafenib in radioactive iodine-refractory localy
advanced or metastatic differentiated thyroid cancer: a randomized double-blind phase 3 trial (DECISION)Brose M. et al. 2014
или
Lenvatinib versus Placebo in Radioiodine-Refractory Thyroid Cancer. Phase 3 Study of (E7080) Lenvatinib in Differentiated Cancer of the Thyroid (SELECT)
Schlumberger M. et al. 2015
* По данным обновленного анализа исследования SELECT, дата среза данных: 31 Августа 2015г.CC: Abstract #: 6089, American Society of Clinical Oncology (ASCO), Chicago, IL, 3–7 June 2016С
ДИ, доверительный интервал; ВБП, выживаемость без прогрессирования; ЧОО, частота объективного ответа
Слайд 47Клинические рекомендации NCCN v. 1.2017: Рак щитовидной железы
Ленватиниб рекомендован в
качестве препарата предпочтительного выбора при папилярном, фоликулярном и Гюртлеклеточном раке
щитовидной железыаааа Решение о выборе препарата Ленватиниб (предпочтительно) или Сорафениб должно приниматься индивидуально для каждого пациента, на основании данных по частоте ответов и наличию сопутствующих заболеваний