Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Спирты
Содержание
- 1. Спирты
- 2. Спирты Спирты - соединения алифатического ряда, содержащие
- 3. Номенклатура спиртовСистематические названия даются по названию углеводорода
- 4. Номенклатура спиртовНумерация ведется от ближайшего к ОН-группе конца цепи:
- 5. Номенклатура спиртовВ многоатомных спиртах положение и число ОН-групп указывают суффиксами диол, триол и цифрами:
- 6. Классификация спиртов1.По числу гидроксильных групп спирты подразделяются
- 7. Классификация спиртов2.В зависимости от того, с каким
- 8. Классификация спиртов3. По строению радикалов, связанных с
- 9. Слайд 9
- 10. Физические свойстваНизшие спирты (до C15) — жидкости,
- 11. 1. Кислотные свойства спиртов выражены очень слабо.
- 12. 2. При действии на спирты органических кислот
- 13. 3. Спирты окисляются под действием дихромата или
- 14. Горение спиртов:С2Н5ОН+ 3О2
- 15. При более слабом нагревании происходит межмолекулярная дегидратация
- 16. Получение1. Самый общий способ получения спиртов, имеющий
- 17. 2. Другой общий способ получения спиртов —
- 18. 4. Этанол получают при спиртовом брожении глюкозы:С6Н12О6 → 2С2Н5ОН + 2СО2↑.
- 19. Применение спиртовСпирты главным образом используют в промышленности
- 20. Простые эфиры Простыми эфирами называют органические вещества,
- 21. Простые эфиры Простые эфиры рассматриваются как производные
- 22. Скачать презентанцию
Спирты Спирты - соединения алифатического ряда, содержащие одну или несколько гидроксильных групп. Общая формула спиртов с одной гидроксигруппой R–OH. Общая формула гомологического ряда предельных одноатомных спиртов — CnH2n+1OH.
Слайды и текст этой презентации
Слайд 2Спирты
Спирты - соединения алифатического ряда, содержащие одну или несколько
гидроксильных групп.
формула гомологического ряда предельных одноатомных спиртов — CnH2n+1OH.Слайд 3Номенклатура спиртов
Систематические названия даются по названию углеводорода с добавлением суффикса
-ол и цифры, указывающей положение гидроксигруппы (если это необходимо):
Слайд 5Номенклатура спиртов
В многоатомных спиртах положение и число ОН-групп указывают суффиксами
диол, триол и цифрами:
Слайд 6Классификация спиртов
1.По числу гидроксильных групп спирты подразделяются на
одноатомные (одна
группа -ОН),
многоатомные (две и более групп -ОН).
Современное название многоатомных
спиртов - полиолы (диолы, триолы и т.д):двухатомный спирт – этиленгликоль (этандиол)
HO–СH2–CH2–OH
трехатомный спирт – глицерин (пропантриол-1,2,3)
HO–СH2–СН(ОН)–CH2–OH
Слайд 7Классификация спиртов
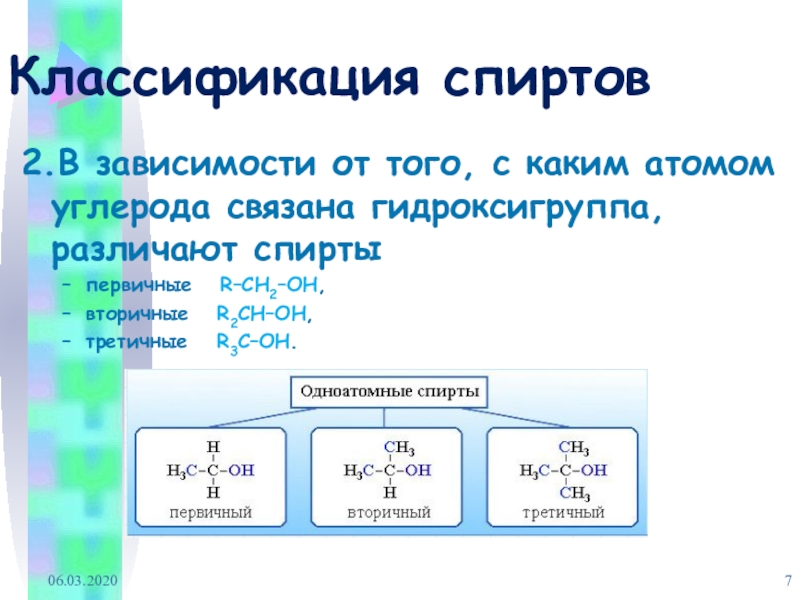
2.В зависимости от того, с каким атомом углерода связана
гидроксигруппа, различают спирты
первичные R–CH2–OH,
вторичные R2CH–OH,
третичные R3C–OH.
Слайд 8Классификация спиртов
3. По строению радикалов, связанных с атомом кислорода, спирты
подразделяются на:
предельные, или алканолы (СH3CH2–OH)
непредельные, или алкенолы (CH2=CH–CH2–OH)
ароматические (C6H5CH2–OH).
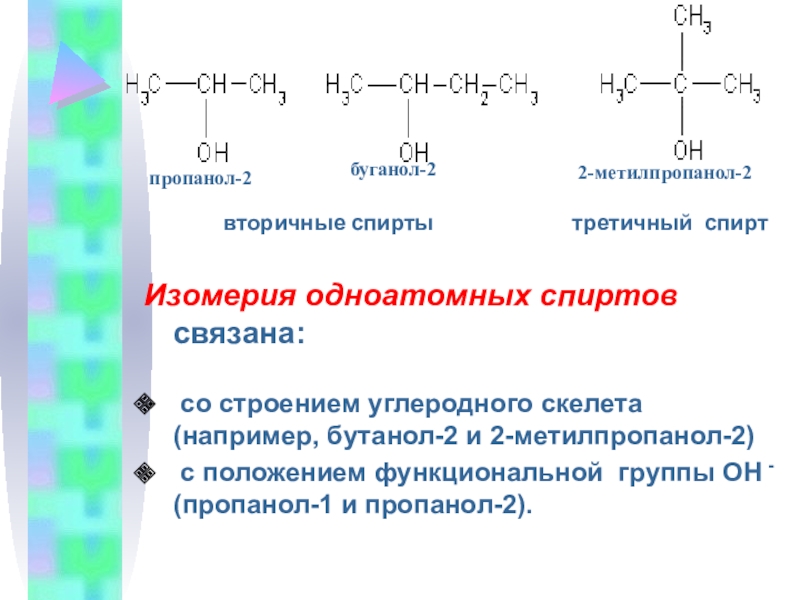
Слайд 9 вторичные спирты
третичный спирт
Изомерия одноатомных спиртов связана:
со строением углеродного скелета (например, бутанол-2 и 2-метилпропанол-2)
с положением функциональной группы ОН - (пропанол-1 и пропанол-2).
пропанол-2
буганол-2
2-метилпропанол-2
Слайд 10Физические свойства
Низшие спирты (до C15) — жидкости, высшие — твердые
вещества.
Метанол и этанол смешиваются с водой в любых соотношениях.
С ростом молекулярной массы растворимость спиртов в воде падает.По сравнению с соответствующими углеводородами, спирты имеют высокие температуры плавления и кипения, что объясняется сильной ассоциацией молекул спирта в жидком состоянии за счет образования водородных связей .
Слайд 111. Кислотные свойства спиртов выражены очень слабо. Низшие спирты бурно
реагируют со щелочными металлами:
2С2Н5-ОН + 2K→ 2С2Н5-ОK + Н2↑
В присутствии
следов влаги соли спиртов (алкоголяты) разлагаются до исходных спиртов:С2Н5ОK + Н2О → С2Н5ОН + KОН.
Это доказывает, что спирты — более слабые кислоты, чем вода.
С увеличением длины углеводородного радикала скорость этой реакции замедляется
Реакции с разрывом связи О-Н
Слайд 122. При действии на спирты органических кислот и минеральных кислот
образуются сложные эфиры (реакция этерификации).
Образование сложных эфиров протекает по
механизму нуклеофильного присоединения-отщепления :С2Н5ОН + СН3СООН СН3СООС2Н5 + Н2О этилацетат
Слайд 13
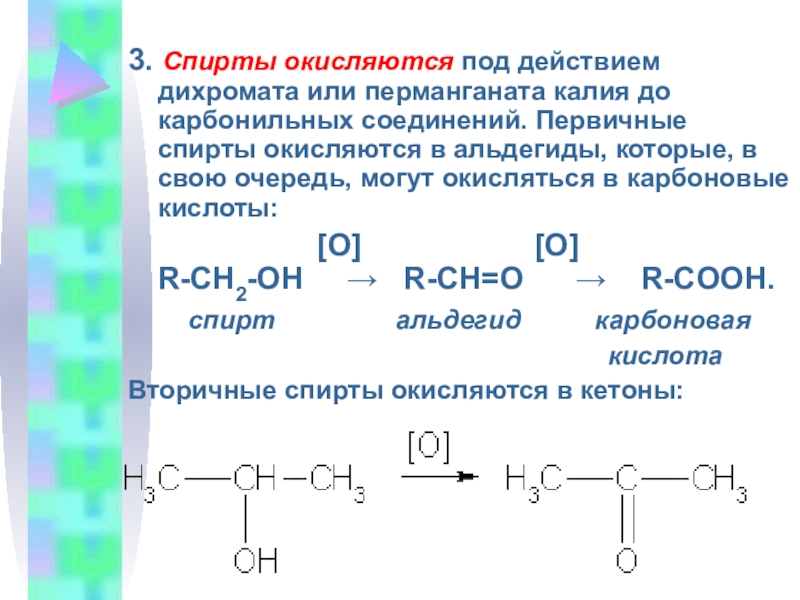
3. Спирты окисляются под действием дихромата или перманганата калия до
карбонильных соединений. Первичные спирты окисляются в альдегиды, которые, в свою
очередь, могут окисляться в карбоновые кислоты:[O] [О] R-CH2-OH → R-CH=O → R-COOH.
спирт альдегид карбоновая
кислота
Вторичные спирты окисляются в кетоны:
Слайд 14 Горение спиртов:
С2Н5ОН+ 3О2
2СО2 + 3Н2О
Реакции дегидратации протекают при
нагревании спиртов с водоотнимающими веществами. При сильном нагревании происходит внутримолекулярная дегидратация с образованием алкенов:H2SO4 ,t >140°С СН3-СН2-СН2-ОН
СН3-СН=СН2 + Н2О.
Слайд 15При более слабом нагревании происходит межмолекулярная дегидратация с образованием простых
эфиров:
H2SO4,t< 140°С
2CH3-CH2-OH C2H5-O-C2H5 + H2O.
медленно.
Слайд 16Получение
1. Самый общий способ получения спиртов, имеющий промышленное значение, —
гидратация алкенов. Реакция идет при пропускании алкена с парами воды
над фосфорнокислым катализатором: H3PO4СН2=СН2 + Н2О → СН3—СН2—ОН
Из этилена получается этиловый спирт, из пропена — изопропиловый. Присоединение воды идет по правилу Марковникова, поэтому из первичных спиртов по данной реакции можно получить только этиловый спирт.
Слайд 172. Другой общий способ получения спиртов — гидролиз алкилгалогенидов под
действием водных растворов щелочей:
R—Br +
NaOH → R—OH + NaBr.По этой реакции можно получать первичные, вторичные и третичные спирты.
Слайд 19Применение спиртов
Спирты главным образом используют в промышленности органического синтеза.
Метанол –
сильный яд, при приеме внутрь вызывает слепоту, в больших дозах
– смертьЭтанол - важное сырье пищевой промышленности. В фармации используется для приготовления настоек и экстрактов. В медицине как наружное антисептическое средство для дезинфекции рук и хирургических инструментов.
Слайд 20Простые эфиры
Простыми эфирами называют органические вещества, молекулы которых состоят
из углеводородных радикалов, соединенных атомом кислорода: R'–O–R", где R' и
R" - различные или одинаковые радикалы.Слайд 21Простые эфиры
Простые эфиры рассматриваются как производные спиртов.
Названия этих
соединений строятся из названий радикалов (в порядке возрастания молекулярной массы)
и слова "эфир":CH3OCH3 - диметиловый эфир;
C2H5OCH3 - метилэтиловый эфир.