Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
СРС по органической химии. Тема: Химические и физические свойства карбоновых
Содержание
- 1. СРС по органической химии. Тема: Химические и физические свойства карбоновых
- 2. Карбоновые кислоты Физические свойства карбоновых кислот.Низшие карбоновые
- 3. Химические свойства карбоновых кислот1. Диссоциация в водных
- 4. Характерные свойства для карбоновых кислот 1.
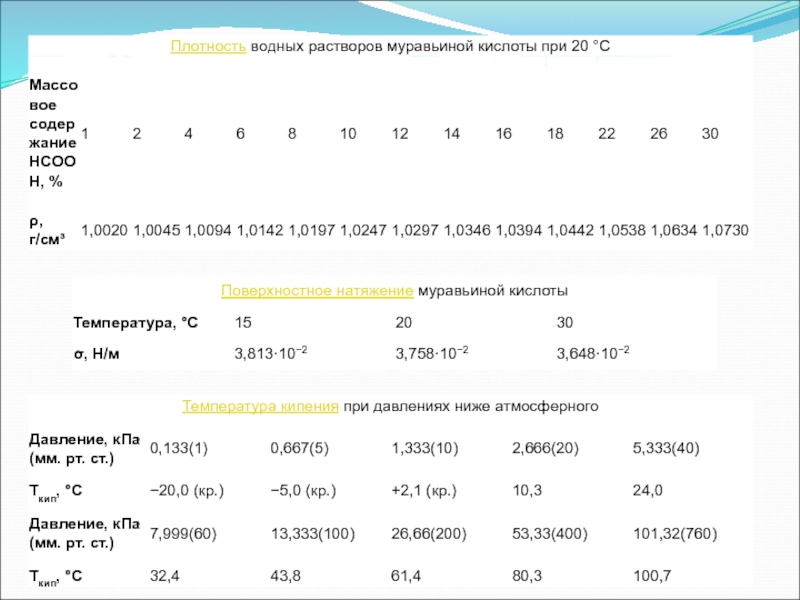
- 5. Муравьиная кислотаФизические и термодинамические свойстваПри нормальных условиях
- 6. Слайд 6
- 7. Слайд 7
- 8. Химические свойстваКонстанта диссоциации : 1,772·10−4.Муравьиная кислота, кроме
- 9. Уксусная кислота Физические свойстваУксусная кислота представляет собой
- 10. Уксусная кислота образует тройные азеотропные смесис водой
- 11. Химические свойства Уксусная кислота обладает всеми свойствами карбоновых
- 12. итог:Уксусная кислота вступает во все реакции, характерные
- 13. Скачать презентанцию
Слайды и текст этой презентации
Слайд 1СРС по органической химии. Тема: Химические и физические свойства карбоновых кислот. Свойства
муравьиной и уксусной кислоты.
ХТМб-11-1Слайд 2Карбоновые кислоты
Физические свойства карбоновых кислот.
Низшие карбоновые кислоты — жидкости с
острым запахом, хорошо растворимые в воде. С повышением относительной молекулярной
массы растворимость кислот в воде и их плотность уменьшаются, а температура кипения повышается. Высшие кислоты, начиная с пеларгоновой (н-нонановой) СН3-(СН2)7-СООН, — твердые вещества, без запаха, нерастворимые в воде. Низшие карбоновые кислоты в безводном виде и в виде концентрированных растворов раздражают кожу и вызывают ожоги, особенно муравьиная кислота и уксусная кислота.На физических свойствах карбоновых кислот сказывается значительная степень ассоциации вследствие образования водородных связей. Кислоты в отличие от спиртов, образуют более прочные водородные связи, вследствие того что связи в них в большей степени поляризованы по типу Кроме того, у карбоновых кислот имеется возможность образования водородных связей с кислородом карбонильного диполя, обладающим значительной электроотрицательностью, а не только с кислородом другой гидроксильной группы. Действительно, в твердом и жидком состояниях карбоновые кислоты существуют в основном в виде циклических димеров.
Слайд 3Химические свойства карбоновых кислот
1. Диссоциация в водных растворах (среда кислая,
индикаторы меняют окраску):
СH3–COOH ↔ СH3–COO- + H+
2.Взаимодействие с металлами,
стоящими в электрохимическом ряду напряженийдо водорода:
2СН3СООН + Мg = H2 + ( CH3COO)2 Mg
2СН3СООН + Zn = H2 + ( CH3COO)2 Zn
Наиболее важные химические свойства, характерные для большинства карбоновых кислот:
3. Карбоновые кислоты при реакции с металлами, их оксидами или их осно́вными гидроксидами дают соли соответствующих металлов:
4. Карбоновые кислоты могут вытеснять более слабую кислоту из её соли, например:
5. Карбоновые кислоты в присутствии кислого катализатора реагируют со спиртами, образуя сложные эфиры (реакция этерификации):
6. При нагревании аммонийных солей карбоновых кислот образуются их амиды:
7. Под действием карбоновые кислоты превращаются в соответствующие хлорангидриды:
8.Взаимодействие уксусной кислоты с карбонатом натрия
2СН3СООН + Na2CO3 = H2O + CO2 + 2CH3COONa
Слайд 4Характерные свойства для карбоновых кислот
1. Реакция этерификации
СН3СООН + СН3ОН→СН3СООСН3+Н2О
уксусная к-та метанол метилацетат
2. Реакции замещения
галогенирование
СН3 – СООН + Cl2→CH2Cl – COOH + HCl
хлоруксусная кислота
3.Горение уксусной кислоты
СН3СООН + 2О2 = 2H2О + 2СО2
Слайд 5Муравьиная кислота
Физические и термодинамические свойства
При нормальных условиях муравьиная кислота представляет
собой бесцветную жидкость. Растворима в ацетоне, бензоле, глицерине, толуоле. Смешивается
с водой, диэтиловым эфиром, этаноломСлайд 8Химические свойства
Константа диссоциации : 1,772·10−4.
Муравьиная кислота, кроме кислотных свойств, проявляет
также некоторые свойства альдегидов, в частности, восстановительные. При этом она окисляется
до углекислого газа. Например:2KMnO4 + 5HCOOH + 3H2SO4 → K2SO4 + 2MnSO4 + 5CO2↑ + 8H2O
При нагревании с сильными водоотнимающими средствами (H2SO4 (конц.) или P4O10) разлагается на воду и моноксид углерода:
HCOOH →(t) CO↑ + H2O
Слайд 9Уксусная кислота
Физические свойства
Уксусная кислота представляет собой бесцветную жидкость с характерным резким запахом и кислымвкусом. Гигроскопична.
Неограниченно растворима в воде. Смешивается со многими растворителями; в уксусной кислоте хорошо
растворимы неорганические соединения и газы, такие как HF, HCl, HBr, HI и другие. Существует в виде циклических и линейных димеров.Абсолютная уксусная кислота называется ледяной, ибо при замерзании образует льдовидную массу (см. изображение справа).
Давление паров (в мм. рт. ст.):
10 (17,1 °C)
40 (42,4 °C)
100 (62,2 °C)
400 (98,1 °C)
560 (109 °C)
1520 (143,5 °C)
3800 (180,3 °C)
Диэлектрическая проницаемость: 6,15 (20 °C)
Динамическая вязкость жидкостей и газов (в мПа·с): 1,155 (25,2 °C); 0,79 (50 °C)
Поверхностное натяжение: 27,8 мН/м (20 °C)
Удельная теплоемкость при постоянном давлении: 2,01 Дж/г·K (17 °C)
Стандартная энергия Гиббса образования ΔfG0 (298 К, кДж/моль): −392,5 (ж)
Стандартная энтропия образования ΔfS0 (298 К, Дж/моль·K): 159,8 (ж)
Энтальпия плавления ΔHпл: 11,53 кДж/моль
Температура вспышки в воздухе: 38 °C
Температура самовоспламенения на воздухе: 454 °C
Теплота сгорания: 876,1 кДж/моль
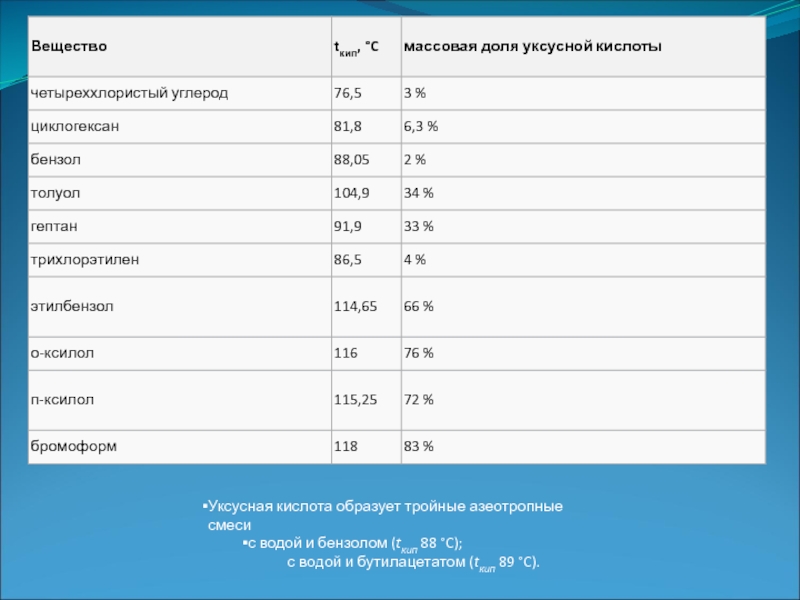
Уксусная кислота образует двойные азеотропные смеси со следующими веществами.
Слайд 10
Уксусная кислота образует тройные азеотропные смеси
с водой и бензолом (tкип 88 °C);
с водой и бутилацетатом (tкип 89 °C).
Слайд 11Химические свойства
Уксусная кислота обладает всеми свойствами карбоновых кислот. Связь между водородом
и кислородом
карбоксильной группы (−COOH) карбоновой кислоты является сильно полярной, вследствие чего
эти соединения способны легко диссоциировать и проявляют кислотные свойства.
В результате диссоциации уксусной кислоты образуется ацетат-ион CH3COO− и протон H+. Уксусная кислота
является слабой одноосновной кислотой со значением pKa в водном растворе равным 4,75. Раствор с
концентрацией 1.0 M (приблизительная концентрация пищевого уксуса) имеет pH 2,4, что соответствует степени
диссоциации 0,4 %.
Исследования показывают, что в кристаллическом состоянии молекулы образуют димеры, связанные
водородными связями.
Уксусная кислота способна взаимодействовать с активными металлами. При этом выделяется водород и
образуются соли — ацетаты.
Mg(тв) + 2CH3COOH → (CH3COO)2Mg + H2
Уксусная кислота может хлорироваться действием газообразного хлора. При этом образуется хлоруксусная кислота.
CH3COOH + Cl2 → CH2ClCOOH + HCl
Этим путем могут быть получены также
дихлоруксусная (CHCl2COOH) и
трихлоруксусная (CCl3COOH) кислоты.