Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Ток в электролитах
Содержание
- 1. Ток в электролитах
- 2. Электролиты – это водные растворы солей, кислот,
- 3. Диссоциация – это процесс расщепления молекул электролита на положительные и отрицательные ионы под действием растворителя.
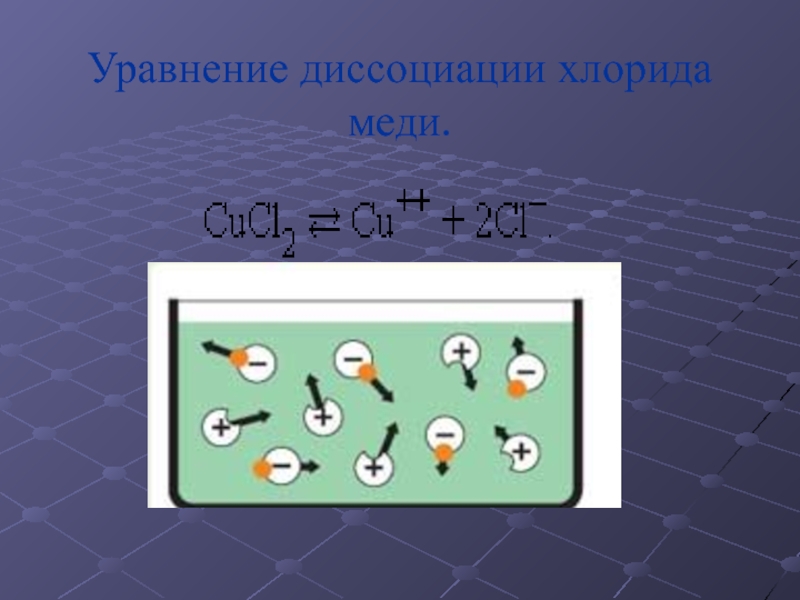
- 4. Уравнение диссоциации хлорида меди.
- 5. Рекомбинация – это процесс соединение ионов в
- 6. Ток в электролитах – это упорядоченное движение положительных и отрицательных ионов. +-Катод_Анод+Направление тока в электролите
- 7. При прохождении электрического тока через электролит наблюдается
- 8. Закон Фарадея для электролиза формулируется так: Масса m
- 9. Применение электролиза.
- 10. 1.Гальваностегия – это… декоративное или антикоррозийное
- 11. 2.Гальванопластика – это… электролитическоеизготовление металлических копий, рельефныхпредметов.
- 12. 3.Электрометаллургия – это…получение чистых металлов (Al, Na, Mg, Be)при электролизе расплавленных руд.
- 13. 4.Рафинирование металлов – это… очистка металлов
- 14. Скачать презентанцию
Электролиты – это водные растворы солей, кислот, щелочей. Носителями заряда в электролитах являются положительные и отрицательные ионы.
Слайды и текст этой презентации
Слайд 2 Электролиты – это водные растворы солей, кислот, щелочей. Носителями заряда
в электролитах являются положительные и отрицательные ионы.
Слайд 3 Диссоциация – это процесс расщепления молекул электролита на положительные
и
отрицательные ионы под действием растворителя.
Слайд 5Рекомбинация – это процесс соединение ионов в нейтральную молекулу. Если
в электролите нет электрического поля, то ионы движутся непрерывно и
хаотично.Если в электролите создать ЭП, то ионы начнут двигаться. Положительные ионы меди - к аноду, а отрицательные ионы хлора - к катоду.
Слайд 6Ток в электролитах – это упорядоченное движение
положительных и отрицательных ионов.
+
-
Катод
_
Анод
+
Направление
тока в электролите
Слайд 7 При прохождении электрического тока через электролит наблюдается выделение веществ, входящих
в
электролит, на электродах. Электролиз – это явление выделения на
электродах веществ, входящих в состав электролита, при протекании через него электрического тока.Слайд 8Закон Фарадея для электролиза формулируется так:
Масса m вещества, выделившегося на
электроде, прямо пропорциональна
заряду q, прошедшему через электролит:
m = kq = kIt. Величину k называют электрохимическим
эквивалентом и находят для разных веществ в таблице.