Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
ТРЭ_заочники
Содержание
- 1. ТРЭ_заочники
- 2. Введение.Определение понятия «редкий элемент»Редкие элементы – условное
- 3. Введение.Определение понятия «редкий элемент»К «редким» не относят
- 4. Введение.Определение понятия «редкий элемент» Редкие металлы, обладающие общностью
- 5. Редкие металлы в Периодической системе
- 6. Слайд 6
- 7. Редкие металлы определяют научно-технический прогресс в важнейших
- 8. Введение. Основные области применения редких металловПромышленно-экономический
- 9. Атомная энергетикаВе –основной материал для изготовления отражателей
- 10. Ta – незаменимым материалом в производстве конденсаторов,
- 11. Одна из секций установки Т-15 Токамак со сверхпроводящими магнитными катушками на основе Nb3Sn
- 12. Соединения лития широко применяют для производства химических
- 13. Наибольший объем потребления РМ связан с производством
- 14. Универсальная ракетно-космическая транспортная система "Энергия" и космический корабль «Буран» в полете
- 15. Для производство титановых сплавов, востребованных в авиастроении
- 16. Звезды сделаны из селенового рубина - стекла,
- 17. Сырье для производства редких металловПроизводство РМ было
- 18. Типы сырьяминералы РМминералы других элементоввторичные источники сырьяСырье для производства редких металлов
- 19. Сподумен LiAl[Si2O6] алюмосиликат лития.Лепидолит KLi2Al[Si4O10](F,OH)2 алюмосиликат из группы литиевых слюдСырье для производства редких металлов
- 20. Поллуцит – водный алюмосиликат цезия: (Cs,Na)[AlSi2O6].nH2OСырье для производства редких металлов
- 21. В процессе выветривания горных пород и минералов
- 22. Берилл 3BeO.Al2O3.6SiO2 – алюмосиликат бериллия.Сырье для производства редких металлов
- 23. Лопарит (Ln,Na,Ca)2(Ti,Nb)2O6 титанат-ниобат РЗЭ, Na, CaМонацит (Ln,Th)PO4
- 24. уранинит U3O8гуммит UO3∙xH2Oнастуран UO2+хСырье для производства редких металлов
- 25. Каронотит K2(UO2)2(VO4)2·3H2O ванадат уранила и калияТюямунит
- 26. Циркон ZrSiO4 ортосиликат цирконияБадделеит ZrO2оксид цирконияСырье для производства редких металлов
- 27. Колумбит-танталит – ниобат-танталат железа и марганца: (Fe,Mn)[(Nb,TaO3)2]
- 28. Карналлит (Li, Rb, Cs) – KCl∙MgCl2∙6H2O .Сырье для производства редких металлов
- 29. Апатит (РЗЭ) – Сa5(PO4)3F .Сырье для производства редких металлов
- 30. Титаномагнетиты (V) – Fe3O4∙TiO2Сырье для производства редких металлов
- 31. Вторичные источникиУран – переработка ОЯТТа – отработанные конденсаторыNb - сверхпроводникиСырье для производства редких металлов
- 32. Общая ситуация с сырьем РМ в РоссииЭндогенный
- 33. Оптимальная стратегия : восстановление и развитие уже
- 34. Развитие новых месторождений –Этыкинское (Li, Be, Nb,
- 35. Обогащение рудЦель процесса – максимальное обогащение бедной
- 36. Обогащение руд. МонацитДля обогащения монацита используется 2
- 37. Монацитовый концентратДезинтеграция и мокрое грохочение+ 5 ммв
- 38. Аппаратурное оформлениеДезинтеграцию и мокрое грохочение осуществляют в
- 39. Обогащение руд. ЦирконГравитационное обогащениеПервичное обогащение (выделение всех
- 40. Обогащение руд. ЦирконЭлектростатическая сепарацияОснована на различии в
- 41. Обогащение руд. ЦирконФлотация Флотация – способ
- 42. Флотация Флотация – способ разделения минералов,
- 43. ФлотацияЭффективность флотации определяется:Смачиваемостью частиц минерала водойПродолжительностью контакта
- 44. Обогащение руд. ЦирконФлотация цирконаКоллективная флотация: Собиратель –
- 45. Обогащение руд. ЦирконОбогащение ТЦРВ России и на
- 46. Принципиальная схема переработки ТЦР на ВГГМКПески ТЦРДезинтеграцияГрохочение
- 47. СушкаЭлектростатическая сепарацияПроводящая фракция (рутил, ильменит)Электромагнитная сепарацияМагнитная
- 48. Переработка концентратов минералов редких металловПереработка концентратов подразумевает
- 49. Переработка концентратов минералов редких металловПри выборе технологической
- 50. Физико-химические основы процесса вскрытия: 1). (Li,Na)Al[Si2O6]
- 51. Очистка от примесей: 1). Сa(OH)2 +
- 52. Схема переработки сподуменового концентрата сернокислотым способомДекрипитация, T=1100
- 53. Осаждение, T=90 0CФильтрованиеПромывкаФильтрованиеСушкаLi2CO3H2ONa2CO3
- 54. Переработка концентратов минералов редких металлов. СподуменАппаратураОбжиг и
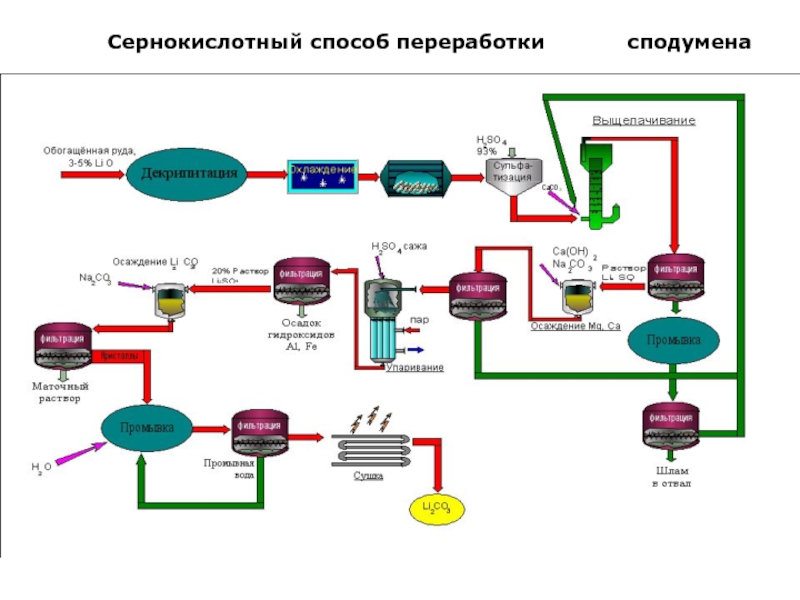
- 55. Сернокислотный способ переработки сподумена
- 56. Сухой карбонат лития в качестве основных примесей
- 57. Следует отметить основные преимущества сернокислотной схемы:Простота операций
- 58. Переработка концентратов минералов редких металлов. АпатитПереработка апатитаКольский
- 59. Переработка апатита. ХимизмВскрытиеCa5(PO4)3F + 10 HNO3 =
- 60. Переработка апатита. ХимизмОтделение кальцияВ HNO3(конц) при -15
- 61. Переработка апатита. ОсобенностиРазложение ведут азотной кислотой (избыток
- 62. фильтратосадокHNO3концАпатитовый концентратH2OSiO2Разложение (50 0С, 1.5 часа)Сгущение, фильтрацияосадокосадок
- 63. сбросрастворКонцентрат РЗЭ (25%TR2O3, 12.5%CaO, 33%P2O5)фильтратосадокна утилизацию фтораосадокПромывкаNH4OHПромывка
- 64. Переработка апатита. Выделение РЗЭПри переработке РЗЭ-концентрата необходимо
- 65. Хлорирование в расплаве. Химизм(Nb,Ta)2O5 +2.5C + 5Cl2
- 66. Переработка концентратов минералов редких металлов. ЛопаритХлорирование в
- 67. Переработка концентратов минералов редких металлов. ЛопаритХлорирование в
- 68. Хлорирование в расплаве. Система конденсацииНа 1-ой ступени
- 69. Хлорирование в расплаве. КонденсацияПоведение примесейВместе с Nb
- 70. Переработка концентратов минералов редких металлов. ЛопаритХлорирование в
- 71. Хлорирование в расплавеПродукты хлорированияПлав, содержащий ~
- 72. Переработка концентратов минералов редких металлов. ЛопаритДохлорирование. Химизм2
- 73. Переработка концентратов минералов редких металлов. ЛопаритРектификация. ОсобенностиТехнологическая
- 74. Ректификация. ОсобенностиВысокая агрессивность газожидкостных потоковЧасть W в
- 75. Хлорная технологияИзвлечение продуктовNb -
- 76. Получение чистых соединенийОсуществляется химическими процессами в водных
- 77. Технический Be(OH)21-й способ2-й способ3-й способ4-й способВодный раствор
- 78. Производство редких металловИспользуют пирометаллургические и электрохимические методы.
- 79. Производство редких металлов. МеталлотермияМеталлотермияМеталлотермические процессы – это
- 80. Производство редких металлов. МеталлотермияМеталлотермия. Основные терминыМеталлотермическая шихта
- 81. Производство редких металлов. МеталлотермияМеталлотермия. Основные терминыСплавообразующие добавки
- 82. Производство редких металлов. МеталлотермияМеталлотермия. Требования к флюсамНе
- 83. Производство редких металлов. МеталлотермияМеталлотермия. Термодинамика процессаПротекание металлотермического
- 84. Производство редких металлов. МеталлотермияМеталлотермия. Закономерности кинетикиМеталлотермические процессы
- 85. Производство редких металлов. МеталлотермияМеталлотермия. Выбор восстановителяОпределение Gр-ции=f(T)Сравнение
- 86. Производство редких металлов. МеталлотермияМеталлотермия. Классификация1. По форме
- 87. Производство редких металлов. МеталлотермияМеталлотермия. Классификация2. По типу
- 88. Производство редких металлов. МеталлотермияПолучение металла в виде
- 89. Производство редких металлов. МеталлотермияПолучение металла в виде
- 90. Производство редких металлов. МеталлотермияПолучение металла в виде
- 91. Производство редких металлов. МеталлотермияВозможные причины образования «губки»Недостаточный
- 92. Производство редких металлов. МеталлотермияПолучение металла в виде
- 93. Производство редких металлов. МеталлотермияПолучение металла в дисперсном
- 94. Производство редких металлов. МеталлотермияСлучаи образования дисперсного металлаЕсли
- 95. Производство редких металлов. МеталлотермияСлучаи образования дисперсного металлаПри
- 96. Производство редких металлов. Металлотермия. Рубидий и цезий Исторически
- 97. Производство редких металлов. Металлотермия. Рубидий и цезий 1-
- 98. Производство редких металлов. ЭлектролизЭлектролиз Электролизом называется
- 99. Производство редких металлов. ЭлектролизПреимущества электрохимического восстановленияПродукты восстановления
- 100. Производство редких металлов. ЭлектролизЭлектролизБольшинство редких металлов (в
- 101. Производство редких металлов. ЭлектролизЭлектролизЭлектрохимические свойства на границе
- 102. Производство редких металлов. ЭлектролизЭлектролизСумму равновесных потенциалов анода
- 103. Производство редких металлов. ЭлектролизПоляризацияПри электролизе расплавов катодный
- 104. Производство редких металлов. ЭлектролизПредельная плотность тока:где D
- 105. Производство редких металлов. ЭлектролизЭлектролизВ технологии наиболее часто
- 106. Производство редких металлов. ЭлектролизЭлектролиз. Выход по токуПричины
- 107. Производство редких металлов. Электролиз. ЛитийЭлектролиз расплавленных солей
- 108. Электрохимические основы процесса:Катод: Li+ + e- →
- 109. Для получения наиболее чистого продукта следует:очистить электролит
- 110. Токовая нагрузка 16-18 кА Производительность ванны 25
- 111. Состав лития, полученного электролизом Производство редких металлов. Электролиз. Литий
- 112. Рафинирование редких металлов. ВанадийМетоды рафинированияиодидное рафинированиевакуумная дуговая
- 113. Рафинирование редких металлов. ВанадийЭлектронно-лучевая плавка (ЭЛП)Характеристики плавки:Остаточное
- 114. Рафинирование редких металлов. ВанадийЭлектронно-лучевая плавкаМетод ЭЛП не
- 115. Рафинирование редких металлов. ВанадийЭлектронно-лучевая плавкаДостоинстваВысокая чистота металла
- 116. Рафинирование редких металлов. ВанадийЭлектролитическое рафинированиеЭлектролиты – солевые
- 117. Рафинирование редких металлов. ВанадийЭлектролитическое рафинирование процесс ведут
- 118. Рафинирование редких металлов. ВанадийЭлектролитическое рафинированиеДостоинстваВысокая чистота металла
- 119. Рафинирование редких металлов. ВанадийНаиболее чистые металлы могут
- 120. Рафинирование редких металлов. ЦирконийИодидное рафинированиеВ технологии циркония
- 121. Рафинирование редких металлов. ЦирконийЙодидное рафинирование Zr. ОсобенностиИод
- 122. Рафинирование редких металлов. ЦирконийИодидное рафинирование. ОсобенностиТемпературу нити
- 123. Рафинирование редких металлов. ЦирконийИодидное рафинирование. АппаратураУстановка для
- 124. Слайд 124
- 125. Электролитический ZrПрессование и спекание (вакуум, 1050 0С)Получение
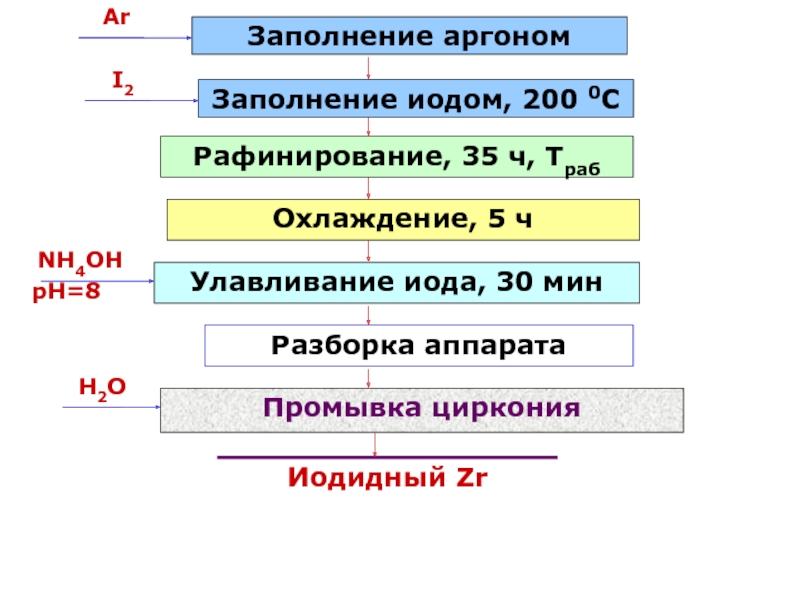
- 126. Заполнение аргономArЗаполнение иодом, 200 0СI2Рафинирование, 35 ч, ТрабОхлаждение, 5 чУлавливание иода, 30 минNH4OHpH=8Разборка аппаратаПромывка цирконияH2OИодидный Zr
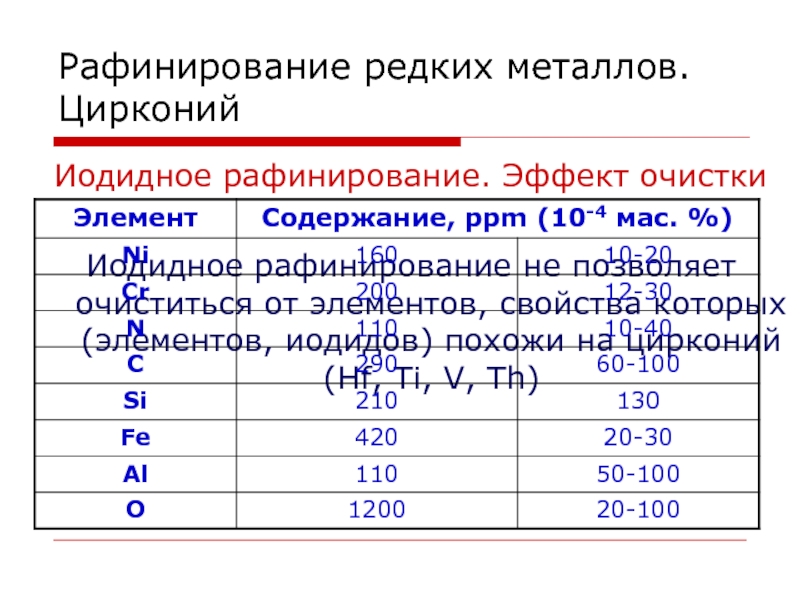
- 127. Рафинирование редких металлов. ЦирконийИодидное рафинирование. Эффект очисткиИодидное
- 128. Скачать презентанцию
Слайды и текст этой презентации
Слайд 2Введение.Определение понятия «редкий элемент»
Редкие элементы – условное название группы химических
элементов относительно новых в плане технического использования.
геохимический критерий отнесения элемента к категории «редкий». Основная граница деления проходит по содержанию элемента в земной коре (включая литосферу, гидросферу и атмосферу) на уровне 0.1 %.Слайд 3Введение.Определение понятия «редкий элемент»
К «редким» не относят барий, хром, никель,
кобальт, бор, хотя их содержание в земной коре имеет порядок
10-2 %. Такое решение мотивировано широким применением этих элементов в промышленности.Еще 9 элементов не считают редкими, как известные с глубокой древности. Это золото, серебро, ртуть, свинец, олово, сурьма, цинк, медь, мышьяк, содержание которых много меньше выбранного предела.
Говоря о редких элементах, подразумевают, как правило, только металлы, т.е. исключают так же благородные газы и галогены.
Слайд 4Введение.Определение понятия «редкий элемент»
Редкие металлы, обладающие общностью физических или химических
свойств, выделены в особые группы:
легких (Li, Rb, Cs, Be);
тугоплавких (Zr,
Hf, V, Nb, Ta, Mo, W, Re);платиноидов (6 элементов);
редкоземельных элементов (иттрий, лантан и 14 лантаноидов)
радиоактивных (U, Th, Pu, Tc и т.д.);
рассеянных (Rb, Ga, In, Tl, Ge, Hf, Se, Te, Re).
Слайд 7Редкие металлы определяют научно-технический прогресс в важнейших областях промышленности:
атомной энергетике,
авиа и ракетостроении,
электровакуумной и полупроводниковой технике,
производстве специальных сталей,
твердых, жаропрочных и антикоррозионных сплавов, нефтехимии,
производстве стекла, керамики и огнеупоров и многих других.
Введение. Основные области применения редких металлов
Слайд 8Введение. Основные области
применения редких металлов
Промышленно-экономический уровень развития современных государств
определяется масштабами потребления не столько чугуна и стали, сколько редких
металлов.Для большинства редких металлов в первые десятилетия ХХI века прогнозируются высокие темпы роста их потребления, опережающие в 3 – 5 раз соответствующие показатели для многих цветных и черных металлов.
Слайд 9Атомная энергетика
Ве –основной материал для изготовления отражателей и замедлителей нейтронов,
Hf – используемый для производства стержней – регуляторов работы ядерного
реактора,Li - применяемый как теплоноситель,
Nb и Zr - материалы для изготовления оболочек ТВЭЛов.
Введение. Основные области
применения редких металлов
Слайд 10Ta – незаменимым материалом в производстве конденсаторов,
Nb широко использующихся
в производстве сверхпроводников,
соединения РЗМ в производстве люминофоров.
Развитие электроники
связано с нарастающим потреблением РМ:Введение. Основные области
применения редких металлов
Слайд 11Одна из секций установки Т-15 Токамак со сверхпроводящими магнитными катушками
на основе Nb3Sn
Слайд 12Соединения лития широко применяют для производства химических источников тока и
аккумуляторов
Введение. Основные области
применения редких металлов
Слайд 13Наибольший объем потребления РМ связан с производством сплавов
Сплавы с
РМ широко используются в авиа и ракетостроении. Сплав «склерон» Al-Li
конструкционный материал для авиации.Более половины производимого бериллия идет на производство сплавов для авиа и ракетостроения типа АВ (локалой) и АМB (Al-Mg-Be)
Никель-кобальтовые сплавы с Nb, W, Mo, Zr, Re обладают уникальной жаропрочностью, жаростойкостью, коррозионной устойчивостью при температуре до 1400 0С (cуперсплавы), они так же незаменимы в авиа и ракетостроении.
Введение. Основные области
применения редких металлов
Слайд 14Универсальная ракетно-космическая транспортная система "Энергия" и космический корабль «Буран» в
полете
Слайд 15Для производство титановых сплавов, востребованных в авиастроении используют лигатуры V-Al
и Mo-Al
Введение. Основные области
применения редких металлов
Слайд 16Звезды сделаны из селенового рубина - стекла, содержащего селен
Введение. Основные
области
применения редких металлов
Керамика на основе диоксида циркония используется для
производства зубных коронок, имплантов и т.д.Слайд 17Сырье для производства редких металлов
Производство РМ было основано в середине
ХХ века.
Рудное сырье, содержащее редкие металлы, как правило, весьма
бедное. Содержание ценного компонента обычно составляет 0.001-0.01 мас. %Дополнительную сложность представляет многокомпонентность состава руды.
Слайд 18Типы сырья
минералы РМ
минералы других элементов
вторичные источники сырья
Сырье для производства редких
металлов
Слайд 19Сподумен LiAl[Si2O6]
алюмосиликат лития
.
Лепидолит KLi2Al[Si4O10](F,OH)2 алюмосиликат из группы литиевых слюд
Сырье
для производства редких металлов
Слайд 20Поллуцит – водный алюмосиликат цезия: (Cs,Na)[AlSi2O6].nH2O
Сырье для производства редких металлов
Слайд 21В процессе выветривания горных пород и минералов литий, рубидий и
цезий вымываются и попадают в соляные рассолы и отложения.
Сырье для
производства редких металловСлайд 23Лопарит (Ln,Na,Ca)2(Ti,Nb)2O6
титанат-ниобат РЗЭ, Na, Ca
Монацит (Ln,Th)PO4
фосфат РЗЭ и Th
Минералы
- комплексные
Сырье для производства редких металлов
Слайд 25Каронотит K2(UO2)2(VO4)2·3H2O
ванадат уранила и калия
Тюямунит
Ca(UO2)2(VO4)2·6H2O ванадат уранила и
кальция
Минералы - комплексные
Сырье для производства редких металлов
Слайд 26Циркон ZrSiO4 ортосиликат циркония
Бадделеит ZrO2оксид циркония
Сырье для производства редких металлов
Слайд 27Колумбит-танталит – ниобат-танталат железа и марганца: (Fe,Mn)[(Nb,TaO3)2]
.
Танталит-колумбит, представляет собой
изоморфный ряд метаниобатов-метатанталатов
Сырье для производства редких металлов
Слайд 31Вторичные источники
Уран – переработка ОЯТ
Та – отработанные конденсаторы
Nb - сверхпроводники
Сырье
для производства редких металлов
Слайд 32Общая ситуация с сырьем РМ в России
Эндогенный характер месторождений
Богатейшие запасы
в неосвоенных районах
Комплексный характер руд
Сырье для производства редких металлов
Слайд 33Оптимальная стратегия : восстановление и развитие уже существующих ГОКов
Ловозерский ГОК
(Кольский полуостров) Nb, Ta, Zr, Hf, РЗМ
Забайкальский ГОК (Читинская область):
Li, Rb, Cs, Be, Ta, NbКовдорский ГОК (Zr)
Малышевское РУ (Be, Li)
ДАЛУР, Хиагда (U)
Качканарский ГОК (V)
Сырье для производства редких металлов
Слайд 34Развитие новых месторождений –Этыкинское (Li, Be, Nb, Ta), Туганское (Zr),
Лукояновское (Zr), Чинейское (Fe, V, Ti)
Переработка техногенных отходов – монацитовый
концентрат (Ln, Th), шлаки оловянных заводов (Nb, Ta).Сырье для производства редких металлов
Слайд 35Обогащение руд
Цель процесса – максимальное обогащение бедной рудной массы по
ценному компоненту для удешевления последующей переработки
Результат процесса – рудный концентрат,
состоящий, в основном, из минерала ценного компонентаСлайд 36Обогащение руд. Монацит
Для обогащения монацита используется 2 метода
Комбинацией гравитационного и
магнитного методов получают концентраты с содержанием монацита более 90 %
В
ходе обогащения монацита необходимо соблюдать меры радиационной безопасностиГравитационный
Электромагнитный
Отделение монацита от пустой породы – полевого шпата, кварца – легких минералов
Монацит слабомагнитен, отделение от минералов железа и немагнитных минералов
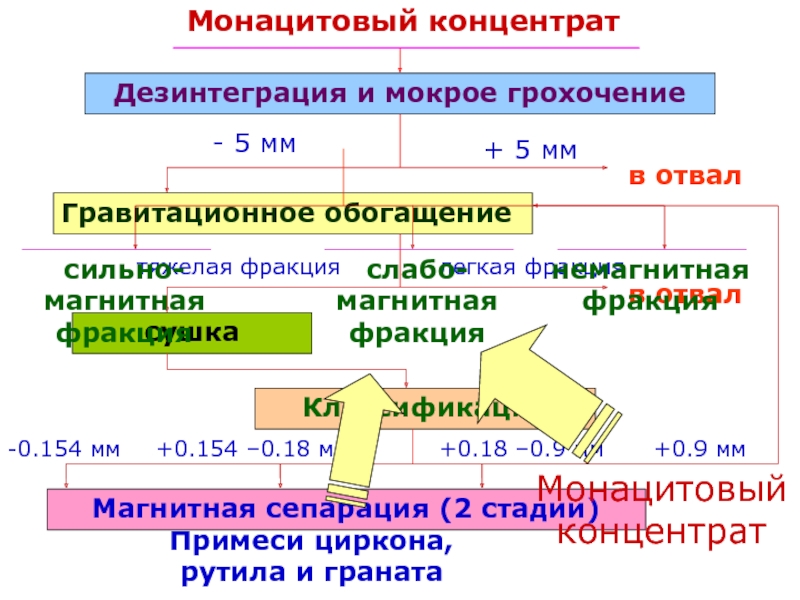
Слайд 37Монацитовый концентрат
Дезинтеграция и мокрое грохочение
+ 5 мм
в отвал
- 5
мм
Гравитационное обогащение
легкая фракция
в отвал
тяжелая фракция
сушка
Классификация
+0.9 мм
-0.154 мм
+0.154 –0.18 мм
+0.18
–0.9 ммМагнитная сепарация (2 стадии)
сильно-магнитная фракция
слабо-магнитная фракция
немагнитная фракция
Монацитовый концентрат
Примеси циркона, рутила и граната
Слайд 38Аппаратурное оформление
Дезинтеграцию и мокрое грохочение осуществляют в одном аппарате –
скруббер-бутаре
Гравитационное обогащение проводят в каскаде гидроциклонов и концентрационных столов
Магнитную сепарацию
ведут на электромагнитных сепараторахОбогащение руд. Монацит
Слайд 39Обогащение руд. Циркон
Гравитационное обогащение
Первичное обогащение (выделение всех тяжелых минералов в
концентрат) осуществляют в конусных сепараторах
На стадии доводки используют винтовые сепараторы
и концентрационные столыЭлектромагнитное обогащение
Применяют высокопроизводительные и высокоградиентные сепараторы
Необходимо максимальное извлечение ценных минералов
Производительность их в 10-20 раз выше, чем у концентрационных столов
Сепарация – сухая
1 – расходная насадка;
2,5,8,9,12 – трубы; 3 – цилиндр;
4 – клин; 6,13,14 – узел регулировки;
7 – рама;
10 – патрубок;
11 – кольцевой желоб;
15 – отсекатель;
16 – отклоняющее кольцо; 17 – регулировочный болт; 18 – конус;
19 – конусное кольцо;
20 – перегородка
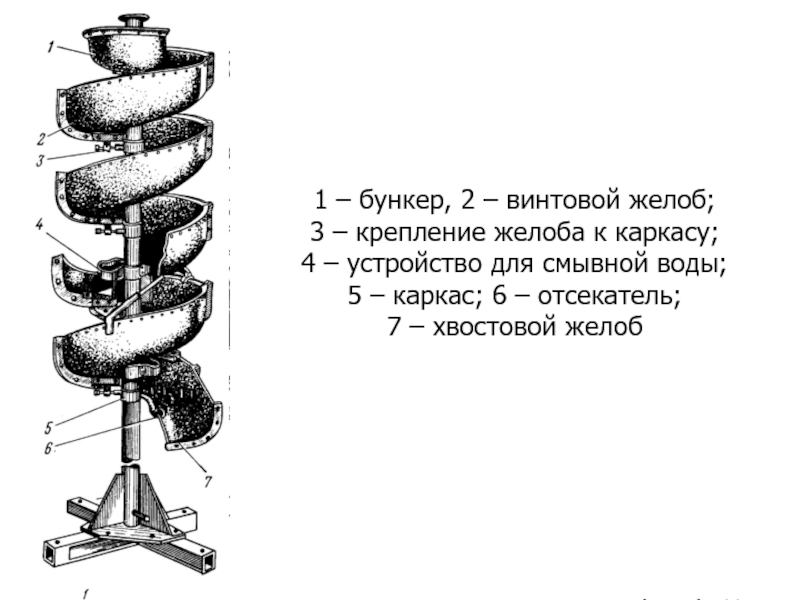
1 – бункер, 2 – винтовой желоб;
3 – крепление желоба к каркасу;
4 – устройство для смывной воды;
5 – каркас; 6 – отсекатель;
7 – хвостовой желоб
Слайд 40Обогащение руд. Циркон
Электростатическая сепарация
Основана на различии в электропроводности материалов
Все минералы
в электростатическом поле поляризуются, а затем притягиваются к вращающемуся электроду
Частицы
непроводящих минералов остаются на электроде, а частицы проводящих — передают свой заряд электроду, заряжаются одноименно с электродом и отталкиваются от него Проводники: магнетит, ильменит, рутил, хромит FeCrO4
Непроводники: циркон, алюмосиликаты (гранат
(Mg,Fe,Mn)3Al2(SiO4)3 , ставролит
Fe(II)Al4[SiO4]4O2(OH)2, дистен Al2O[SiO4],
турмалин
(Na, Ca)(Mg, Fe, Li)3Al6[Si6O18][BO3]3(OH)4),
монацит, кварц
Слайд 41Обогащение руд. Циркон
Флотация
Флотация – способ разделения минералов, основанный
на различии в их смачиваемости
Основные термины:
1. Собиратель –
вещество, способное адсорбироваться на поверхности минерала и придать ей гидрофобные свойства2. Активатор – вещество, активирующее переход ценного минерала во флотационную пульпу
Слайд 42Флотация
Флотация – способ разделения минералов, основанный на различии
в их смачиваемости
Основные термины:
3. Депрессор – вещество, препятствующее
переходу ценного минерала во флотационную пульпу4. Пенообразователь – вещество, благодаря которым на поверхности жидкости образуется пена, удерживающая частицы минералов
Обогащение руд. Циркон
Слайд 43Флотация
Эффективность флотации определяется:
Смачиваемостью частиц минерала водой
Продолжительностью контакта с реагентами
Плотностью пульпы
Температурой
Группы
собирателей:
анионные – органические кислоты, мыла и т.д.
катионные – амины, соли
аминов и т.д.аполярные – минеральные и древесные масла и смолы, не диссоциирующие в воде
Процесс флотации ведут во флотационных машинах
Обогащение руд. Циркон
Слайд 44Обогащение руд. Циркон
Флотация циркона
Коллективная флотация:
Собиратель – аэрированная эмульсия олеиновой
кислоты с керосином (1:1, 1.25 кг/т)
Депрессор пустой породы: Na2SiF6 (400
г/т)pH пульпы = 5.9÷6.4
Селективная флотация:
Депрессор циркона: Na2SiF6 (1.2÷1.9 кг/т)
pH пульпы = 4÷4.2
Доводку ведут на концентрационных столах
Титаноцирконовые россыпи (ТЦР) перерабатывают по коллективно-селективной схеме (Австралия, ЮАР, США)
Слайд 45Обогащение руд. Циркон
Обогащение ТЦР
В России и на Украине флотацию для
переработки ТЦР не применяют
На I этапе осуществляют дезинтеграцию в скрубберах,
обесшламливание в гидроциклонах и струйных зумпфах и гравитационное обогащение на многоярусных конусных сепараторахДля получения индивидуальных концентратов используют сочетание электростатической и электромагнитной сепарации
Последовательность операций доводки зависит от состава концентрата
Если в коллективном концентрате преобладают
рутил, циркон и алюмосиликаты, то процесс
доводки начинается обычно с передела
электростатической сепарации
Если же в коллективном концентрате преобладает
магнитный ильменит, то технологический процесс
начинается с передела магнитной сепарации
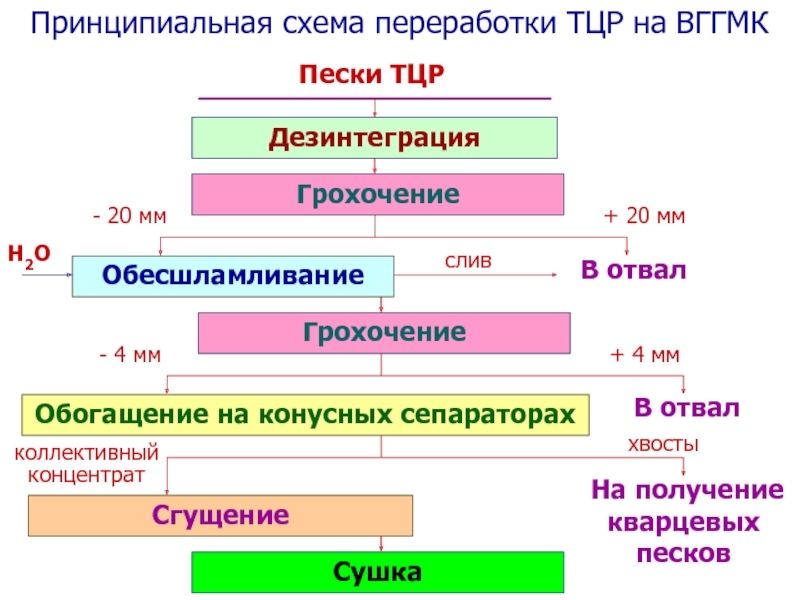
Слайд 46Принципиальная схема переработки ТЦР на ВГГМК
Пески ТЦР
Дезинтеграция
Грохочение
В отвал
+ 20
мм
- 20 мм
Обесшламливание
H2O
cлив
Грохочение
В отвал
+ 4 мм
- 4 мм
Обогащение на
конусных сепараторах На получение
кварцевых
песков
хвосты
коллективный
концентрат
Сгущение
Сушка
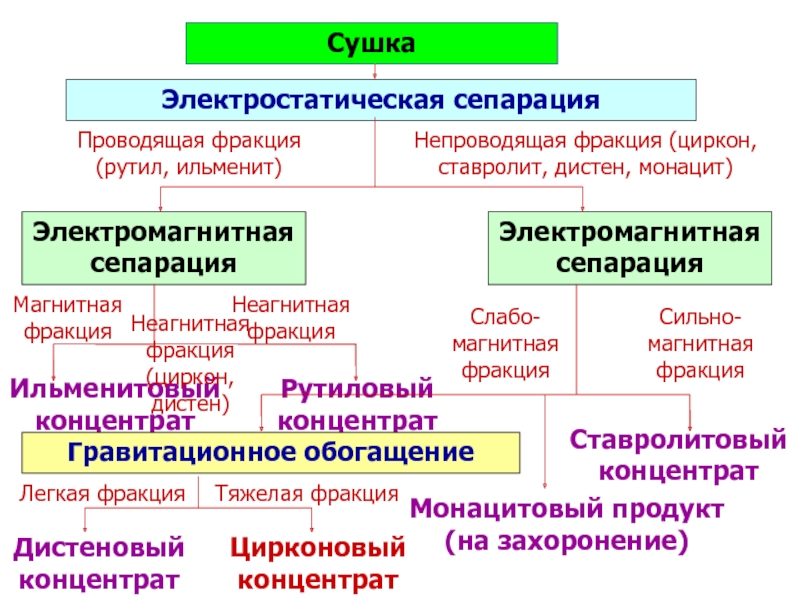
Слайд 47Сушка
Электростатическая сепарация
Проводящая фракция
(рутил, ильменит)
Электромагнитная сепарация
Магнитная
фракция
Неагнитная
фракция
Ильменитовый
концентрат
Рутиловый
концентрат
Непроводящая фракция (циркон, ставролит, дистен,
монацит)
Электромагнитная сепарация
Сильно-магнитная
фракция
Неагнитная
фракция
(циркон, дистен)
Монацитовый продукт (на захоронение)
Ставролитовый
концентрат
Слабо-магнитная
фракция
Гравитационное обогащение
Легкая фракция
Тяжелая фракция
Дистеновый
концентрат
Цирконовый
концентрат
Слайд 48Переработка концентратов минералов редких металлов
Переработка концентратов подразумевает отделение извлекаемого металла
от основной массы сопровождающих элементов и концентрирование его в растворе
или осадке.Цель достигается пирометаллургическими процессами (спекание, обжиг, возгонка) или гидрометаллургическими методами (обработка кислотами, растворами щелочей и т.п.)
Слайд 49Переработка концентратов минералов редких металлов
При выборе технологической схемы переработки концентратов
необходимо учитывать:
Степень извлечения основного компонента
Возможность комплексной переработки концентрата
Безотходность (минимум отходов)
Экологичность
Использование
недефицитных реагентовЭнергоемкость
Простоту аппаратурного оформления
Численность обслуживающего персонала
Слайд 50
Физико-химические основы процесса вскрытия:
1). (Li,Na)Al[Si2O6] Li(Na)[AlSi2O6]
α-сподумен 1100 0С β-сподумен
2).
Li[AlSi2O6] + H2SO4 → Li2SO4 + H[AlSi2O6]Переработка концентратов минералов редких металлов. Сподумен
Выщелачивание:
1). СaCO3 + H2SO4 → CaSO4 + H2O + CO2
2). 5СaCO3 + 2 H[AlSi2O6] → 4CaSiO3 + Ca(AlO2)2
+H2O + 5CO2
3) Li2SO4 (тв) → Li2SO4 (р-р)
Слайд 51
Очистка от примесей:
1). Сa(OH)2 + MgSO4 → CaSO4
+ Mg(OH)2
pH = 12-14
2). Na2CO3 +
CaSO4 → CaCO3 + Na2SO43). 4NaAlO2 + 2H2SO4 + 4H2O → 4 Al(OH)3 + 2Na2SO4
4NaFeO2 + 2H2SO4 + 4H2O → 4 Fe(OH)3 +2Na2SO4
pH = 7
4). Li2SO4 + Na2СO3 → Li2CO3 + Na2SO4
Переработка концентратов минералов редких металлов. Сподумен
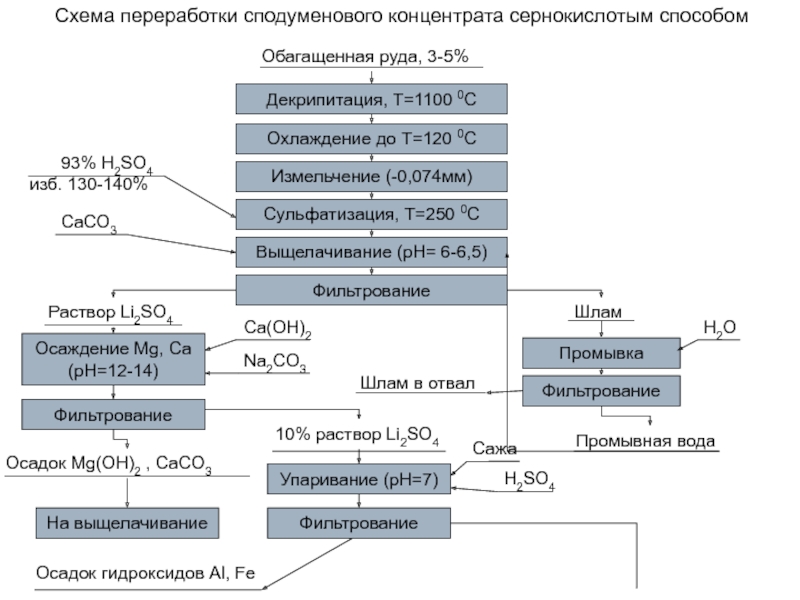
Слайд 52Схема переработки сподуменового концентрата сернокислотым способом
Декрипитация, T=1100 0C
Охлаждение до T=120
0C
Измельчение (-0,074мм)
Сульфатизация, Т=250 0С
Выщелачивание (pH= 6-6,5)
Фильтрование
Осаждение Mg, Ca (pH=12-14)
Фильтрование
На
выщелачиваниеУпаривание (pH=7)
Фильтрование
Фильтрование
Промывка
93% H2SO4
CaCO3
Ca(OH)2
Na2CO3
H2O
Сажа
H2SO4
изб. 130-140%
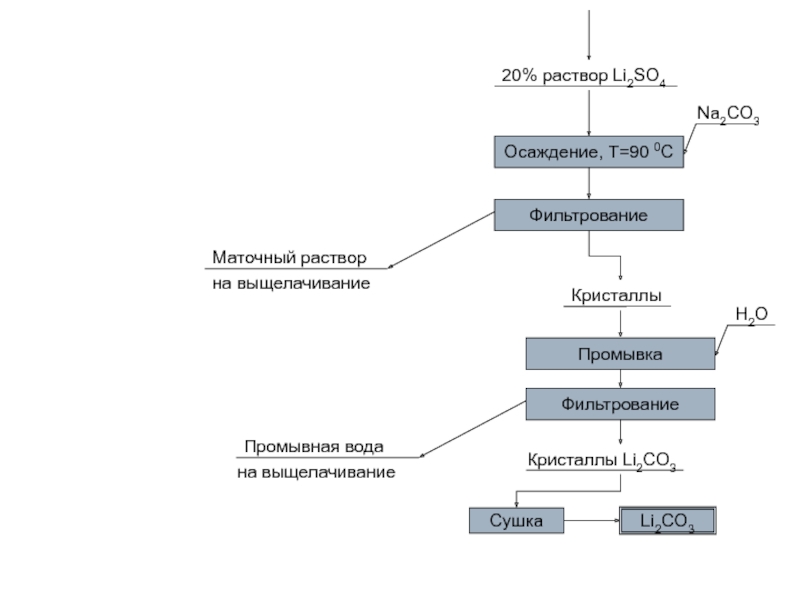
Слайд 54Переработка концентратов минералов редких металлов. Сподумен
Аппаратура
Обжиг и сульфатизацию проводят в
вращающихся трубчатых печах
Выщелачивание сульфатной массы ведут
в реакторе при непрерывном
перемешивании сжатым воздухом Операции фильтрации и промывку осуществляют на барабанном вакуум-фильтре
Карбонат лития отделяют от маточного раствора центрфугированием
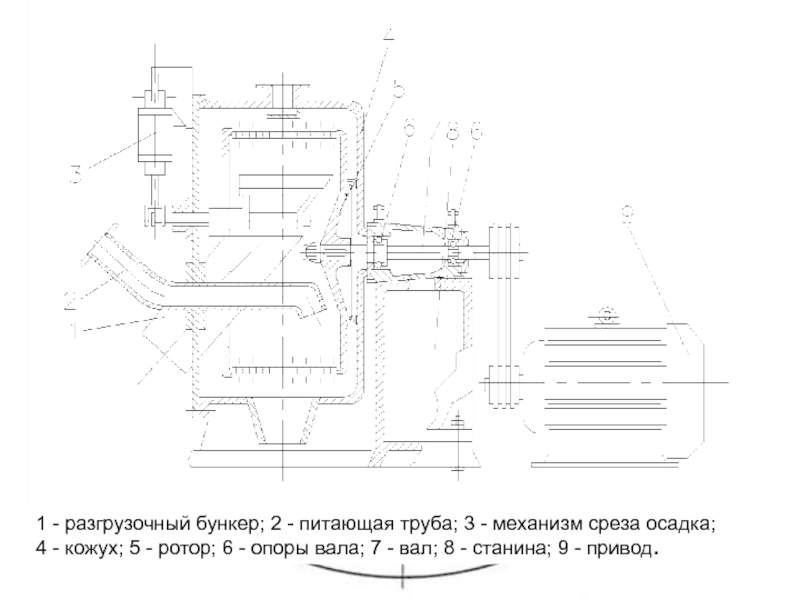
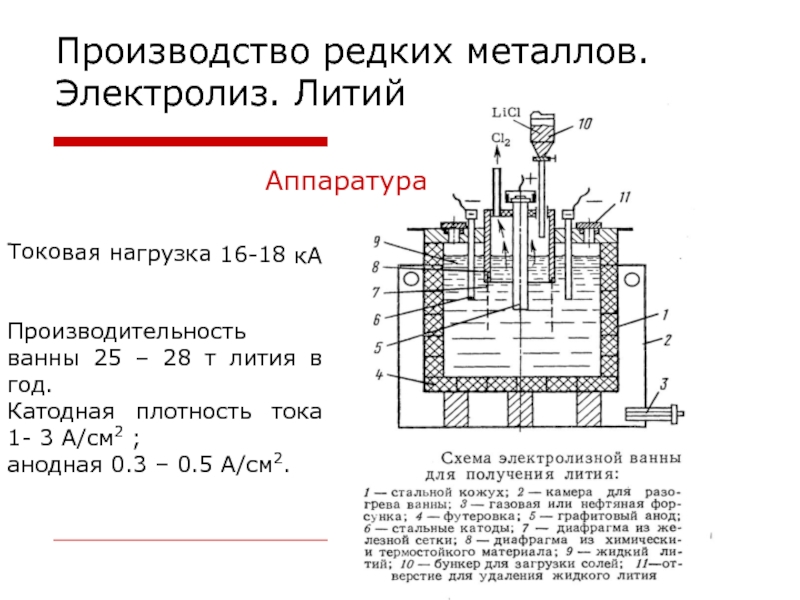
1 - разгрузочный бункер; 2 - питающая труба; 3 - механизм среза осадка;
4 - кожух; 5 - ротор; 6 - опоры вала; 7 - вал; 8 - станина; 9 - привод.
Слайд 56Сухой карбонат лития в качестве основных примесей содержит 0.18 %
(Na2O+K2O), 0.04 % CaO, 0.35 % SO42-.
При переработке концентратов
степень извлечения лития составляет 85 –90 %, в целом, за счет потерь при обогащении, выход лития в карбонат из руды составляет 50 – 55 %.Прямая переработка руды, содержащей 1.5 % Li2O дает до 80 % извлечения лития.
Переработка концентратов минералов редких металлов. Сподумен
Слайд 57 Следует отметить основные преимущества сернокислотной схемы:
Простота операций (нет смешения твердых
реагентов);
Использование нелетучей серной кислоты;
Отсутствие длительных энергоемких операций.
Современные направления совершенствования этой
технологии предполагают использование автоклавного вскрытия серной кислотой при температуре до 400 0С без предварительной декрипитацииПереработка концентратов минералов редких металлов. Сподумен
Слайд 58Переработка концентратов минералов редких металлов. Апатит
Переработка апатита
Кольский апатитовый концентрат –
перспективное и уникальное сырье для комплексной переработки, содержит соединения стронция,
редкоземельных элементов и фтораПри применяемом сернокислотном методе РЗМ не извлекают
Перспективна азотнокислая схема переработки апатита
В конце 80-х гг прошлого века эта схема прошла промышленные испытания и была рекомендована к внедрению на ОАО «Апатит»
В настоящее время азотнокислая схема переработки апатита внедряется на ОАО «Акрон»
Слайд 59Переработка апатита. Химизм
Вскрытие
Ca5(PO4)3F + 10 HNO3 = 5Ca(NO3)2 + 3H3PO4
+ HF
Ln(Sr)PO4 + 3HNO3 = Ln(NO3)3+Sr(NO3)2 + H3PO4
Связывание НF (вводят
кремнегель)4 HF + SiO2 = SiF4 + 2 H2О
6 HF + SiO2 = H2SiF6 + 2 H20
SiF4 + 2 HF = H2SiF6
Выделение стронция
В HNO3(конц) Sr(NO3)2 высаливается из раствора уже при 50-55 0C
Переработка концентратов минералов редких металлов. Апатит
Слайд 60Переработка апатита. Химизм
Отделение кальция
В HNO3(конц) при -15 0C около 90
% Сa(NO3)2 «вымораживается» в твердую фазу из растворов в виде
Сa(NO3)2∙4H2OВыделение фтора (вводят соду)
Na2CO3 + H2SiF6 = Na2SiF6 + H2O + CO2
Осаждение РЗЭ (нейтрализуют аммиаком)
При pH=1.5-2 РЗЭ и оставшийся кальций выпадают в виде фосфатов
Переработка концентратов минералов редких металлов. Апатит
Слайд 61Переработка апатита. Особенности
Разложение ведут азотной кислотой (избыток - 10-15 %)
в течение 1.5 ч при 50-55 0С в каскаде реакторов
из нержавеющей стали«Вымораживание» Сa(NO3)2 осуществляют в 3 ступени при 10, 0 и -15 0C
Na2SiF6 осаждают при 20-40 0C в присут-ствии поверхностно-активных веществ (ПАВ) за 60-90 минут
Степень вскрытия апатита – 99 %
Переработка концентратов минералов редких металлов. Апатит
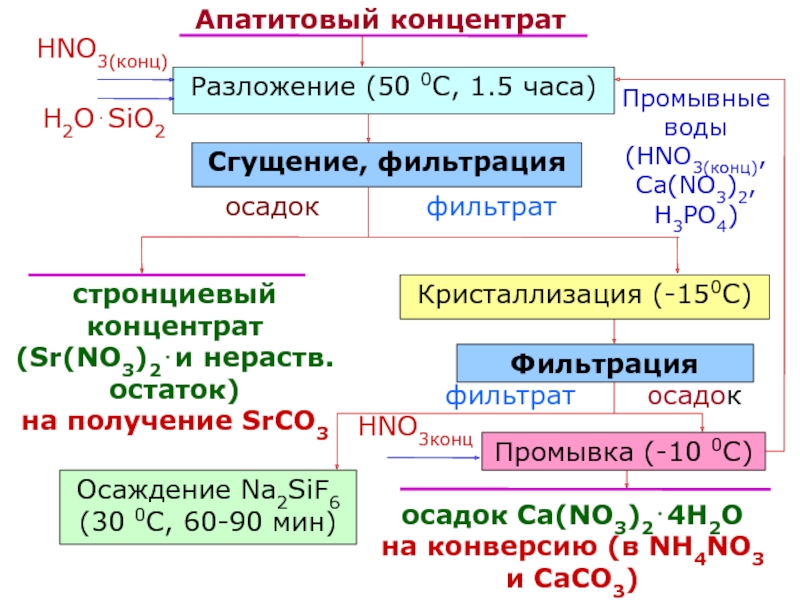
Слайд 62фильтрат
осадок
HNO3конц
Апатитовый концентрат
H2OSiO2
Разложение (50 0С, 1.5 часа)
Сгущение, фильтрация
осадок
осадок Ca(NO3)24H2O
на конверсию
(в NH4NO3 и СaCO3)
фильтрат
Фильтрация
Кристаллизация (-150С)
Осаждение Na2SiF6
(30 0C, 60-90 мин)
стронциевый
концентрат (Sr(NO3)2и нераств. остаток) на получение SrCO3
Промывка (-10 0С)
Промывные воды (HNO3(конц), Сa(NO3)2, H3PO4)
HNO3(конц)
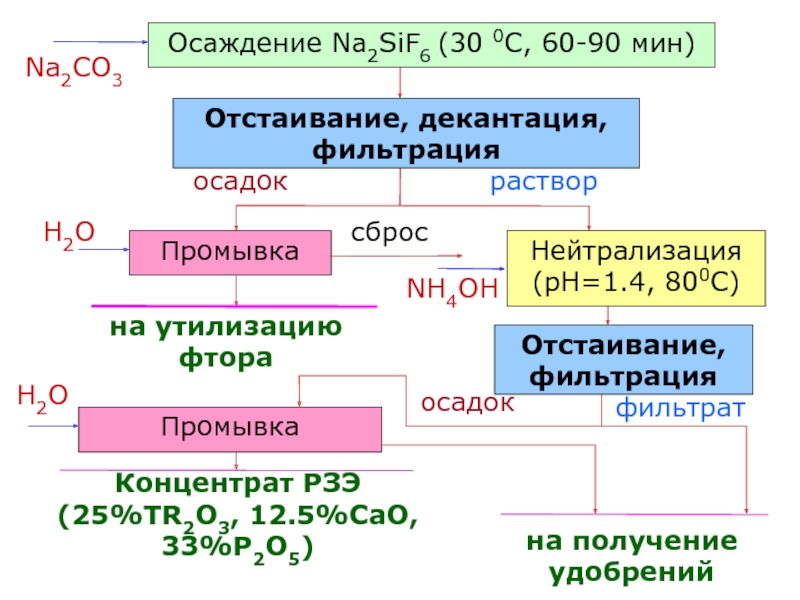
Слайд 63сброс
раствор
Концентрат РЗЭ
(25%TR2O3, 12.5%CaO, 33%P2O5)
фильтрат
осадок
на утилизацию фтора
осадок
Промывка
NH4OH
Промывка
Отстаивание, декантация, фильтрация
Осаждение Na2SiF6
(30 0C, 60-90 мин)
Нейтрализация (pH=1.4, 800C)
на получение удобрений
Отстаивание, фильтрация
H2O
Na2CO3
H2O
Слайд 64Переработка апатита. Выделение РЗЭ
При переработке РЗЭ-концентрата необходимо обеспечить возврат фосфора
в основную технологическую схему
В концентрате содержится около 3% от
содержащегося в апатите фосфораКонцентрат растворяют в азотной кислоте, а затем осаждают оксалаты РЗЭ щавелевой кислотой
Из концентрата щелочью осаждают гидроксиды РЗЭ, переводя фософор в Na3PO4
Так как апатит является главным образом источником фосфора, то технология выделения РЗЭ должна рассматриваться как побочный процесс
Переработка концентратов минералов редких металлов. Апатит
Слайд 65Хлорирование в расплаве. Химизм
(Nb,Ta)2O5 +2.5C + 5Cl2 = =2(Nb,Ta)Cl5 +
2.5 CO2
(Nb,Ta)2O5 +1.5C + 3Cl2 = =2(Nb,Ta)OCl3 + 1.5
CO2 Продукты хлорирования
Газы CO,CO2, HCl, Cl2, COCl2
Низкокипящие жидкие при нормальных условиях хлориды TiCl4, SiCl4 CСl4
Низкокипящие твердые хлориды AlCl3, FeCl3, NbCl5, TaCl5, NbOCl3
Высококипящие твердые хлориды CaCl2, MgCl2, FeCl2, NaCl, KCl, MnCl2, LnCl3
Солевая ванна
Переработка концентратов минералов редких металлов. Лопарит
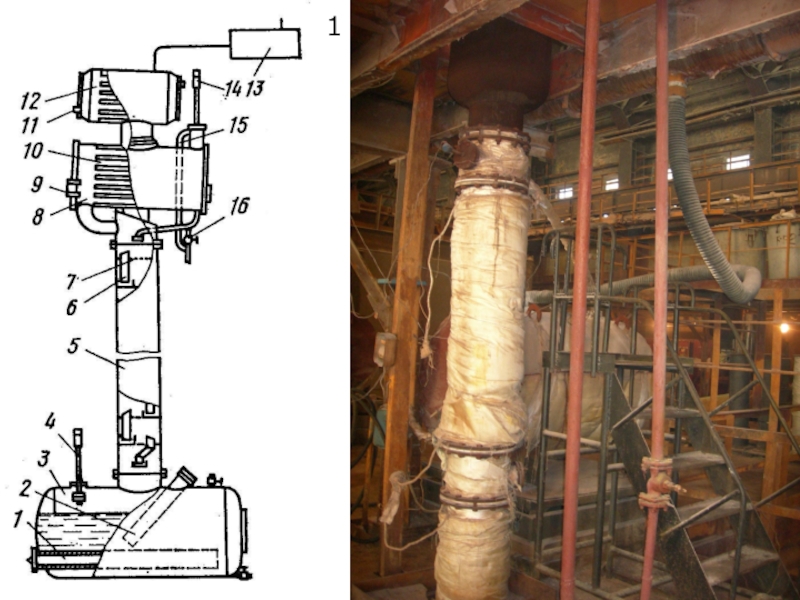
Слайд 66Переработка концентратов минералов редких металлов. Лопарит
Хлорирование в расплаве. Аппаратура
Хлоратор представляет
собой шахту прямоугольного сечения с высотой уровня расплава около 3
метровНагрев хлоратора ведут специальными графитовыми нагревателями смонтированными в стенах аппарата
Температура процесса 850 –900 0С
Содержание концентрата в расплаве около 1.5 % , углерода около 5 %
1 - бункер для концентрата и кокса;
2 - шнековый питатель;
3 - хлоратор;
4 - фурмы;
5 - расплав;
6 - миксер;
7 - летка;
8 - охлаждаемый газоход;
9 - патрубок вывода ПГС.
Хлоратор
Слайд 67Переработка концентратов минералов редких металлов. Лопарит
Хлорирование в расплаве. Очистка от
Fe и Al
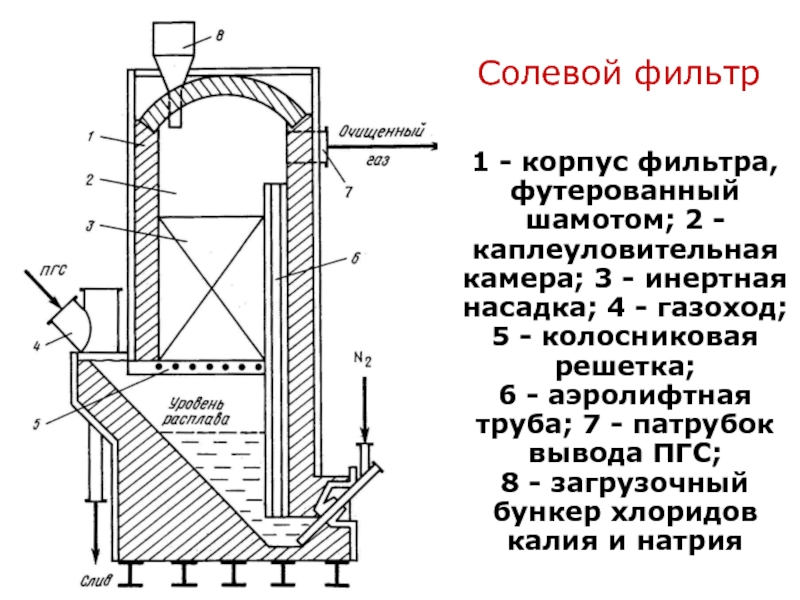
Парогазовую смесь (ПГС) подвергают очистке от хлоридов Fe
и Al на солевых фильтрах Принцип солевой очистки состоит в образовании устойчивых соединений при взаимодействии пара хлоридов железа и алюминия с NaCl
Прочность комплексных соединений на основе Fe и Al значительно выше, чем у Nb, Ta и Ti
Солевой фильтр
1 - корпус фильтра, футерованный шамотом; 2 - каплеуловительная камера; 3 - инертная насадка; 4 - газоход; 5 - колосниковая решетка;
6 - аэролифтная труба; 7 - патрубок вывода ПГС;
8 - загрузочный бункер хлоридов калия и натрия
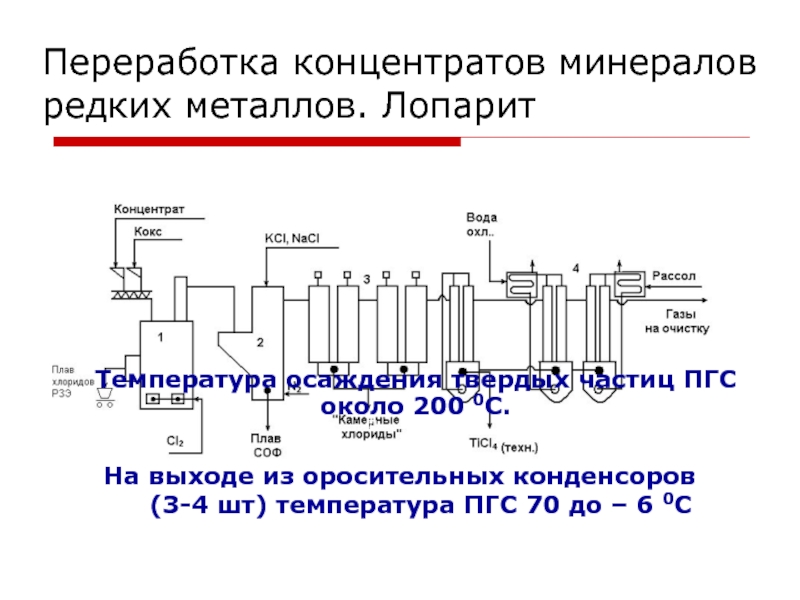
Слайд 68Хлорирование в расплаве. Система конденсации
На 1-ой ступени в специальных камерных
конденсаторах осаждают основную часть твердых хлоридов тантала и ниобия
Окончательное улавливание
твердых хлоридов происходит в оросительных конденсорах (орошение ведут TiCl4), здесь же конденсируются и пары TiCl4 Температура осаждения твердых частиц ПГС около 200 0С.
На выходе из оросительных конденсоров (3-4 шт) температура ПГС 70 до – 6 0С
Переработка концентратов минералов редких металлов. Лопарит
Слайд 69Хлорирование в расплаве. Конденсация
Поведение примесей
Вместе с Nb и Ta в
камерных конденсаторах осаждается вольфрам в виде оксихлорида WOCl4 («камерные» хлориды).
Пульпа
после оросительных конденсаторов, содержащая примеси TaCl5, NbOCl3 и в меньшей степени, WOCl4, SiCl4 и VOCl3 поступает на участок вакуумной выпарки Переработка концентратов минералов редких металлов. Лопарит
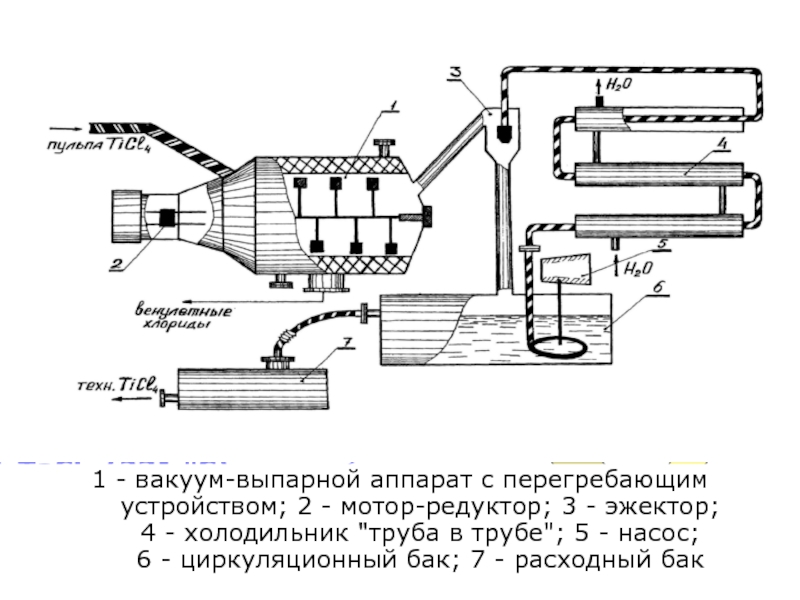
Слайд 70Переработка концентратов минералов редких металлов. Лопарит
Хлорирование в расплаве. Вакуум-выпарка
Цель операции
– получение технического TiCl4(tкип=136 0С)
Смесь хлоридов
Вакуум-выпарка
TiCl4 (136
0C)
VOCl3(127 0C)
SiCl4 (58 0C)
SnCl4 (112 0C)на ректификацию
на дохлорирование
NbCl5 (248 0C)
NbOCl3(400 0C)
TaCl5 (231 0C)
WOCl4 (204 0C)
«венулетные»
хлориды
1 - вакуум-выпарной аппарат с перегребающим устройством; 2 - мотор-редуктор; 3 - эжектор;
4 - холодильник "труба в трубе"; 5 - насос;
6 - циркуляционный бак; 7 - расходный бак
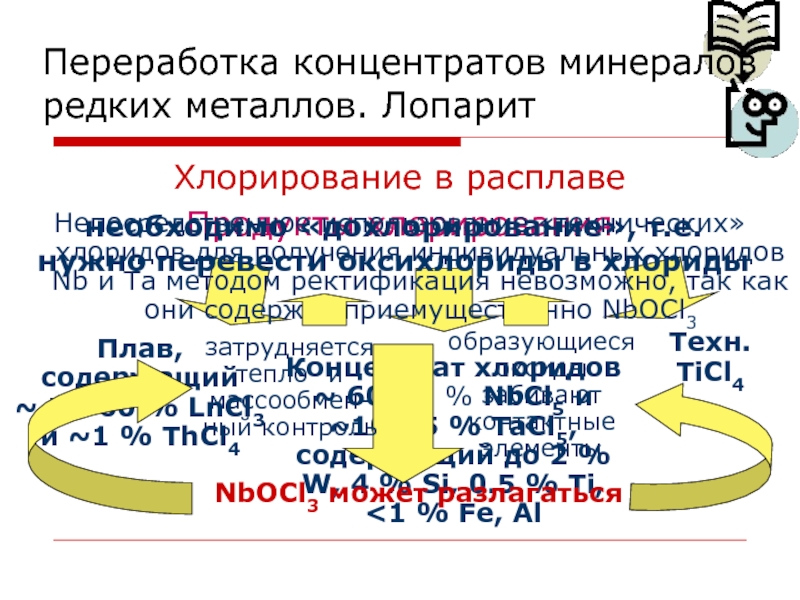
Слайд 71Хлорирование в расплаве
Продукты хлорирования
Плав, содержащий
~ 50-60 % LnCl3 и
~1 % ThCl4
Техн.
TiCl4
Концентрат хлоридов ~ 60-75 %
NbCl5 и ~10-15 % TaCl5, содержащий до 2 % W, 4 % Si, 0.5 % Ti, <1 % Fe, Al Непосредственное использование «технических» хлоридов для получения индивидуальных хлоридов Nb и Ta методом ректификация невозможно, так как они содержат приемущественно NbOCl3
NbOCl3 может разлагаться
затрудняется тепло- и массообмен-ный контроль
образующиеся оксиды забивают контактные элементы
необходимо «дохлорирование», т.е. нужно перевести оксихлориды в хлориды
Переработка концентратов минералов редких металлов. Лопарит
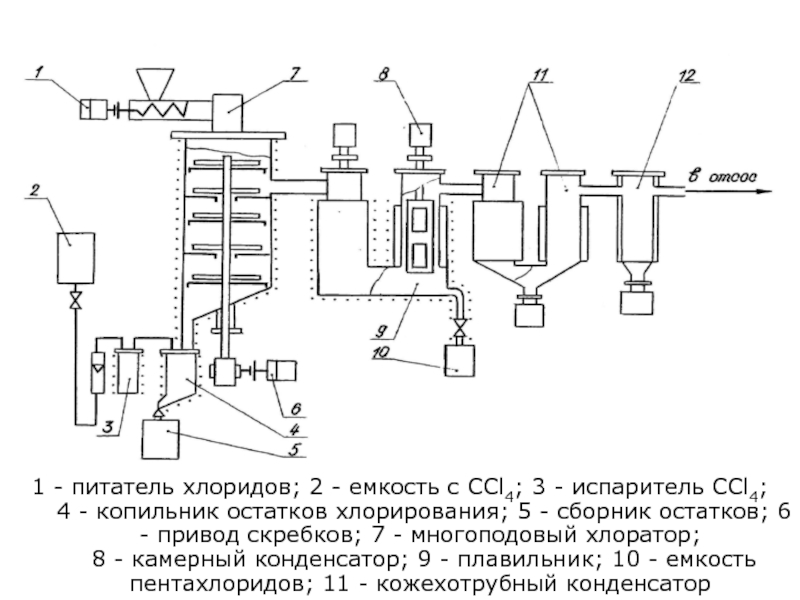
Слайд 72Переработка концентратов минералов редких металлов. Лопарит
Дохлорирование. Химизм
2 MOCl3 + CCl4
= 2 MCl5 + CO2 (M=Nb,Ta)
2 WOCl4 + CCl4
= 2 WCl6 + CO2Tкип (WCl6) =348 0С
200-220 0С
330-360 0С
360-400 0С
WCl6, LnCl3, FeCl3 (304 0C)
Ta(Nb)Cl5, WCl6, AlCl3 (180 0C), SiCl4, TiCl4
на ректификацию
1 - питатель хлоридов; 2 - емкость с ССl4; 3 - испаритель ССl4;
4 - копильник остатков хлорирования; 5 - сборник остатков; 6 - привод скребков; 7 - многоподовый хлоратор;
8 - камерный конденсатор; 9 - плавильник; 10 - емкость пентахлоридов; 11 - кожехотрубный конденсатор
Слайд 73Переработка концентратов минералов редких металлов. Лопарит
Ректификация. Особенности
Технологическая схема включает 3
основных операции:
предварительная ректификация для отделения примесей от суммы TaCl5 и
NbCl5 ;ректификационное получение чистого NbCl5 с отделением концентрата TaCl5;
ректификацию концентрата TaCl5 с получением чистого танталового продукта.
1 - основной электронагреватель куба;
2 - пусковой электронагреватель; 3 - куб колонны; 4 -датчик монометра;
5 - ректификационная колонна; 6 - переливной патрубок; 7 - дырчатая тарелка; 8 - конденсатор;
9 - смотровое окно;
10 - труба конденсатора;
11 - штуцер подачи воды;
12 - холодильник паров теплоносителя; 13 -система регулироания давления;
14 - датчик манометра;
15 - линия сброса давления в колонне; 16 - кран отбора дистиллята
Слайд 74Ректификация. Особенности
Высокая агрессивность газожидкостных потоков
Часть W в виде WCl5 (tкип=2860С)
сопровождает тантал
Аппаратура из спецсталей на основе Cr и Ni,
эмалирование конструкцийДля очистке от W, а также от примесей
Fe, Si, Ti и Al полученные вещества
направляют на химико-сорбционную очистку
Суть ее: пропускание хлоридов через слой активной насадки, состоящей из смеси латунной стружки и угля БАУ
сорбция Ti и Si активированным углем
переходе высших летучих хлоридов Fe и W в менее летучие низшие
Переработка концентратов минералов редких металлов. Лопарит
Слайд 75Хлорная технология
Извлечение продуктов
Nb - 93 – 94
%
Ta - 86 – 88 %
Ti -
96.5 – 97 % РЗМ - 95.5 – 96 %
Переработка концентратов минералов редких металлов. Лопарит
Слайд 76Получение чистых соединений
Осуществляется химическими процессами в водных растворах (экстракция, ионный
обмен, осаждение, кристаллизация и др.).
Для дополнительной очистки могут применяться
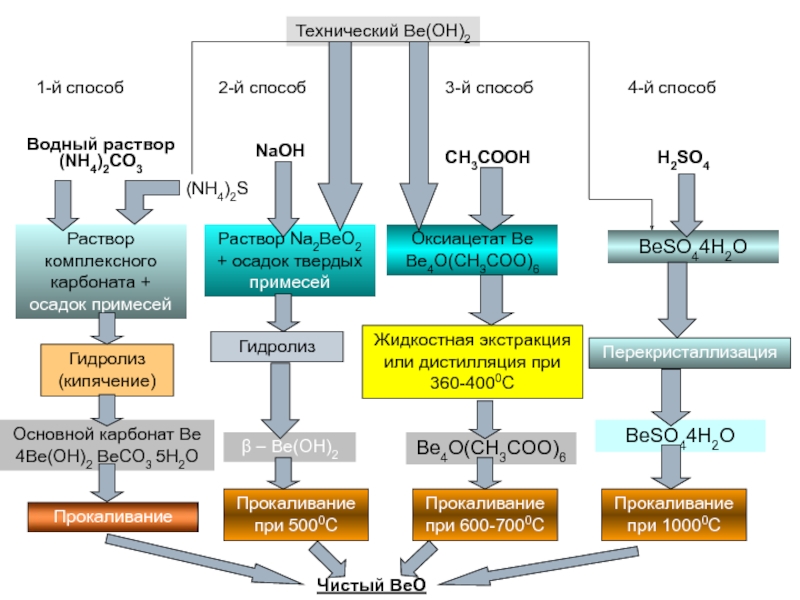
и высокотемпературные процессы – возгонка хлоридов, ректификация галогенидов и т.п. Слайд 77Технический Be(OH)2
1-й способ
2-й способ
3-й способ
4-й способ
Водный раствор
(NH4)2CO3
NaOH
CH3COOH
H2SO4
(NH4)2S
Раствор комплексного карбоната
+ осадок примесей
Гидролиз (кипячение)
Основной карбонат Be 4Be(OH)2 BeCO3 5H2O
Раствор Na2BeO2
+ осадок твердых примесейГидролиз
β – Be(OH)2
Прокаливание при 5000С
Оксиацетат Be Be4O(CH3COO)6
Жидкостная экстракция или дистилляция при 360-4000С
Be4O(CH3COO)6
Прокаливание при 600-7000С
Прокаливание при 10000С
Перекристаллизация
BeSO44H2O
BeSO44H2O
Чистый BeO
Слайд 78Производство редких металлов
Используют пирометаллургические и электрохимические методы.
Часть металлов может
быть получена из водных растворов цементацией (обменной реакцией) или электролизом
(Ga, In, Tl, Ge, Re)Некоторые металлы осстановлением оксидов или солей H2, CO, C при повышенных температурах (W,Mo,Re,Ge,Nb,Ta)
Восстановлением из оксидов или солей металлами (металлотермия) или электролизом в расплавах солей получают Li, Rb, Cs, Be, РЗМ, Th, U, Zr, Hf, V, Ta, Nb.
Слайд 79Производство редких металлов. Металлотермия
Металлотермия
Металлотермические процессы – это процессы восстановления металлов
из их соединений более активными металлами, протекающие с выделением тепла
Химизм:
где
MnXm – восстанавливаемое соединение;M’ – металл-восстановитель
M’nXp – образующееся соединение (шлак)
p/n MnXm + mM’ = pM + m/nM’nXp + Q
Слайд 80Производство редких металлов. Металлотермия
Металлотермия. Основные термины
Металлотермическая шихта –
смесь MnXm
и M’, загружаемая в аппарат для проведения процесса
Термиты (тепловыделяющие добавки)
– соединения, способные взаимодействовать с большим экзотермическим эффектом, чем при протекании основной реакцииБалластные (теплопоглощающие) добавки – вещества, реагирующие с металлом-восстановителем с меньшим тепловым эффектом, чем основной сырьевой компонент
Слайд 81Производство редких металлов. Металлотермия
Металлотермия. Основные термины
Сплавообразующие добавки –
металлические частицы
или соединения металлов (восстанавливаемые в металлотермическом процессе до металла), служащие
для образования сплава с основным продуктом металлотермической реакцииФлюсы – соединения, предназначенные для изменения температуры плавления, вязкости и других свойств шлака
Слайд 82Производство редких металлов. Металлотермия
Металлотермия. Требования к флюсам
Не должны взаимодействовать с
восстановителем и получаемым по реакции металлом
Должен снижать температуру кристаллизации и
вязкость шлакаБыть негигроскопичным, устойчивым соединением, обладающим низким давлением паров при температуре процесса
Химическая чистота
Низкая стоимость
Слайд 83Производство редких металлов. Металлотермия
Металлотермия. Термодинамика процесса
Протекание металлотермического процесса возможно при:
GTр-ции
GTр-ции= m/n·GTM’X + p ·GTM – - p/n·GTMX - m
·GTM’Восстановление металлов при GTр-ции>0 невозможно без создания специальных условий, сдвигающих равновесие металлотермических реакций
Проведение
процесса
в вакууме
Химическое связывание продукта с помощью специальных добавок к шихте
Слайд 84Производство редких металлов. Металлотермия
Металлотермия. Закономерности кинетики
Металлотермические процессы относятся к твердофазным
реакциям
Скорость металлотермии при одном и том же тепловом эффекте зависит
от температурыВ отличии от других ТФР при металлотермии происходит изменение агрегатного состояния компонентов шихты
Определить скорости реакции – сложно
Для реакций металлотермического
восстановления характерны закономерности,
описанные для твердофазных реакций
Повышение температуры вызывает увеличение
скорости реакции, что ведет к росту скорости
выделения тепла (самоускорение реакции)
Лимитирующая стадия может меняться
Слайд 85Производство редких металлов. Металлотермия
Металлотермия. Выбор восстановителя
Определение Gр-ции=f(T)
Сравнение температур получаемых продуктов
между собой, а также их температур плавления и кипения
Технико-экономические
показатели (простота организации процесса, стоимость, доступность, чистота, устойчивость в атмосфере)Слайд 86Производство редких металлов. Металлотермия
Металлотермия. Классификация
1. По форме организации процесса
Металлотермические процессы
Печные
Внепечные
Тепла,
выделяющегося во время реакции, недостаточно для получения продуктов в жидком
состоянии и полноты расслаивания фазВыделяющегося тепла достаточно для расплавления и
перегрева продуктов плавки
Четкой границы нет, так как тепловой баланс даже одного и того же процесса зависит от масштаба, состава шихты и т.п.
Слайд 87Производство редких металлов. Металлотермия
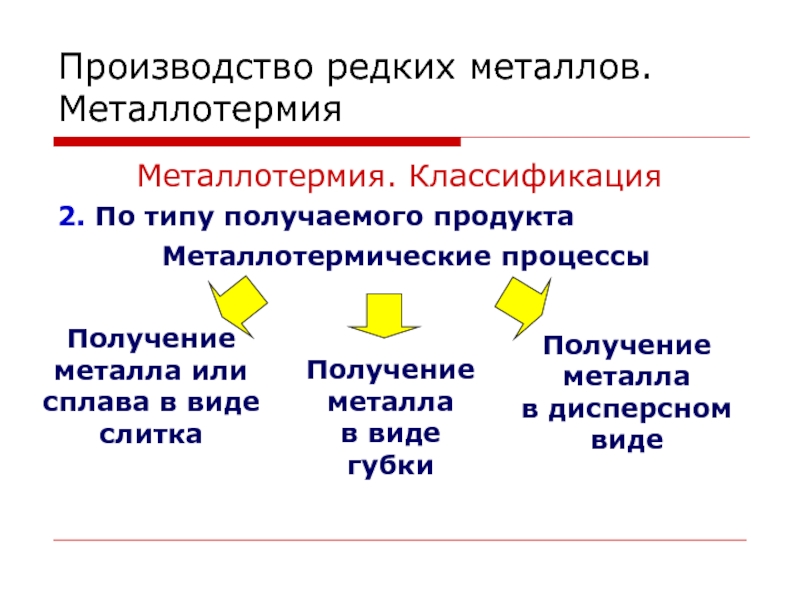
Металлотермия. Классификация
2. По типу получаемого продукта
Металлотермические процессы
Получение
металла или сплава в виде слитка
Получение металла
в виде
губки
Получение
металла
в дисперсном видеСлайд 88Производство редких металлов. Металлотермия
Получение металла в виде слитка
Получение металла в
виде слитков наиболее желательно с точки зрения технологии
Позволяет сократить цикл
металлотермииПозволяет упростить отделение металла (или сплава) от шлака
Позволяет уменьшить загрязнение продукта примесями
Условие формирования слитка:
выделяющегося в ходе реакции и подводимого извне тепла достаточно для расплавления и расслаивания металлической и шлаковой фаз при интенсивном теплоотводе (через стенки, дно тигля и с поверхности расплава)
Слайд 89Производство редких металлов. Металлотермия
Получение металла в виде слитка
Основные стадии
Предварительный нагрев
шихты или инициирование металлотермической операции
Горение шихты
Расслаивание металлической и шлаковой
фазОхлаждение и кристаллизация продуктов восстановительной плавки
Слайд 90Производство редких металлов. Металлотермия
Получение металла в виде губки
Металлическая «губка» -
это конгломерат скоалесцировавшихся и закристаллизовавшихся струй металла
Губка образуется в результате
горения металлотермической смеси, когда скорость кристаллизации продуктов взаимодействия превышает скорости расслаивания металлической и шлаковой фазСлайд 91Производство редких металлов. Металлотермия
Возможные причины образования «губки»
Недостаточный для компенсации тепловых
потерь экзотермический эффект реакции (например, при малом масштабе плавки)
При высокой
летучести шлака, интенсивное испарение которого препятствует расслаиваниюПри раздельном вводе компонентов в реакционную зону из-за длительности процесса и рассеяния тепла
Метод Кролля – магниетермия хлоридов титана, циркония и гафния
Метод Хантера – натриетермия хлорида титана
Слайд 92Производство редких металлов. Металлотермия
Получение металла в виде губки
Основные стадии
Плавление и
сублимация исходных реагентов
Формирование частиц губки
Спекание частиц губки
Слив шлака из реактора
Слайд 93Производство редких металлов. Металлотермия
Получение металла в дисперсном виде
Металлы получают в
дисперсном виде при условиях, когда исключается возможность не только коалесценции
капель, но и агрегирования кристаллических частиц между собой с образованием губки и дендритовМеталлы в дисперсном виде – это порошки, гранулы, корольки
Наихудший вариант
Слайд 94Производство редких металлов. Металлотермия
Случаи образования дисперсного металла
Если тепловой эффект металлотермической
реакции недостаточен для полного расплавления металла, шлака или обоих продуктов
При
больших тепловых потерях, которые имеют место в маломасштабных процессах или при получении тугоплавких продуктовЕсли образуются легколетучие продукты, отводящие тепло при испарении и ухудшающие условия расслаивания
Слайд 95Производство редких металлов. Металлотермия
Случаи образования дисперсного металла
При обратимых металлотермических реакциях,
протекающих в сторону образования исходных компонентов при температурах, близких к
температуре кристаллизации продуктовЕсли процесс сильно растянут во времени из-за диффузионных затруднений при использовании крупных частиц шихты
В случае замедленного расслоения шлака и металла из-за близости их плотностей
Слайд 96Производство редких металлов. Металлотермия. Рубидий и цезий
Исторически первый способ разработан
Н.Н. Бекетовым:
4RbOH + 2 Al Rb2O.Al2O3 + 2Rb +
2H2Извлечение составляло около 30 % от теоретического.
В промышленности используют способ Гакшпиля:
2MeCl + Ca 2Me + CaCl2 ; -ΔНRb=15 кДж/моль
-ΔНCs=20 кДж/моль
Извлечение 90 – 95 %
Перспективный способ:
2Me2CrO4 + 2.5 Zr 4 Me + Cr2O3 + 2.5 ZrO2
при 1000 0С извлечение 90-96 %.
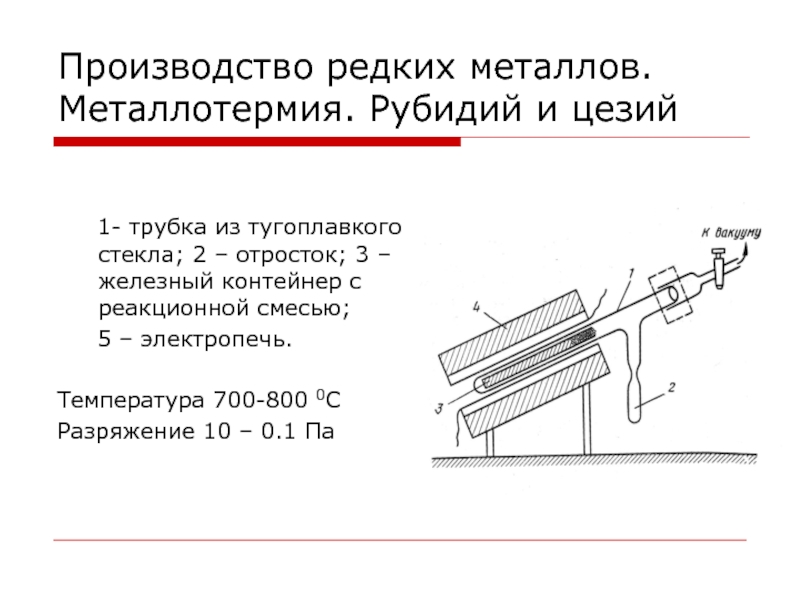
Слайд 97Производство редких металлов. Металлотермия. Рубидий и цезий
1- трубка из тугоплавкого
стекла; 2 – отросток; 3 – железный контейнер с реакционной
смесью;5 – электропечь.
Температура 700-800 0С
Разряжение 10 – 0.1 Па
Слайд 98Производство редких металлов. Электролиз
Электролиз
Электролизом называется разложение электролитов постоянным
электрическим током, которое сопровождается образованием новых веществ
Анод
Окисление
Анионы отдают электроны
Катод
Восстановление
Катионы принимают
электроныСлайд 99Производство редких металлов. Электролиз
Преимущества электрохимического восстановления
Продукты восстановления не загрязняются остатками
металла-восстановителя и примесями, присутствующими в нем
Возможна очистка от более электроположительных
примесей, содержащихся в исходном сырьеДешевизна и доступность восстановителя
Возможность получения катодных осадков с заданными свойствами (размеров и т.п.)
Слайд 100Производство редких металлов. Электролиз
Электролиз
Большинство редких металлов (в том числе Zr,
Hf, Th, РЗМ) характеризуется отрицательным значением стандартного электродного потенциала
Получение их
из водных растворов невозможно из-за выделения водородаЭлектролиз ведут из расплавленных солей (галогенидов, оксигалогенидов)
Слайд 101Производство редких металлов. Электролиз
Электролиз
Электрохимические свойства на границе электрод/раствор(расплав) характеризуют величиной
электродного потенциала
Если электродная реакция протекает в равновесных условиях (при токе,
стремящимся к нулю), скачок потенциала между электродом и электролитом называют равновесным потенциаломЗначение равновесного потенциала определяется уравнением Нернста
Потенциал
катода/катиона
Потенциал
анода/аниона
Слайд 102Производство редких металлов. Электролиз
Электролиз
Сумму равновесных потенциалов анода и катода называют
напряжением разложения
Для осуществления электролиза в равновесных условиях необходимо приложить внешнее
напряжение на бесконечно малую величину, превышающее напряжение разложенияПри прохождении тока через систему происходит сдвиг потенциалов электродов от их равновесного значения
ПОЛЯРИЗАЦИЯ – следствие замедленности одного или нескольких процессов, протекающих на электроде при прохождении тока
Слайд 103Производство редких металлов. Электролиз
Поляризация
При электролизе расплавов катодный процесс чаще всего
контролируется диффузией (массопереносом), а анодный – диффузией и фазообразованием
Увеличение плотности
тока приводит к явлению наступления предельного тока, когда все подходящие ионы разряжаются и их концентрация в приэлектродном слое равна нулю Концентрационная
Электрохимическая
Химическая
Лимитирующая стадия
Диффузия разряжающихся ионов к поверхности электрода
Электрохимическая реакция
Побочная химическая (фазовая)
реакция
Слайд 104Производство редких металлов. Электролиз
Предельная плотность тока:
где D – коэффициент диффузии;
n – число электронов;
С0 –
концентрация ионов в объеме; - толщина диффузионного слоя
Концентрационная поляризация:
Слайд 105Производство редких металлов. Электролиз
Электролиз
В технологии наиболее часто применяют гальваностатический режим
электролиза
Катодную плотность тока выбирают так, чтобы она была выше предельных
плотностей примесей (особенно электропо-ложительных) и ниже предельной плотности тока выделения основного металлаВыбор анодной плотности тока обусловлен исключением явления анодного эффекта
Явление резкого увеличения напряжения на ванне и уменьшения силы тока, вызванное образованием газовой пленки, отделяющей анод от электролита
Слайд 106Производство редких металлов. Электролиз
Электролиз. Выход по току
Причины снижения выхода по
току:
Совместный разряд ионов-примесей
Растворение выделяющихся на катоде металлов в расплаве
Образование соединений
в низшей степени окисления на катоде и в высшей – на анодеИспарение металлов
Побочные реакции продуктов электролиза с материалом электролизера и между собой
Потери при обработке катодных осадков
Выход по току – коэффициент полезного использования тока, равный отношению количества электричеств, теоретически и практически расходуемого на единицу массы катодного продукта
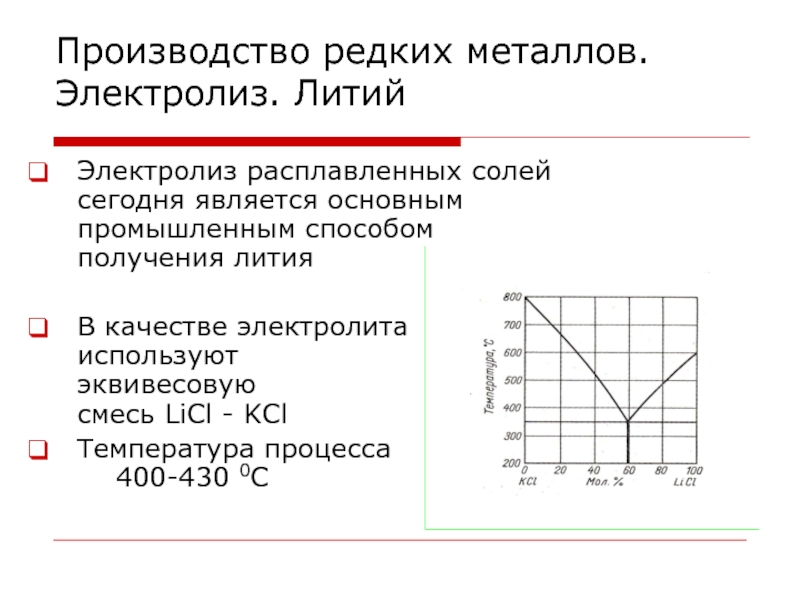
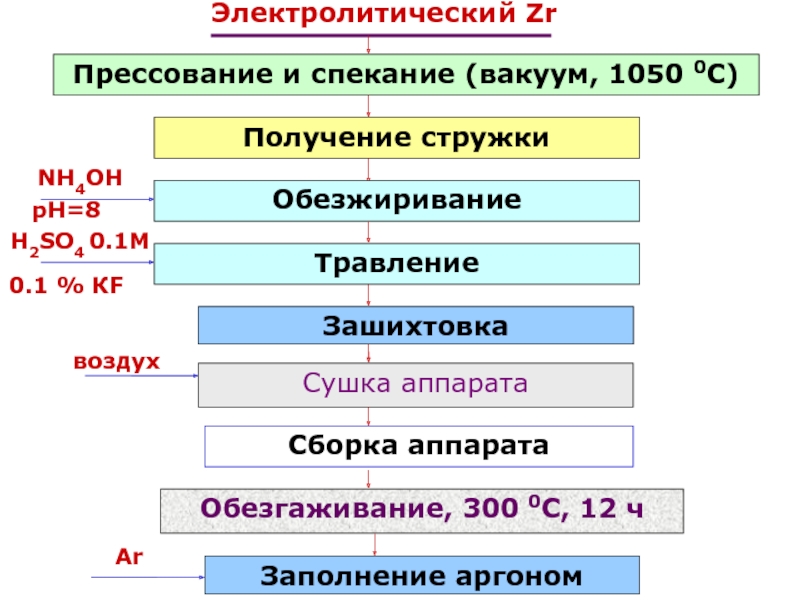
Слайд 107Производство редких металлов. Электролиз. Литий
Электролиз расплавленных солей сегодня является основным
промышленным способом получения лития
В качестве электролита
используют
эквивесовую
смесь LiCl - KCl
Температура
процесса
400-430 0ССлайд 108 Электрохимические основы процесса:
Катод: Li+ + e- → Li φLi+/Li=
-3.78 В;φК+/К= -3.89 В;
Анод: 2Cl- - 2e → Cl2
Возможен
совместный разряд ионов лития и калия :при снижении концентрации хлорида лития в электролите за счет сдвига потенциала выделения при концентрационной поляризации;
за счет сближения потенциалов выделения при сплавообразовании.
Производство редких металлов. Электролиз. Литий
Слайд 109 Для получения наиболее чистого продукта следует:
очистить электролит от солей кальция,
магния и натрия;
постоянно регулировать содержание расходуемого в процессе электролиза
хлорида лития в электролите, сохраняя его на уровне 57- 59 мол. %;поддерживать оптимальную величину катодной плотности тока;
поддерживать в заданном интервале температуру ванны.
Производство редких металлов. Электролиз. Литий
Слайд 110
Токовая нагрузка 16-18 кА
Производительность ванны 25 – 28 т
лития в год.
Катодная плотность тока 1- 3 А/см2 ;
анодная
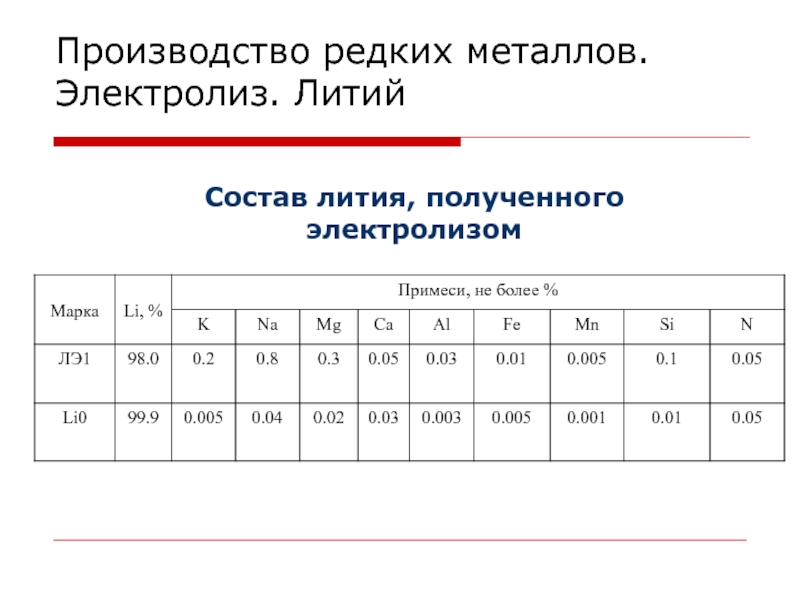
0.3 – 0.5 А/см2.Производство редких металлов. Электролиз. Литий
Аппаратура
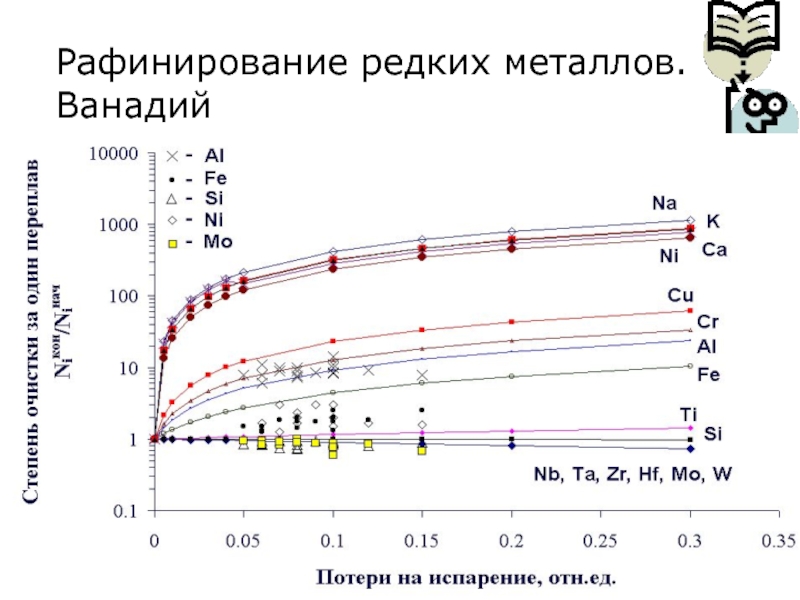
Слайд 112Рафинирование редких металлов. Ванадий
Методы рафинирования
иодидное рафинирование
вакуумная дуговая плавка
электронно-лучевая плавка
электролитическое рафинирование
черновой
ванадий реагирует с иодом при 800-900 0С с образованием паров
VI2, которые затем разлагаются на ванадиевой проволоке с образованием чистого металла при 1300-1400 0Сневозможно очистить ванадий от хрома, циркония и других элементов, иодиды которых имеют близкие к VI2 термические свойства
За счет использования вакуума удается защитить металл от загрязнения вследствие взаимодействия его с атмосферой и обеспечить удаление газовых примесей и низкокипящих металлов
из-за относительно высокого давления в зоне дуги и короткого времени пребывания металла в расплавленном состоянии не удается удалить примеси с относительно высокими Tкип
более низкие давления и медленные скорости плавки
вытеснил электронно-дуговую плавку
Слайд 113Рафинирование редких металлов. Ванадий
Электронно-лучевая плавка (ЭЛП)
Характеристики плавки:
Остаточное давление 10-4-10-5 мм
рт. ст.
Скорость плавки 1.5 – 2.0 кг/час
Потери на испарение 8
– 12 %Мощность пушки 40-50 кВт
Для повышения эффективности очистки используют многократный переплав
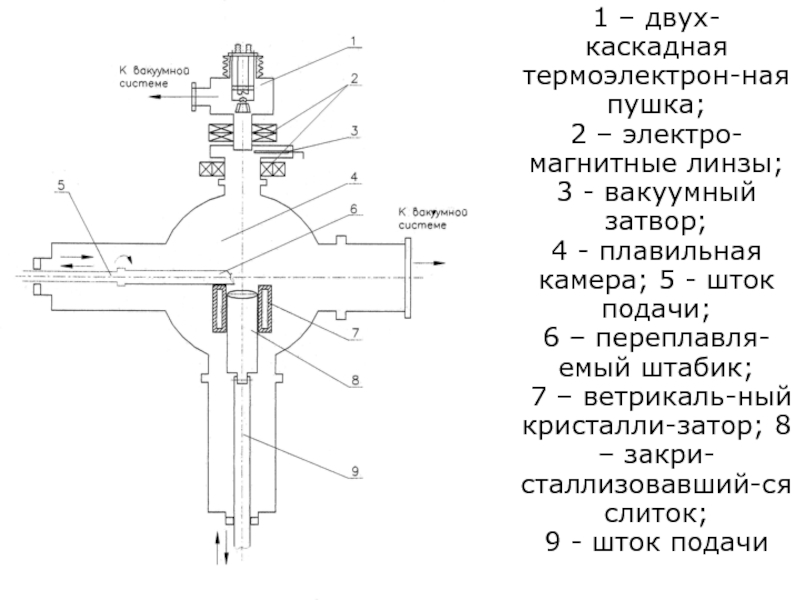
1 – двух-каскадная термоэлектрон-ная пушка;
2 – электро-магнитные линзы;
3 - вакуумный затвор;
4 - плавильная камера; 5 - шток подачи;
6 – переплавля-емый штабик;
7 – ветрикаль-ный кристалли-затор; 8 – закри-сталлизовавший-ся слиток;
9 - шток подачи
Слайд 114Рафинирование редких металлов. Ванадий
Электронно-лучевая плавка
Метод ЭЛП не позволяет очистить металлы
от примесей с большей температурой плавления и образующих тугоплавкие соединения
Для
снижения концентрации кислорода в расплав вводят алюминийСлайд 115Рафинирование редких металлов. Ванадий
Электронно-лучевая плавка
Достоинства
Высокая чистота металла
Продуктом является компактный
металл
Отсутствие невозвратимых потерь
Недостатки
Очень высокий расход э/энергии
Невозможность очистки от некоторых примесей
Сложность
аппаратурыНизкая производительность
Слайд 116Рафинирование редких металлов. Ванадий
Электролитическое рафинирование
Электролиты – солевые расплавы
При анодном растворении
в расплав вместе с металлом переходят электроположительные ионы, которые при
катодном осаждении остаются в электролитеДвухстадийным электрорафинированием получен ванадий с суммарным содержанием примесей 0.0121 мас. %, а трехстадийным - 9.310-3 мас. %
Хлоридные
(Na-K)Clэкв
2 VCl3 + V = 3 VCl2
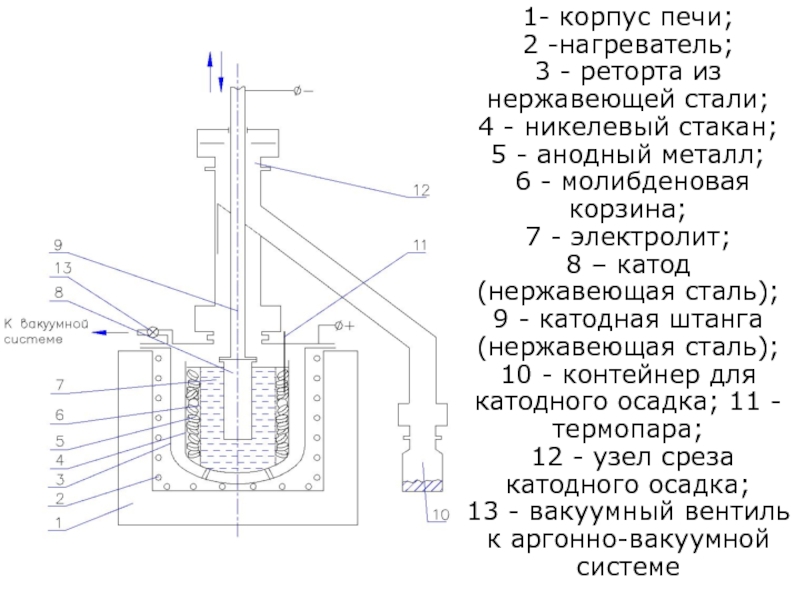
Слайд 117Рафинирование редких металлов. Ванадий
Электролитическое рафинирование
процесс ведут в электролизерах с
центральным катодом выполненным из молибдена или нержавеющей стали
черновой металл помещают
в специальные анодные корзины из молдибдена вдоль стенок никелевого тигля - контейнера в аппарате поддерживают инертную атмосферу очищенного аргона
1- корпус печи;
2 -нагреватель;
3 - реторта из нержавеющей стали;
4 - никелевый стакан;
5 - анодный металл;
6 - молибденовая корзина;
7 - электролит;
8 – катод (нержавеющая сталь);
9 - катодная штанга (нержавеющая сталь); 10 - контейнер для катодного осадка; 11 - термопара;
12 - узел среза катодного осадка;
13 - вакуумный вентиль к аргонно-вакуумной системе
Слайд 118Рафинирование редких металлов. Ванадий
Электролитическое рафинирование
Достоинства
Высокая чистота металла
Высокая производительность
Относительно низкий
расход э/энергии
Недостатки
Большие потери (10-20 %)
Невозможность очистки от некоторых примесей
Сложность аппаратуры
Получают
порошки металловСлайд 119Рафинирование редких металлов. Ванадий
Наиболее чистые металлы могут быть получены при
комбинировании методов электронно-лучевого переплава и электролитического рафинирования
Слайд 120Рафинирование редких металлов. Цирконий
Иодидное рафинирование
В технологии циркония наибольшее распространение для
рафинирования металла транспортными реакциями получило йодидное рафинирование
Химизм:
Zr + I2
ZrI4 Zr + I2Зона 2 – циркониевая нить (проволока) длиной 26-28 м с диаметром 1.5-2.5 мм
Слайд 121Рафинирование редких металлов. Цирконий
Йодидное рафинирование Zr. Особенности
Иод реагирует с цирконием
при температурах выше 150 0С
При температурах выше 300 0С возможно
образование низших иодидов, имеющих более низкие температуры кипенияПри температурах ниже 1500 0С и высоком давлении тетраиодида возможно образование на нити «черного тумана» низших иодидов циркония
Скорость переноса циркония снижается
Цирконий не образуется, а происходит разъедание нити
Слайд 122Рафинирование редких металлов. Цирконий
Иодидное рафинирование. Особенности
Температуру нити контролируют, пропуская через
нее заданный электрический ток
С течением времени толщина нити увеличивается, что
приводит к уменьшению сопротивления и возрастанию электрического токаПроцесс ведут по заранее рассчитанным вольтамперным характеристикам, исходя из зависимости: I·U3=const
Для сохранения условий (температуры) необходимо уменьшить напряжение на нити
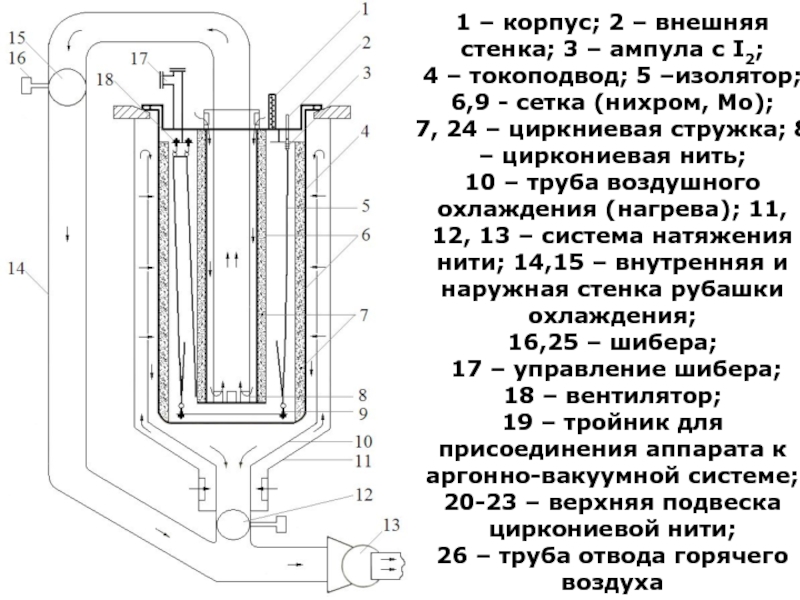
Слайд 123Рафинирование редких металлов. Цирконий
Иодидное рафинирование. Аппаратура
Установка для иодидного рафинирования состоит
из цилиндрического реактора из жаропрочной спецстали с герметичной крышкой, вакуумной
системы, электрической и контрольно-измерительной аппаратуры1 – корпус; 2 – внешняя стенка; 3 – ампула с I2;
4 – токоподвод; 5 –изолятор; 6,9 - сетка (нихром, Mo);
7, 24 – циркниевая стружка; 8 – циркониевая нить;
10 – труба воздушного охлаждения (нагрева); 11, 12, 13 – система натяжения нити; 14,15 – внутренняя и наружная стенка рубашки охлаждения;
16,25 – шибера;
17 – управление шибера;
18 – вентилятор;
19 – тройник для присоединения аппарата к аргонно-вакуумной системе; 20-23 – верхняя подвеска циркониевой нити;
26 – труба отвода горячего воздуха

















![ТРЭ_заочники Сподумен LiAl[Si2O6] алюмосиликат лития.Лепидолит KLi2Al[Si4O10](F,OH)2 алюмосиликат из группы литиевых слюдСырье для производства редких металлов Сподумен LiAl[Si2O6] алюмосиликат лития.Лепидолит KLi2Al[Si4O10](F,OH)2 алюмосиликат из группы литиевых слюдСырье для производства редких металлов](/img/thumbs/a921364988dd8414924d6c85a63c66b1-800x.jpg)
![ТРЭ_заочники Поллуцит – водный алюмосиликат цезия: (Cs,Na)[AlSi2O6].nH2OСырье для производства редких металлов Поллуцит – водный алюмосиликат цезия: (Cs,Na)[AlSi2O6].nH2OСырье для производства редких металлов](/img/thumbs/d076edcccfe60b8a1c2d4d4bfb885103-800x.jpg)






![ТРЭ_заочники Колумбит-танталит – ниобат-танталат железа и марганца: (Fe,Mn)[(Nb,TaO3)2] .Танталит-колумбит, представляет собой изоморфный Колумбит-танталит – ниобат-танталат железа и марганца: (Fe,Mn)[(Nb,TaO3)2] .Танталит-колумбит, представляет собой изоморфный ряд метаниобатов-метатанталатовСырье для производства редких металлов](/img/thumbs/16d60f0cddaf2da2b1aa4351c2ced685-800x.jpg)

















![ТРЭ_заочники Физико-химические основы процесса вскрытия: 1). (Li,Na)Al[Si2O6] Li(Na)[AlSi2O6] α-сподумен Физико-химические основы процесса вскрытия: 1). (Li,Na)Al[Si2O6] Li(Na)[AlSi2O6] α-сподумен 1100 0С β-сподумен](/img/thumbs/a1482c9e4b4f2bc3fab8ac75450023ff-800x.jpg)