Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Внедрение системы менеджмента качества в рамках Евразийского экономического
Содержание
- 1. Внедрение системы менеджмента качества в рамках Евразийского экономического
- 2. Договор о Евразийском экономическом союзе (п. 2
- 3. Основные понятия
- 4. Требования к внедрению системы менеджмента качества медицинских изделий в зависимости от потенциального риска их примененияОБЯЗАНЫВПРАВЕ
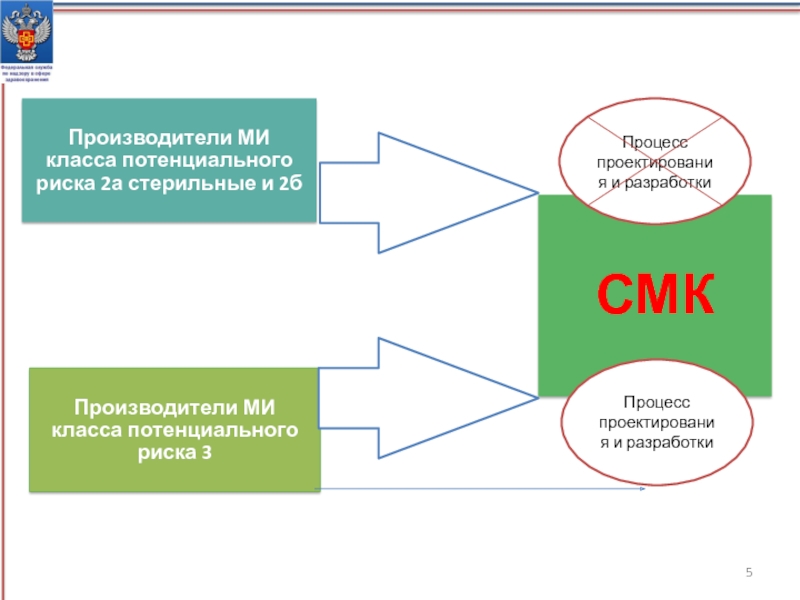
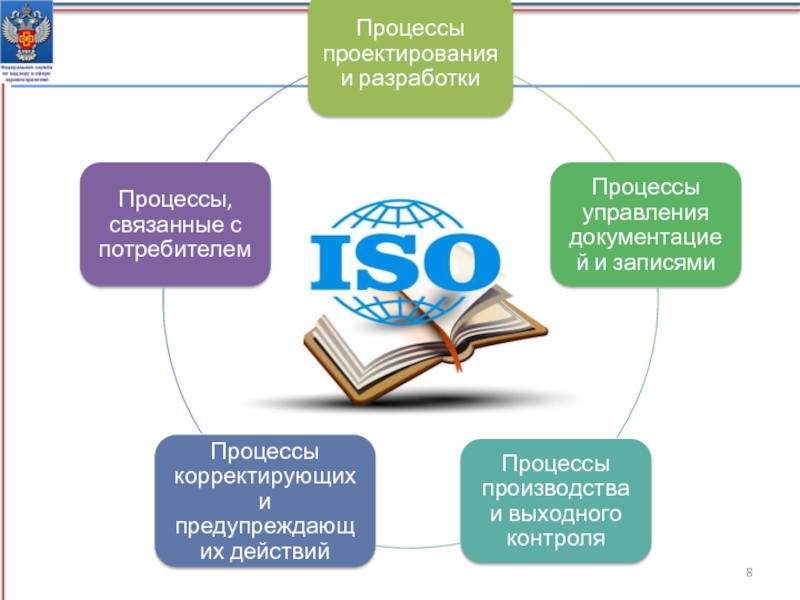
- 5. Процесс проектирования и разработкиПроцесс проектирования и разработкиВНЕДРЕНИЕ
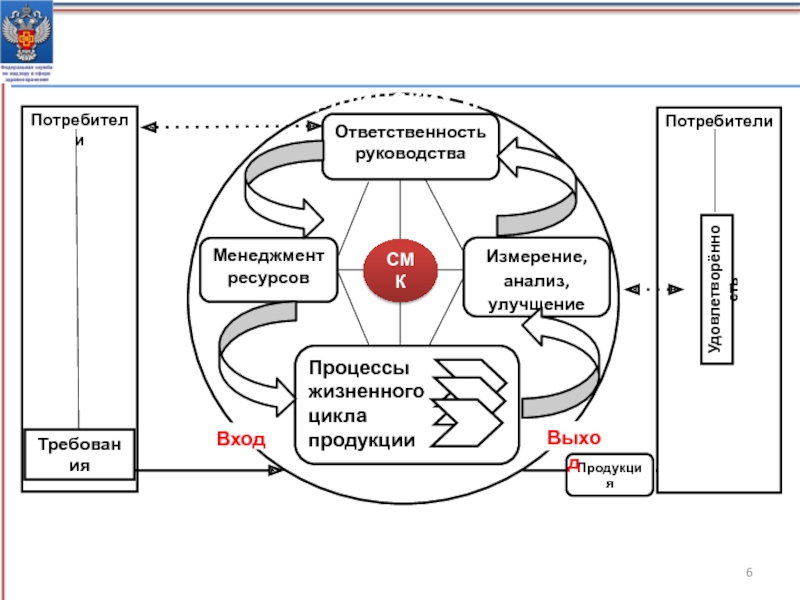
- 6. Требования к системе менеджмента качества медицинских изделийСМК
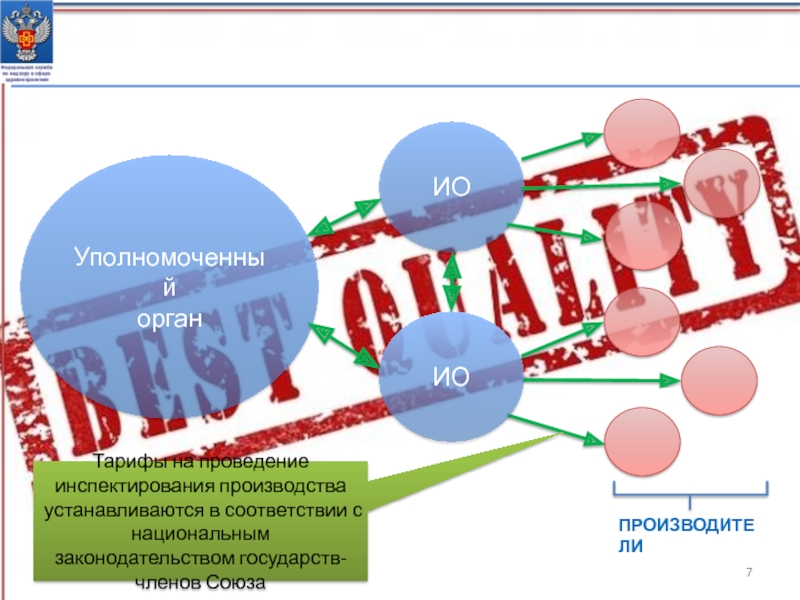
- 7. Общий порядок проведения инспектированияУполномоченныйорганИОТарифы на проведение инспектирования производства устанавливаются в соответствии с национальным законодательством государств-членов СоюзаПРОИЗВОДИТЕЛИИО
- 8. Оценка системы менеджмента качества медицинских изделий
- 9. Оценка процессов проектирования и разработки СМК включает
- 10. Оценка процессов управления документацией и записями СМК
- 11. Оценка процессов производства и выходного контроля СМК
- 12. Оценка процессов корректирующих и предупреждающих действий СМК
- 13. Оценка процессов, связанных с потребителем СМК, включает
- 14. Оценка системы менеджмента качества медицинских изделийВнеплановое инспектированиепроизводства Первичное инспектированиепроизводства Периодическое (плановое)инспектированиепроизводства
- 15. Первичное инспектирование производства проводится в ходе процедуры
- 16. Периодическое (плановое) инспектирование производства проводится один раз
- 17. Анализ представленных на инспектирование документов (не более
- 18. При проведении периодического (планового) инспектирования производства оцениваетсяПоддержание
- 19. Производитель медицинского изделия вправе обратиться в инспектирующую
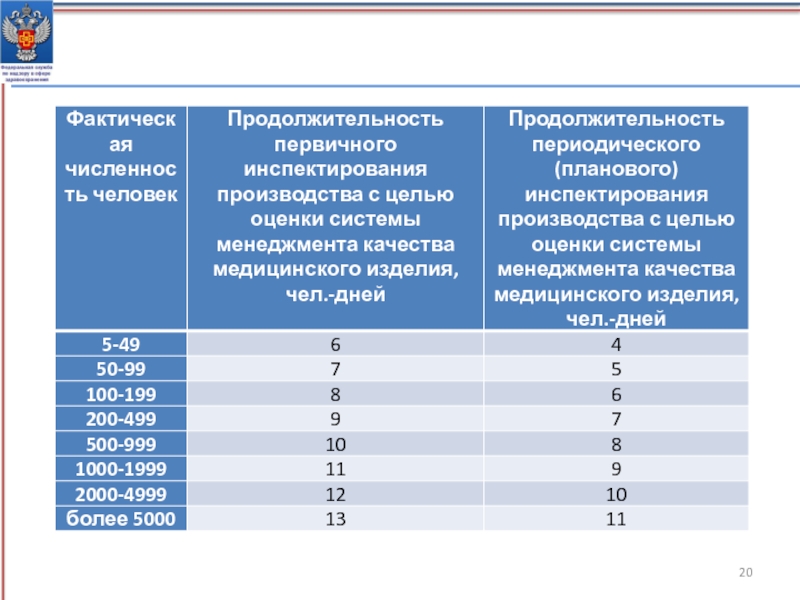
- 20. Нормативная продолжительность инспектирования производства
- 21. Классификация несоответствий системы менеджмента качества проводится в
- 22. В соответствие с классификационной матрицей все выявленные
- 23. Применения повышающих баллов, начисляемых за наличие следующих
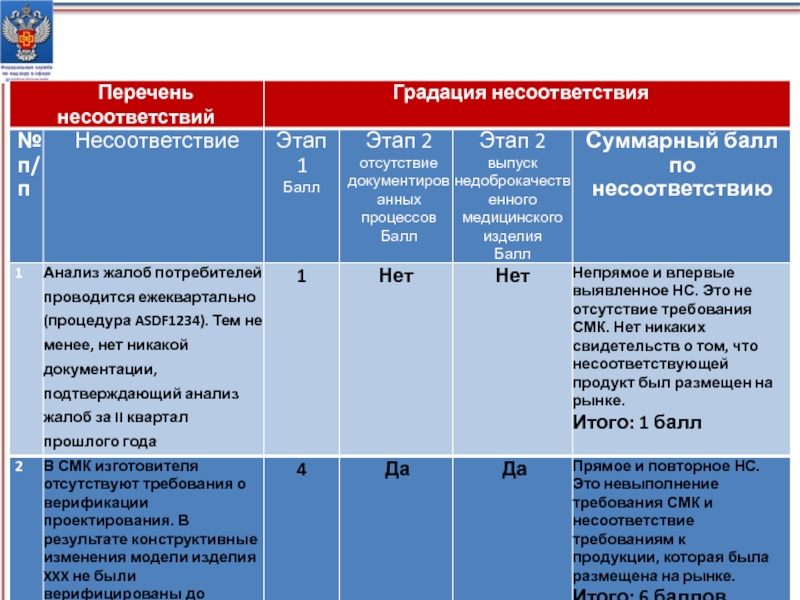
- 24. Примеры, иллюстрирующие градацию несоответствий
- 25. Спасибо за внимание!Э.И. Ахтямов заместитель начальника Управления Федеральной службы по надзору в сфере здравоохраненияAhtyamovEI@roszdravnadzor.ru
- 26. Скачать презентанцию
Слайды и текст этой презентации
Слайд 1Внедрение системы менеджмента качества в рамках Евразийского экономического союза. Инспектирование
производства медицинских изделий
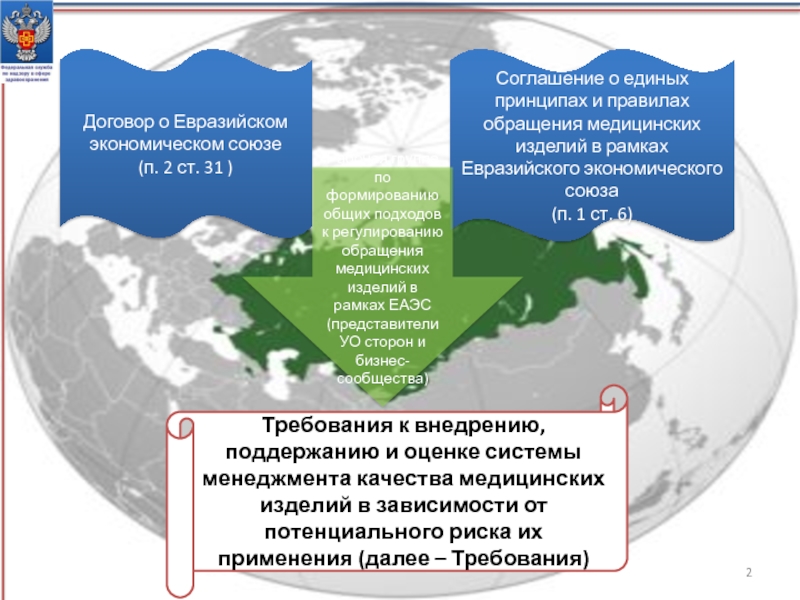
заместитель начальника Управления Федеральной службы по надзору в сфере здравоохраненияСлайд 2Договор о Евразийском экономическом союзе
(п. 2 ст. 31 )
Соглашение
о единых принципах и правилах обращения медицинских изделий в рамках
Евразийского экономического союза(п. 1 ст. 6)
Рабочая группа по формированию общих подходов к регулированию обращения медицинских изделий в рамках ЕАЭС (представители УО сторон и бизнес-сообщества)
Требования к внедрению, поддержанию и оценке системы менеджмента качества медицинских изделий в зависимости от потенциального риска их применения (далее – Требования)
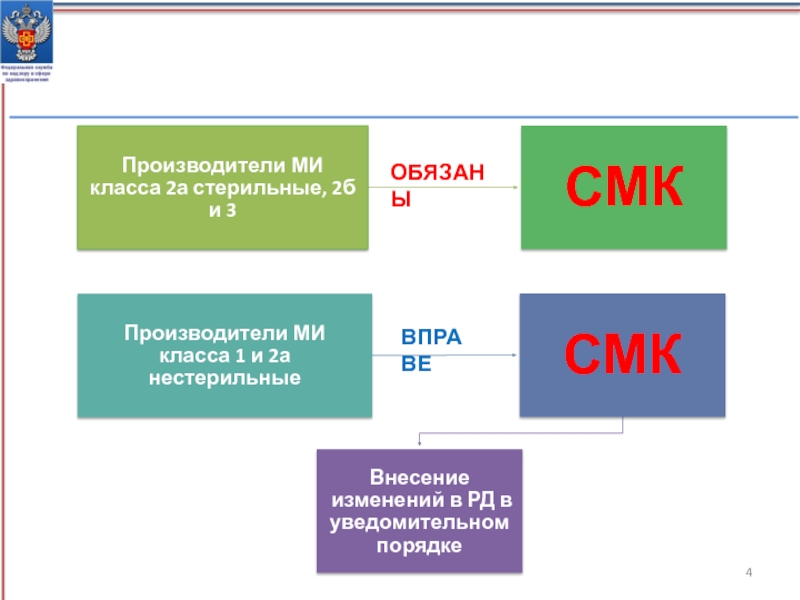
Слайд 4Требования к внедрению системы менеджмента качества медицинских изделий в зависимости
от потенциального риска их применения
ОБЯЗАНЫ
ВПРАВЕ
Слайд 7Общий порядок проведения инспектирования
Уполномоченный
орган
ИО
Тарифы на проведение инспектирования производства устанавливаются в
соответствии с национальным законодательством государств-членов Союза
ПРОИЗВОДИТЕЛИ
ИО
Слайд 9Оценка процессов проектирования и разработки СМК включает в себя
Подтверждение того,
что деятельность по менеджменту риска определена и осуществлена, критерии допустимости
риска установлены и являются соответствующими, любой остаточный риск оценен и, если необходимо, доведен до сведения потребителя с помощью маркировок и инструкций по эксплуатации в соответствии с Общими требованиями безопасности и эффективностиПодтверждение того, что входные данные проектирования были разработаны с учетом назначения и соответствующих положений Общих требований безопасности и эффективности
Анализ спецификаций на медицинские изделия для подтверждения того, что были определены выходные данные проекта, обеспечивающие безопасность и эффективность медицинского изделия при применении в соответствии с назначением
Подтверждение на основе выбранных записей по проектированию медицинского изделия того, что процедуры проектирования и разработки были установлены и применены
Анализ документов, описывающих процедуру проектирования и охватывающий модельный ряд медицинского изделия
Подтверждение наличия процедур проектирования и разработки, включая управление рисками
Слайд 10Оценка процессов управления документацией и записями СМК включает в себя
Подтверждение
того, что разработаны процедуры идентификации, хранения и удаления (уничтожения) документов
и записей (включая управление изменениями)Подтверждение наличия документов, необходимых для того, чтобы организация могла обеспечить планирование, осуществление и управление производственными процессами
Подтверждение того, что документация на медицинское изделие включает в себя:
свидетельства соответствия требованиям, в том числе требованиям применяемых стандартов;
описание медицинского(их) изделия(ий), включая инструкции по применению, материалы и спецификацию;
сводную документацию по верификации и валидации проекта(ов), включая данные клинических исследований (испытаний);
маркировку;
документы по менеджменту риска
Слайд 11Оценка процессов производства и выходного контроля СМК включает в себя
Анализ
производственных процессов изготовления серийной продукции, включая условия производства
Оценка процессов стерилизации,
в том числе:- определение того, что процессы стерилизации документированы, записи параметров процесса стерилизации для каждой стерилизуемой партии медицинских изделий поддерживаются в рабочем состоянии;
- определение того, что процесс стерилизации валидирован;
- определение того, что процесс стерилизации проводится в соответствии с установленными параметрами
Подтверждение того, что процессы производства являются управляемыми и контролируемыми и функционируют в установленных пределах
Подтверждение идентификации и прослеживаемости медицинских изделий и процессов их производства, а также их соответствия установленным требованиям
Подтверждение того, что деятельность по выходному контролю медицинских изделий обеспечивает соответствие медицинских изделий установленным требованиям и документирована
Слайд 12Оценка процессов корректирующих и предупреждающих действий СМК включает в себя
Подтверждение
того, что разработаны процедуры корректирующих и предупреждающих действий
Подтверждение того, что
средства управления препятствуют распространению несоответствующей продукцииПодтверждение того, что корректирующие и предупреждающие действия являются результативными
Подтверждение того, что производитель медицинского изделия разработал эффективную процедуру выпуска и применения уведомлений по безопасности медицинских изделий
Слайд 13Оценка процессов, связанных с потребителем СМК, включает в себя
Подтверждение того,
что производитель медицинского изделия принял меры для установления связи с
потребителями с целью выполнения необходимых корректирующих и предупреждающих действий, имеет и поддерживает в актуальном состоянии систему сбора и анализа данных о безопасности и эффективности медицинских изделий на постпродажном этапе, а также направляет в уполномоченный орган отчеты по постпродажному мониторингу безопасности и эффективности медицинских изделийПодтверждение того, что обратная связь с потребителем анализируется в ходе процессов жизненного цикла продукции и используется для повторной оценки риска и, при необходимости, для актуализации деятельности по менеджменту риска
Слайд 14Оценка системы менеджмента качества медицинских изделий
Внеплановое инспектирование
производства
Первичное инспектирование
производства
Периодическое
(плановое)
инспектирование
производства
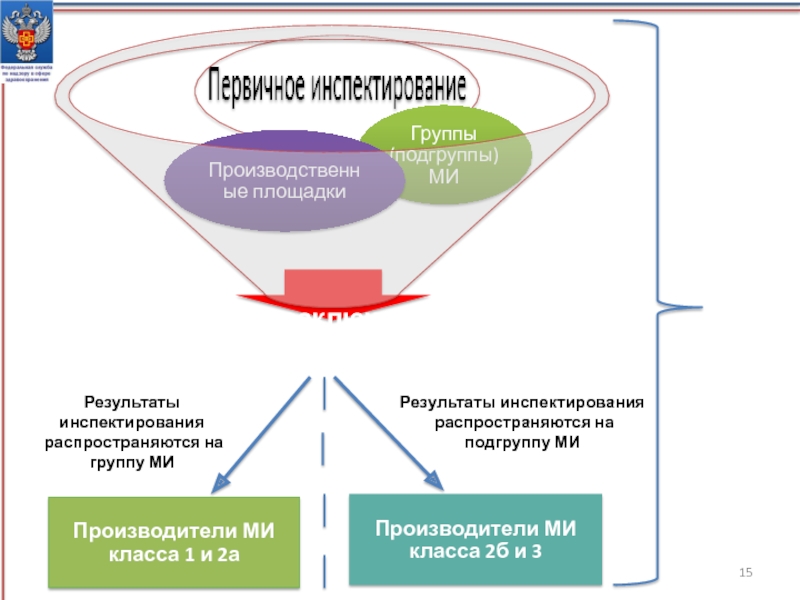
Слайд 15Первичное инспектирование производства проводится
в ходе процедуры регистрации МИ в
рамках Союза
Результаты инспектирования
распространяются на группу МИ
Результаты инспектирования
распространяются на
подгруппу МИСлайд 16Периодическое (плановое) инспектирование производства проводится один раз в три года
Инспектирующая
организация
Производитель
1. Заявка на проведение инспектирования с указанием медицинских изделий с
отнесением их к соответствующим группам (подгруппам) и производственных площадок, входящих в область инспектирования;2. Справка о фактической численности персонала, участвующего в процессах оцениваемой системы менеджмента качества;
3. Технический(ие) файл(ы) на медицинское(ие) изделие(я) на русском языке в электронном формате с возможностью поиска;
4. Копия отчета по результатам последнего инспектирования производства;
5. Копия отчета по результатам последнего аудита системы менеджмента качества органом по сертификации (при наличии)
Слайд 17Анализ представленных на инспектирование документов (не более 10 дней)
Договор
о проведении инспектирования
1) Несоответствие представленного комплекта документов перечню обязательных к
представлению документов;2) Несоответствие технического(их) файла(ов) установленным требованиям;
3) Отсутствие полномочий у инспектирующей организации на проведение инспектирования заявленных групп (подгрупп) МИ
Слайд 18При проведении периодического (планового) инспектирования производства оценивается
Поддержание соответствия системы менеджмента
качества медицинского изделия Требованиям к системе менеджмента качества
Результативность системы менеджмента
качества в обеспечении соответствия выпускаемых в обращение медицинских изделий применимым к ним общим требованиям безопасности и эффективностиПериодическое (плановое) инспектирование производства проводится на выбранных инспектирующей организацией производственных площадках на примере представительных медицинских изделий для каждой группы или подгруппы производимых медицинских изделий в зависимости от класса потенциального риска
Слайд 19Производитель медицинского изделия вправе обратиться в инспектирующую организацию с заявлением
о проведении внепланового инспектирования производства в целях
Внесения изменений в перечень
производственных площадок, в перечень групп (подгрупп) медицинских изделий, на которые распространяется действие отчета об инспектировании производстваПодтверждения устранения нарушений по результатам инспектирования производства
Подтверждения устранения причин, которые привели к выпуску недоброкачественных медицинских изделий, путем включения отчета о внеплановом инспектировании в заключительный отчет о корректирующих действиях по форме согласно приложению № 2 к Правилам проведения мониторинга безопасности, качества и эффективности медицинских изделий
Слайд 21Классификация несоответствий системы менеджмента качества проводится в два этапа
I этап
II
этап
Применение классификационной матрицы, которое обеспечивает предварительную оценку степени значимости несоответствий
Применение
повышающих баллов для определения окончательной оценки степени значимости несоответствийСлайд 22В соответствие с классификационной матрицей все выявленные в несоответствия подразделяются
на четыре группы (I этап)
Повторно выявленное
Впервые выявленное
Влияние несоответствия
на безопасность, эффективность и качество медицинского изделия считается непрямым, если оно затрагивает требования, связанные с общим функционированием системы менеджмента качества, и прямым, если оно касается требований, относящихся к процессам проектирования и разработки, а также к контролю производственных процессов медицинского изделияСлайд 23Применения повышающих баллов, начисляемых за наличие следующих несоответствий (II этап)
Отсутствие
документированных процессов, относящихся к процессам проектирования и разработки медицинских изделий,
контролю производственных процессов, а также к постпродажному мониторингу, необходимых для обеспечения безопасности и эффективностиВыпуск в обращение недоброкачественного медицинского изделия в течение отчетного периода
Отрицательное заключение в случае если одно или более нарушений оценены на 5 или 6 баллов или более двух нарушений оценены на 4 балла