Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
ВЗАЄМОДІЯ АНТИГЕН-АНТИТІЛО. МЕТОДИ ЇЇ ВИЗНАЧЕННЯ
Содержание
- 1. ВЗАЄМОДІЯ АНТИГЕН-АНТИТІЛО. МЕТОДИ ЇЇ ВИЗНАЧЕННЯ
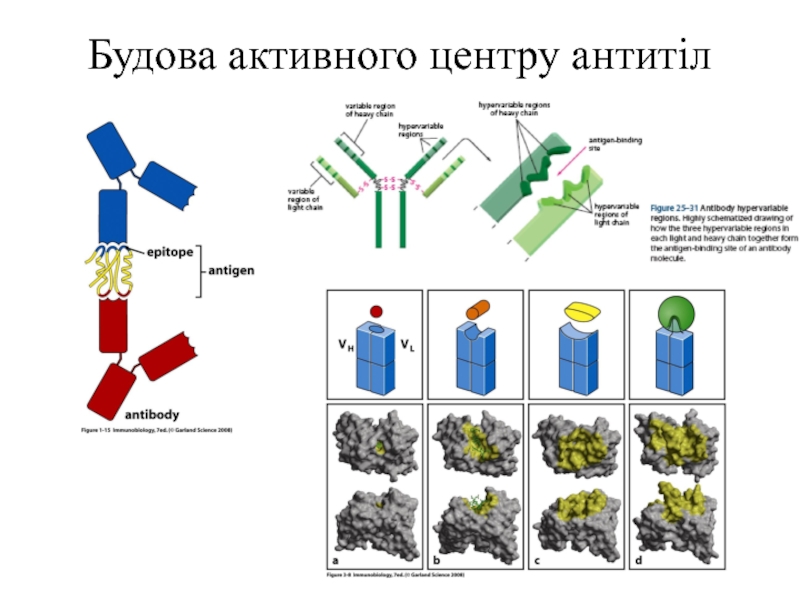
- 2. Будова активного центру антитіл
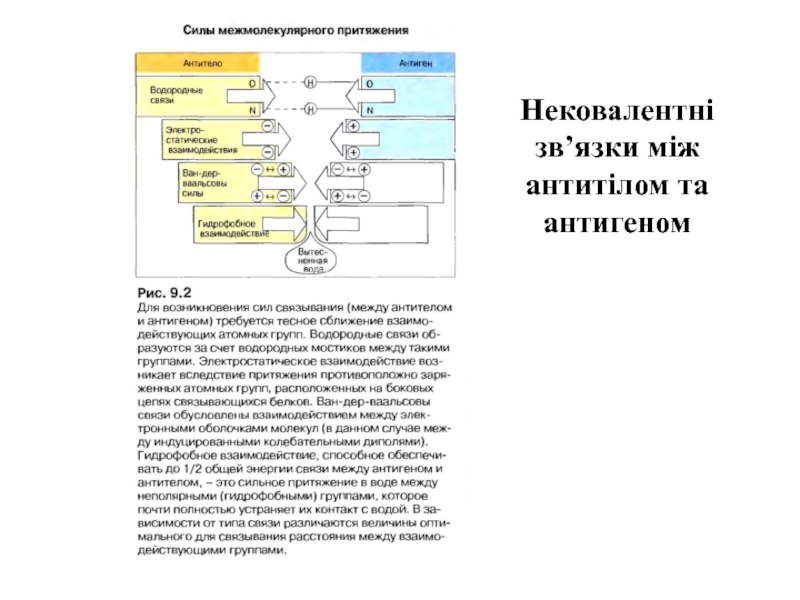
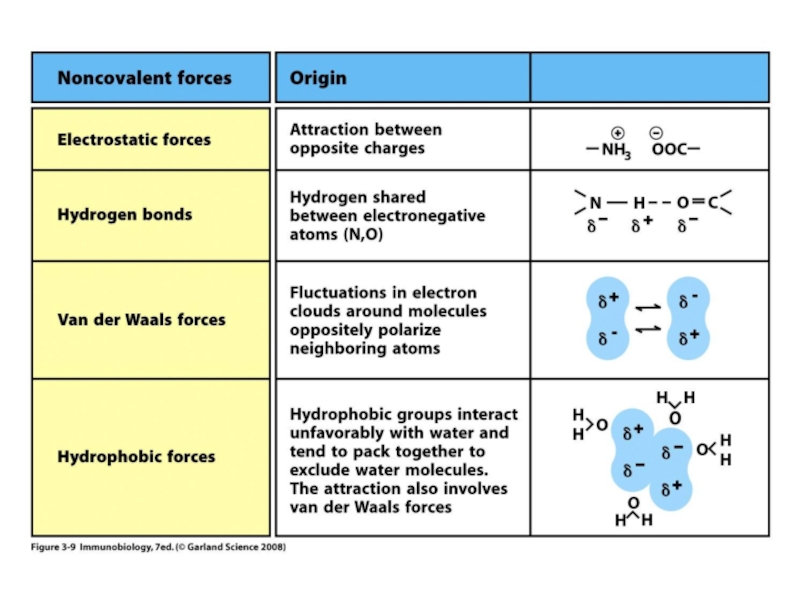
- 3. Нековалентні зв’язки між антитілом та антигеном
- 4. Слайд 4
- 5. АФІННІСТЬ АНТИТІЛ Афінністю або спорідненістю антитіл
- 6. (1) хімічна реакція першого порядку
- 7. Розрахунок афінності антитіл
- 8. Kd=1/ Ka - константа дисоціації;Ka>105M-1 - cпецифічне зв′язування; Ka>108M-1 -високоспецифічне зв′язування;Ka
- 9. (1) хімічна реакція першого порядку
- 10. Кінетичні розрахункиЗгідно з (1) та (2) і
- 11. При розрахунку Ка визначають таку концентрацію антигену
- 12. Слайд 12
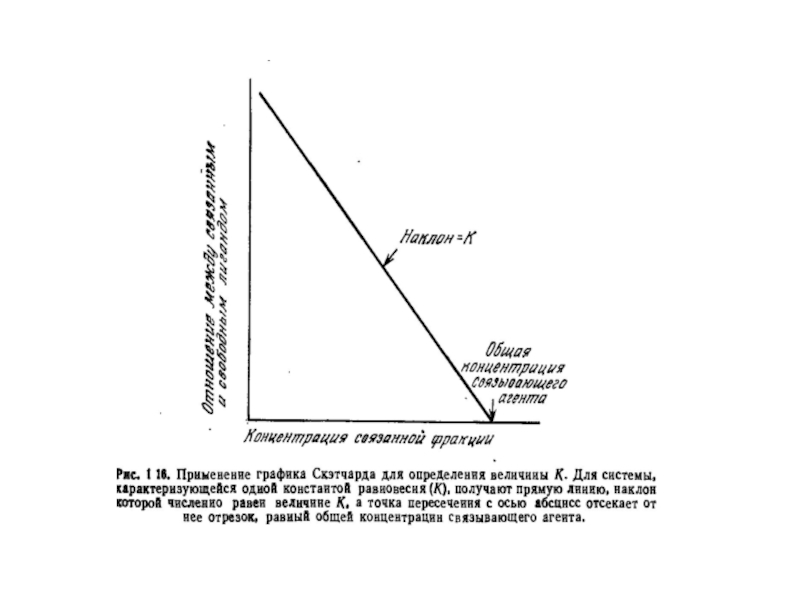
- 13. Рівняння Скетчарда: B - концентрація зв'язаного антигену;
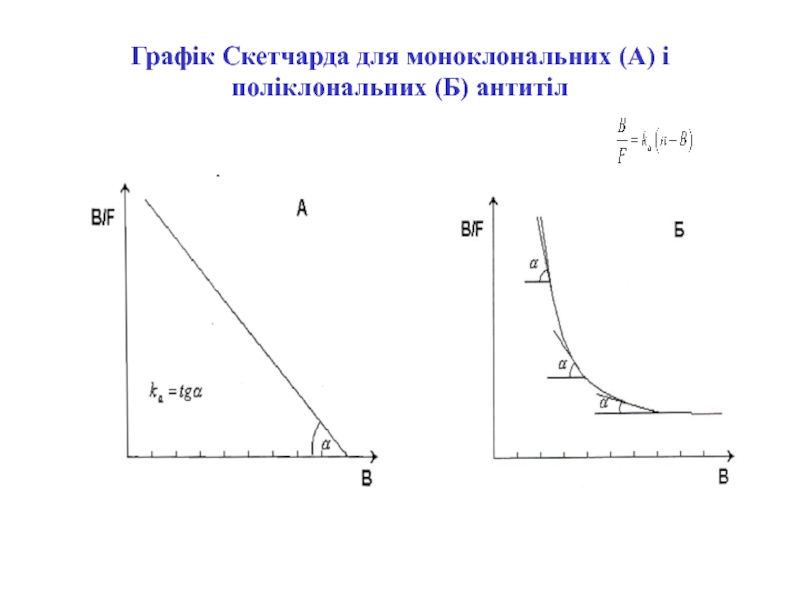
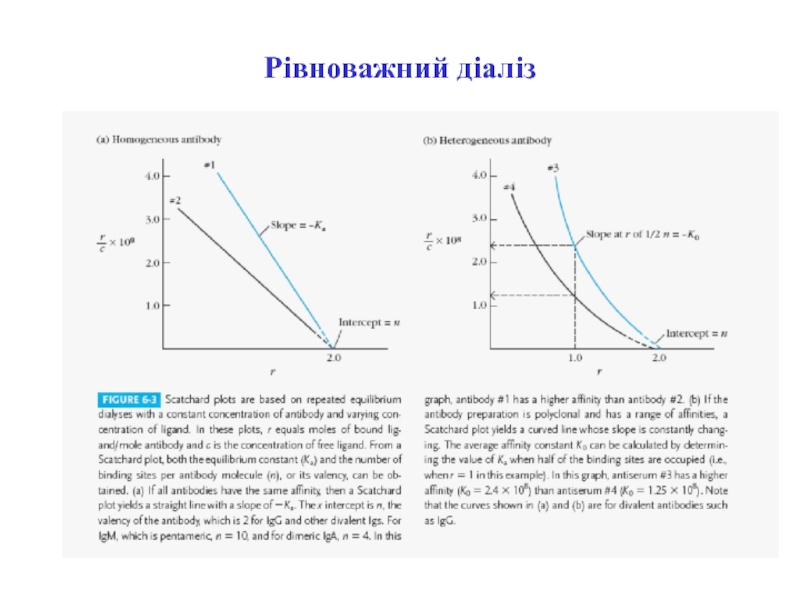
- 14. Графік Скетчарда для моноклональних (А) і поліклональних (Б) антитіл
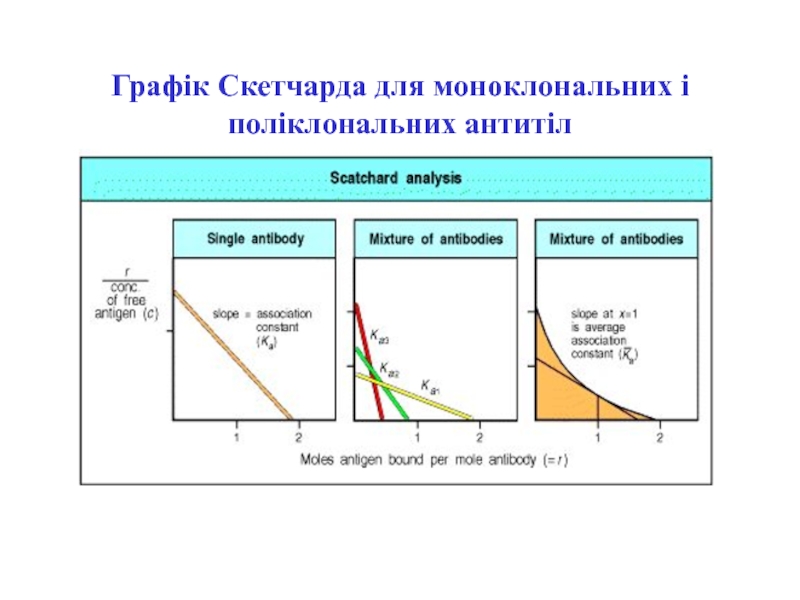
- 15. Графік Скетчарда для моноклональних і поліклональних антитіл
- 16. Слайд 16
- 17. МЕТОДИ ДОСЛІДЖЕННЯ ВЗАЄМОДІЇ АНТИГЕН-АНТИТІЛО. ІМУНОХІМІЧНИЙ АНАЛІЗ.
- 18. Методи імунохімічного аналізуПрямі (безпосередні) методи визначення реакції
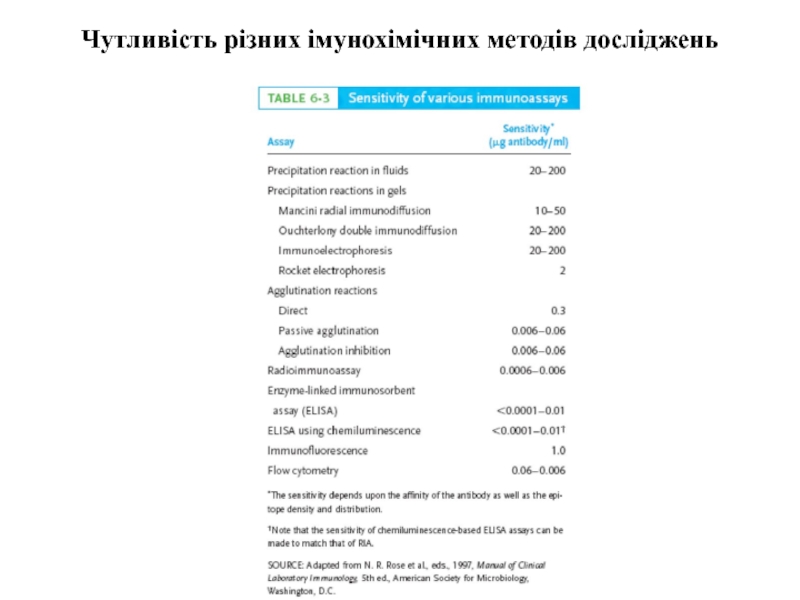
- 19. Чутливість різних імунохімічних методів досліджень
- 20. Експериментальні підходи, які використовуються в імунохімічних методахМетодичні
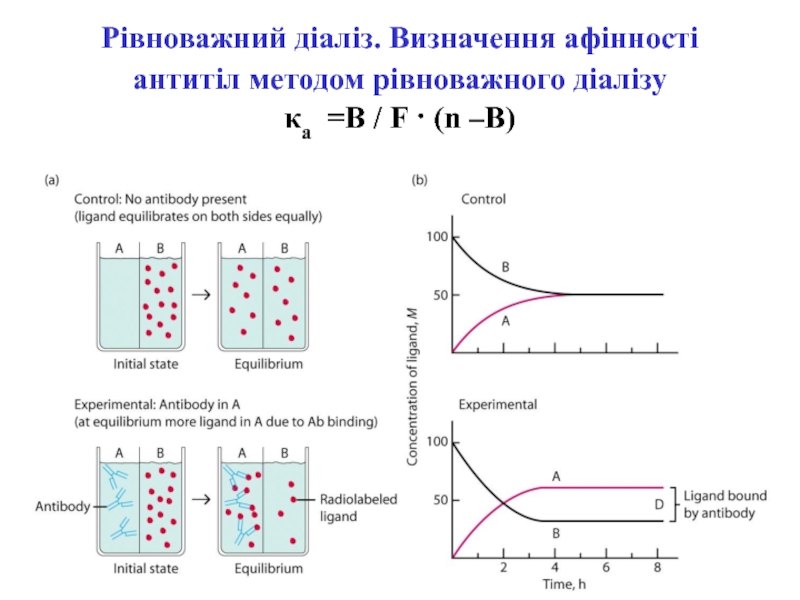
- 21. Рівноважний діаліз. Визначення афінності антитіл методом рівноважного діалізу κа =В / F · (n –B)
- 22. Рівноважний діаліз
- 23. РЕАКЦІЇ ПРЕЦИПІТАЦІЇ
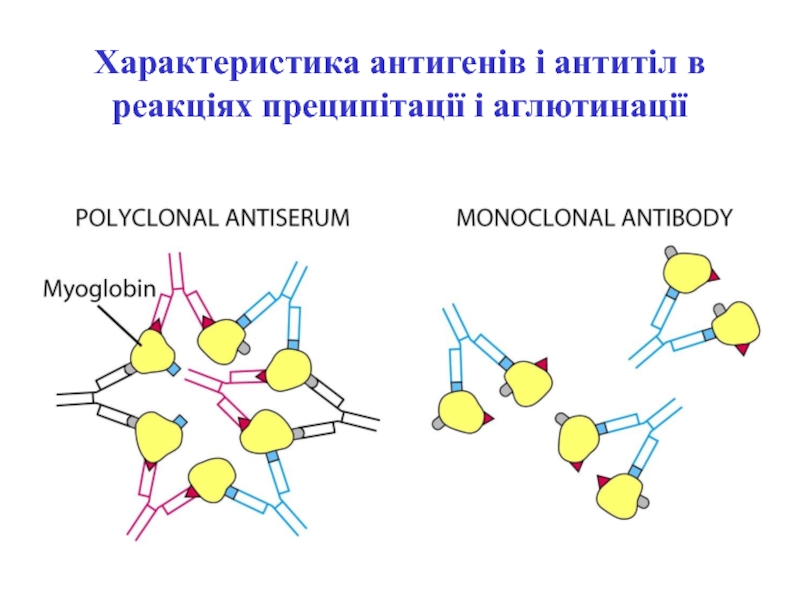
- 24. Характеристика антигенів і антитіл в реакціях преципітації і аглютинації
- 25. Крива преципітації Гейдельберга і типи утворених імунних комплексів при різних співвідношеннях вмісту антигену і антитіл
- 26. Співвідношення концентрацій антигенів і антитіл, коли спостерігається
- 27. Слайд 27
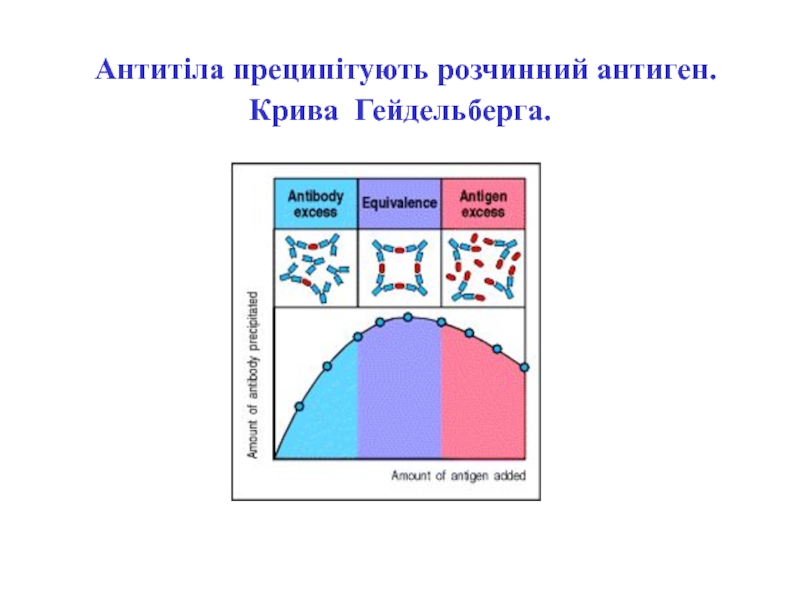
- 28. Антитіла преципітують розчинний антиген. Крива Гейдельберга.
- 29. Слайд 29
- 30. Реакції аглютинації – осадження антитілами корпускулярних антигенів
- 31. Слайд 31
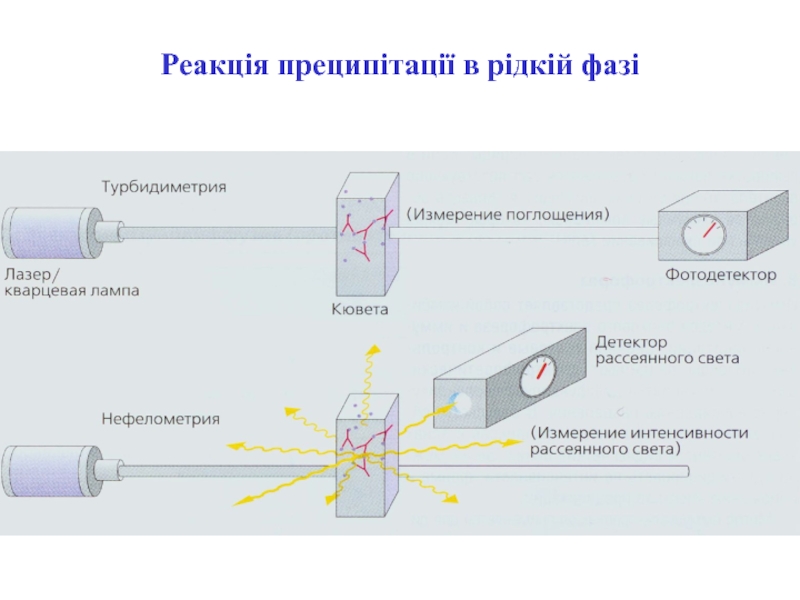
- 32. Реакція преципітації в рідкій фазі
- 33. Реакції преципітації в гелі
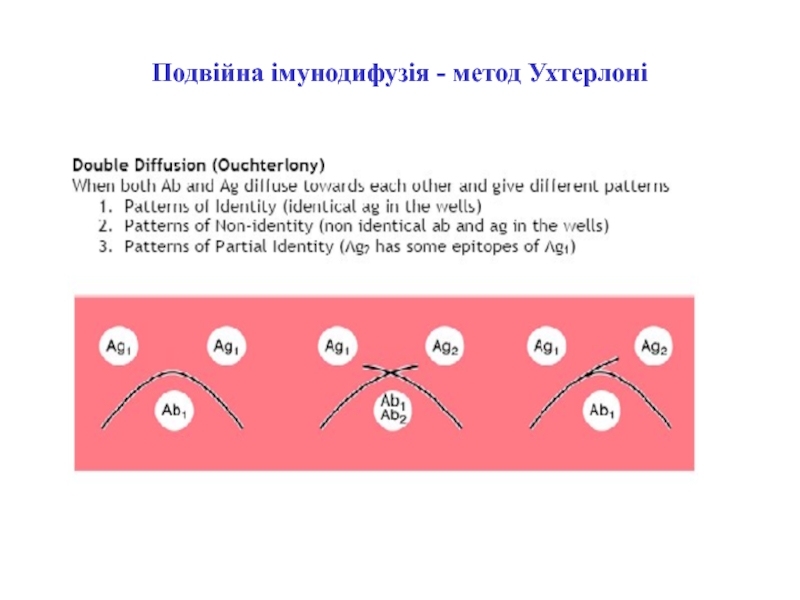
- 34. Подвійна імунодифузія- метод Ухтерлоні
- 35. Подвійна імунодифузія-метод Ухтерлоні Використовується одна
- 36. Подвійна імунодифузія - метод Ухтерлоні
- 37. Подвійна імунодифузія - метод Ухтерлоні
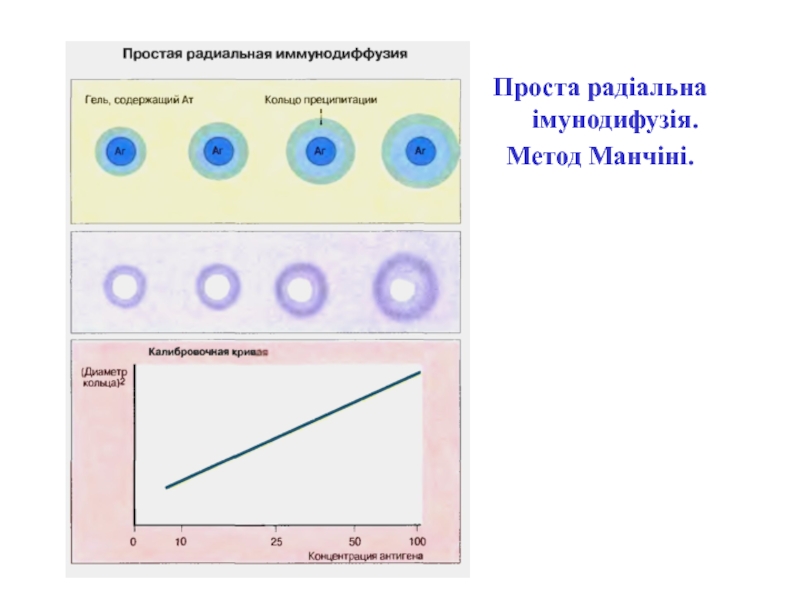
- 38. Проста радіальна імунодифузія.Метод Манчіні.
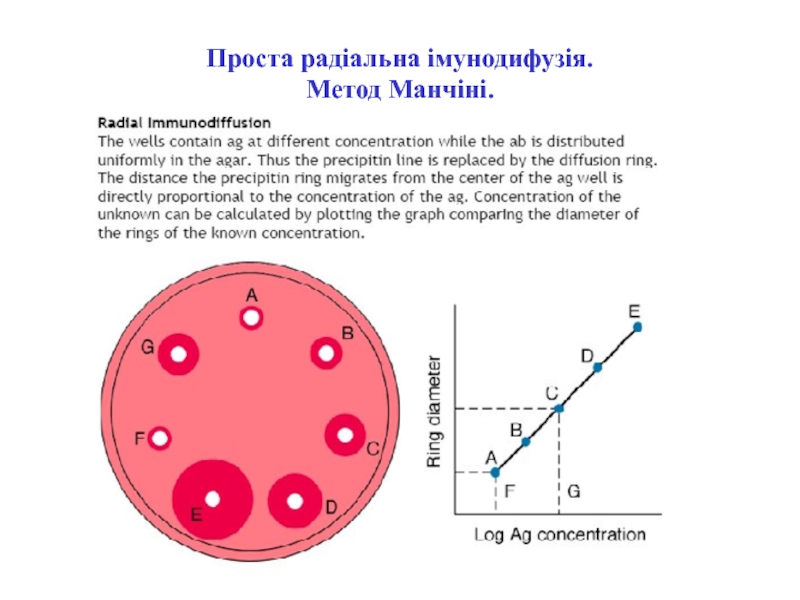
- 39. Проста радіальна імунодифузія. Метод Манчіні.
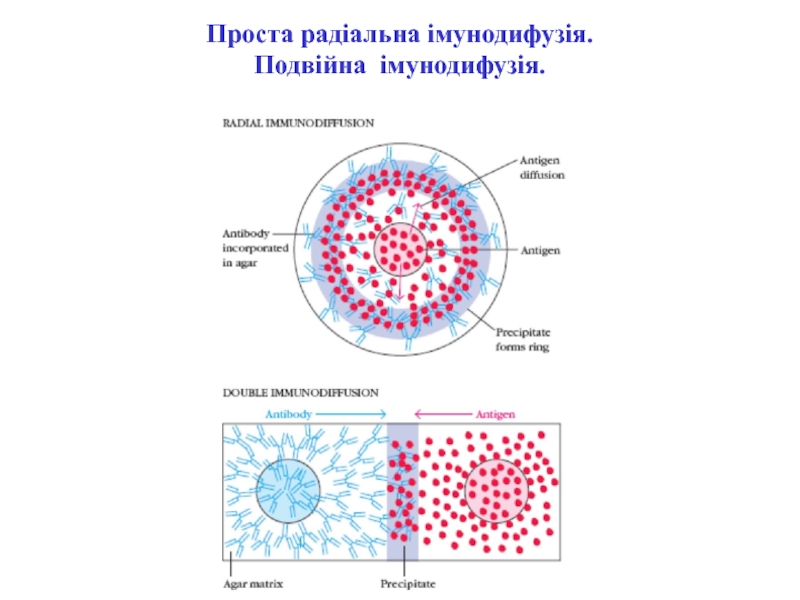
- 40. Проста радіальна імунодифузія. Подвійна імунодифузія.
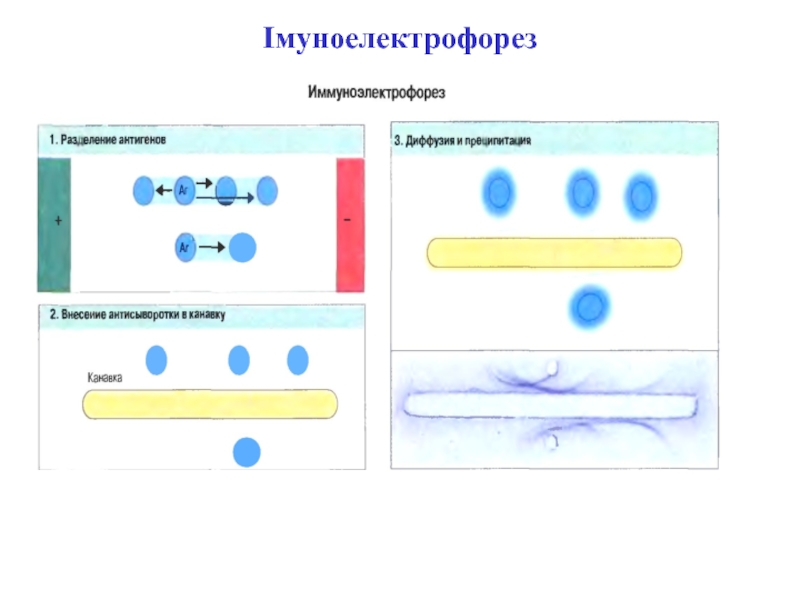
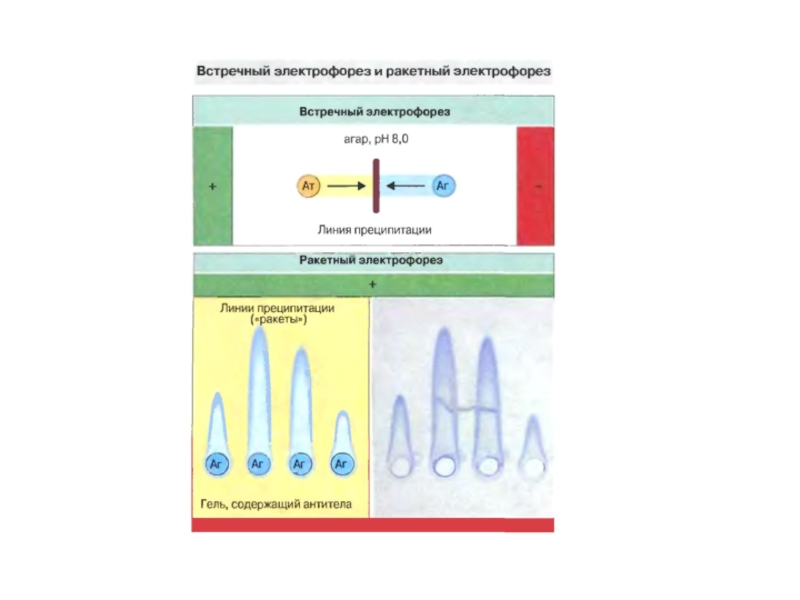
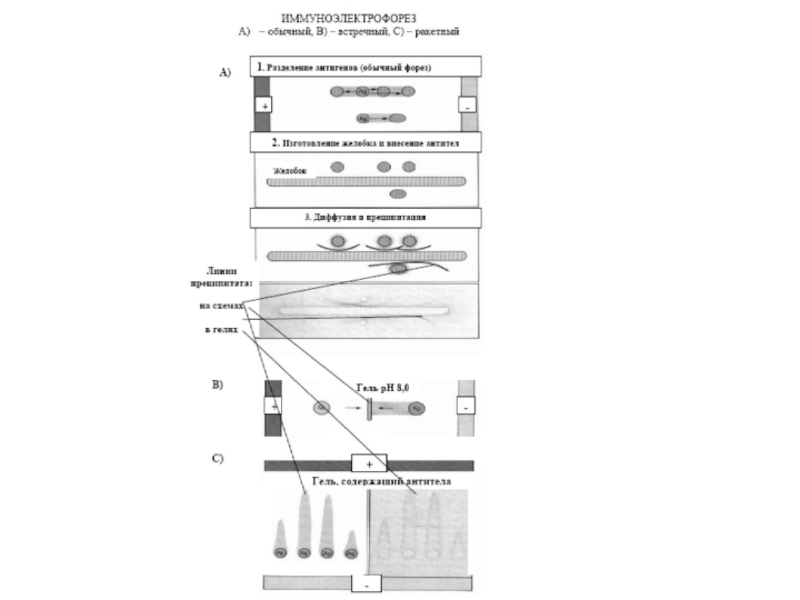
- 41. Імуноелектрофорез
- 42. Слайд 42
- 43. Слайд 43
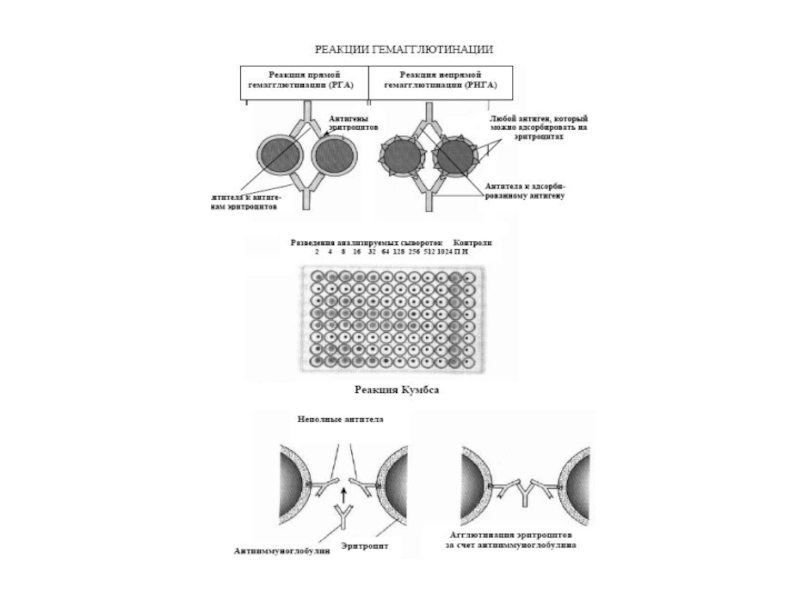
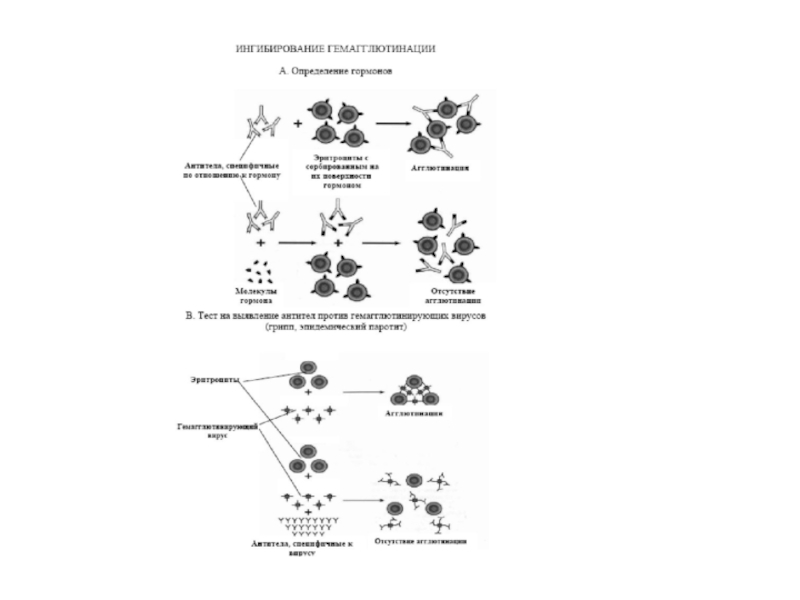
- 44. Реакції гемаглютинації та аглютинації
- 45. Слайд 45
- 46. Слайд 46
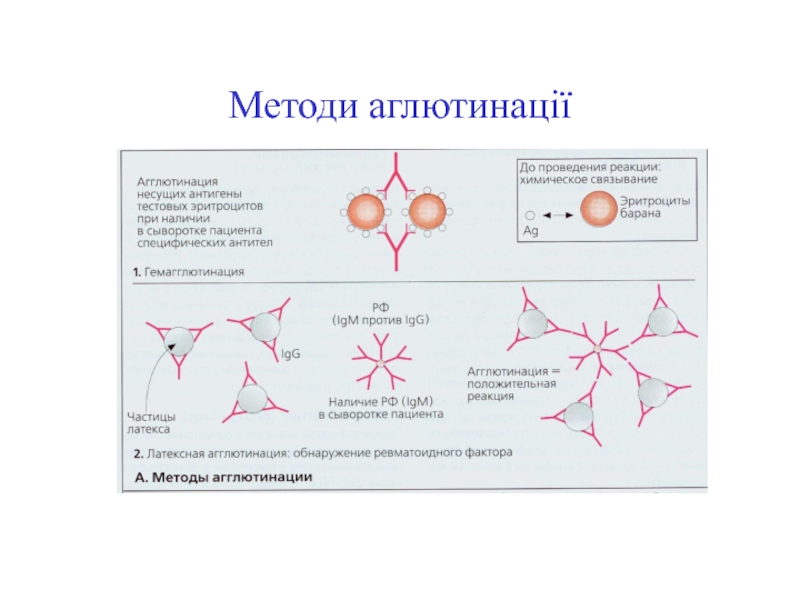
- 47. Методи аглютинації
- 48. Слайд 48
- 49. РІА радіоімунний аналізRoger Guillemin
- 50. Конкурентні імунохімічні методи Amount of label bound
- 51. РІА радіоімунний аналізВ основі РІА – конкуренція
- 52. Аналіз зв'язування антигену з антитілом. Для
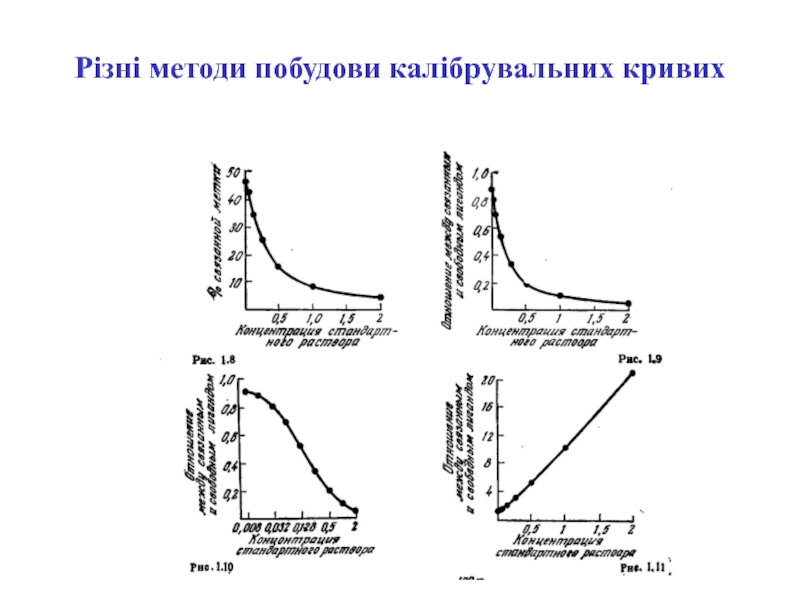
- 53. Різні методи побудови калібрувальних кривих
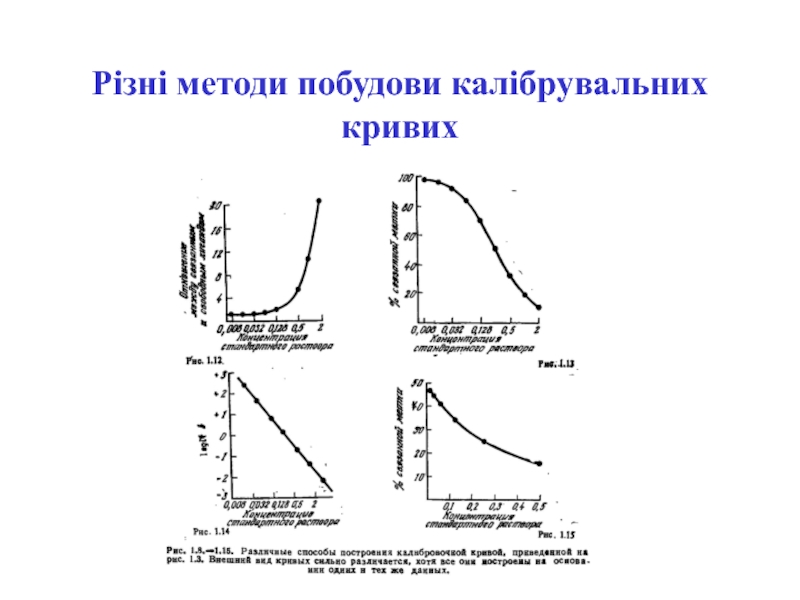
- 54. Різні методи побудови калібрувальних кривих
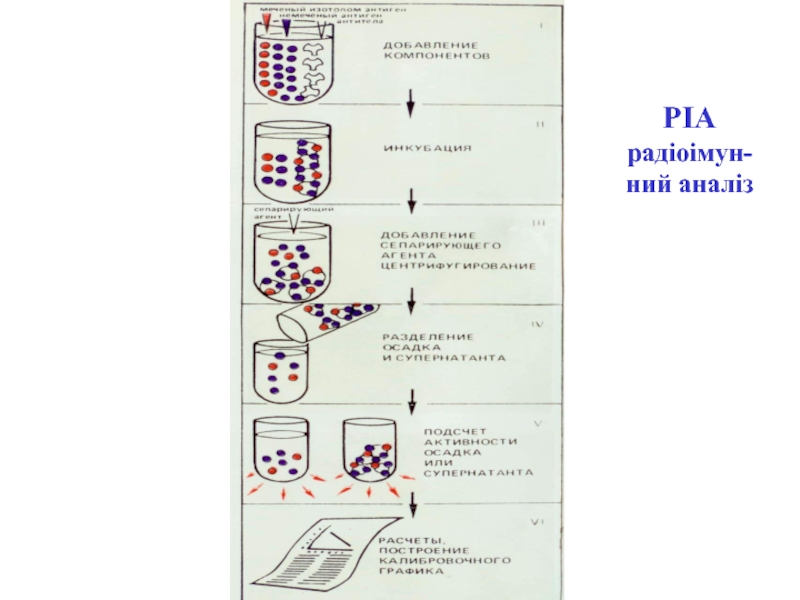
- 55. РІА радіоімун- ний аналіз
- 56. В - рівень зв’язаного в результаті реакції
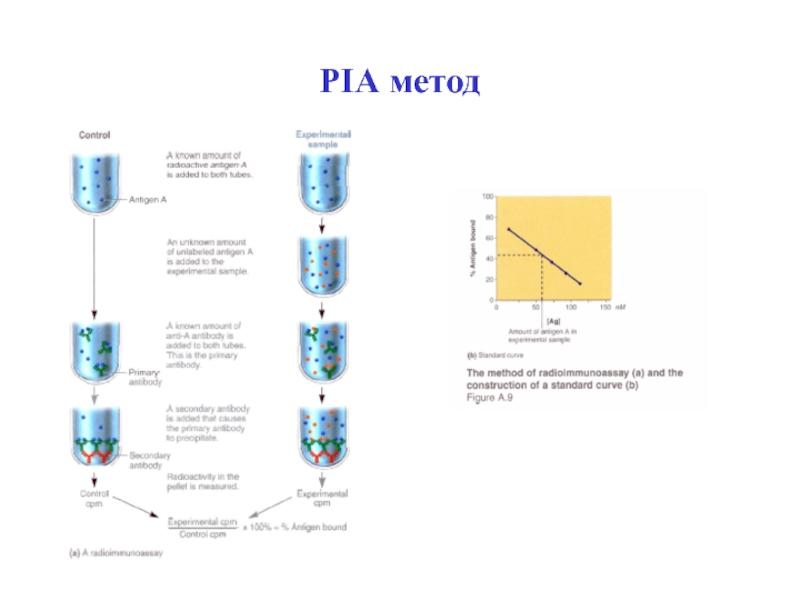
- 57. РІА метод
- 58. Слайд 58
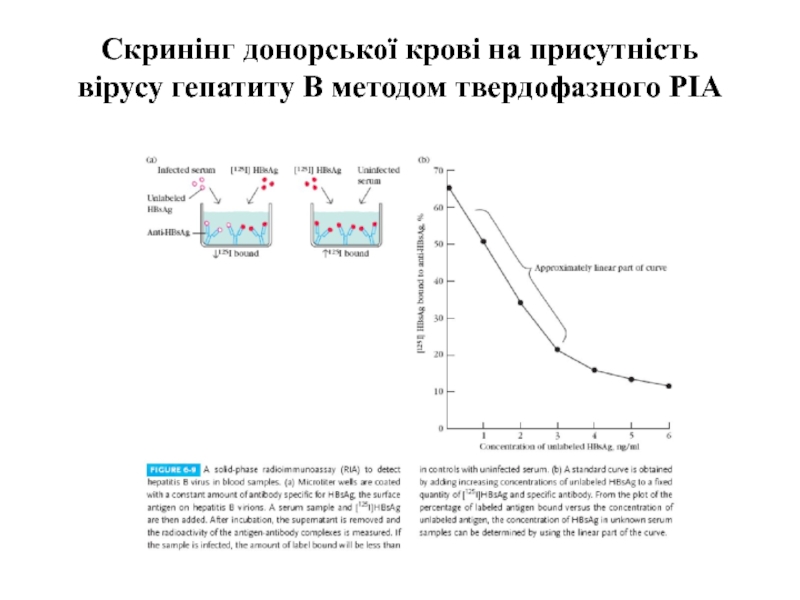
- 59. Cкринінг донорської крові на присутність вірусу гепатиту В методом твердофазного РІА
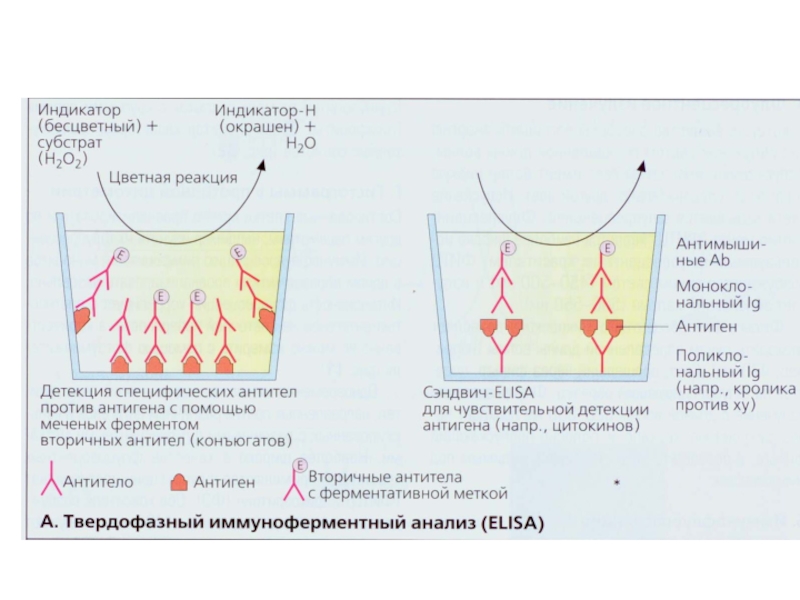
- 60. Імуноферментний аналіз
- 61. Слайд 61
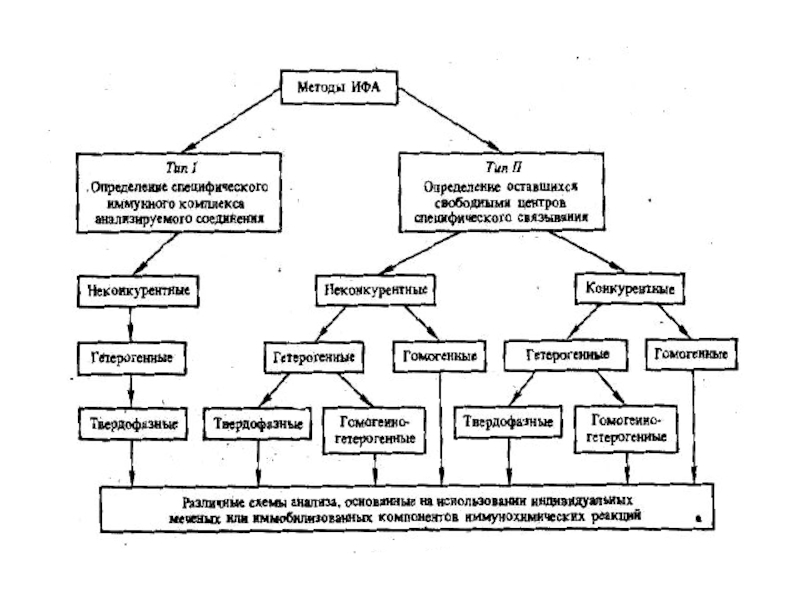
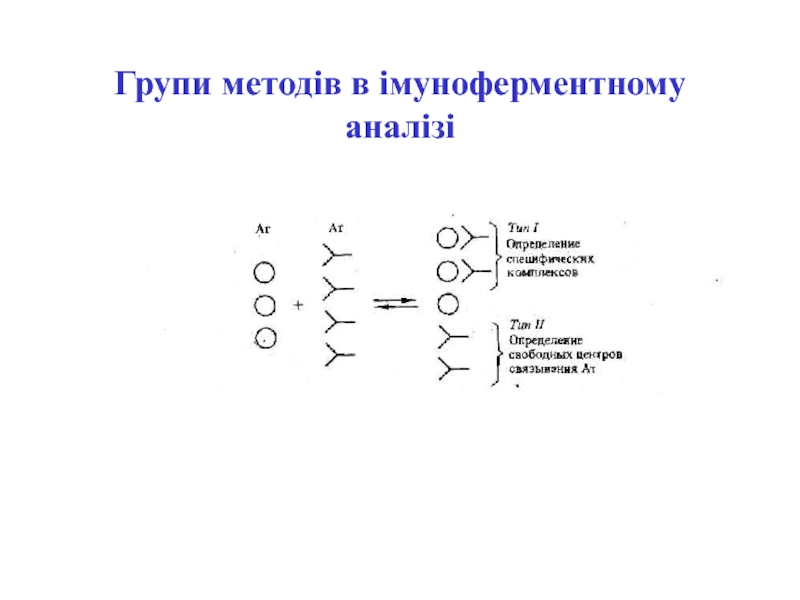
- 62. Групи методів в імуноферментному аналізі
- 63. Варианты гомогенного иммуноферментного анализа А- эффект
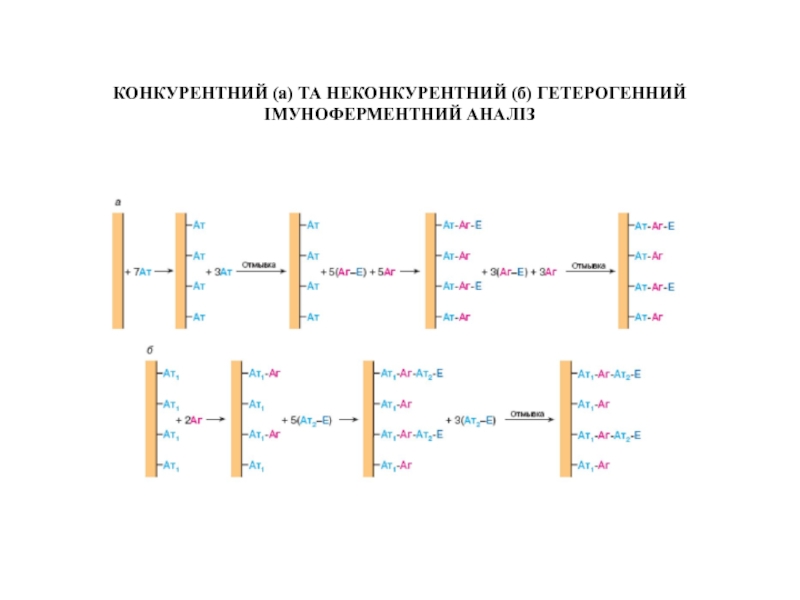
- 64. КОНКУРЕНТНИЙ (а) ТА НЕКОНКУРЕНТНИЙ (б) ГЕТЕРОГЕННИЙ ІМУНОФЕРМЕНТНИЙ АНАЛІЗ
- 65. ОСОБЛИВОСТІ ІМУНОФЕРМЕНТНОГО АНАЛІЗУІмуносорбентиТвердофазні носіїІмобілізація антигенів чи антитіл на твердій фазіФерменти і субстратиКон’югати та їх створення
- 66. ОСОБЛИВОСТІ ІМУНОФЕРМЕНТНОГО АНАЛІЗУФерменти і субстратиПероксидаза хрону (ПХ)-Нorse
- 67. Кон’югат з використанням пари біотин- стрепт(авідин)Система
- 68. Слайд 68
- 69. ОСОБЛИВОСТІ ІМУНОФЕРМЕНТНОГО АНАЛІЗУ Отримання кон’югату - комплексу
- 70. Отримання комплексу антигена і фермента методом гібридних антитіл. 2етап- власне створення гібридних антитіл.
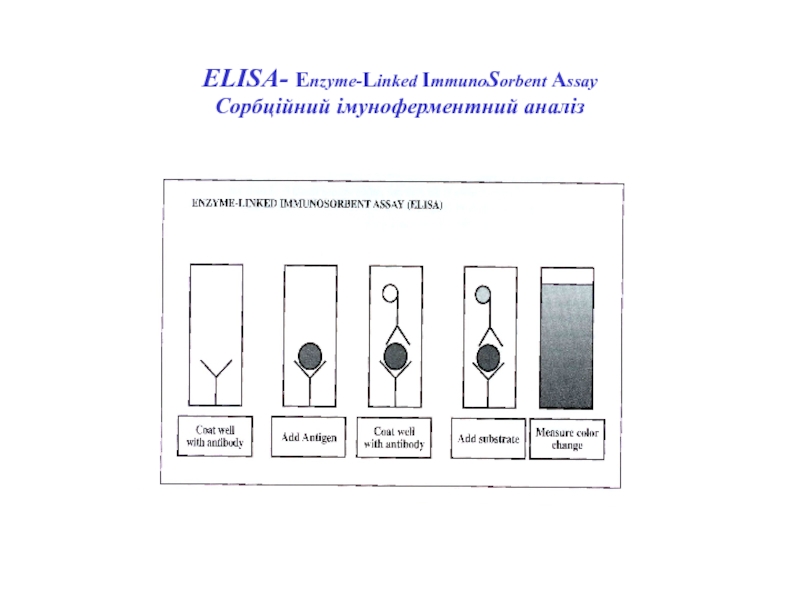
- 71. ELISА- Enzyme-Linked ImmunoSorbent Assay Сорбційний імуноферментний аналіз
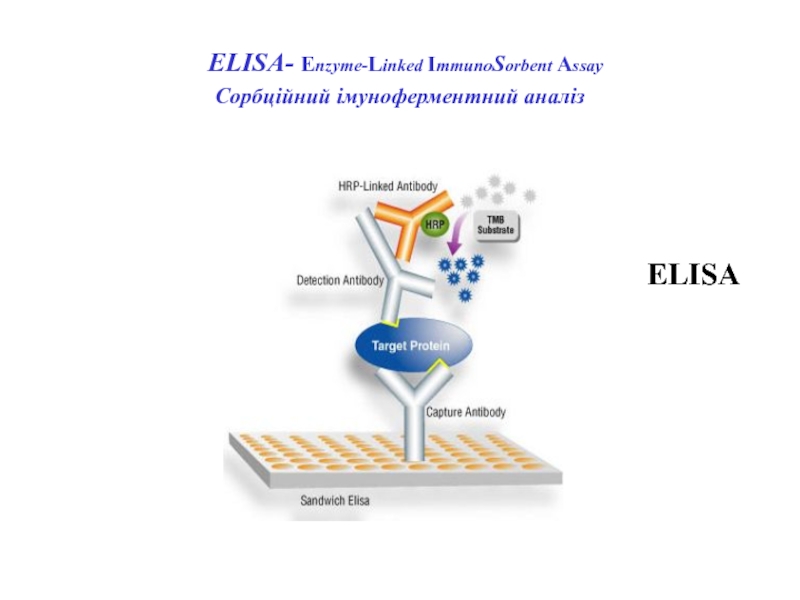
- 72. ELISА- Enzyme-Linked ImmunoSorbent Assay Сорбційний імуноферментний аналіз ELISA
- 73. Слайд 73
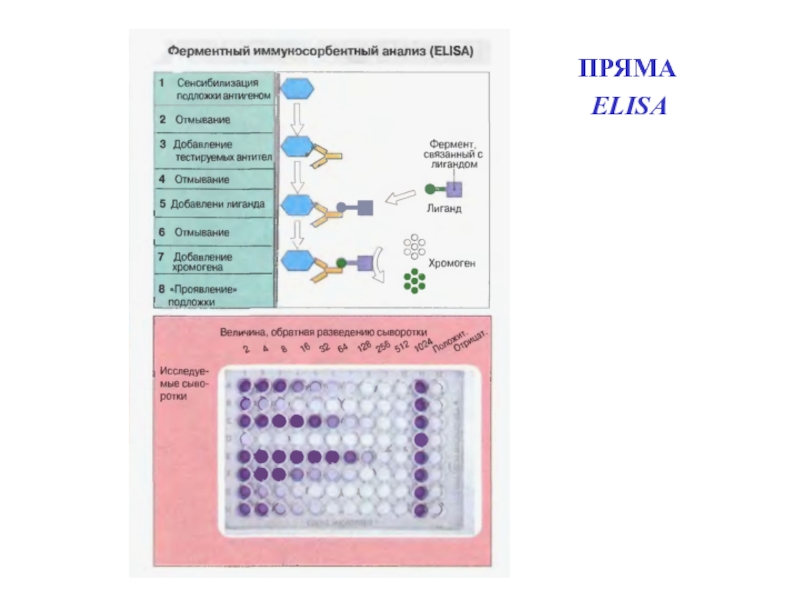
- 74. ПРЯМА ELISА
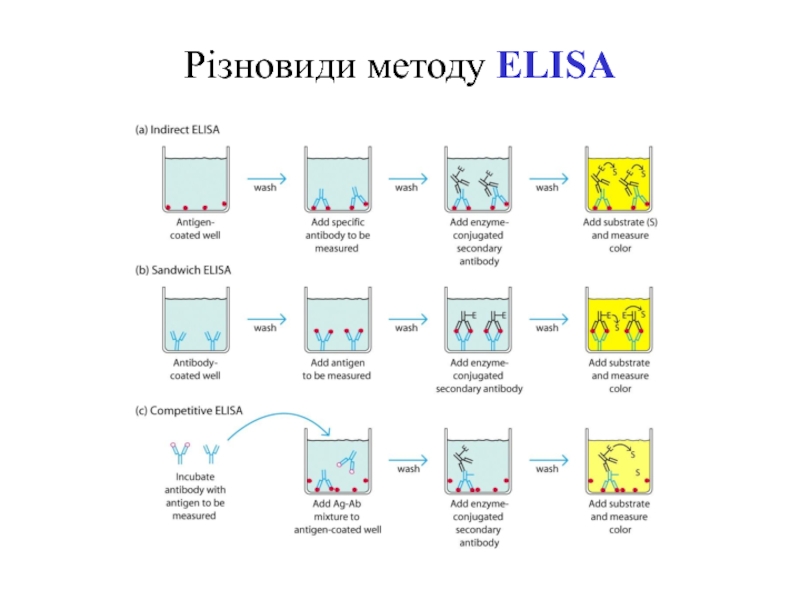
- 75. Різновиди методу ELISA
- 76. ELISА-Enzyme-Linked ImmunoSorbent Assay Сорбційний імуноферментний аналіз (1)
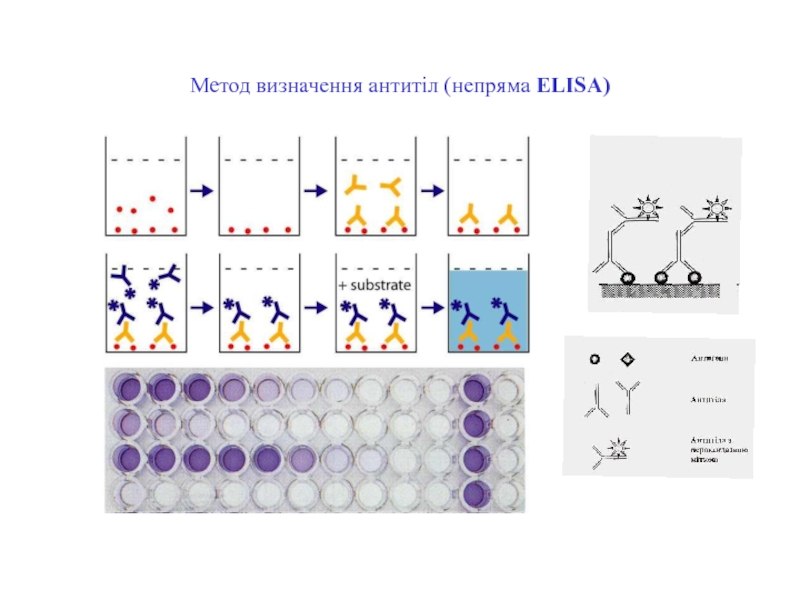
- 77. Метод визначення антитіл (непряма ELISA)
- 78. ELISA :1- сандвіч-метод визначення антигену ; 2-конкурентний
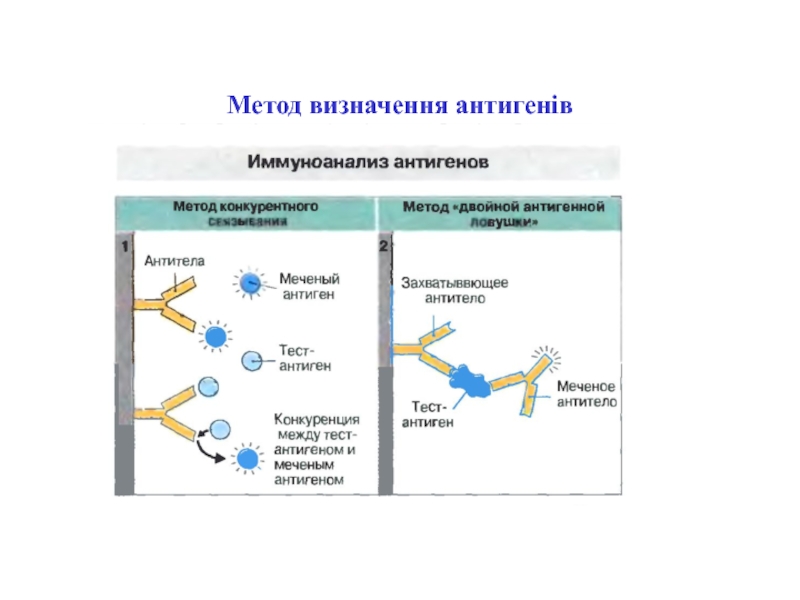
- 79. Метод визначення антигенів
- 80. ELISA ActivityAn HIV ELISA, sometimes called an
- 81. The ELISA MethodPartially purified, inactivated HIV antigens
- 82. Positive ELISA Test Negative ELISA Test
- 83. Above is ELISA data from three
- 84. Перша російська тест-система для виявлення сумарних антитіл до ВІЛ-1,2
- 85. Використання методу ELISA для детекції рівня клітинної
- 86. Метод імунофлуоресценції ФІТЦ- флуоресцеїн-ізотіоціанат- довжина хвилі збудження- 450-500 нм, випромінення (емісії)-500-550 нм
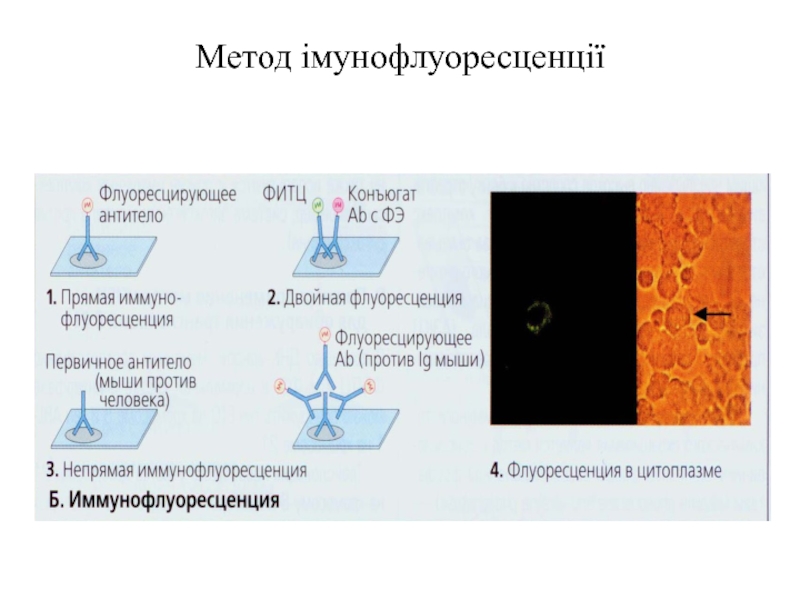
- 87. Метод імунофлуоресценції
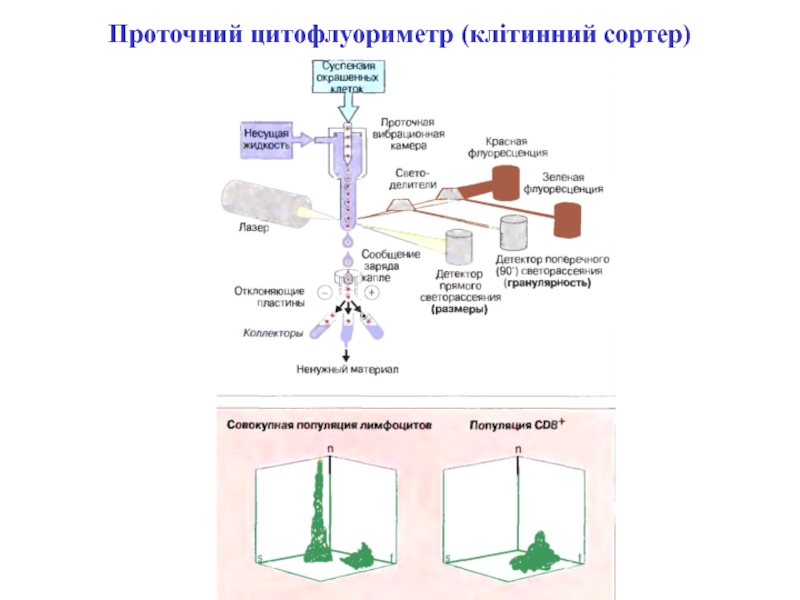
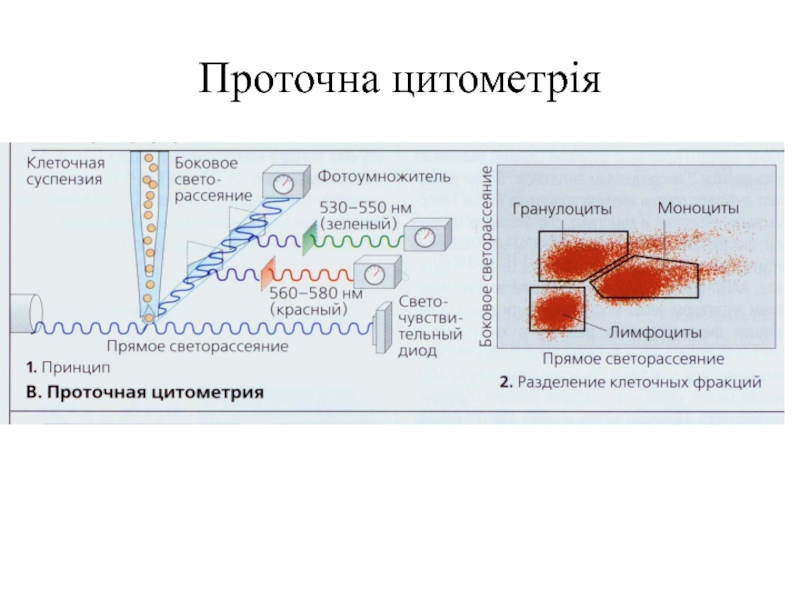
- 88. Проточний цитофлуориметр (клітинний сортер)
- 89. Проточна цитометрія
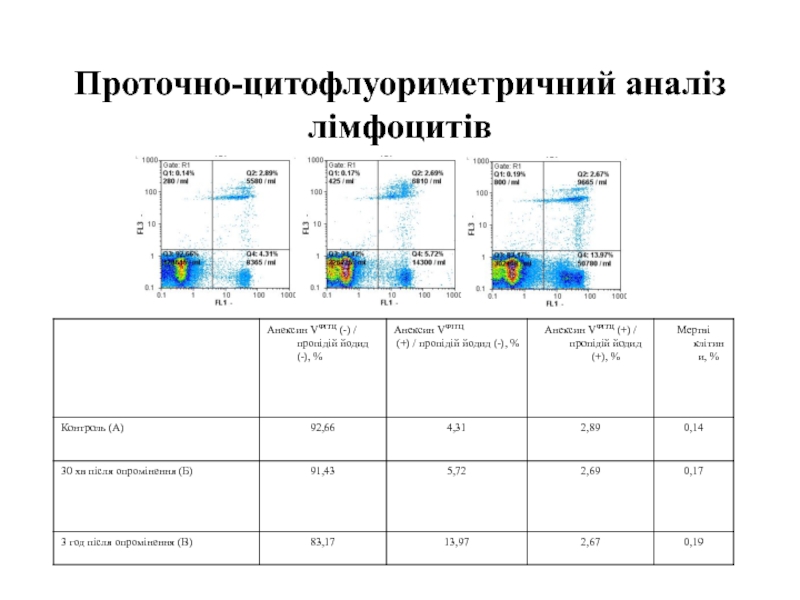
- 90. Проточно-цитофлуориметричний аналіз лімфоцитів
- 91. Рис. Проточно-цитофлуориметричний аналіз лімфоцитів тимусу (А) та
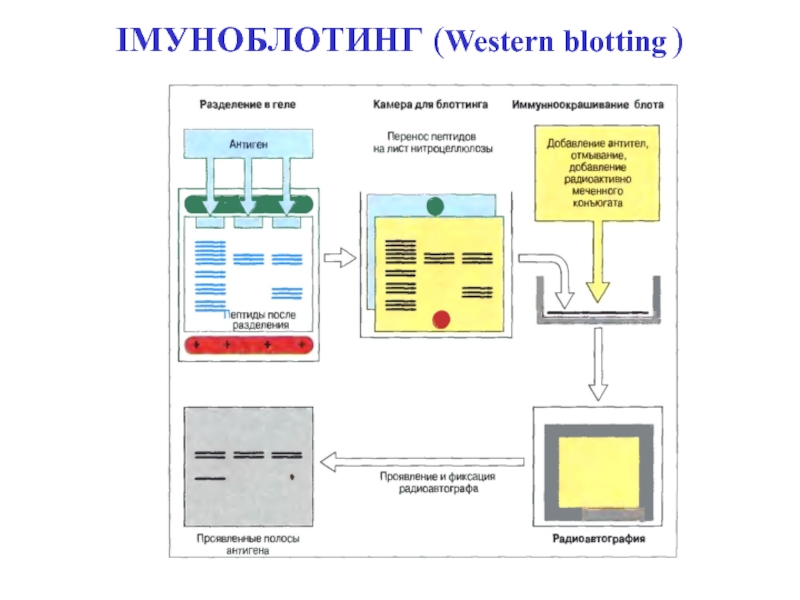
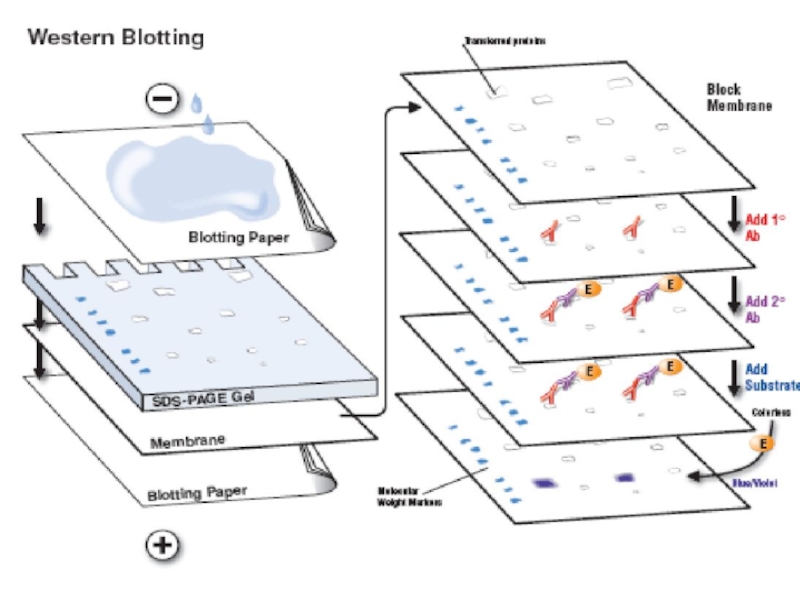
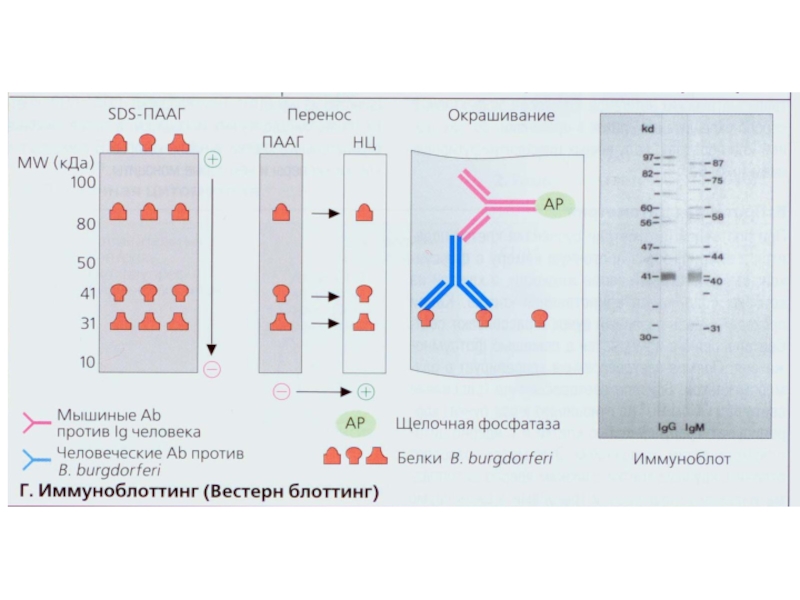
- 92. ІМУНОБЛОТИНГ (Western blotting )
- 93. Слайд 93
- 94. ВІЗУАЛІЗАЦІЯ
- 95. Western blotting is used to identify antibodies
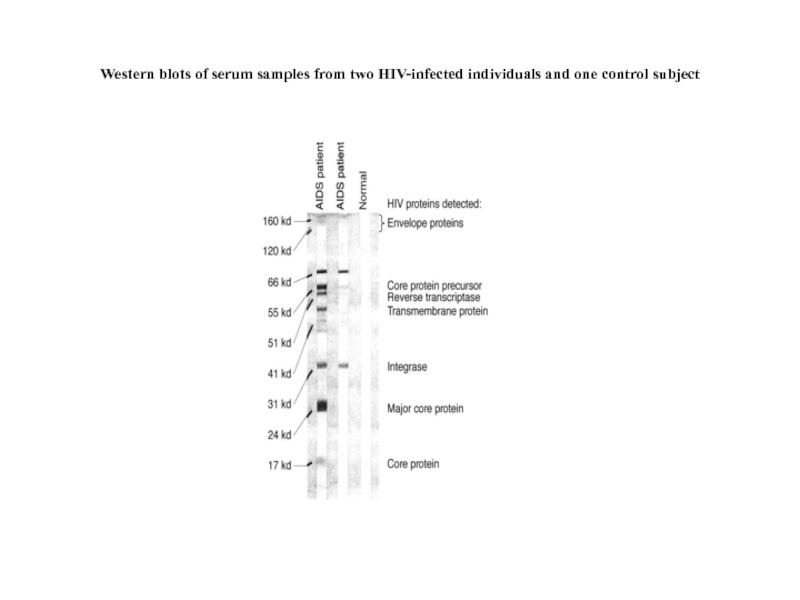
- 96. Western blots of serum samples from two HIV-infected individuals and one control subject
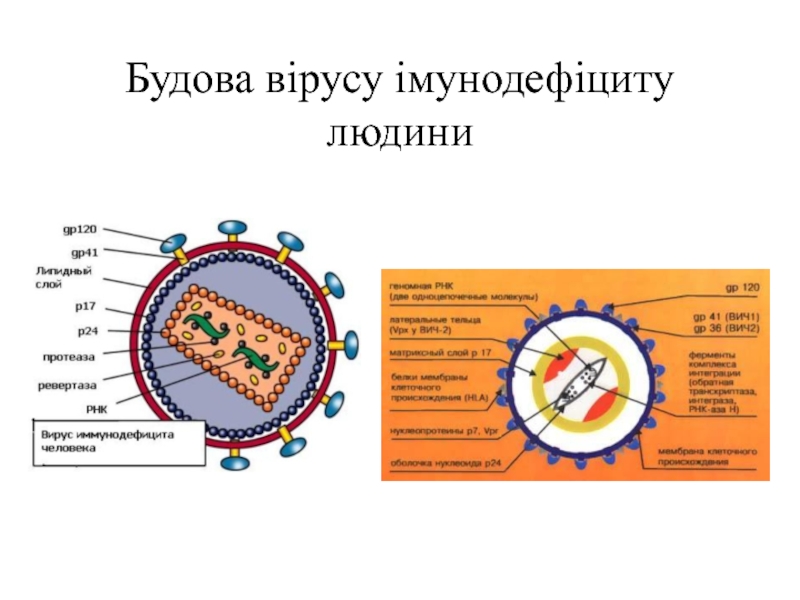
- 97. Будова вірусу імунодефіциту людини
- 98. No bands presentNegativeBands at either p31 OR
- 99. Люмінесценцією називають природне світіння, що супроводжує ряд
- 100. Використання хемілюмінесцентних підходів в імуно - блот
- 101. Слайд 101
- 102. Слайд 102
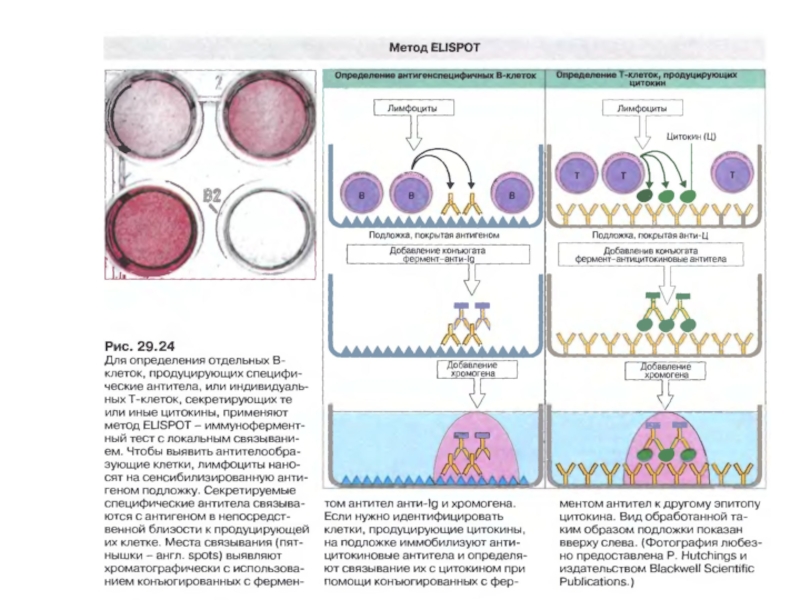
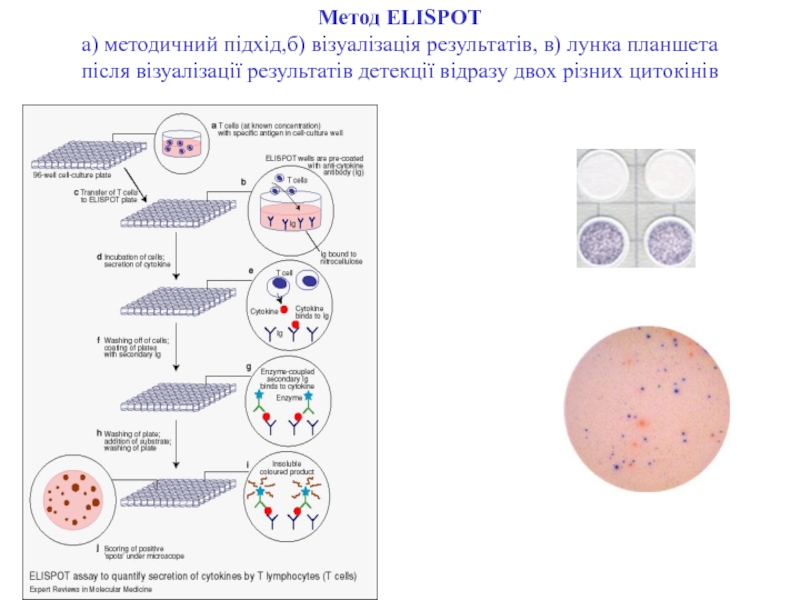
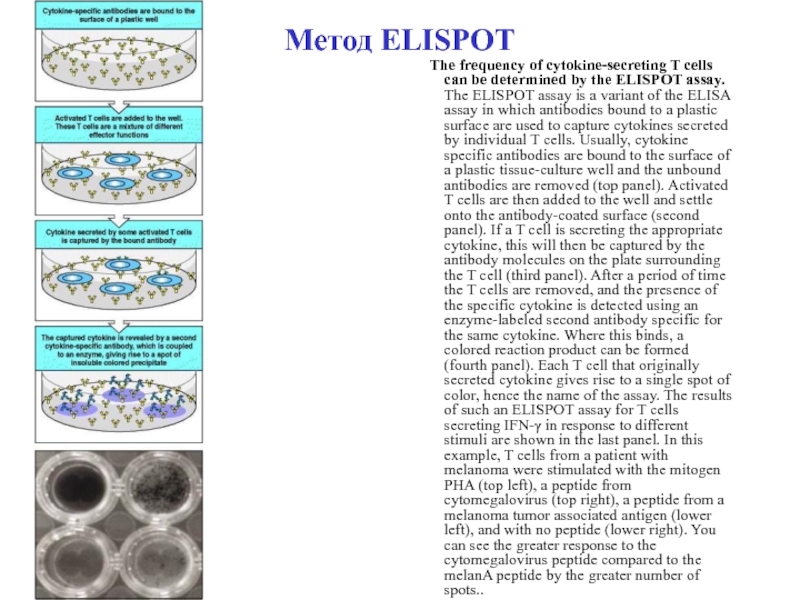
- 103. Метод ELISPOT а) методичний підхід,б) візуалізація
- 104. Метод ELISPOT The frequency of cytokine-secreting
- 105. Слайд 105
- 106. Скачать презентанцию
Слайды и текст этой презентации
Слайд 6 (1) хімічна реакція першого порядку [ АГ ] +
[ АТ ] [АГАТ
] АГ – вільний антиген; АТ – вільне антитіло; АГАТ – комплекс антиген-антитіло; κ1 - константа швидкості асоціації; κ2 - константа швидкості дисоціації комплексу антиген-антитіло (АГАТ) V1 = k1 ·[АГ] · [АТ] V2= k2 · [АГАТ] За умов рівноваги, коли V1 = V2 , можна записати: k1· [АГ][АТ] = k2·[АГАТ] Константа афінності (2)=
=
, М-1 або л/моль
Слайд 8Kd=1/ Ka - константа дисоціації;
Ka>105M-1 - cпецифічне зв′язування;
Ka>108M-1 -високоспецифічне зв′язування;
Ka
- R T ln Ka, де R- газова постійна;T- абсолютна температура (Кельвін); Δ F - зміна вільної енергії взаємодії АГ-АТ.Слайд 9 (1) хімічна реакція першого порядку [ АГ ] +
[ АТ ] [АГАТ
] АГ – вільний антиген; АТ – вільне антитіло; АГАТ – комплекс антиген-антитіло; κ1 - константа швидкості асоціації; κ2 - константа швидкості дисоціації комплексу антиген-антитіло (АГАТ) V1 = k1 ·[АГ] · [АТ] V2= k2 · [АГАТ] За умов рівноваги, коли V1 = V2 , можна записати: k1· [АГ][АТ] = k2·[АГАТ] Константа афінності (2)=
=
, М-1 або л/моль
Слайд 10Кінетичні розрахунки
Згідно з (1) та (2) і системою рівнянь матеріального
балансу
[АТ]з = [АТ] +[ АГ·АТ ]
[АГ]з = [АГ] +[ АГ·АТ ] (3), де [АТ]з і [АГ]з- загальна концентрація
АТ і АГ,
[ АГ·АТ ] - концентрація зв’язаних АТ чи АГ,
[АТ] і [АГ]- концентрація вільних АТ чи АГ, одержуємо (4)
[ АГ·АТ ] = ка [АТ]з [АГ] / 1+ ка [АГ]
За умови - [АГ]з >> [АТ]з , отримуємо (5)
[ АГ·АТ ]=
ка [АТ]з [АГ]з / 1+ ка [АГ]з - аналог рівняння Міхаеліса-Ментен;
при високих концентраціях [АГ]з
[АГ·АТ] = [АТ]з – концентрація комплексу спрямована до загальної концентрації антитіл (графік).
Слайд 11При розрахунку Ка визначають таку концентрацію антигену [АГ]'з , при
якій половина антитіл знаходиться у вигляді комплексу з антигеном [АГ·АТ]
= [АТ]з /2 . Враховуючи (3) і (4), отримуємо (6): [АГ]з'=1/ ка +[АТ]з/2Слайд 13Рівняння Скетчарда: B - концентрація зв'язаного антигену; F - концентрація вільного антигену;
n - кількість центрів зв'язування антитіл
[АГ·АТ] /
[АГ]= ка [АТ]з - ка[АГ·АТ] = = ка([АТ]з-[АГ·АТ]) - згідно з рівняннями 1, 2, 5
Слайд 18Методи імунохімічного аналізу
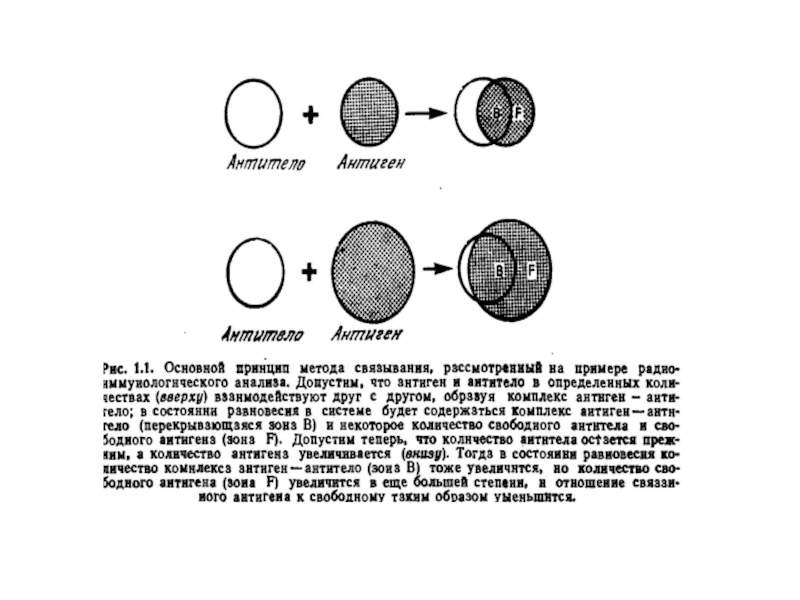
Прямі (безпосередні) методи визначення реакції антиген-антитіло. Комплекси, що
при цьому утворюються, ідентифікують візуально або за допомогою простих оптичних
приладів. До таких методів належать преципітація в розчині, гелі, аглютинація бактерій, аглютинація еритроцитів вірусами, антитілами (пряма гемаглютинація).Реакції пасивної аглютинації (тобто аглютинації частинок, з поверхнею яких зв’язані АТ чи АГ). Це - методи пасивної (непрямої) гемаглютинації, латексаглютинації, коаглютинації.
Індикаторні методи, засновані на використанні різних міток (ізотопних, флуоресцентних, парамагнітних, ферментних), для виявлення реакції антиген-антитіло. Це - імуноферментний, імунофлуоресцентний, радіоімунологічний аналіз, імунохроматографічний аналіз і т.д.
Метод імуносенсорів та метод генного зондування (Fish method).
Слайд 20Експериментальні підходи, які використовуються в імунохімічних методах
Методичні підходи, що засновані
на зміні фізико-хімічних властивостей антигенів (антитіл) під час утворення комплексу:
зміна флуоресценції, зміна ступеня поляризації флуоресценції і т.д.Розділення вільного і зв'язаного антигену, яке відбувається з залученням методів фракційного осадження (центрифугування), рівноважного діалізу, гель-фільтрації.
Слайд 21Рівноважний діаліз. Визначення афінності антитіл методом рівноважного діалізу κа =В
/ F · (n –B)
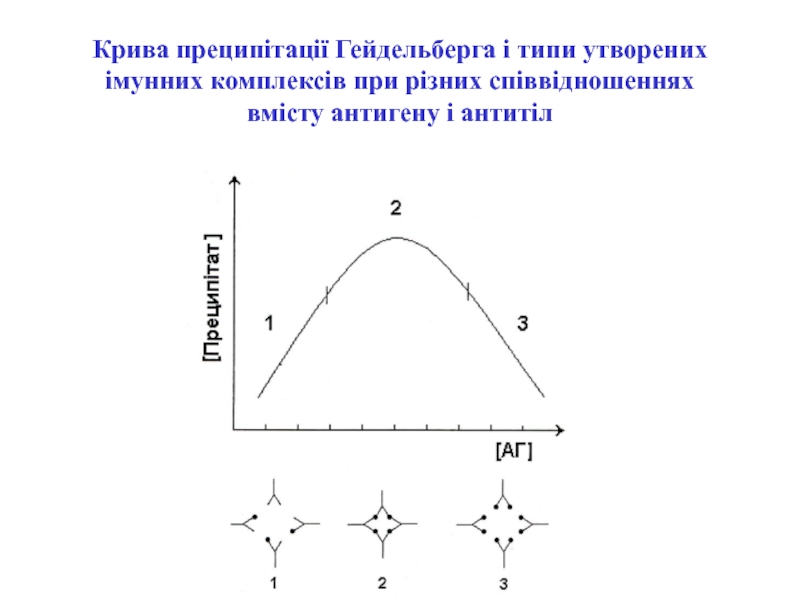
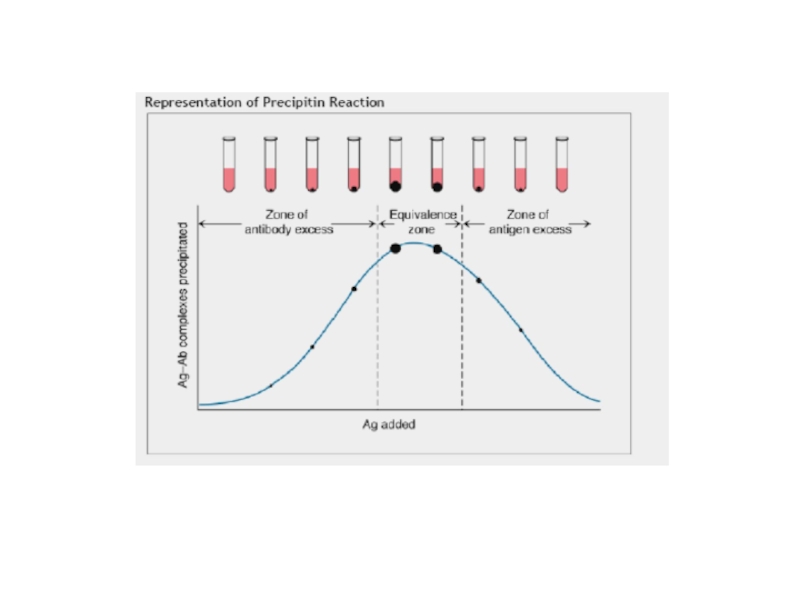
Слайд 25Крива преципітації Гейдельберга і типи утворених імунних комплексів при різних
співвідношеннях вмісту антигену і антитіл
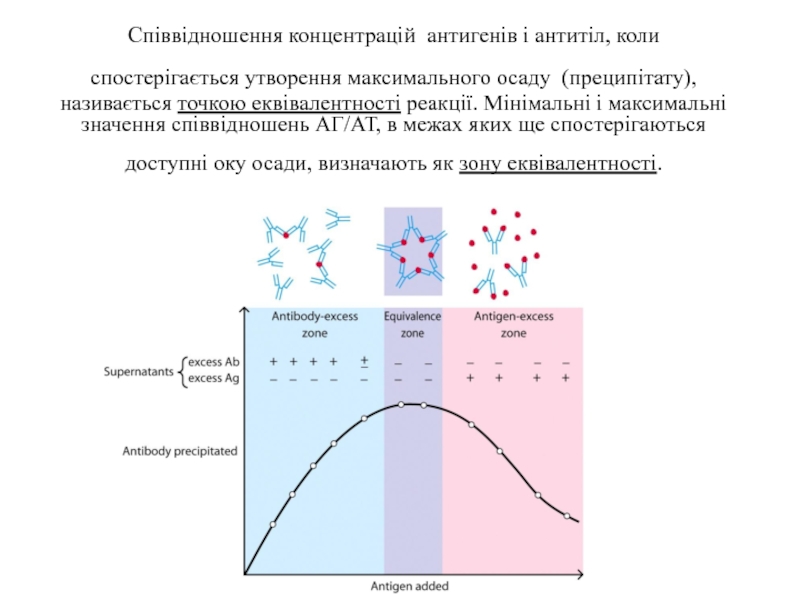
Слайд 26Співвідношення концентрацій антигенів і антитіл, коли спостерігається утворення максимального осаду
(преципітату), називається точкою еквівалентності реакції. Мінімальні і максимальні значення співвідношень
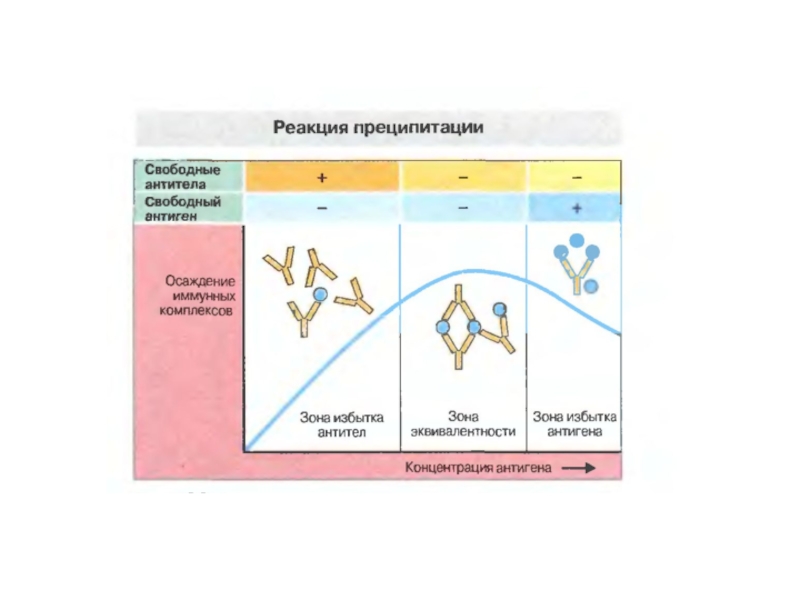
АГ/АТ, в межах яких ще спостерігаються доступні оку осади, визначають як зону еквівалентності.Слайд 30Реакції аглютинації – осадження антитілами корпускулярних антигенів (клітин, вірусних часточок
і т.д), реакції преципітації- осадження молекул, що мають антигенні властивості. Реакції
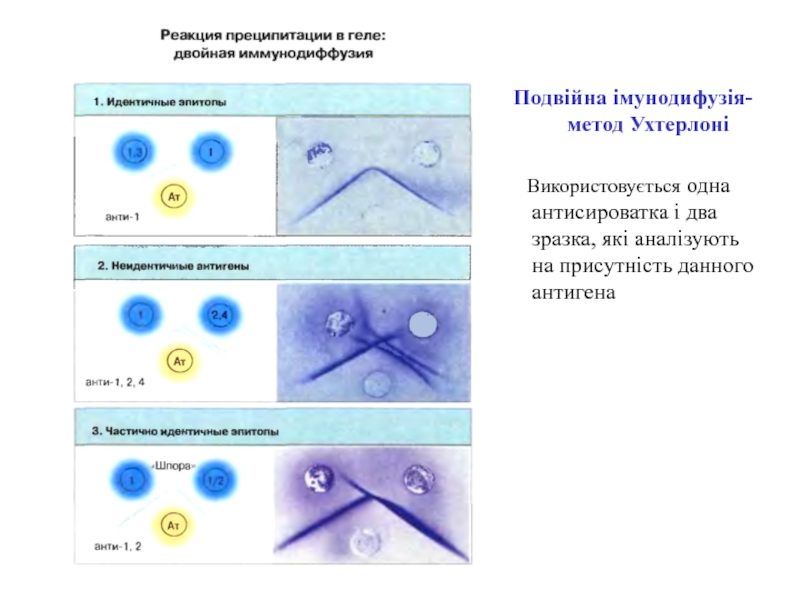
преципітації використовують для високодисперсних антигенів, які визначаються окремими молекулами. На відміну від реакцій аглютинації -реакція утворення осаду в реакції преципітації йде досить повільно, сам преципітат має нижчу щільність і може з часом дисоціювати.Слайд 35Подвійна імунодифузія-метод Ухтерлоні
Використовується одна антисироватка і два
зразка, які аналізують на присутність данного антигена
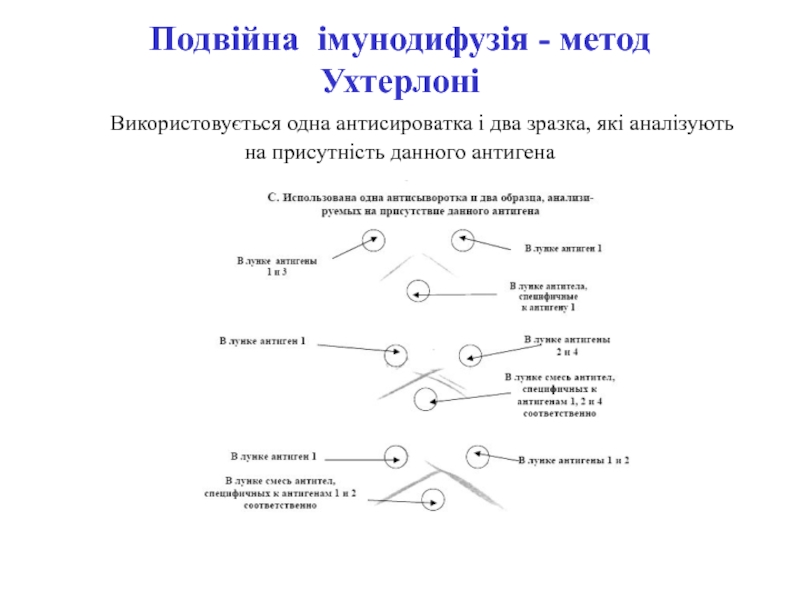
Слайд 36Подвійна імунодифузія - метод Ухтерлоні Використовується одна антисироватка
і два зразка, які аналізують на присутність данного антигена
Слайд 49РІА
радіоімунний аналіз
Roger Guillemin Andrew
V. Schally
Rosalyn YalowThe Nobel Prize in Physiology or Medicine 1977 was divided, one half jointly to Roger Guillemin and Andrew V. Schally "for their discoveries concerning the peptide hormone production of the brain" and the other half to Rosalyn Yalow "for the development of radioimmunoassays of peptide hormones".
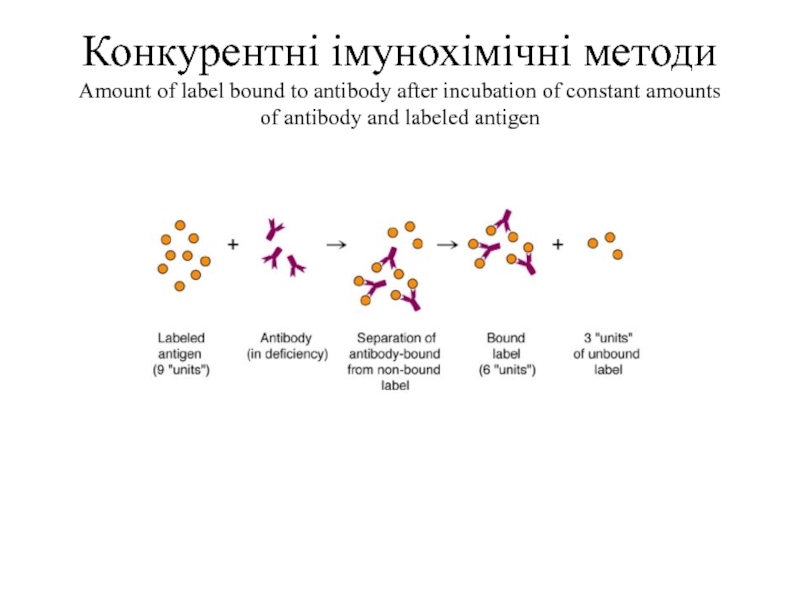
Слайд 50Конкурентні імунохімічні методи Amount of label bound to antibody after incubation
of constant amounts of antibody and labeled antigen
Слайд 51РІА
радіоімунний аналіз
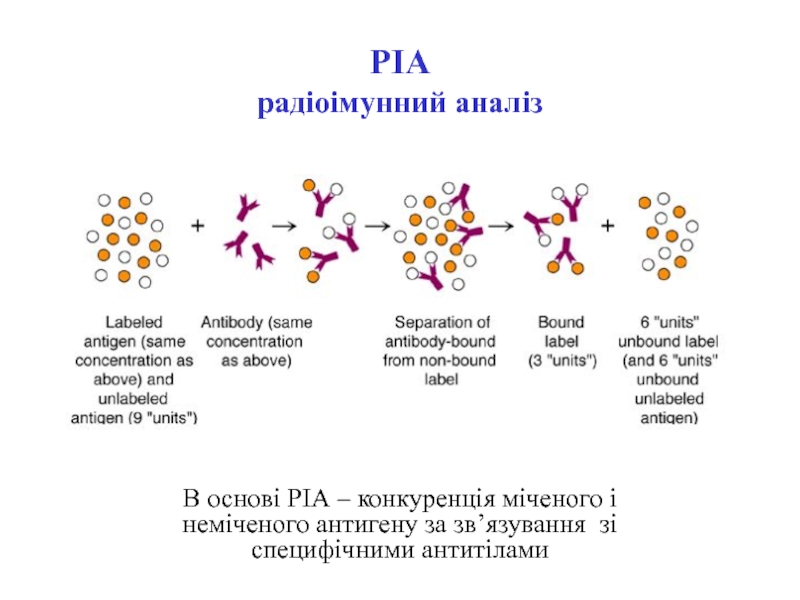
В основі РІА – конкуренція міченого і неміченого антигену
за зв’язування зі специфічними антитілами
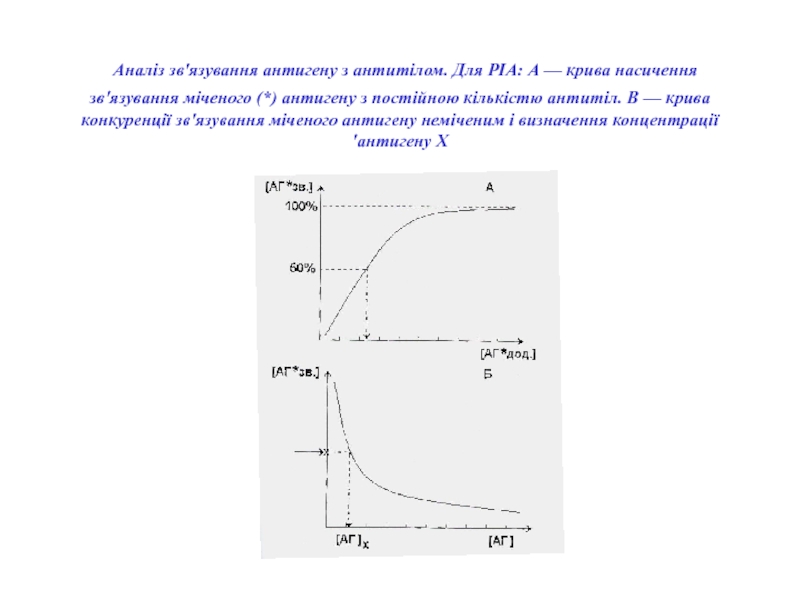
Слайд 52 Аналіз зв'язування антигену з антитілом. Для РІА: А —
крива насичення зв'язування міченого (*) антигену з постійною кількістю антитіл.
В — крива конкуренції зв'язування міченого антигену неміченим і визначення концентрації 'антигену XСлайд 56В - рівень зв’язаного в результаті реакції АГ-АТ міченого 125І-АГ; В0
- загальний рівень радіоактивно-міченого 125І-АГ, внесений в пробірку Естріол – стероїдний
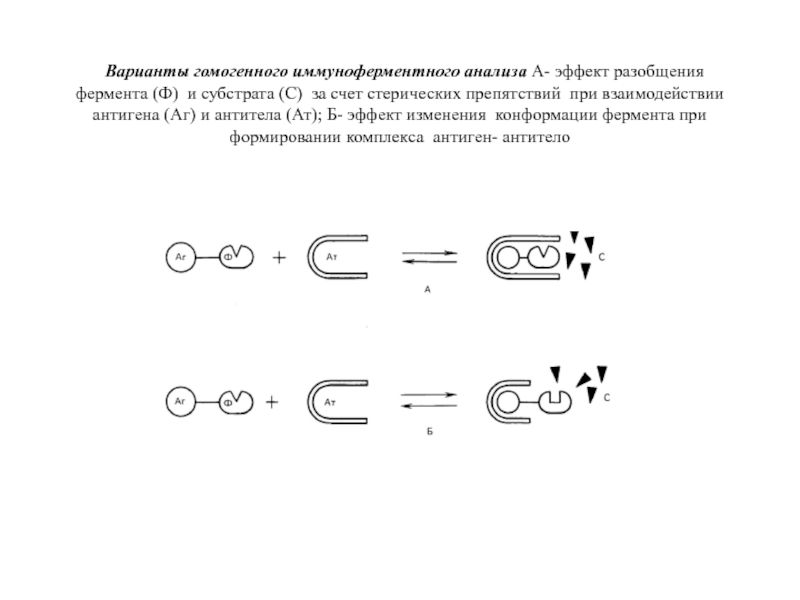
гормон, різкі зміни рівня якого при вагітності можуть свідчити про порушення у розвитку плодуСлайд 63 Варианты гомогенного иммуноферментного анализа А- эффект разобщения фермента (Ф)
и субстрата (С) за счет стерических препятствий при взаимодействии антигена
(Аг) и антитела (Ат); Б- эффект изменения конформации фермента при формировании комплекса антиген- антителоСлайд 65ОСОБЛИВОСТІ ІМУНОФЕРМЕНТНОГО АНАЛІЗУ
Імуносорбенти
Твердофазні носії
Імобілізація антигенів чи антитіл на твердій фазі
Ферменти
і субстрати
Кон’югати та їх створення
Слайд 66ОСОБЛИВОСТІ ІМУНОФЕРМЕНТНОГО АНАЛІЗУ
Ферменти і субстрати
Пероксидаза хрону (ПХ)-Нorse radish peroxidase (HRP)-субстрат
при фотометрії -тетраметилбензидин
( англ.TMB)
Лужна фосфатаза – субстрат при фотометрії
– паранітрофенілфосфатГалактозидаза-субстрат при фотометрії –нітрофенілгалактозид
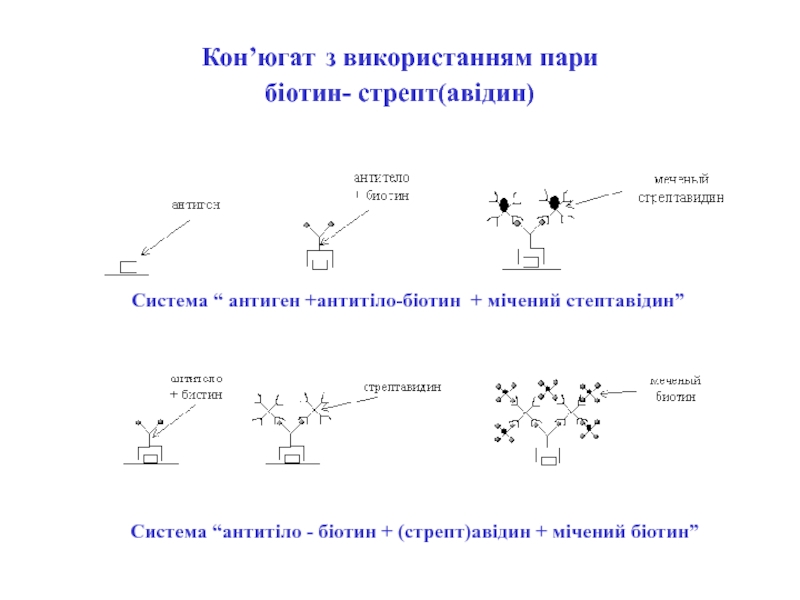
Слайд 67Кон’югат з використанням пари
біотин- стрепт(авідин)
Система “антитіло - біотин +
(стрепт)авідин + мічений біотин”
Система “ антиген +антитіло-біотин + мічений стептавідин”
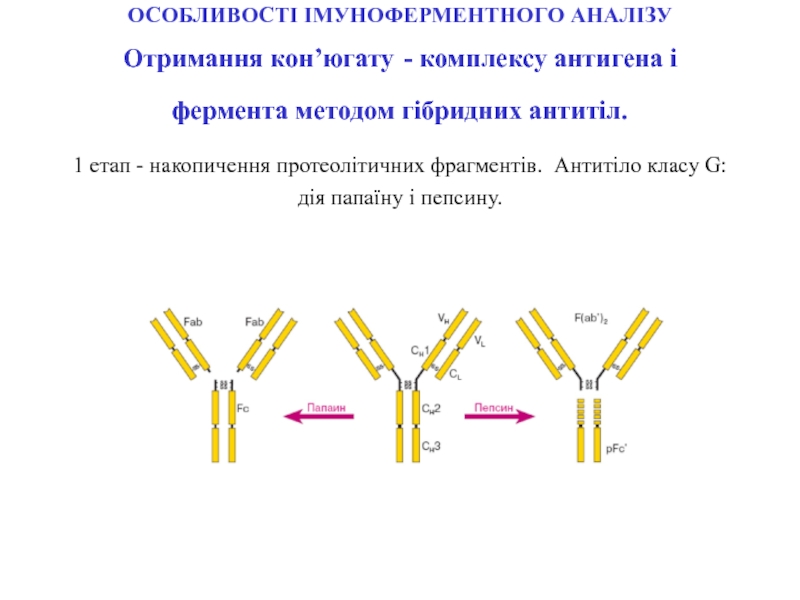
Слайд 69ОСОБЛИВОСТІ ІМУНОФЕРМЕНТНОГО АНАЛІЗУ Отримання кон’югату - комплексу антигена і фермента
методом гібридних антитіл. 1 етап - накопичення протеолітичних фрагментів. Антитіло
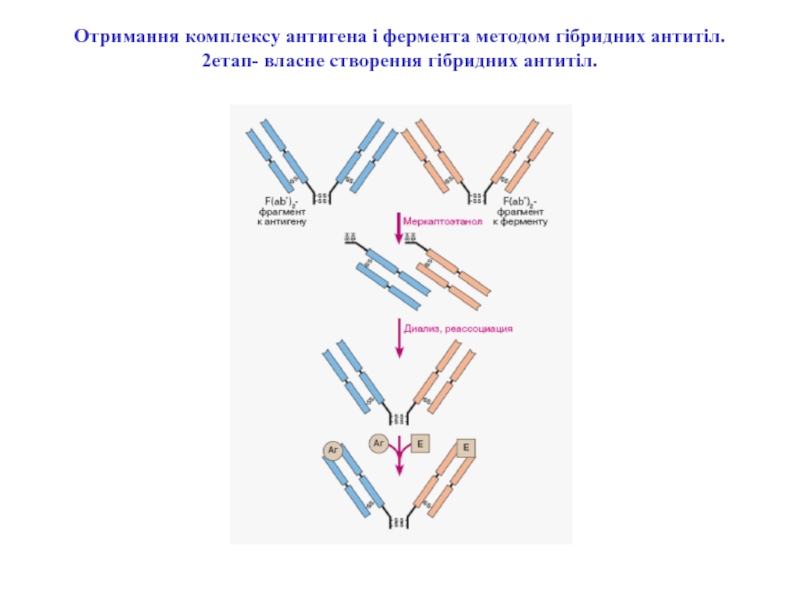
класу G: дія папаїну і пепсину.Слайд 70Отримання комплексу антигена і фермента методом гібридних антитіл. 2етап- власне
створення гібридних антитіл.
Слайд 76ELISА-Enzyme-Linked ImmunoSorbent Assay
Сорбційний імуноферментний аналіз (1) непрямий метод
What you need
to do the assay
Purified antigen (if you want to detect
or quantify antibody). Purified antibody (if you want to detect or quantify antigen).
Standard solutions (positive and negative controls).
Sample to be tested.
Microtiter dishes: plastic trays with small wells in which the assay is done.
Wash fluid (buffer).
Enzyme-labeled antibody and enzyme substrate.
ELISA reader (spectrophotometer) for quantitative measurements.
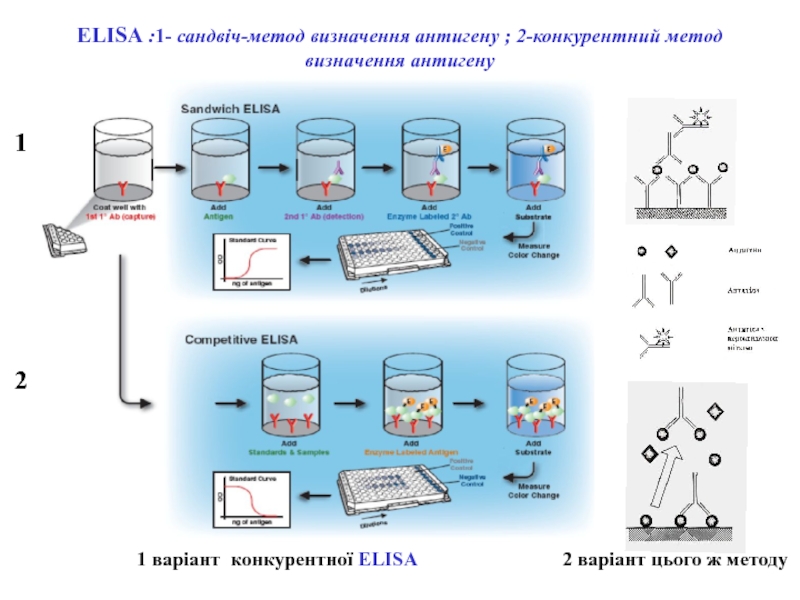
Слайд 78ELISA :1- сандвіч-метод визначення антигену ; 2-конкурентний метод визначення антигену
1
варіант конкурентної ELISA
2 варіант цього ж методу
1
2
Слайд 80ELISA Activity
An HIV ELISA, sometimes called an HIV enzyme immunoassay
(EIA) is the first and most basic test to determine
if an individual is positive for a selected pathogen, such as HIV. The test is performed in a 8 cm x 12 cm plastic plate which contains an 8 x 12 matrix of 96 wells, each of which are about 1 cm high and 0.7 cm in diameter. The next page illustrates how an HIV ELISA is performed.Plate ELISA
Слайд 81The ELISA Method
Partially purified, inactivated HIV antigens pre-coated onto an
ELISA
plate
Patient serum which contains antibodies. If the patient
is HIV+, then this serum will contain antibodies to HIV, and those antibodies will bind to the HIV antigens on the plate. Anti-human immunoglobulin coupled to an enzyme. This is the second antibody, and it binds to human antibodies.
Chromogen or substrate which changes color when cleaved by the enzyme attached to the second antibody.
Слайд 83
Above is ELISA data from three patients. Numbers are expressed
as optical density at 450 nm. The cutoff value indicating
a positive result is 0.500. Optical densities of 0.300 to 0.499 are indeterminate and need to be retested. Values below 0.300 are considered to be negative. In most cases, a patient will be retested if the serum gives a positive result. If the ELISA retests are positive, the patient will then be retested by western blotting analysis ELISA Activity
ELISA data from three patients
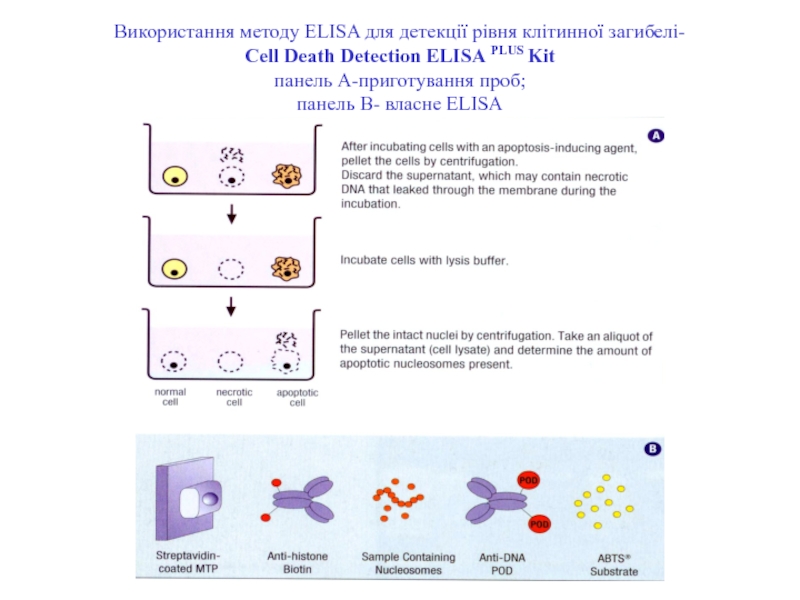
Слайд 85Використання методу ELISA для детекції рівня клітинної загибелі- Сell Death Detection
ELISA PLUS Kit
панель А-приготування проб;
панель В- власне ELISA
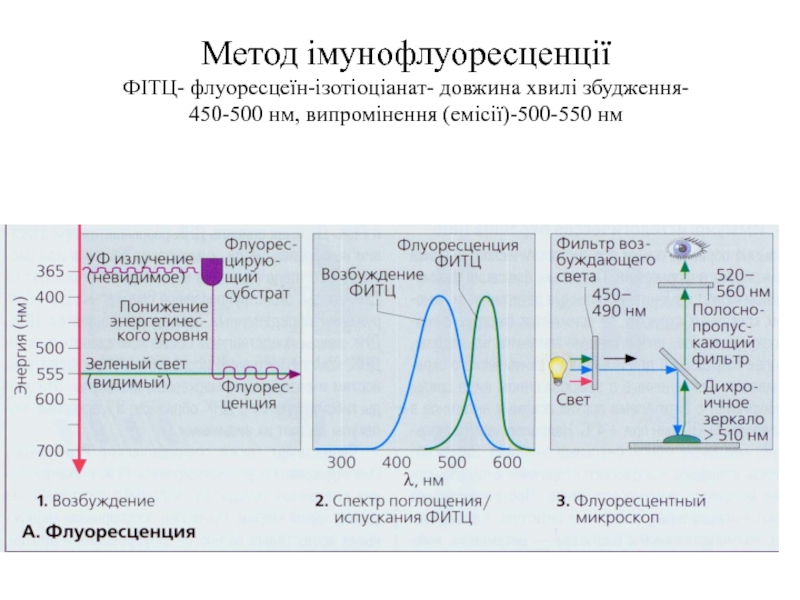
Слайд 86 Метод імунофлуоресценції ФІТЦ- флуоресцеїн-ізотіоціанат- довжина хвилі збудження- 450-500 нм, випромінення (емісії)-500-550
нм
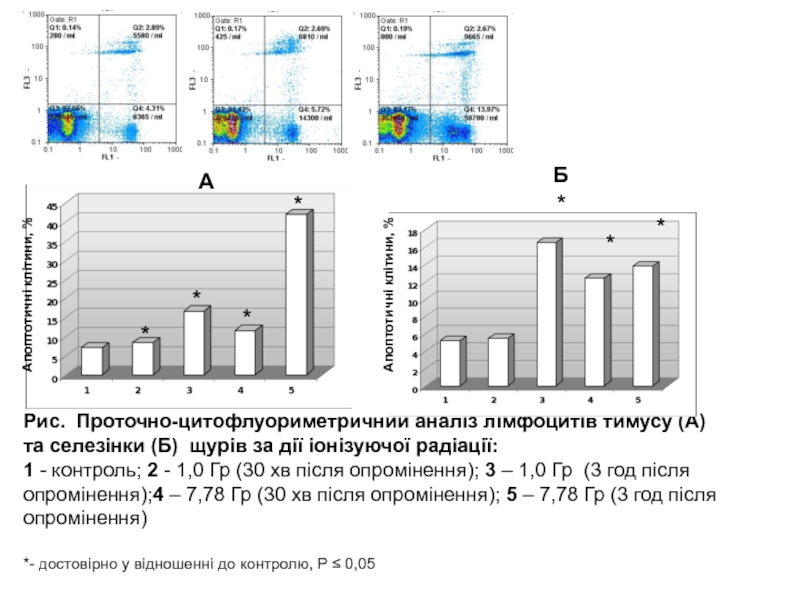
Слайд 91Рис. Проточно-цитофлуориметричний аналіз лімфоцитів тимусу (А) та селезінки (Б) щурів
за дії іонізуючої радіації:
1 - контроль; 2 - 1,0
Гр (30 хв після опромінення); 3 – 1,0 Гр (3 год після опромінення);4 – 7,78 Гр (30 хв після опромінення); 5 – 7,78 Гр (3 год після опромінення) *- достовірно у відношенні до контролю, Р 0,05
А
Б
*
*
*
*
*
*
*
Апоптотичні клітини, %
Апоптотичні клітини, %
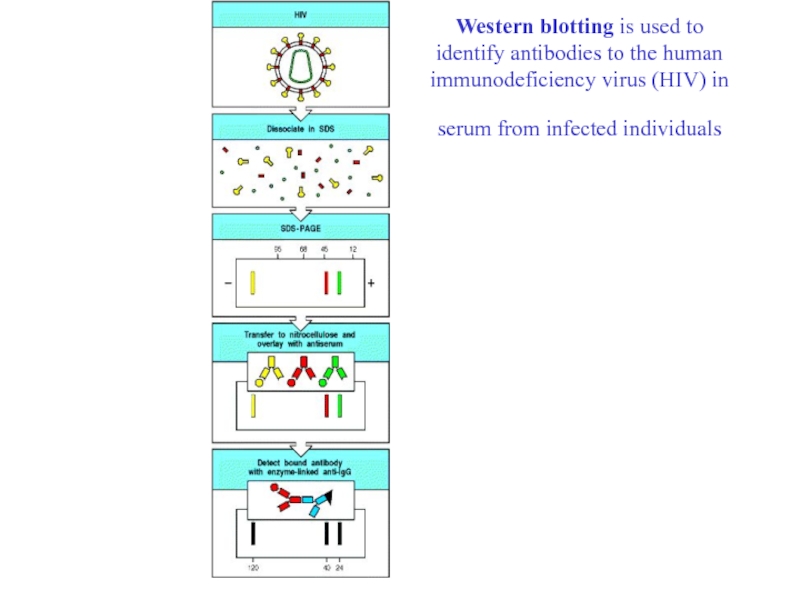
Слайд 95Western blotting is used to identify antibodies to the human
immunodeficiency virus (HIV) in serum from infected individuals
Слайд 98No bands presentNegativeBands at either p31 OR p24 AND bands
present at either gp160 OR gp120PositiveBands present, but pattern does
not meet criteria for positivityIndeterminateBand pattern Interpretation
Lane 1, HIV+ serum (positive control)
Lane 2, HIV- serum (negative control)
Lane A, Patient A
Lane B, Patient B
Lane C, Patient C
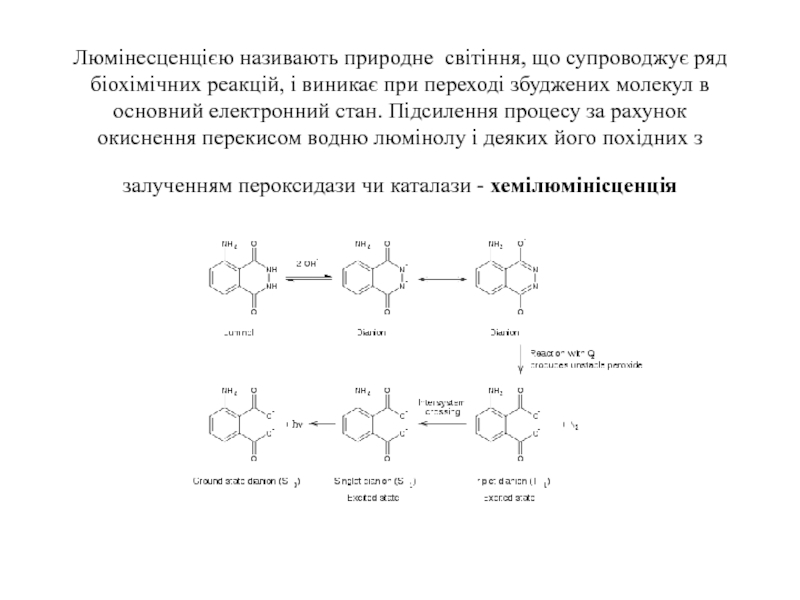
Слайд 99Люмінесценцією називають природне світіння, що супроводжує ряд біохімічних реакцій, і
виникає при переході збуджених молекул в основний електронний стан. Підсилення
процесу за рахунок окиснення перекисом водню люмінолу і деяких його похідних з залученням пероксидази чи каталази - хемілюмінісценціяСлайд 100Використання хемілюмінесцентних підходів в імуно - блот аналізі
Можливі
2 варіанти
при аналізі по прямій схемі перексид водню окислює
люмінол (+ пероксидаза);
по непрямій схемі- антиген мітиться хемілюмінесціюючою групою (люмінолом чи його похідними). Така мітка у вільному стані окислюється з виділенням світла. У разі утворення комплексу з антитілом, вона втрачає можливість окислюватись, отже світіння буде відсутнє. В цьому випадку інтенсивність сигналу пропорційна тій кількості мітки, якій антиген не дав зв’язатись з антитілом.
Насьогодні широко використовується метод посиленної хемілюмінесценції ECL- метод (Enhanced Chemiluminescence). В реакції пероксидаза хрону, коньюгована з вторинними антитілами, каталізує окиснення люмінолу до діаніону при додаванні перексиду водню , що пов’язано з емісією квантів світла. Чутливість реакції посилюється при додаванні фенольної похідної – кумарової кислоти. Візуалізація результатів відбувається з використанням рентгенівської плівки, з подальшим її проявленням.


![ВЗАЄМОДІЯ АНТИГЕН-АНТИТІЛО. МЕТОДИ ЇЇ ВИЗНАЧЕННЯ (1) хімічна реакція першого порядку [ АГ ] + [ (1) хімічна реакція першого порядку [ АГ ] + [ АТ ]](/img/tmb/4/341932/53f25da628f630d2f98e60f83a529ab4-800x.jpg)


![ВЗАЄМОДІЯ АНТИГЕН-АНТИТІЛО. МЕТОДИ ЇЇ ВИЗНАЧЕННЯ (1) хімічна реакція першого порядку [ АГ ] + [ (1) хімічна реакція першого порядку [ АГ ] + [ АТ ]](/img/tmb/4/341932/1c3b3efb6472f4716adb9dd81b9f6c90-800x.jpg)
![ВЗАЄМОДІЯ АНТИГЕН-АНТИТІЛО. МЕТОДИ ЇЇ ВИЗНАЧЕННЯ Кінетичні розрахункиЗгідно з (1) та (2) і системою рівнянь матеріального балансу Кінетичні розрахункиЗгідно з (1) та (2) і системою рівнянь матеріального балансу [АТ]з = [АТ] +[](/img/tmb/4/341932/3b5a8dc6a059f61b5dd450ffe97029f7-800x.jpg)
![ВЗАЄМОДІЯ АНТИГЕН-АНТИТІЛО. МЕТОДИ ЇЇ ВИЗНАЧЕННЯ При розрахунку Ка визначають таку концентрацію антигену [АГ]'з , при якій При розрахунку Ка визначають таку концентрацію антигену [АГ]'з , при якій половина антитіл знаходиться у вигляді](/img/thumbs/b7ee47311edcfc53511db8ce1b77d98d-800x.jpg)