Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Злокачественные опухоли женских половых органов В. М. Нечушкина, О. Н
Содержание
- 1. Злокачественные опухоли женских половых органов В. М. Нечушкина, О. Н
- 2. Злокачественные опухоли женских половых органовРак тела маткиРак шейки маткиЗлокачественные опухоли яичниковТрофобластические опухолиРак вульвыРак влагалищаРак маточной трубы
- 3. Заболеваемость женщин злокачественными новообразованиями в России (стандартизованный
- 4. Структура заболеваемости женщин злокачественными новообразованиями в России
- 5. Структура заболеваемости женщин злокачественными новообразованиями в странах
- 6. Смертность женщин от злокачественных новообразований в России
- 7. Структура смертности женщин от злокачественных новообразований в
- 8. Структура смертности женщин от злокачественных новообразований в
- 9. Злокачественные опухоли женских половых органовРак тела маткиЗлокачественные опухоли яичниковРак маточной трубыРак шейки маткиРак вульвыРак влагалищаТрофобластические опухоли
- 10. Рак шейки матки, вульвы и влагалищаВирус папилломы человекаПредраковые заболевания: CIN, VIN, VAINСкрининг
- 11. Злокачественные опухоли женских половых органовРак тела маткиЗлокачественные
- 12. Факторы рискаРак тела маткиРаннее менархеПоздняя менопаузаОтсутствие родовЗаместительная
- 13. СкринингРак тела маткиСкрининг отсутствуетРанние клинические проявленияу 85—90%
- 14. Злокачественные опухоли женских половых органовРак тела маткиЗлокачественные опухоли яичниковРак маточной трубы (
- 15. РАК ТЕЛА МАТКИ
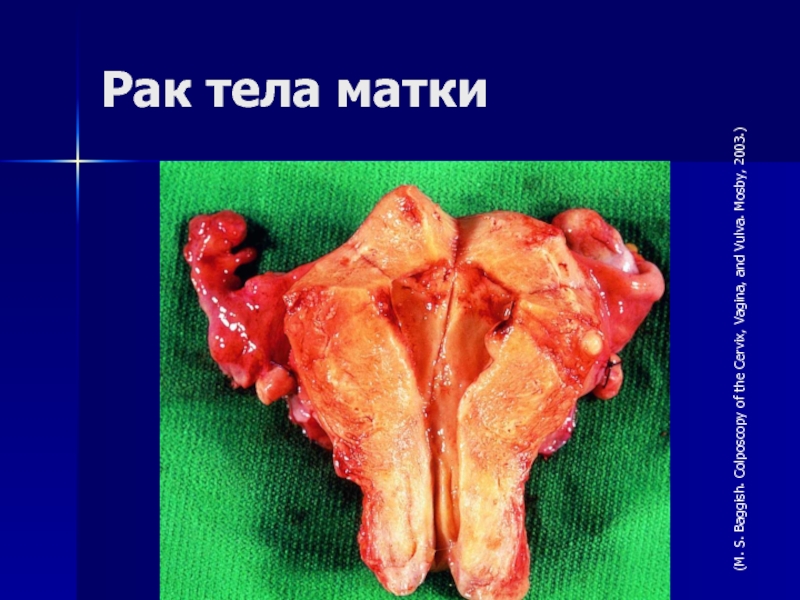
- 16. Рак тела матки(M. S. Baggish. Colposcopy of the Cervix, Vagina, and Vulva. Mosby, 2003.)
- 17. Заболеваемость раком тела матки (стандартизованный мировой показатель, все возрасты, на 100 000 женщин)
- 18. Смертность от рака тела матки (стандартизованный мировой показатель, все возрасты , на 100 000 женщин)
- 19. ЭпидемиологияСамая частая опухоль женских половых органов в
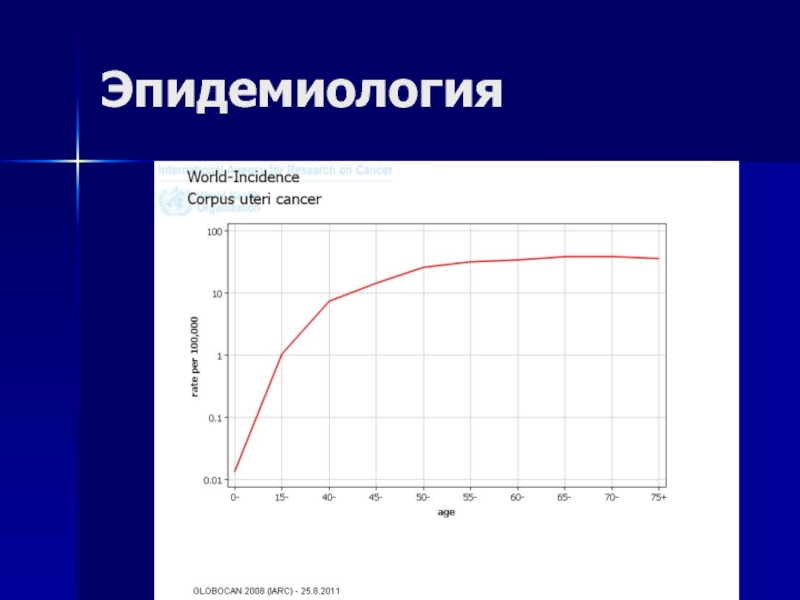
- 20. Эпидемиология
- 21. Заболеваемость в Россиивыросла на 12,9% (2005—2010)1-е место
- 22. Этиология и патогенезРак тела матки — гормонально-зависимая опухольПатогенетические варианты (Я. В. Бохман, 1972)I патогенетический вариант (60—70%)II патогенетический вариант (30—40%)
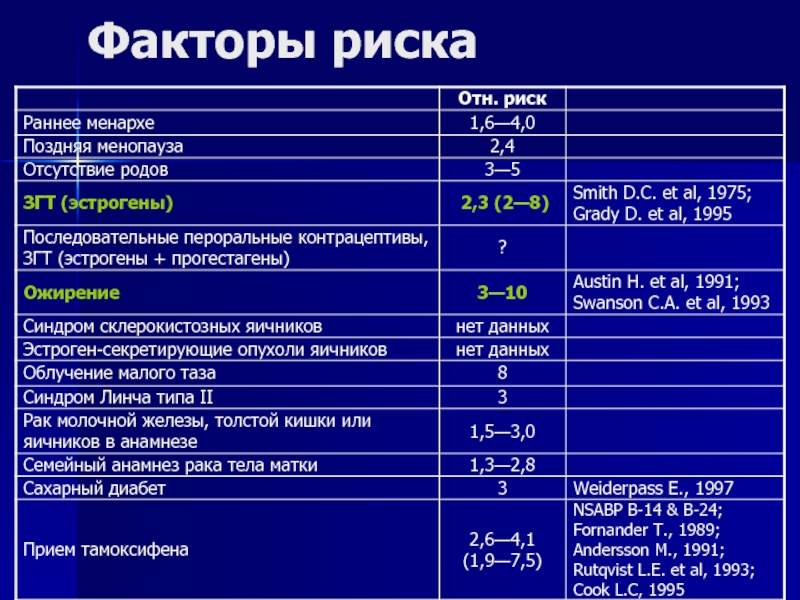
- 23. Факторы риска
- 24. Факторы рискаГиперплазия эндометрия — частота малигнизациипростая без атипии — 1%сложная без атипии — 3%простая атипическая — 8%сложная атипическая — 29%
- 25. Факторы, снижающие рискКомбинированные пероральные контрацептивы↓ риск на
- 26. СкринингУ 70—80% больных распространенность опухоли соответствует I—II стадиям
- 27. Клиническая картинаКровянистые выделения из половых путей и
- 28. Кровянистые выделения из половых путейВероятность того, что
- 29. ДиагностикаМорфологическое подтверждение диагнозаОсновной метод — аспирационная биопсия
- 30. ПатоморфологияАденокарцинома (80% больных)аденокарцинома с плоскоклеточной метаплазией (25%
- 31. ПатоморфологияПрогностически неблагоприятные гистологические типы (15% больных)плоскоклеточный раксветлоклеточный
- 32. Пути метастазированияЛимфогенныйдно матки — поясничные лимфатические узлысредняя
- 33. ОбследованиеПервичная опухоль, местное распространениефизикальное исследование (гинекологическое исследование)раздельное
- 34. ОбследованиеОтдаленные метастазыфизикальное исследование (пальпация живота, паховых и
- 35. ОбследованиеОценка общего состоянияобщий анализ крови и мочи,
- 36. Клинические стадии (FIGO, 1971)Стадия I Опухоль ограничена телом матки IA Длина
- 37. Морфологические стадии (FIGO, 1988)Стадия I IA Опухоль в пределах эндометрия IB Инвазия
- 38. Морфологические стадии (FIGO, 2009)Стадия I IA Опухоль в пределах эндометрия,
- 39. Преимущества определения морфологической стадии(FIGO Annual Report. J
- 40. Лечение I стадия(65—70%) (R. R. Barakat, M. W.
- 41. Хирургическое лечениеОперация — первый этап лечения большинства
- 42. Экстрафасциальная экстирпация матки с придаткамиПри метастазах в
- 43. Хирургическое лечениеУ 38% больных раком тела матки
- 44. I клиническая стадиятазовые лимфатические узлы — 10%поясничные
- 45. Хирургическое лечениеBoronow R.C. et al, 1984; Creasman W.T et al, 1987; Schink J.C. et al, 1987
- 46. Хирургическое лечениеМетастатически измененные лимфатические узлы на момент
- 47. Хирургическое лечениеЦели лимфаденэктомииуточнение стадииопределение тактики дальнейшего леченияулучшение выживаемости
- 48. Хирургическое лечение(J. S. Berek. Novak’s Gynecology (12th ed.). Williams & Wilkins, 1996.)
- 49. Хирургическое лечениеПоказания к лимфаденэктомиинизкодифференцированная аденокарциномаинвазия миометрия более
- 50. Хирургическое лечениеАнеуплоидия повышает риск на 1 уровеньFuller A.F., Jr., ESGO Meeting, 2005
- 51. Хирургическое лечениеFuller A.F., Jr., ESGO Meeting, 2005
- 52. Лучевая терапия снижает частоту рецидивов и метастазов
- 53. Послеоперационная дистанционная лучевая терапия на область малого
- 54. Лучевая терапия как самостоятельный метод леченияпротивопоказания к
- 55. ГормонотерапияМедроксипрогестерона ацетат, мегестрола ацетат и тамоксифенПреимуществасистемное действиенизкая
- 56. Лечение II стадия(10—15%) (R. R. Barakat, M. W.
- 57. II клиническая стадиятазовые лимфатические узлы — 36%поясничные
- 58. ЛечениеРасширенная экстирпация матки с придатками, селективная поясничная лимфаденэктомия + сочетанная лучевая терапия
- 59. (N. F. Hacker. Practical Gynecologic Oncology (2nd ed.). Baltimore: Williams & Wilkins, 1994.)Хирургическое лечение
- 60. Лечение III стадия(10—15%) (R. R. Barakat, M. W.
- 61. ЛечениеИндивидуальный план леченияОперация на первом этапе обязательна,
- 62. Лечение IIIC стадия (R. R. Barakat, M. W.
- 63. ЛечениеХирургическое лечение, определение стадии, удаление метастазовРиск смерти
- 64. Лечение IV стадия(3%) (R. R. Barakat, M. W.
- 65. Лечение обычно комплексное и включает операцию, лучевую,
- 66. ГормонотерапияЭффективность при диссеминированном раке тела матки и
- 67. Химиотерапия
- 68. ХимиотерапияПри прогрессировании РТМ применяют различные комбинации препаратов
- 69. Факторы прогнозаВозрастГистологический тип опухолиСтепень дифференцировки опухолиГлубина инвазии
- 70. Факторы прогнозаСодержание рецепторов прогестерона и эстрогенов в
- 71. ЗЛОКАЧЕСТВЕННЫЕ ОПУХОЛИ ЯИЧНИКОВ
- 72. Гистогенез злокачественных опухолей яичниковОоциты — герминогенные опухоли
- 73. Заболеваемость раком яичников (стандартизованный мировой показатель, все возрасты, на 100 000 женщин)
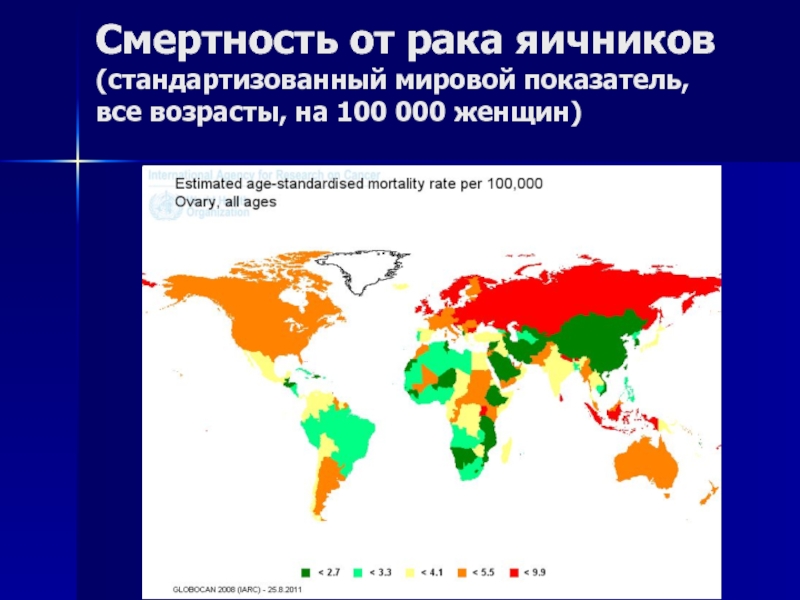
- 74. Смертность от рака яичников (стандартизованный мировой показатель, все возрасты, на 100 000 женщин)
- 75. Эпидемиология2-я по частоте опухоль женских половых органов
- 76. Эпидемиология2-я по частоте опухоль женских половых органов
- 77. Заболеваемость в Россиивыросла на 4,7% (2005—2010)Средний возраст
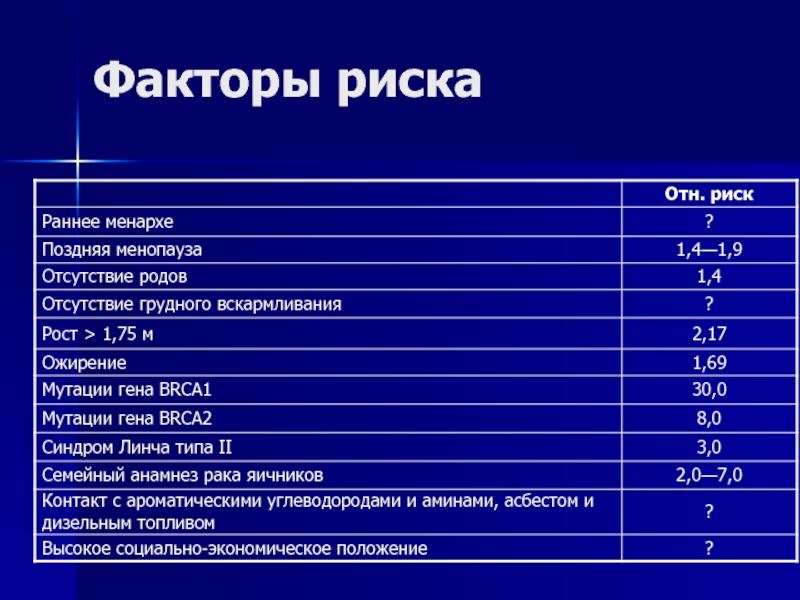
- 78. Факторы риска
- 79. Факторы рискаЧастота семейного рака яичников 5—10%Семейный рак
- 80. Факторы, снижающие рискКомбинированные пероральные контрацептивыболее эффективны препараты
- 81. СкринингНет методов, пригодных для скринингаУ 75% больных
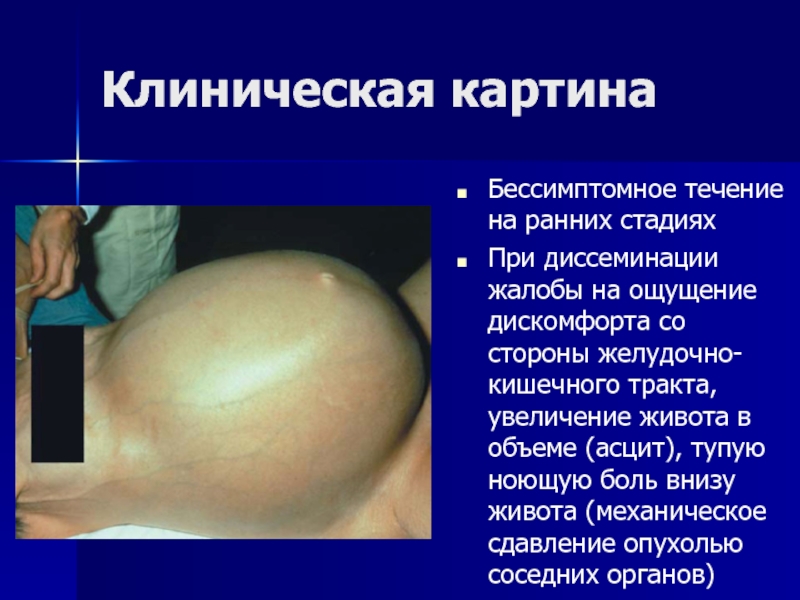
- 82. Клиническая картинаБессимптомное течение на ранних стадияхПри диссеминации
- 83. ДиагностикаМорфологическое подтверждение диагнозацитологическое исследование асцитической жидкостигистологическое исследование удаленной опухоли
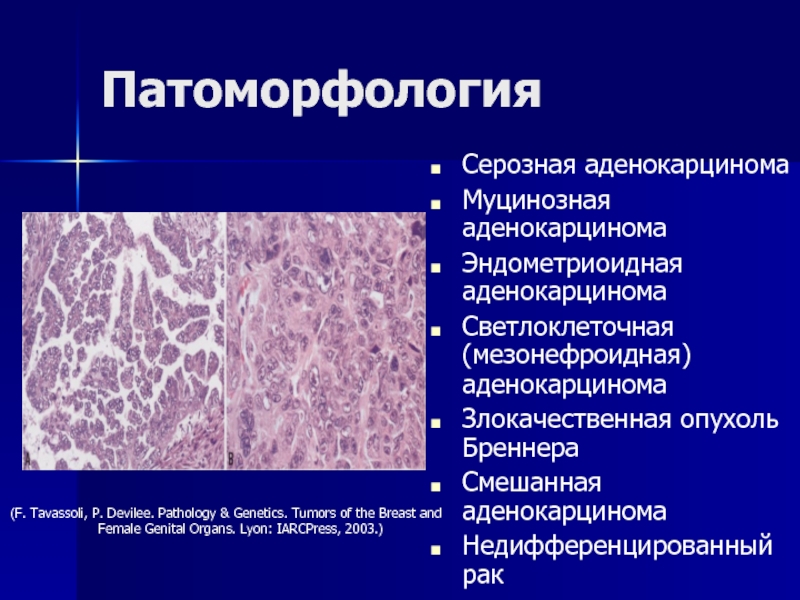
- 84. ПатоморфологияСерозная аденокарцинома Муцинозная аденокарцинома Эндометриоидная аденокарцинома Светлоклеточная
- 85. Пути метастазированияИмплантационныйЛимфогенныйпоясничные лимфатические узлытазовые лимфатические узлыпаховые лимфатические узлыРаспространение на соседние органыГематогенный
- 86. ОбследованиеПервичная опухоль, местное распространениефизикальное исследование (гинекологическое исследование)УЗИ
- 87. ОбследованиеОтдаленные метастазыфизикальное исследование (пальпация шейных лимфатических узлов)УЗИ органов брюшной полости (печени)рентгенография грудной клеткиКТпозитронно-эмиссионная томография (ПЭТ)
- 88. ОбследованиеОценка общего состоянияобщий анализ крови и мочи,
- 89. ЛечениеI этап лечения — операция:определение стадиипервичная циторедукцияцель
- 90. Осмотр париетальной и висцеральной брюшиныСмывы из брюшной
- 91. Морфологические стадии (UICC, 7-й пересмотр)
- 92. Морфологические стадии (UICC, 7-й пересмотр)а Метастазы по капсуле
- 93. ЛечениеВысокодифференцированные опухоли — наблюдениеУмеренно- и низкодифференцированные опухоли
- 94. I—II стадиипоясничные лимфатические узлы —20% Лечение(J. S. Berek. Novak’s Gynecology (12th ed.). Williams & Wilkins, 1996.)
- 95. Группировка по стадиям
- 96. Лечение (R. R. Barakat, M. W. Bevers, D.
- 97. ЛечениеХимиотерапияпаклитаксел / доцетаксел + карбоплатин3—6 курсов
- 98. Лечение
- 99. Лечение
- 100. ЛечениеОптимальная циторедукция — максимальный размер остаточной опухоли
- 101. ЛечениеНеоптимальная циторедукция — максимальный размер остаточной опухоли
- 102. ЛечениеПрогрессирование наблюдается у большинства больных раком яичников
- 103. ЛечениеОперации «second-look»нет клинических признаков заболевания после завершения
- 104. Факторы прогнозаСтадияНаличие и размер остаточной опухолиГистологический типСтепень дифференцировки опухолиПлоидность, содержание клеток в S-фазе клеточного циклаЭкспрессия HER-2/neu
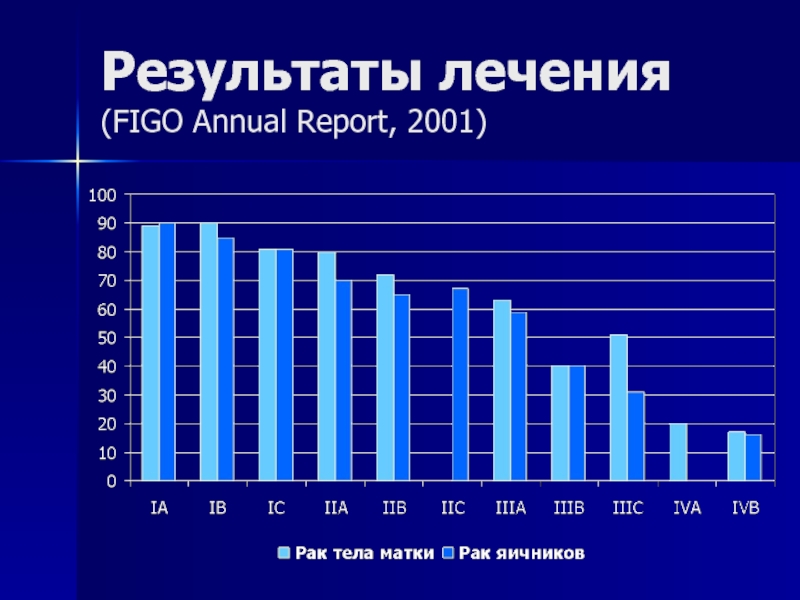
- 105. Результаты лечения (FIGO Annual Report, 2001)
- 106. Неэпителиальные опухоли яичников
- 107. Слайд 107
- 108. Герминогенные опухоли яичников20—30% опухолей яичников, 95% из
- 109. Vera M. Abeler, G. Rustin, 15th International Meeting of ESGO, Berlin, 2007Герминогенные опухоли яичников
- 110. Герминогенные опухоли яичниковСвоевременная диагностикаОрганосохраняющее лечение в детородном
- 111. Герминогенные опухоли яичников
- 112. ТРОФОБЛАСТИЧЕСКИЕ ОПУХОЛИ
- 113. ЭпидемиологияСоставляют 1% опухолей женских половых органовБольные детородного возраста
- 114. ОсобенностиДо начала 1970-х гг. почти все больные
- 115. ПатоморфологияПузырный заносполныйчастичныйИнвазивный пузырный заносХориокарциномаОпухоль плацентарного ложаЭпителиоидная трофобластическая опухоль
- 116. ПатоморфологияПоскольку диагноз трофобластической опухоли не требует морфологической
- 117. КлассификацияПузырный занос (полный и частичный)Трофобластические опухолиИнвазивный пузырный заносХориокарциномаОпухоль плацентарного ложаЭпителиоидная трофобластическая опухольНедиссеминированныеДиссеминированные Трофобластическаяболезнь
- 118. Частичный пузырный заносНаличие эмбриона или плодаТриплоидия —
- 119. Полный пузырный заносОтсутствие эмбриона или плода0,5 на
- 120. ПатогенезТрофобластические опухоли развиваются в исходе:пузырного заноса —
- 121. Диагностика и лечение пузырного заносаКровянистые выделения из
- 122. Диагностика трофобластических опухолейПлато (1, 7, 14, 21-й
- 123. Диагностика трофобластических опухолейТрофобластическая опухоль возможна у любой
- 124. Стадии трофобластических опухолей (FIGO, 2000)
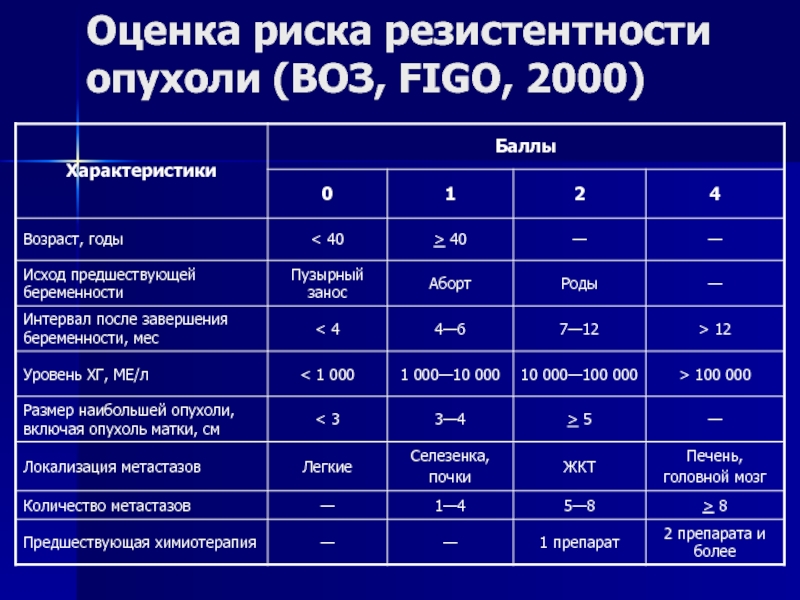
- 125. Оценка риска резистентности опухоли (ВОЗ, FIGO, 2000)
- 126. Оценка риска резистентности опухоли (FIGO, 2002)Сумма баллов
- 127. ЛечениеЛечение больных (в том числе получавших нестандартные
- 128. ЛечениеВысокая чувствительность к химиотерапии жесткое соблюдение режима лечения
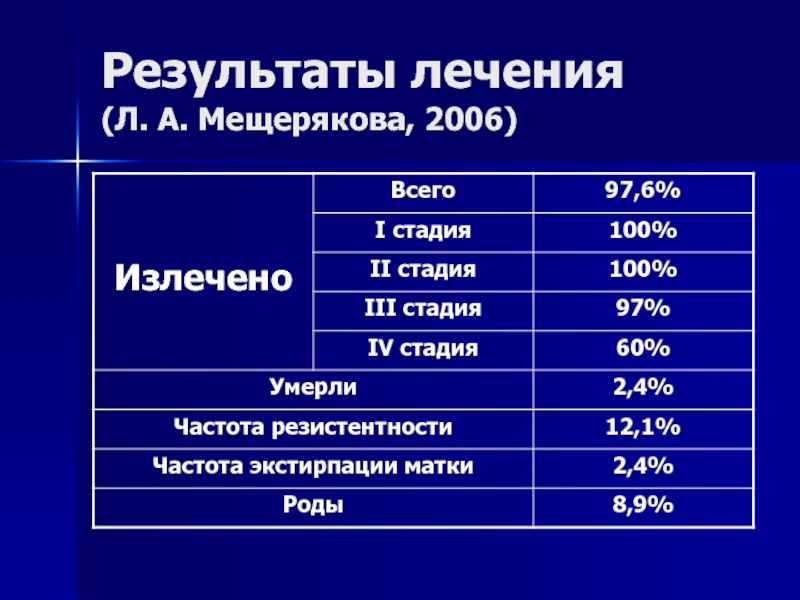
- 129. Результаты лечения (Л. А. Мещерякова, 2006)
- 130. Скачать презентанцию
Слайды и текст этой презентации
Слайд 1Злокачественные опухоли женских половых органов В. М. Нечушкина, О. Н. Стрельцова гинекологическое
отделение
НИИ клинической онкологии
РОНЦ им. Н. Н. Блохина РАМН
Слайд 2Злокачественные опухоли женских половых органов
Рак тела матки
Рак шейки матки
Злокачественные опухоли
яичников
Трофобластические опухоли
Рак вульвы
Рак влагалища
Рак маточной трубы
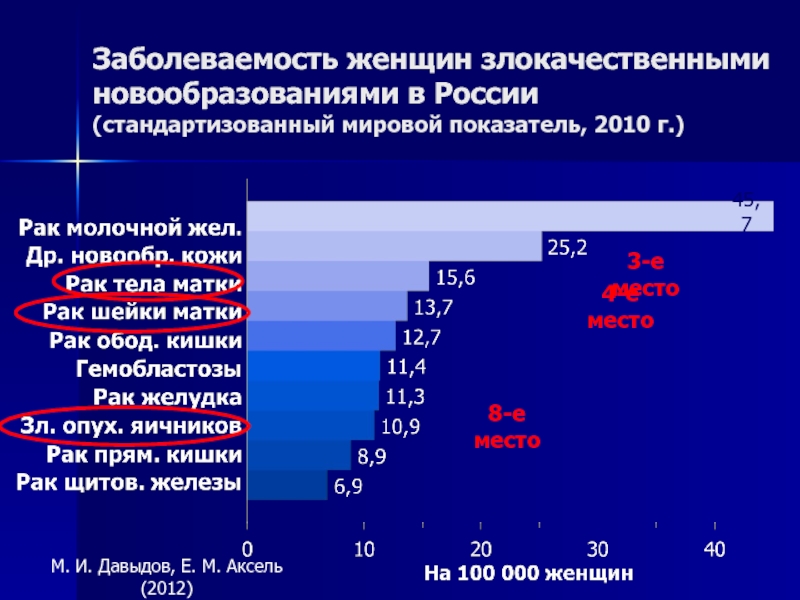
Слайд 3Заболеваемость женщин злокачественными новообразованиями в России
(стандартизованный мировой показатель, 2010 г.)
М.
И. Давыдов, Е. М. Аксель (2012)
3-е место
4-е место
8-е место
45,7
Слайд 4Структура заболеваемости женщин злокачественными новообразованиями
в России в 2010 г.
Рак тела
матки — 7,1%
Рак шейки матки — 5,3%
Злокачественные опухоли
яичников — 4,7%
М.
И. Давыдов, Е. М. Аксель (2012)17,1%
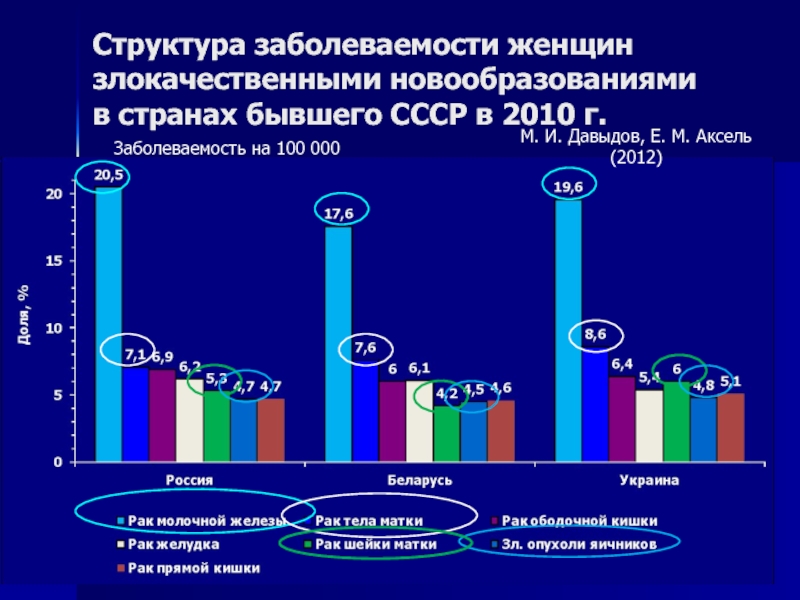
Слайд 5Структура заболеваемости женщин злокачественными новообразованиями в странах бывшего СССР в 2010
г.
М. И. Давыдов, Е. М. Аксель (2012)
Заболеваемость на 100 000
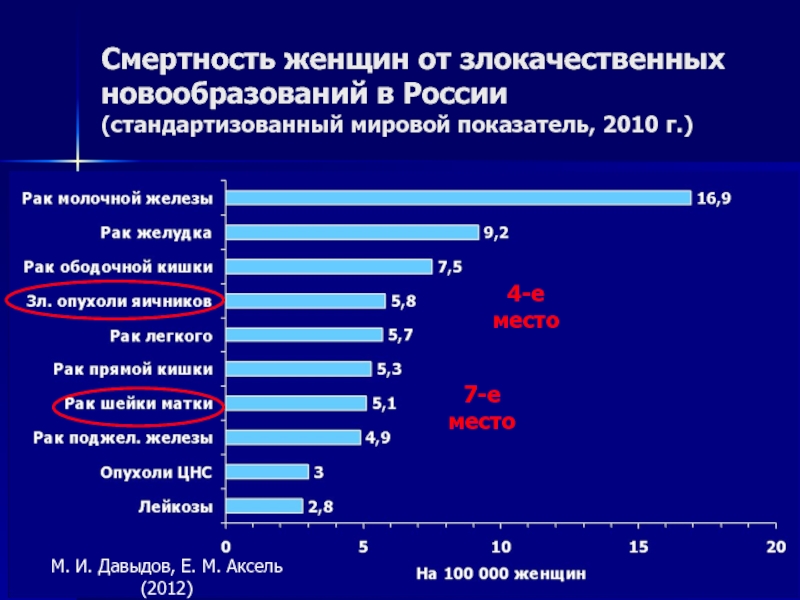
Слайд 6Смертность женщин от злокачественных новообразований в России (стандартизованный мировой показатель, 2010
г.)
М. И. Давыдов, Е. М. Аксель (2012)
4-е место
7-е место
Слайд 7Структура смертности женщин от злокачественных новообразований
в России в 2010 г.
Злокачественные
опухоли
яичников — 5,8%
Рак шейки матки — 4,6%
М. И. Давыдов, Е.
М. Аксель (2012)10,4%
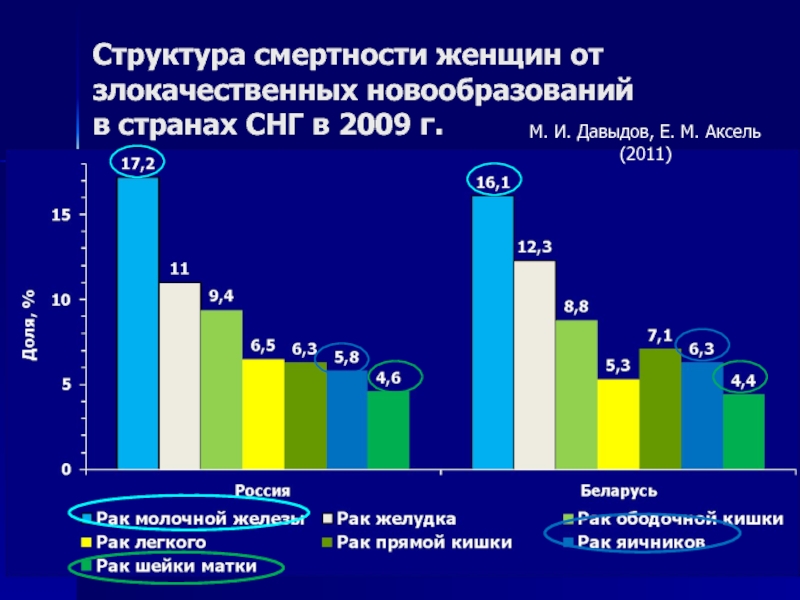
Слайд 8Структура смертности женщин от злокачественных новообразований в странах СНГ в 2009
г.
М. И. Давыдов, Е. М. Аксель (2011)
Слайд 9Злокачественные опухоли женских половых органов
Рак тела матки
Злокачественные опухоли яичников
Рак маточной
трубы
Рак шейки матки
Рак вульвы
Рак влагалища
Трофобластические опухоли
Слайд 10Рак шейки матки, вульвы и влагалища
Вирус папилломы человека
Предраковые заболевания:
CIN, VIN,
VAIN
Скрининг
Слайд 11Злокачественные опухоли женских половых органов
Рак тела матки
Злокачественные опухоли яичников
Рак маточной
трубы
Рак шейки матки
Рак вульвы (5%)
Рак влагалища (1—3%)
Трофобластические опухоли
Слайд 12Факторы риска
Рак тела матки
Раннее менархе
Поздняя менопауза
Отсутствие родов
Заместительная гормонотерапия в постменопаузе
Ожирение
Наследственность
Синдром
склерокистозных яичников
Эстрогенсекретирующие опухоли яичников
Прием тамоксифена
Рак яичников
Раннее менархе
Поздняя менопауза
Отсутствие родов и
грудного вскармливанияЗаместительная гормонотерапия в постменопаузе
Ожирение
Наследственность (BRCA1 и BRCA2)
Высокий рост
Профессиональные вредности
аром. углеводороды и амины, асбест и дизельное топливо
Высокое социально-экономическое положение
Слайд 13Скрининг
Рак тела матки
Скрининг отсутствует
Ранние клинические проявления
у 85—90% больных распространенность опухоли
соответствует I—II стадиям (FIGO)
Рак яичников
Скрининг отсутствует
Поздние клинические проявления
у 70—80% больных распространенность
опухоли соответствует III—IV стадиям (FIGO)Слайд 14Злокачественные опухоли женских половых органов
Рак тела матки
Злокачественные опухоли яичников
Рак маточной
трубы (
Слайд 17Заболеваемость раком тела матки (стандартизованный мировой показатель, все возрасты, на 100 000
женщин)
Слайд 18Смертность от рака тела матки (стандартизованный мировой показатель, все возрасты , на
100 000 женщин)
Слайд 19Эпидемиология
Самая частая опухоль женских половых органов в развитых странах
2-я по
частоте опухоль
в развивающихся странах
(после рака шейки матки)
Заболеваемость в развитых странах
почти в 10 раз выше, чем в развивающихся Слайд 21Заболеваемость в России
выросла на 12,9% (2005—2010)
1-е место среди опухолей репродуктивной
сферы
7-е место среди злокачественных опухолей
у женщин
средний возраст больных в России
62,1 годапричины роста
рост средней продолжительности жизни
распространенность ожирения, сахарного диабета
Эпидемиология
М. И. Давыдов, Е. М. Аксель (2012)
Слайд 22Этиология и патогенез
Рак тела матки — гормонально-зависимая опухоль
Патогенетические варианты
(Я. В. Бохман, 1972)
I патогенетический вариант
(60—70%)
II патогенетический вариант (30—40%)
Слайд 24Факторы риска
Гиперплазия эндометрия — частота малигнизации
простая без атипии — 1%
сложная без атипии —
3%
простая атипическая — 8%
сложная атипическая — 29%
Слайд 25Факторы, снижающие риск
Комбинированные пероральные контрацептивы
↓ риск на 11,7% в год
(Henderson
B.E. et al, 1993; Walnut Creek Contraceptive Drug Study, 1980;
Royal College of general Practitioner’s Oral Contraceptive Study, 1988)↓ риск сохраняется в течение 15 лет и более после отмены
Прием b-каротина, мононенасыщенных жирных кислот, фруктов и овощей
Физическая активность
Умеренное употребление алкоголя
Курение (в постменопаузе)
Слайд 26Скрининг
У 70—80% больных распространенность опухоли соответствует I—II стадиям (FIGO)
(Abeler V.M. et
al, 1991; Pettersson F., 1995)
Опухоль растет достаточно медленно, поэтому отсутствие
скрининга мало влияет на выживаемость (Menczer J. et al., 1995)Нет методов, пригодных для скрининга
Слайд 27Клиническая картина
Кровянистые выделения из половых путей и маточные кровотечения
(70—90% больных)
Боль
внизу живота
Гематометра
Пиометра
Менее чем у 5% больных жалобы отсутствуют
Слайд 28Кровянистые выделения из половых путей
Вероятность того, что кровотечение в постменопаузе
обусловлено раком тела матки (Hawwa Z.M., 1970)
50 лет — 9%
60
лет — 16%70 лет — 28%
80 лет и старше — 60%
Слайд 29Диагностика
Морфологическое подтверждение диагноза
Основной метод — аспирационная биопсия эндометрия / раздельное
диагностическое выскабливание матки
Гистероскопия с прицельной биопсией
(J. S. Berek. Novak’s Gynecology
(12th ed.). Williams & Wilkins, 1996.) Слайд 30Патоморфология
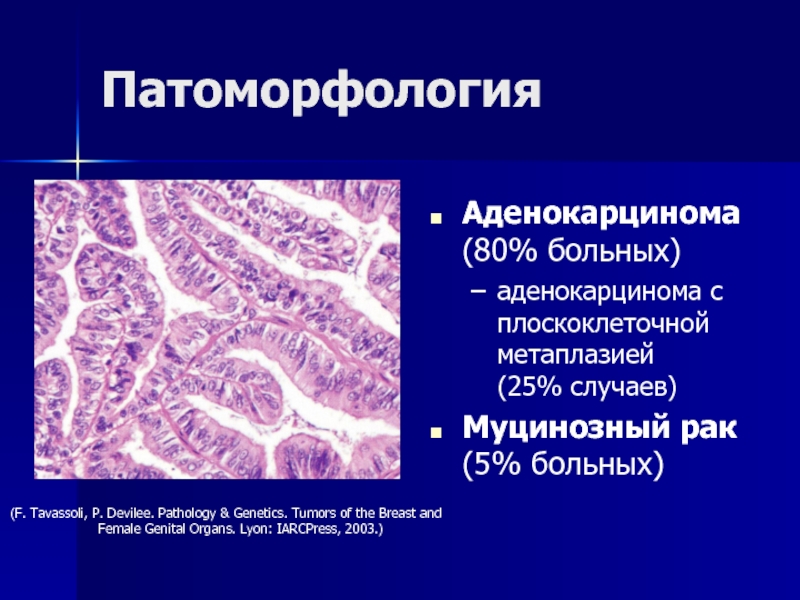
Аденокарцинома
(80% больных)
аденокарцинома с плоскоклеточной метаплазией
(25% случаев)
Муцинозный рак
(5% больных)
(F. Tavassoli, P. Devilee.
Pathology & Genetics. Tumors of the Breast and Female Genital
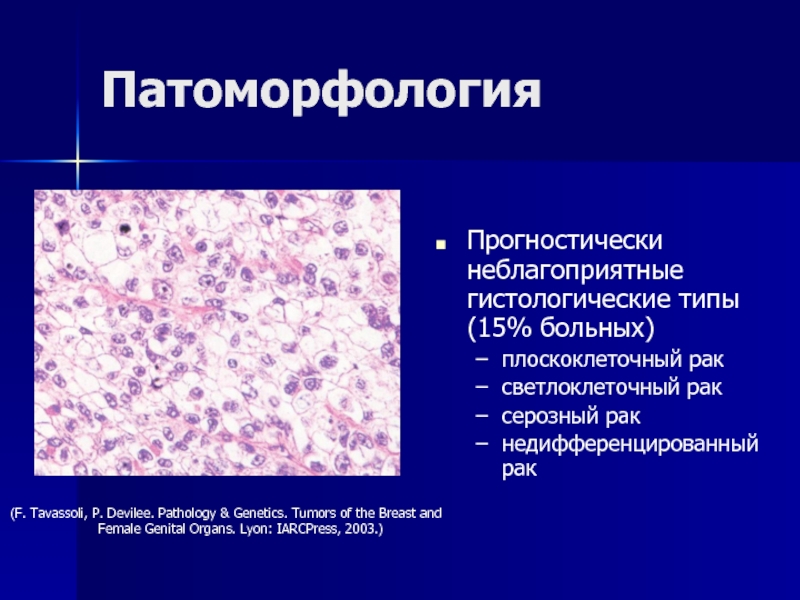
Organs. Lyon: IARCPress, 2003.)Слайд 31Патоморфология
Прогностически неблагоприятные гистологические типы
(15% больных)
плоскоклеточный рак
светлоклеточный рак
серозный рак
недифференцированный рак
(F. Tavassoli,
P. Devilee. Pathology & Genetics. Tumors of the Breast and Female
Genital Organs. Lyon: IARCPress, 2003.)Слайд 32Пути метастазирования
Лимфогенный
дно матки — поясничные лимфатические узлы
средняя и нижняя трети
тела матки —
тазовые лимфатические узлы
Имплантационный
Распространение на соседние органы
Гематогенный
легкие, печень, кости,
головной мозгСлайд 33Обследование
Первичная опухоль, местное распространение
физикальное исследование (гинекологическое исследование)
раздельное диагностическое выскабливание —
гистологический тип и степень дифференцировки
гистероскопия
кольпоскопия
УЗИ малого таза — глубина инвазии
МРТ
цистоскопия
ректороманоскопия
экскреторная
урографияРегионарное распространение
УЗИ малого таза и забрюшинного пространства
экскреторная урография
КТ
Слайд 34Обследование
Отдаленные метастазы
физикальное исследование (пальпация живота, паховых и шейных лимфатических узлов)
УЗИ
органов брюшной полости
рентгенография грудной клетки
КТ
определение уровня CA-125 в сыворотке
позитронно-эмиссионная томография
(ПЭТ)Слайд 35Обследование
Оценка общего состояния
общий анализ крови и мочи, биохимическое исследование крови,
коагулограмма
допплеровское исследование вен нижних конечностей и подвздошных вен
ЭКГ
исследование функции внешнего
дыханияСлайд 36Клинические стадии
(FIGO, 1971)
Стадия I Опухоль ограничена телом матки
IA Длина полости матки не более
8 см
IB Длина полости матки более 8 см
По степени дифференцировки выделяют:
G1 высокодифференцированный рак
G2 умереннодифференцированный рак
G3 низкодифференцированный
рак Стадия II Опухоль переходит на шейку матки, но не выходит за пределы матки
Стадия III Опухоль распространяется в пределах малого таза
Стадия IV Опухоль прорастает слизистую мочевого пузыря или прямой кишки или есть отдаленные метастазы
IVA Опухоль прорастает слизистую мочевого пузыря или прямой кишки
IVB Отдаленные метастазы
Слайд 37Морфологические стадии (FIGO, 1988)
Стадия I
IA Опухоль в пределах эндометрия
IB Инвазия миометрия менее чем
на половину его толщины
IC Инвазия миометрия более чем на половину его
толщины Стадия II
IIA Распространение на железы шейки матки
IIB Распространение на строму шейки матки
Стадия III
IIIA Прорастание серозной оболочки матки, метастазы в маточных трубах или яичниках или наличие опухолевых клеток в смывах из брюшной полости
IIIB Распространение на влагалище
IIIC Метастазы в тазовых или поясничных лимфатических узлах
Стадия IV
IVA Прорастание слизистой мочевого пузыря или прямой кишки
IVB Отдаленные метастазы, в том числе метастазы в пределах брюшной полости, а также метастазы в паховых лимфатических узлах
Слайд 38Морфологические стадии (FIGO, 2009)
Стадия I
IA Опухоль в пределах эндометрия, или инвазия миометрия менее
чем на половину его толщины
IB Инвазия миометрия на половину его толщины
и более Стадия II Распространение на строму шейки м
Стадия III
IIIA Прорастание серозной оболочки матки, метастазы в маточных трубах или яичниках
IIIB Распространение на влагалище и параметрий
IIIC Метастазы в регионарных лимфатических узлах
IIIC1 Метастазы в тазовых лимфатических узлах
IIIC2 Метастазы в поясничных лимфатических узлах
Стадия IV
IVA Прорастание слизистой мочевого пузыря или прямой кишки
IVB Отдаленные метастазы, в том числе метастазы в пределах брюшной полости, а также метастазы в паховых лимфатических узлах
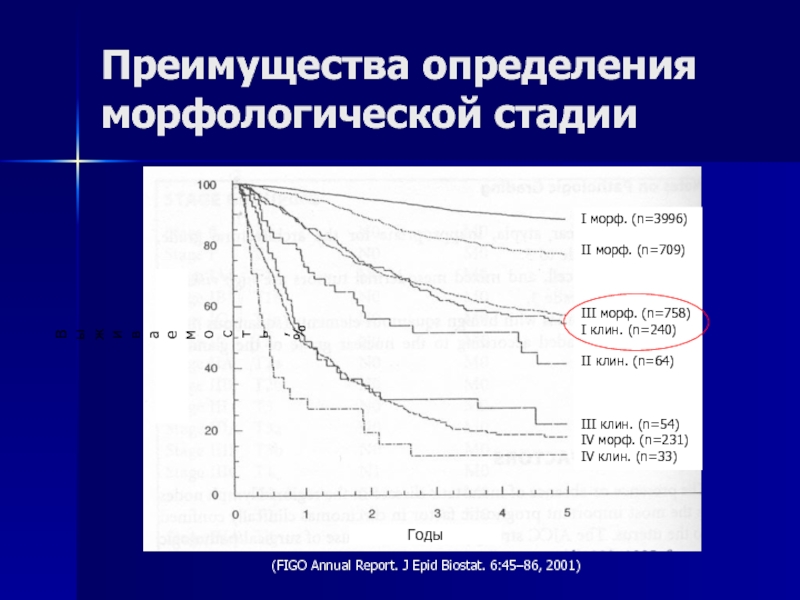
Слайд 39Преимущества определения морфологической стадии
(FIGO Annual Report. J Epid Biostat. 6:45–86,
2001)
Выживаемость, %
Годы
I морф. (n=3996)
II морф. (n=709)
III морф. (n=758)
I клин.
(n=240)II клин. (n=64)
III клин. (n=54)
IV морф. (n=231)
IV клин. (n=33)
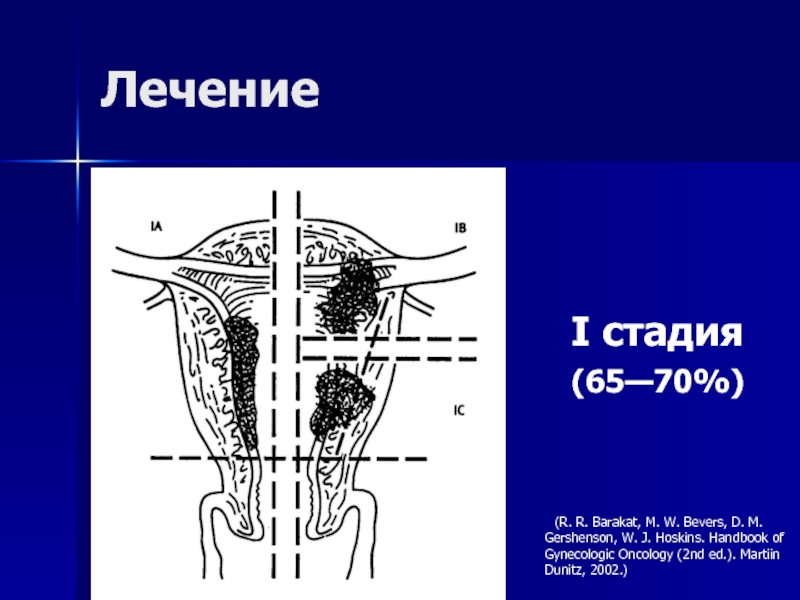
Слайд 40Лечение
I стадия
(65—70%)
(R. R. Barakat, M. W. Bevers, D. M.
Gershenson, W. J. Hoskins. Handbook of Gynecologic Oncology (2nd ed.). Martiin Dunitz,
2002.)Слайд 41Хирургическое лечение
Операция — первый этап лечения большинства больных
Отказ от операции
оправдан только в тех случаях, когда риск летального исхода во
время и после нее превышает риск смерти от прогрессирования рака тела маткиЧастые ошибки при определении клинической стадии, приводящие к неправильному планированию лечения
Слайд 42Экстрафасциальная экстирпация матки с придатками
При метастазах в яичниках и папиллярном
серозном раке тела матки, когда высок риск имплантационного метастазирования, показано
удаление большого сальникаСмывы из брюшной полости для цитологического исследования
Ревизия органов малого таза и брюшной полости, тазовых и поясничных лимфатических узлов, биопсия всех измененных лимфатических узлов и выявленных объемных образований
Хирургическое лечение
Слайд 43Хирургическое лечение
У 38% больных раком тела матки I клинической стадии во
время операции обнаруживаются метастазы в лимфатических узлах, яичниках, маточных трубах,
распространение по париетальной и висцеральной брюшине или опухолевые клетки в смывах из брюшной полости (GOG, Creasman W. T. et al, 1987)Пред- и послеоперационный гистологический диагнозы не совпадают у 27% больных, степень дифференцировки — у 34%, стадия — у 51% (Cowles T. A. et al, 1985)
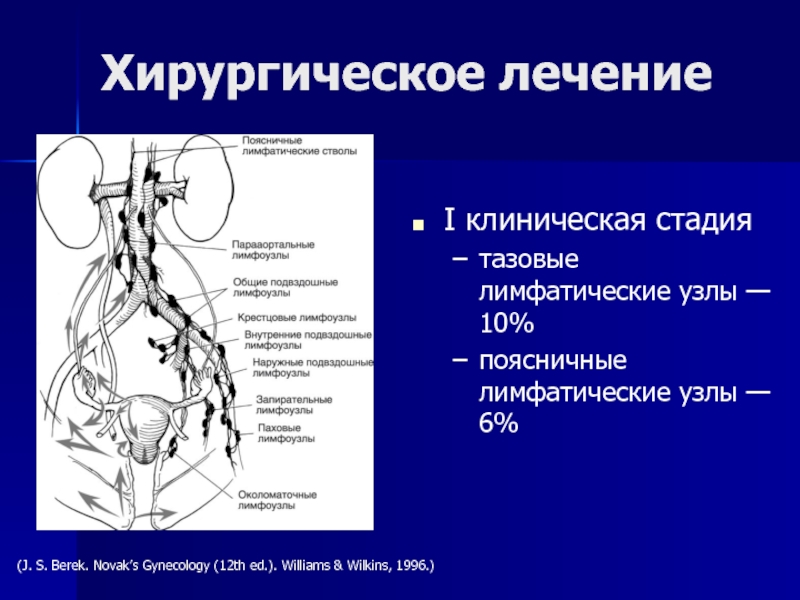
Слайд 44I клиническая стадия
тазовые лимфатические узлы — 10%
поясничные лимфатические узлы —
6%
Хирургическое лечение
(J. S. Berek. Novak’s Gynecology (12th ed.). Williams & Wilkins, 1996.)
Слайд 45Хирургическое лечение
Boronow R.C. et al, 1984; Creasman W.T et al,
1987; Schink J.C. et al, 1987
Слайд 46Хирургическое лечение
Метастатически измененные лимфатические узлы на момент операции оказываются увеличенными
менее чем у 10—40% больных
Оценка состояния тазовых и поясничных лимфатических
узловпредоперационные КТ и МРТ
пальпация и биопсия увеличенных лимфатических узлов
биопсия одного лимфатического узла
селективная лимфаденэктомия
тотальная лимфаденэктомия
Слайд 47Хирургическое лечение
Цели лимфаденэктомии
уточнение стадии
определение тактики дальнейшего лечения
улучшение выживаемости
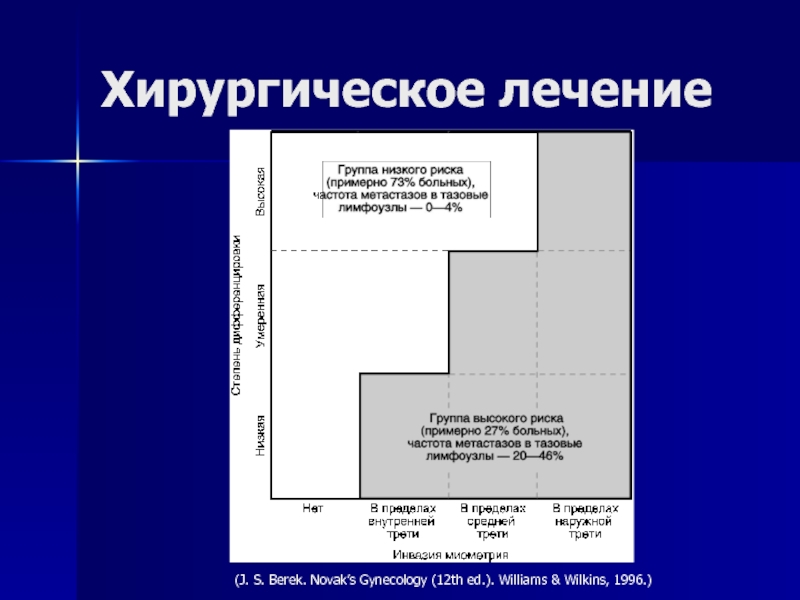
Слайд 48Хирургическое лечение
(J. S. Berek. Novak’s Gynecology (12th ed.). Williams & Wilkins, 1996.)
Слайд 49Хирургическое лечение
Показания к лимфаденэктомии
низкодифференцированная аденокарцинома
инвазия миометрия более чем на половину
его толщины
переход опухоли на перешеек или шейку матки
распространение опухоли за
пределы маткисветлоклеточный, папиллярный серозный, плоскоклеточный и недифференцированный рак
опухоль более 2 см
Слайд 50Хирургическое лечение
Анеуплоидия повышает риск на 1 уровень
Fuller A.F., Jr., ESGO
Meeting, 2005
Слайд 52Лучевая терапия снижает частоту рецидивов и метастазов в тазовых лимфатических
узлах (прогрессирование в зоне облучения), но не влияет на общую
выживаемостьПредоперационную лучевую терапию не проводят
Показания
Европа — в зависимости от степени дифференцировки и глубины инвазии
США и Австралия — в зависимости от наличия опухоли за пределами матки и риска прогрессирования
Лучевая терапия не показана
высокодифференцированные опухоли I стадии
умереннодифференцированные опухоли IA и IB стадий
Лучевая терапия
Слайд 53Послеоперационная дистанционная лучевая терапия на область малого таза (СОД 45—50 Гр)
при определении морфологической стадии опухоли
многие авторы проводят лучевую терапию только
при прогрессированиинизкодифференцированные опухоли IC стадии
Внутриполостная лучевая терапия (СОД 21 Гр) при определении морфологической стадии опухоли
умереннодифференцированные опухоли IC стадии
низкодифференцированные опухоли IA и IB стадий
Лучевая терапия
Слайд 54Лучевая терапия как самостоятельный метод лечения
противопоказания к операции
только внутриполостная (при
выраженном ожирении) или сочетанная лучевая терапия
каждый случай отказа от хирургического
лечения должен быть тщательно аргументированЛучевая терапия
Слайд 55Гормонотерапия
Медроксипрогестерона ацетат, мегестрола ацетат и тамоксифен
Преимущества
системное действие
низкая частота осложнений
Kelley R.M.,
Baker W.H. (1961)
первый опыт применения прогестагенов при диссеминированном раке тела
маткиАдъювантная гормонотерапия неэффективна (Lewis G.C. et al, 1974; Kauppila A., 1984; DePalo G. et al, 1985; MacDonald R.R. et al, 1988; Vergote I. et al, 1989)
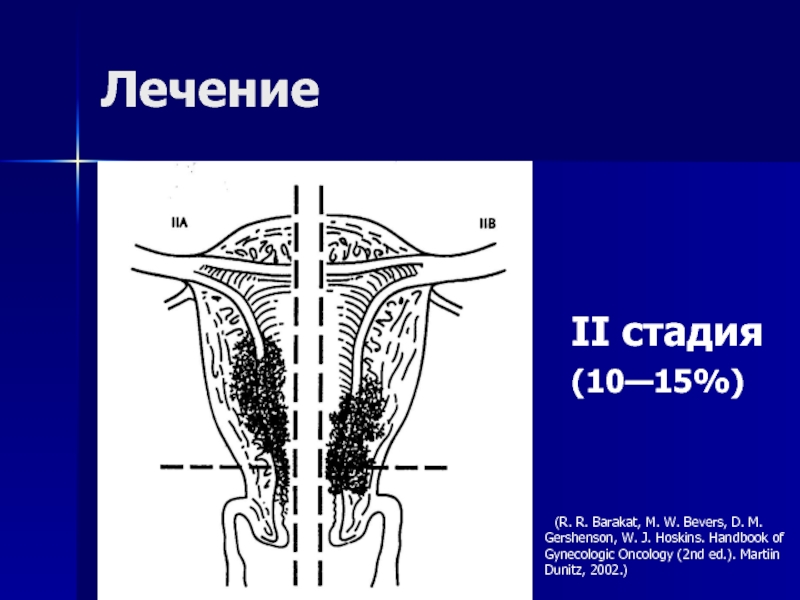
Слайд 56Лечение
II стадия
(10—15%)
(R. R. Barakat, M. W. Bevers, D. M.
Gershenson, W. J. Hoskins. Handbook of Gynecologic Oncology (2nd ed.). Martiin Dunitz,
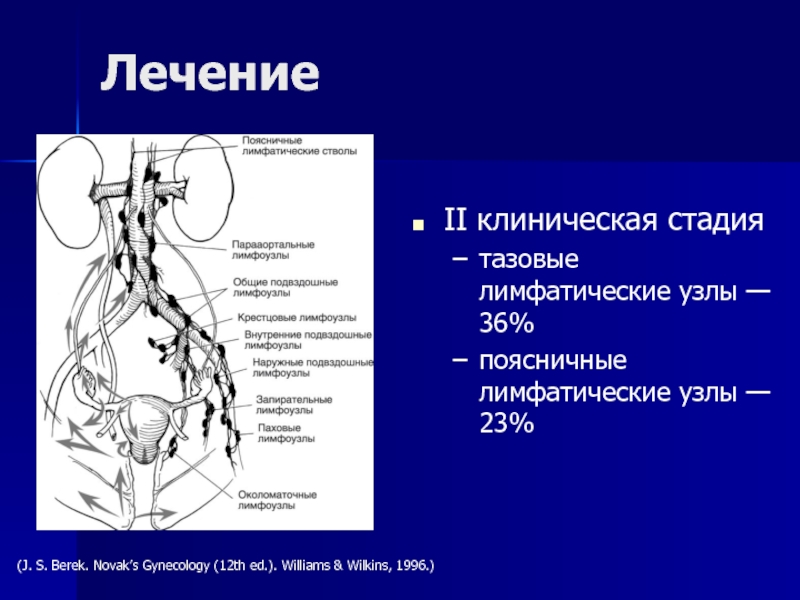
2002.)Слайд 57II клиническая стадия
тазовые лимфатические узлы — 36%
поясничные лимфатические узлы —
23%
Лечение
(J. S. Berek. Novak’s Gynecology (12th ed.). Williams & Wilkins, 1996.)
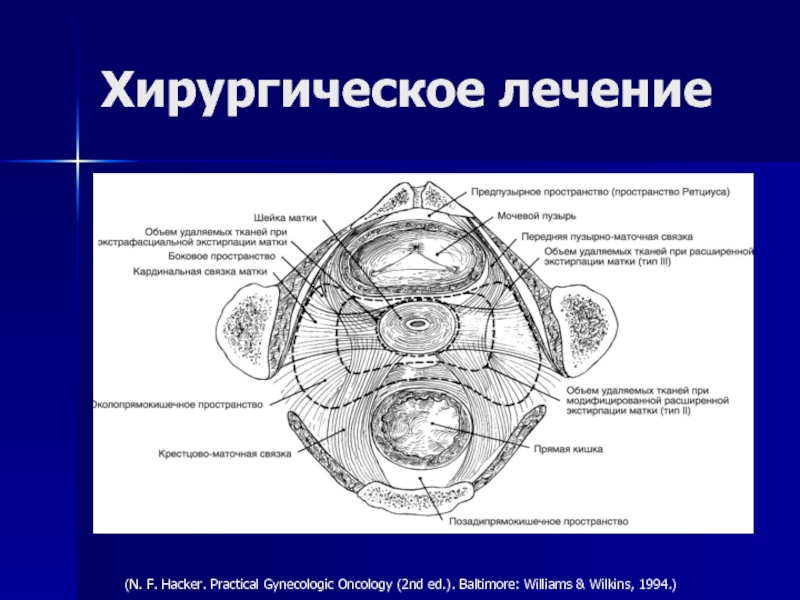
Слайд 58Лечение
Расширенная экстирпация матки с придатками, селективная поясничная лимфаденэктомия + сочетанная
лучевая терапия
Слайд 59(N. F. Hacker. Practical Gynecologic Oncology (2nd ed.). Baltimore: Williams & Wilkins, 1994.)
Хирургическое лечение
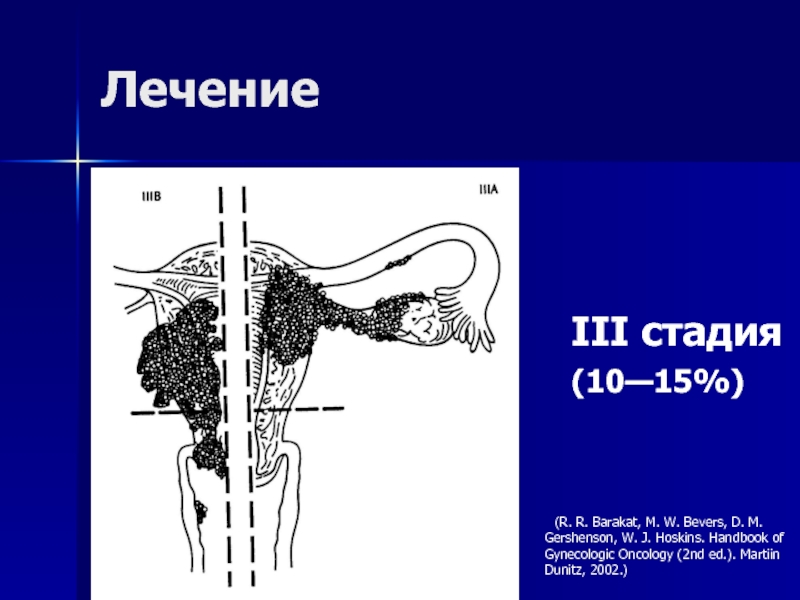
Слайд 60Лечение
III стадия
(10—15%)
(R. R. Barakat, M. W. Bevers, D. M.
Gershenson, W. J. Hoskins. Handbook of Gynecologic Oncology (2nd ed.). Martiin Dunitz,
2002.)Слайд 61Лечение
Индивидуальный план лечения
Операция на первом этапе обязательна, если при обследовании
выявляется объемное образование в области придатков матки
Следует стремиться к максимальному
уменьшению массы опухоли, поскольку это улучшает прогноз. Результаты комбинированного лечения рака тела матки III стадии лучше, чем результаты сочетанной лучевой терапииПри метастазах в яичниках проводят химиотерапию
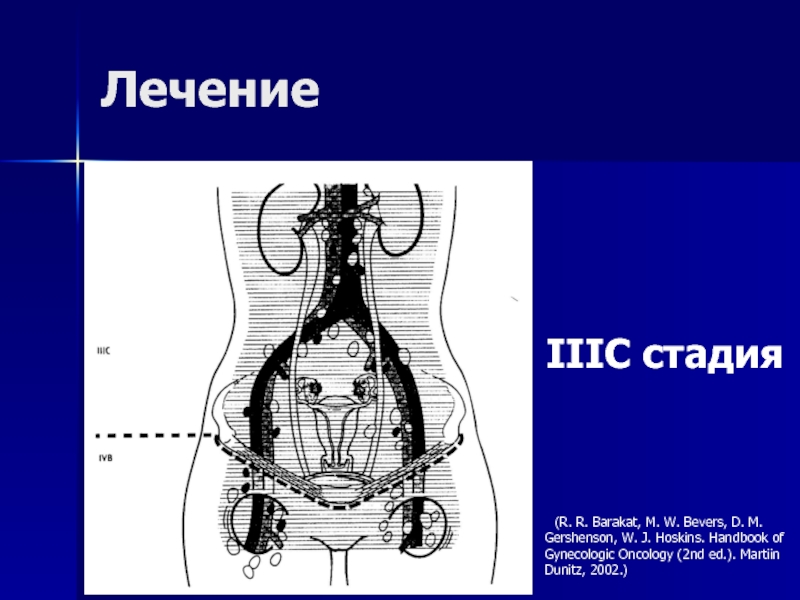
Слайд 62Лечение
IIIC стадия
(R. R. Barakat, M. W. Bevers, D. M.
Gershenson, W. J. Hoskins. Handbook of Gynecologic Oncology (2nd ed.). Martiin Dunitz,
2002.)Слайд 63Лечение
Хирургическое лечение, определение стадии, удаление метастазов
Риск смерти в отсутствие хирургического
лечения 6,85 (ретроспективные данные, Havrilevsky, 2005)
При морфологическом подтверждении поражения тазовых
или поясничных лимфатических узлов — дистанционная лучевая терапия на область малого таза или поясничную область (СОД 45—50 Гр) соответственноСлайд 64Лечение
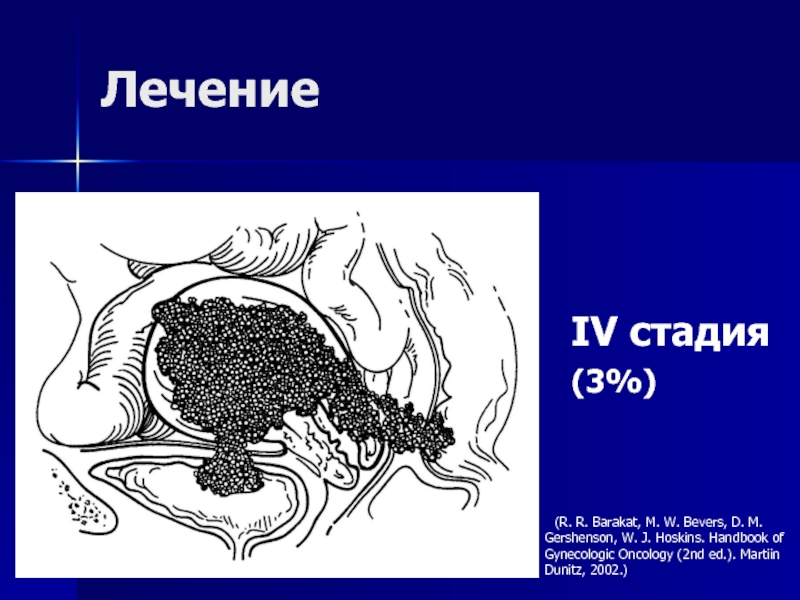
IV стадия
(3%)
(R. R. Barakat, M. W. Bevers, D. M.
Gershenson, W. J. Hoskins. Handbook of Gynecologic Oncology (2nd ed.). Martiin Dunitz,
2002.)Слайд 65Лечение обычно комплексное и включает операцию, лучевую, гормональную терапию или
химиотерапию
Цель операции и лучевой терапии — снизить риск маточного кровотечения, нормализовать
функцию мочевого пузыря и прямой кишкиПри раке тела матки III—IV стадий, если остаточные опухоли не превышают 2 см, химиотерапия доксорубицином и цисплатином эффективнее облучения живота и малого тала (GOG 122, 2006)
Лечение
Слайд 66Гормонотерапия
Эффективность при диссеминированном раке тела матки и при прогрессировании определяется
степенью
дифференцировки
уровнями рецепторов стероидных гормонов в опухоли
Частота частичных и полных ремиссий
11—19%, стабилизации 15—52% (Piver et al., 1980; Podratz et al., 1985; Thigpen et al, 1986)Эффективность лечения не зависит ни от используемого препарата, ни от режима его назначения
Слайд 68Химиотерапия
При прогрессировании РТМ применяют различные комбинации препаратов платины, антрациклинов, таксанов,
5-фторурацила,
циклофосфамида, ифосфамида, этопозида
Наиболее эффективны комбинации, включающие препараты платины, таксаны
и антрациклины
Большинство
ремиссий частичные и непродолжительныеСлайд 69Факторы прогноза
Возраст
Гистологический тип опухоли
Степень дифференцировки опухоли
Глубина инвазии миометрия
Распространение опухоли на
перешеек или
шейку матки
Опухолевые эмболы в кровеносных и лимфатических сосудах
Метастазы в
яичниках и лимфатических узлахДиссеминация по брюшине
Размеры опухоли
Слайд 70Факторы прогноза
Содержание рецепторов прогестерона и эстрогенов
в опухоли
Опухолевые клетки в смывах
из брюшной полости
Плоидность опухолевых клеток и индекс пролиферации
Степень дифференцировки (выраженность
атипии) ядерЭкспрессия отдельных онкогенов (например, ERBB2, кодирующего поверхностный гликопротеид, сходный с рецептором эпидермального фактора роста, — HER-2/neu)
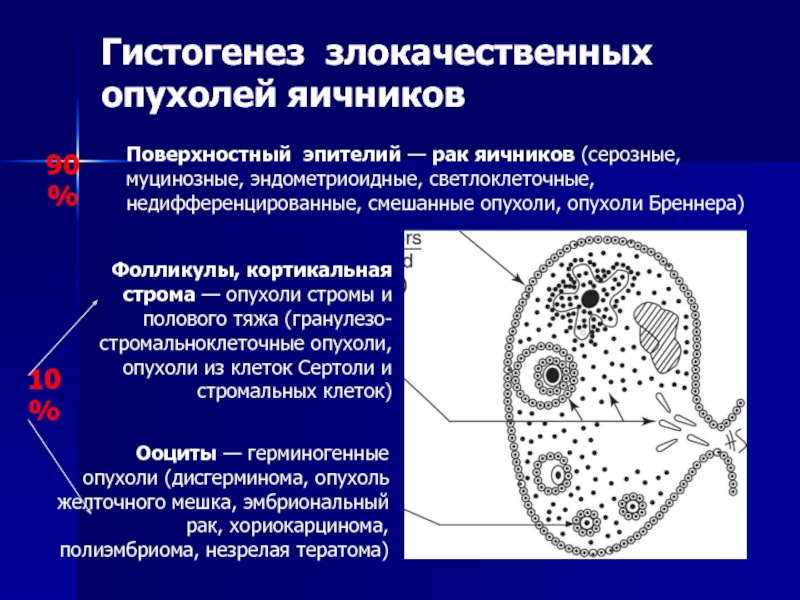
Слайд 72Гистогенез злокачественных опухолей яичников
Ооциты — герминогенные
опухоли (дисгерминома, опухоль желточного мешка,
эмбриональный рак, хориокарцинома, полиэмбриома, незрелая тератома)
Фолликулы, кортикальная строма — опухоли
стромы и полового тяжа (гранулезо-стромальноклеточные опухоли, опухоли из клеток Сертоли и стромальных клеток) Поверхностный эпителий — рак яичников (серозные, муцинозные, эндометриоидные, светлоклеточные, недифференцированные, смешанные опухоли, опухоли Бреннера)
90%
10%
Слайд 73Заболеваемость раком яичников
(стандартизованный мировой показатель,
все возрасты, на 100 000 женщин)
Слайд 74Смертность от рака яичников (стандартизованный мировой показатель, все возрасты, на 100 000
женщин)
Слайд 75Эпидемиология
2-я по частоте опухоль женских половых органов в развитых странах
(после рака тела матки)
3-я по частоте опухоль женских половых органов
в РоссииСамая частая причина смерти женщин от опухолей женских половых органов
Слайд 76Эпидемиология
2-я по частоте опухоль женских половых органов в развитых странах
(после рака тела матки)
3-я по частоте опухоль женских половых органов
в РоссииСамая частая причина смерти женщин от опухолей женских половых органов
Слайд 77Заболеваемость в России
выросла на 4,7% (2005—2010)
Средний возраст больных в России
58,7
года
Эпидемиология
М. И. Давыдов, Е. М. Аксель (2012)
Слайд 79Факторы риска
Частота семейного рака яичников 5—10%
Семейный рак яичников и молочной
железы
аутосомно-доминантно
ген BRCA1 (частота мутаций 1 на 800—1000 женщин)
риск рака молочной железы
у носительниц мутантного гена достигает 85—90%, рака яичников — 40—50%ген BRCA2
риск рака яичников у носительниц мутантного гена достигает 11%
семейный рак яичников
аутосомно-доминантно
относительный риск 3—10
Синдром Линча типа II
наследственный рак толстой кишки без полипоза в сочетании с аденокарциномами других локализаций
относительный риск 3,0
Слайд 80Факторы, снижающие риск
Комбинированные пероральные контрацептивы
более эффективны препараты с высоким содержанием
прогестагенов
↓ риск на 40%
↓ риск на 50% при приеме в
течение 5 лет и болееГрудное вскармливание
↓ риск на 30%
при лактации > 12 мес ↓ риск на 50%
Употребление фруктов, овощей, молочных продуктов, рыбы, белого мяса и растительных масел
↓ риск на 40—60%
Физическая активность
Слайд 81Скрининг
Нет методов, пригодных для скрининга
У 75% больных распространенность опухоли соответствует
III—IV стадиям (FIGO)
При отягощенном семейном анамнезе показано генетическое консультирование
Слайд 82Клиническая картина
Бессимптомное течение на ранних стадиях
При диссеминации жалобы на ощущение
дискомфорта со стороны желудочно-кишечного тракта, увеличение живота в объеме (асцит),
тупую ноющую боль внизу живота (механическое сдавление опухолью соседних органов)Слайд 83Диагностика
Морфологическое подтверждение диагноза
цитологическое исследование асцитической жидкости
гистологическое исследование удаленной опухоли
Слайд 84Патоморфология
Серозная аденокарцинома
Муцинозная аденокарцинома
Эндометриоидная аденокарцинома
Светлоклеточная (мезонефроидная) аденокарцинома
Злокачественная опухоль
Бреннера
Смешанная аденокарцинома
Недифференцированный рак
(F. Tavassoli, P. Devilee. Pathology & Genetics. Tumors of
the Breast and Female Genital Organs. Lyon: IARCPress, 2003.)Слайд 85Пути метастазирования
Имплантационный
Лимфогенный
поясничные лимфатические узлы
тазовые лимфатические узлы
паховые лимфатические узлы
Распространение на соседние
органы
Гематогенный
Слайд 86Обследование
Первичная опухоль, местное распространение
физикальное исследование (гинекологическое исследование)
УЗИ малого таза и
брюшной полости
цистоскопия
ректороманоскопия
экскреторная урография
определение уровня CA-125
лапароскопия
Регионарное распространение
пальпация паховых лимфатических узлов
УЗИ забрюшинного
пространстваКТ
экскреторная урография
Слайд 87Обследование
Отдаленные метастазы
физикальное исследование (пальпация шейных лимфатических узлов)
УЗИ органов брюшной полости
(печени)
рентгенография грудной клетки
КТ
позитронно-эмиссионная томография (ПЭТ)
Слайд 88Обследование
Оценка общего состояния
общий анализ крови и мочи, биохимическое исследование крови,
коагулограмма
допплеровское исследование вен нижних конечностей и подвздошных вен
ЭКГ
исследование функции внешнего
дыханиягастроскопия
колоноскопия / ирригоскопия
Слайд 89Лечение
I этап лечения — операция:
определение стадии
первичная циторедукция
цель циторедуктивной операции —
удаление первичной опухоли и, по возможности, всех метастазов в пределах
брюшной полости; если это невозможно, следует стремиться к их максимальному уменьшениюПри невозможности выполнить оптимальную циторедукцию —химиотерапия (3 курса)
Слайд 90Осмотр париетальной и висцеральной брюшины
Смывы из брюшной полости для цитологического
исследования с диафрагмы, из малого таза, с правой и левой
половин брюшной полостиЭкстрафасциальная экстирпация матки с придатками
Удаление большого сальника
Селективная тазовая и поясничная лимфаденэктомия
Ревизия малого таза и брюшной полости, биопсия всех выявленных объемных образований и спаек
Биопсия неизмененной париетальной брюшины правого купола диафрагмы, пузырно-маточной складки, прямокишечно-маточного углубления, правого и левого латеральных каналов и стенок таза с обеих сторон
Аппендэктомия при муцинозных опухолях
Хирургическое лечение
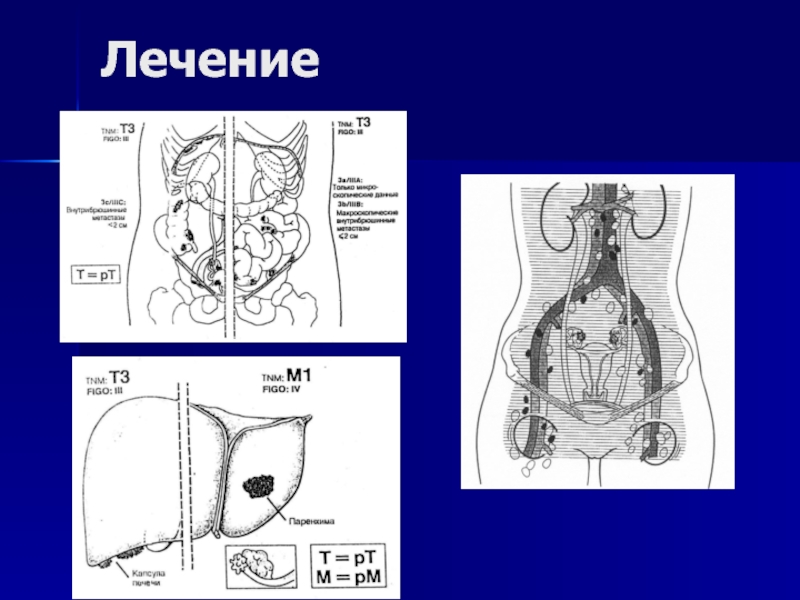
Слайд 92Морфологические стадии (UICC, 7-й пересмотр)
а Метастазы по капсуле печени классифицируют как
ТЗ, метастазы в паренхиме печени и опухолевые клетки в плевральной
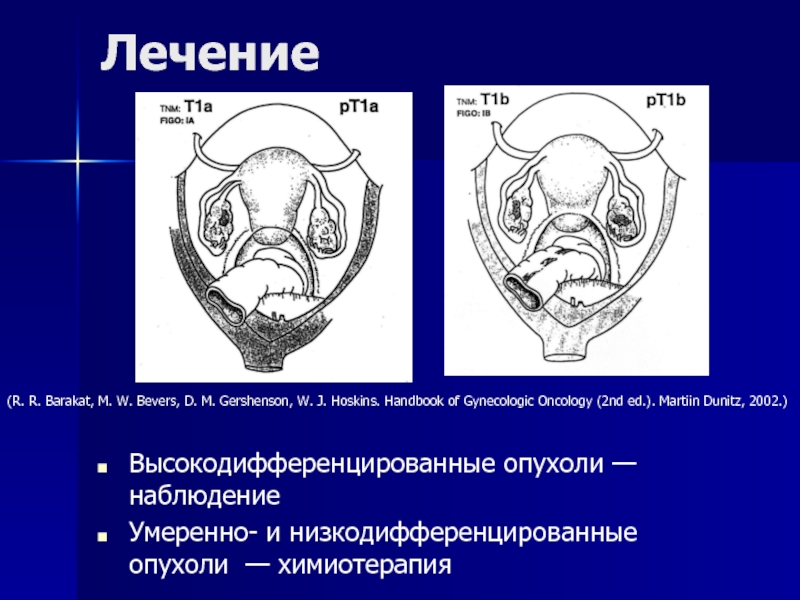
жидкости — как M1.Слайд 93Лечение
Высокодифференцированные опухоли — наблюдение
Умеренно- и низкодифференцированные опухоли — химиотерапия
(R. R.
Barakat, M. W. Bevers, D. M. Gershenson, W. J. Hoskins.
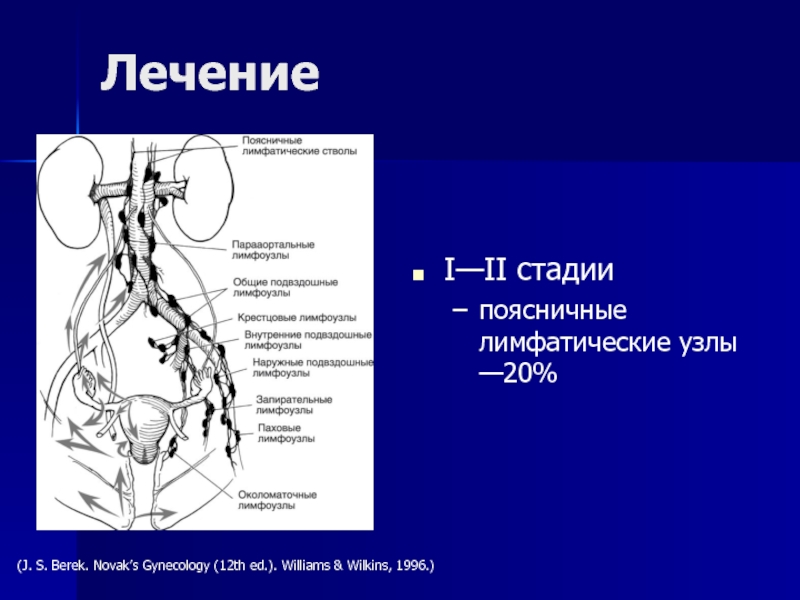
Handbook of Gynecologic Oncology (2nd ed.). Martiin Dunitz, 2002.)Слайд 94I—II стадии
поясничные лимфатические узлы —20%
Лечение
(J. S. Berek. Novak’s Gynecology
(12th ed.). Williams & Wilkins, 1996.)
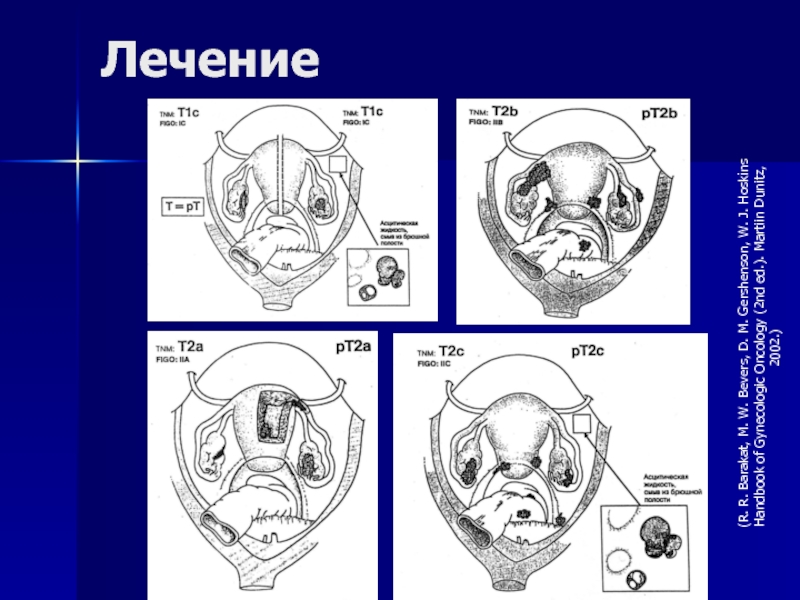
Слайд 96Лечение
(R. R. Barakat, M. W. Bevers, D. M. Gershenson, W.
J. Hoskins
Handbook of Gynecologic Oncology (2nd ed.). Martiin Dunitz, 2002.)
Слайд 100Лечение
Оптимальная циторедукция — максимальный размер остаточной опухоли < 1 см
(GOG) (0—3 см)
паклитаксел / доцетаксел + карбоплатин
6 курсов
Слайд 101Лечение
Неоптимальная циторедукция — максимальный размер остаточной опухоли > 1 см
(GOG) (0—3 см)
паклитаксел / доцетаксел + карбоплатин, 3 курса
промежуточная циторедуктивная
операцияпаклитаксел / доцетаксел + карбоплатин, до 6 курсов
Слайд 102Лечение
Прогрессирование наблюдается у большинства больных раком яичников поздних стадий
Прогрессирование через
> 6 мес (12 мес) после окончания лечения
возврат к 1-й
линии химиотерапии паклитаксел / доцетаксел + карбоплатин
при нейротоксичности гемцитабин или липосомальный доксорубцин вместо таксанов
Прогрессирование через < 6 мес (12 мес) после окончания лечения
2-я линия химиотерапии
гемцитабин, или липосомальный доксорубцин, или топотекан, или этопозид
частота полных и частичных ремиссий при применении самостоятельно или в комбинациях 10—15%
клинические испытания / поисковые режимы
Слайд 103Лечение
Операции «second-look»
нет клинических признаков заболевания после завершения запланированного лечения, для
оценки эффекта
Повторная циторедуктивная операция
в любые сроки после завершения 1-й линии
химиотерапииэффективна при удалении всех макроскопически определяемых образований
Слайд 104Факторы прогноза
Стадия
Наличие и размер остаточной опухоли
Гистологический тип
Степень дифференцировки опухоли
Плоидность, содержание
клеток в S-фазе клеточного цикла
Экспрессия HER-2/neu
Слайд 108Герминогенные опухоли яичников
20—30% опухолей яичников, 95% из них доброкачественные зрелые
кистозные тератомы (дермоидные кисты)
3% злокачественных опухолей яичников
Средний возраст 18 лет
Дисгерминомы
(50%) и недисгерминомы (50%)Агрессивное течение
Повышение уровней a-фетопротеина, β-субъединицы хорионического гонадотропина и активности лактатдегидрогеназы сыворотки
Прогноз более благоприятен при дисгерминомах: при I стадии 5-летняя выживаемость почти 100%
Слайд 109Vera M. Abeler, G. Rustin, 15th International Meeting of ESGO,
Berlin, 2007
Герминогенные опухоли яичников
Слайд 110Герминогенные опухоли яичников
Своевременная диагностика
Органосохраняющее лечение в детородном возрасте
Современные режимы химиотерапии
(BEP)
Высокая чувствительность к химиотерапии —
жесткое соблюдение режима лечения (доз и
сроков введения препаратов)Слайд 114Особенности
До начала 1970-х гг. почти все больные диссеминированной хориокарциномой погибали
Сейчас
большинство больных не только излечиваются, но и сохраняют репродуктивную функцию
ранняя
диагностикаточное определение b-ХГ
эффективная химиотерапия
Слайд 115Патоморфология
Пузырный занос
полный
частичный
Инвазивный пузырный занос
Хориокарцинома
Опухоль плацентарного ложа
Эпителиоидная трофобластическая опухоль
Слайд 116Патоморфология
Поскольку диагноз трофобластической опухоли не требует морфологической верификации (желательна, но
не обязательна), на смену морфологической классификации пришла клиническая
Слайд 117Классификация
Пузырный занос (полный и частичный)
Трофобластические опухоли
Инвазивный пузырный занос
Хориокарцинома
Опухоль плацентарного ложа
Эпителиоидная
трофобластическая опухоль
Недиссеминированные
Диссеминированные
Трофобластическая
болезнь
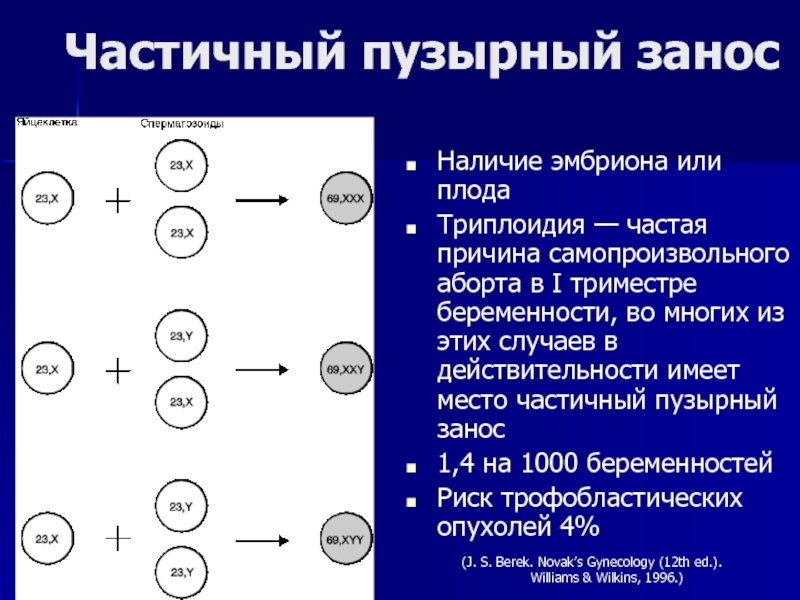
Слайд 118Частичный пузырный занос
Наличие эмбриона или плода
Триплоидия — частая причина самопроизвольного
аборта в I триместре беременности, во многих из этих случаев
в действительности имеет место частичный пузырный занос1,4 на 1000 беременностей
Риск трофобластических опухолей 4%
(J. S. Berek. Novak’s Gynecology (12th ed.).
Williams & Wilkins, 1996.)
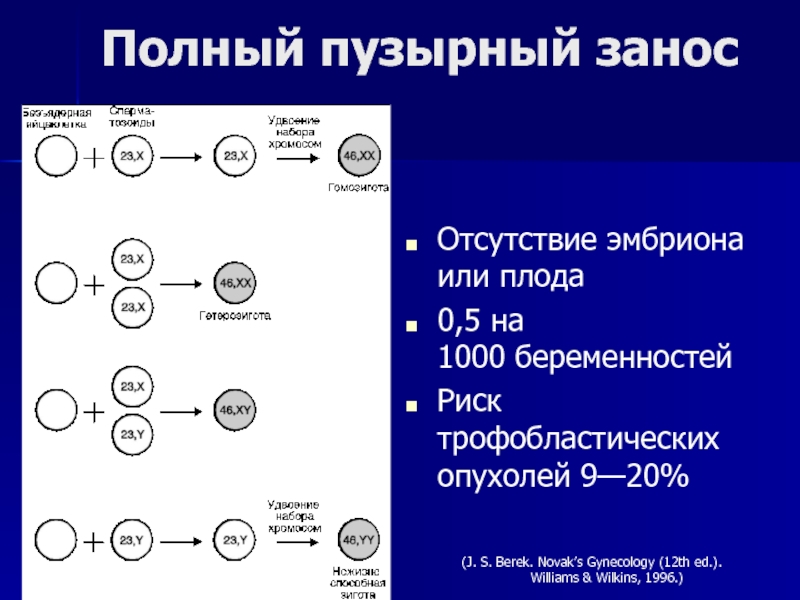
Слайд 119Полный пузырный занос
Отсутствие эмбриона или плода
0,5 на 1000 беременностей
Риск трофобластических опухолей
9—20%
(J. S. Berek. Novak’s Gynecology (12th ed.).
Williams & Wilkins, 1996.)
Слайд 120Патогенез
Трофобластические опухоли развиваются в исходе:
пузырного заноса — 50—60%
самопроизвольного или искусственного
аборта — 30%
нормальной или эктопической беременности — 10—20%
Слайд 121Диагностика и лечение пузырного заноса
Кровянистые выделения из влагалища, рвота беременных
УЗИ
малого таза
Эвакуация пузырного заноса
вакуум-аспирация
экстирпация матки у женщин, не планирующих иметь
детейнельзя настаивать на экстирпации матки, поскольку она не улучшает прогноз
Слайд 122Диагностика трофобластических опухолей
Плато (1, 7, 14, 21-й день) или увеличение
(1, 7, 14-й день) уровня b-ХГ в сыворотке после эвакуации пузырного
заносаВизуализация метастазов
Гистологическая верификация диагноза
Слайд 123Диагностика трофобластических опухолей
Трофобластическая опухоль возможна у любой женщины детородного возраста
Особенно
трудна диагностика трофобластических опухолей в отсутствие пузырного заноса в анамнезе
О
возможности трофобластической опухоли должны помнить врачи всех специальностей. Особое внимание следует уделять больным детородного возраста с нарушениями мозгового кровообращения и больным с рецидивирующей пневмониейСлайд 126Оценка риска резистентности опухоли (FIGO, 2002)
Сумма баллов 6 и менее
— низкий риск прогрессирования и резистентности опухоли к противоопухолевым средствам
Сумма
баллов 7 и более — высокий риск прогрессирования и резистентности опухоли к противоопухолевым средствамСлайд 127Лечение
Лечение больных (в том числе получавших нестандартные режимы) всегда начинают
со стандартной химиотерапии I линии, режим которой определяется риском резистентности
опухолиПри сумме баллов по шкале ВОЗ/FIGO 6 и менее проводят монохимиотерапию метотрексатом с Лейковорином
При сумме баллов по шкале ВОЗ/FIGO 7 и более проводят полихимиотерапию по схеме EMA-CO (этопозид, метотрексат, Лейковорин, дактиномицин, циклофосфамид, винкристин)