пренебречь.
Основное уравнение МКТ идеального газа:
p= 2/3 × n ×
mv2/2Связь давления с температурой:
p = nkT
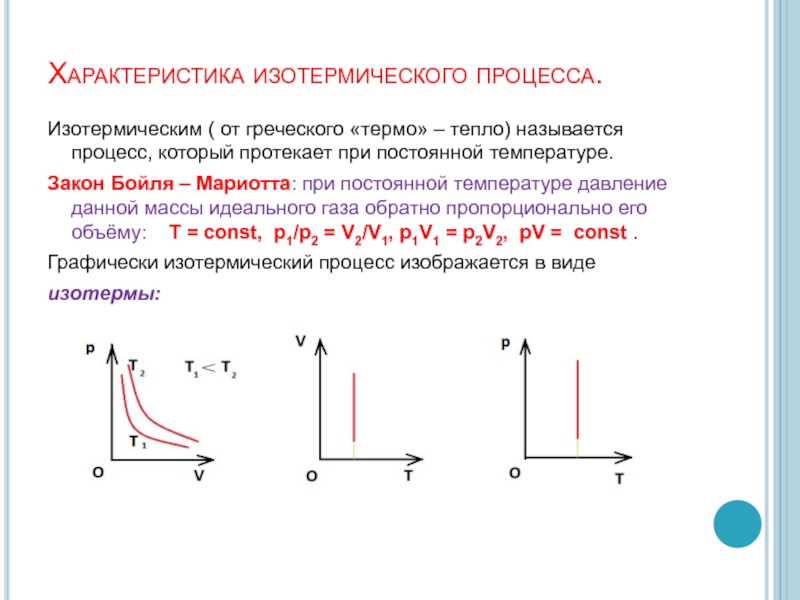
При постоянной массе газа, три макропараметра
связаны уравнением состояния идеального газа:
pV = m/M × RT, pV/T = const (уравнение Менделеева – Клапейрона).
ПАРАМЕТРЫ НОРМАЛЬНОГО СОСТОЯНИЯ (н.у.)
ро = 760 мм рт. ст. = 105 Па
Объём одного моля газа Vo = 22,4л = 22,4 × 10¯³м³
То = 273 К