Слайд 1Тема урока:
«Физико-химические свойства белков и их синтез»
Слайд 2Цели урока:
Закрепить и углубить представление о природных полимерах на примере
белков
Познакомить учащихся со свойствами белков
Расширить представление учащихся о гидролизе на
примере белков, дать понятие о денатурации и условиях вызывающих её
Научить проводить цветные реакции на белки
Выявить причинно-следственную зависимость между составом, строением и свойствами белков
Продолжить развитие навыков самообразования : умения слушать, выделять главное, работать с источниками информации
Развивать межпредметные связи (с биологией)
Продолжать воспитывать интерес к познанию нового
Слайд 4 Вопросы для разминки.
1.Что такое белки?
2.Чем белки отличаются от
пептидов?
3.Что такое аминокислоты и сколько аминокислот принимает участие в строительстве
белков?
4.Какова роль функциональных групп аминокислот?
5.Сколько и какие различают структуры белка? За счет чего они образуются?
глобулярные
(кератин волос, перьев) Б (антитела, ферменты)
Е
протеины протеиды
(альбумин сыв.крови) Л (липопротеины мембр.)
К
гидрофобные И гидрофильные
(коллаген сухожилий) (гемоглобин крови)
Слайд 6Химические свойства
Амфотерность белков
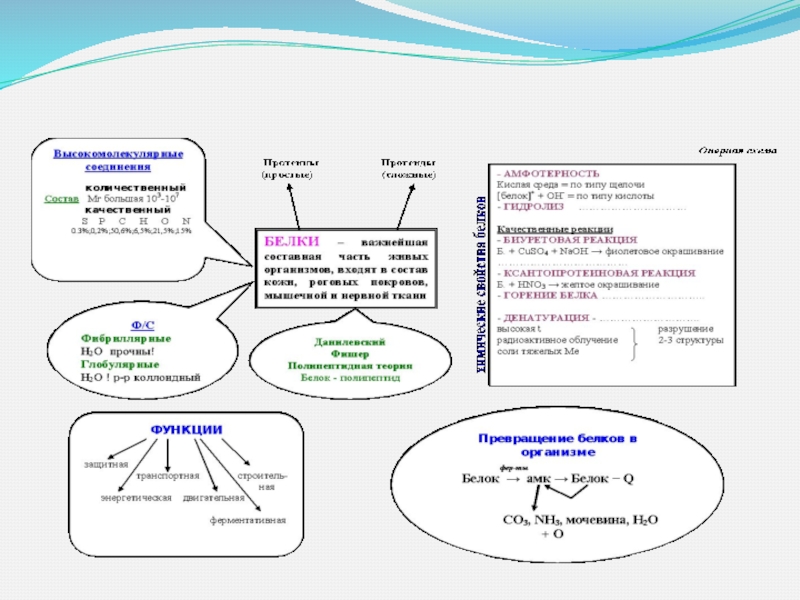
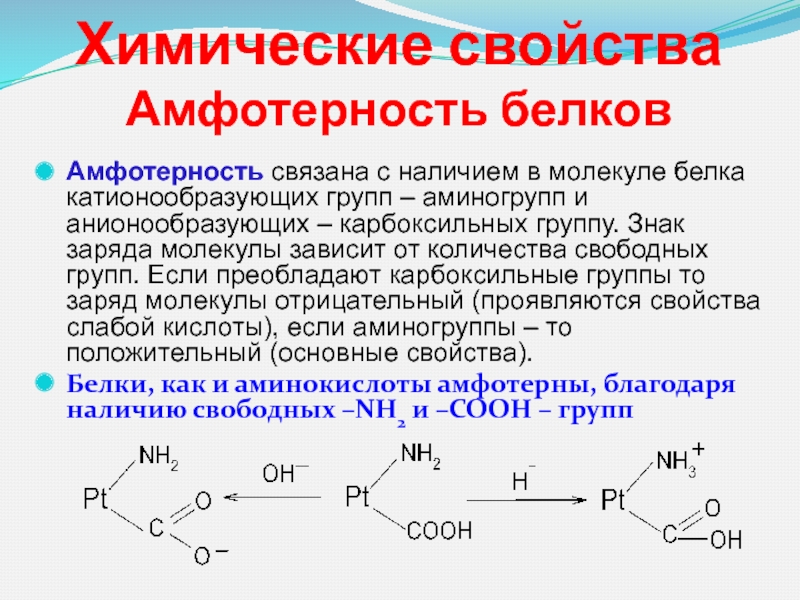
Амфотерность связана с наличием в молекуле белка катионообразующих
групп – аминогрупп и анионообразующих – карбоксильных группу. Знак заряда
молекулы зависит от количества свободных групп. Если преобладают карбоксильные группы то заряд молекулы отрицательный (проявляются свойства слабой кислоты), если аминогруппы – то положительный (основные свойства).
Белки, как и аминокислоты амфотерны, благодаря наличию свободных –NH2 и –СООН – групп
Слайд 7Денатурация белков
В основе денатурации лежат глубокие внутримолекулярные перестройки, приводящие к
изменению специфической конфигурации белковой молекулы (вторичной, третичной структуры)
Физические агенты: нагревание,
УФ-лучи, рентгеновские лучи, ультразвуковое излучение, высокое давление
Химические агенты: концентрированные кислоты и щелочи, соли тяжелых металлов, алкалоидные реактивы, многие органические растворители
Обратимая денатурация
Необратимая денатурация
Слайд 8Денатурация
Обратимая
(под действием концентрированного раствора NаСl)
Необратимая
(под действием солей
тяжелых металлов, концентрированных
кислот и щелочей органических ядов (фенола))
Термическая
(при нагревании)
Химическая
Слайд 9Гидролиз белков
Взаимодействие белков с водой, в ходе которого белок утрачивает
свою первичную структуру
Слайд 10Цветные реакции на белки
Биуретовая
Белок + Cu(OH)2 → фиолетовая окраска →
реакция
на пептидные связи
Ксантопротеиновая
Белок + HNO3(к) → желтая окраска →
реакция на
ароматические циклы
Фоля
Белок + Pb(NO3)2 +NaOH → черный осадок → реакция на серу
Слайд 11 реакция горения
Белки горят с
образованием азота, углекислого газа и воды, а также некоторых других
веществ.
Горение сопровождается характерным запахом жженых перьев.
Слайд 12 Белки представляют собой наиболее
сложные
коллоидные соединения
1. В растворах белки обнаруживают очень низкое осмотическое давление
2.
Незначительная способность к диффузии
3. Высокая вязкость
4. Набухание в очень больших пределах с образованием гелей и студней
5. Способность к адсорбции
6. Амфотерность
7. Ионизация, наличие заряда, электрофоретическая подвижность
8. Гидрофильность, растворимость в воде
9. Склонность к денатурации, осаждению
10. Способность к гидролизу с расщеплением пептидных связей
11. Растворы белков обладают способностью к светорассеянию и способностью к поглощению УФ-излучения при 280 нм
Слайд 14
По данным Всемирной организации здравоохранения примерно половина населения земного шара
находится в состоянии белкового голодания, а мировая нехватка пищевого белка
составляет около 15 млн. тонн в год при норме потребления белка в сутки взрослым человеком 115 грамм
Слайд 151.Связь, образующая первичную структуру белка?
2.Белки имеют большую атомною массу, т.к.
представляют собой…
3.Растворимый в воде белок куриного яйца?
4.Мономер для синтеза белка?
5.Разрушение
молекулы белка до первичной структуры?
6. Белок красного цвета?
7.Фамилия ученого, получившего Нобелевскую за изучение вторичной структуры белка?
Для закрепления материала разгадывание кроссворда.
Слайд 161.Связь, образующая первичную структуру белка?
2.Белки имеют большую атомною массу, т.к.
представляют собой…
3.Растворимый в воде белок куриного яйца?
4.Мономер для синтеза белка?
5.Разрушение
молекулы белка до первичной структуры?
6. Белок красного цвета?
7.Фамилия ученого, получившего Нобелевскую за изучение вторичной структуры белка?
Для закрепления материала разгадывание кроссворда.
Слайд 17 Проверь себя
1. Главным
носителем жизни являются …
2. … - это сложные высокомолекулярные
соединения, построенные из … .
3. Элементный состав белков: … .
4. Молекулярная масса белков изменяется
от … до … .
5. Многие белки растворимы в ….
6. Нерастворимы белки, из которых построены … .
7. В структуре белка различают … структуры.
8. Функции белков в организме … .
ОТВЕТЫ:
1. Белки.
2. Белки; остатков α – аминокислот.
3.
С, Н, О, N, S.
4. Десяти тысяч, миллионов.
5. Воде, растворах солей, кислот.
6.Ткани живых организмов: кожа, сухожилия, мышцы, ногти, волосы.
7.Первичную, вторичную, третичную, четвертичную.
8.Строительная, каталитическая, двигательная, транспортная, защитная, энергетическая.
Слайд 19 КРИТЕРИИ ОЦЕНКИ:
«5» - все
ответы правильные;
«4» - 1-3 неверных ответа;
«3» -4- 5 неверных ответа;
«2» - 6 и более неверных ответов.
Исправление приравнивается к ошибке.
Слайд 20Подведение итогов
Выставление оценок
Домашнее задание.
1.Параграф учебника 49.
2. Письменно:
А) Синтезировать дипептид глицина
и аланина.
Б) Написать уравнение реакции гидролиза любого трипептида.
Слайд 21Я умница!
Надеюсь на лучшее
Так держать!
Рефлексия