Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Химическая связь
Содержание
- 1. Химическая связь
- 2. Цель урока обобщить и систематизировать знания
- 3. План изучения темы урокаПонятие «химическая связь».Ионная химическая связь:механизм образования;характеристики связи;ионная кристаллическая решетка.
- 4. Что такое химическая связь?
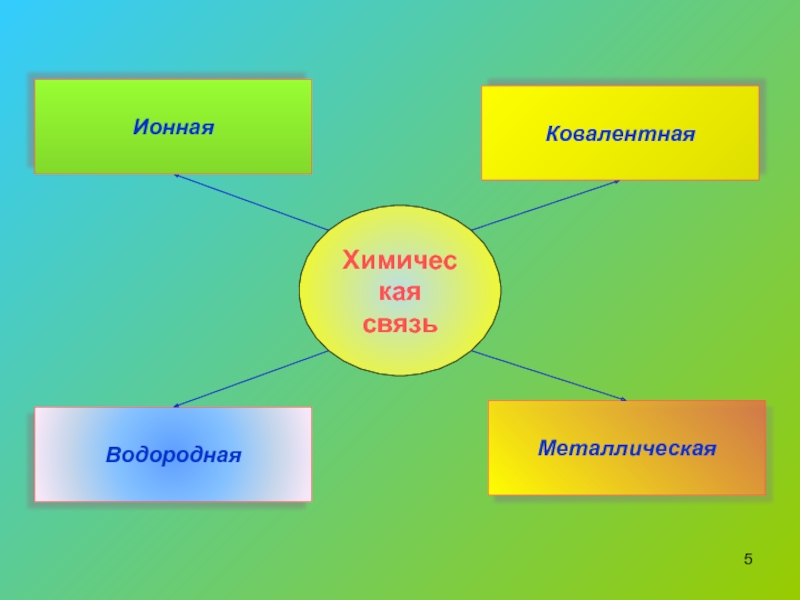
- 5. Химическая связьВодороднаяМеталлическаяКовалентнаяИонная
- 6. Электроотрицательность- способность атомов одних химических элементов притягивать
- 7. 2. Ионная химическая связь - связь, образующаяся
- 8. Механизм образования ионной связи1s22s22p63s11s2s3s2p1s2s3s2p3p1s22s22p63s23p5Na0 – 1e- =Cl20
- 9. Запомни!!!полного перехода электронов при образовании ионной химической
- 10. Электроотрицательность- способность атомов одних химических элементов притягивать
- 11. по составупо зарядупростые:Na+, Ca2+, Cl-сложные:OH-, SO42-, No3-положительные: Ca2+, Na+Ионыотрицательные:OH-, SO42-
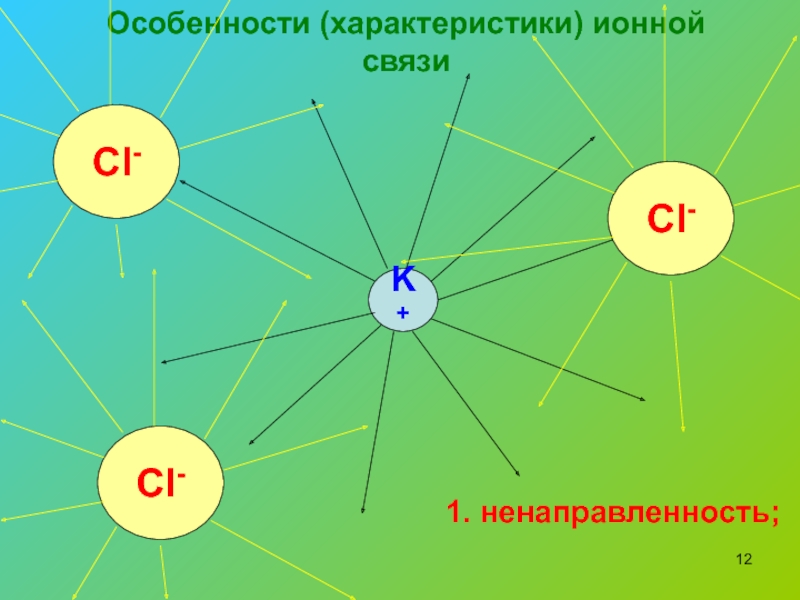
- 12. Особенности (характеристики) ионной связиK+Cl-Cl-Cl-1. ненаправленность;
- 13. Особенности (характеристики) ионной связи2. ненасыщаемость.Кристаллическая решетка ионных
- 14. Домашнее задание§6 (стр. 44-46), упр. 4 на
- 15. Спасибо за внимание!
- 16. Скачать презентанцию
Цель урока обобщить и систематизировать знания о видах химической связи и их классификации как о важнейшем универсальном понятии теоретической химии
Слайды и текст этой презентации
Слайд 1Химическая связь
Муниципальное общеобразовательное учреждение
«Волхонщинская средняя общеобразовательная школа»
Гарифзянов А.Р.
Ионная химическая
связь
Слайд 2Цель урока
обобщить и систематизировать знания о видах химической
связи и их классификации как о важнейшем универсальном понятии теоретической
химииСлайд 3План изучения темы урока
Понятие «химическая связь».
Ионная химическая связь:
механизм образования;
характеристики связи;
ионная
кристаллическая решетка.
Слайд 6Электроотрицательность
- способность атомов одних химических элементов притягивать электроны в соединениях
от атомов других химических элементов
Δ א – разница электроотрицательностей:
Δ א
> 1,7 – ионная химическая связь;0 < Δא < 1,7 – ковалентная химическая связь
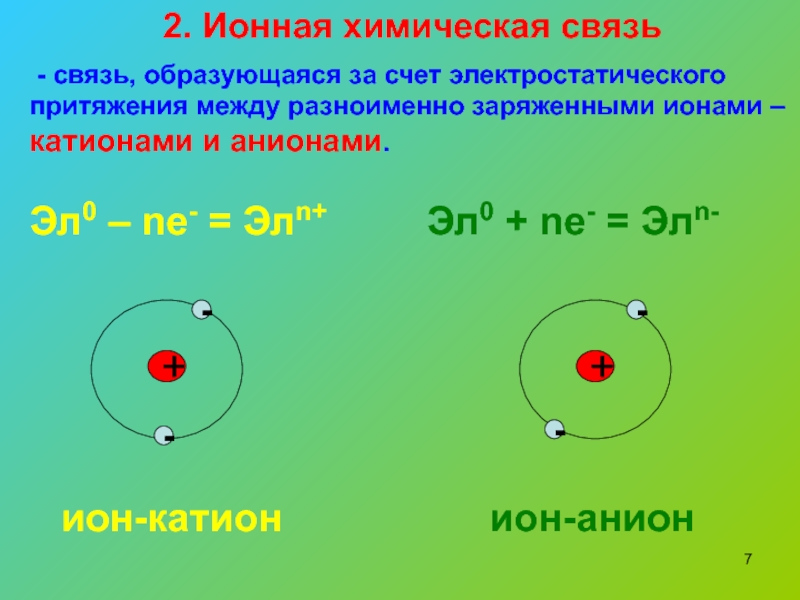
Слайд 72. Ионная химическая связь
- связь, образующаяся за счет электростатического
притяжения между разноименно заряженными ионами – катионами и анионами.
Эл0 –
nе- = Элn+Эл0 + nе- = Элn-
+
-
-
+
-
ион-катион
-
ион-анион
Слайд 8Механизм образования ионной связи
1s22s22p63s1
1s
2s
3s
2p
1s
2s
3s
2p
3p
1s22s22p63s23p5
Na0 – 1e- =
Cl20 + 2e- =
2
Na+
Cl-
хлорид натрия
Na
.
+
Cl
.
.
.
.
.
.
.
=
Na+
Cl
.
.
.
.
.
.
.
[
-[
.
+11Na
+17 Cl
Составьте электронные и графические формулы атомов:
Слайд 9Запомни!!!
полного перехода электронов при образовании ионной химической связи не происходит.
Об этом свидетельствуют величины эффективных зарядов в соединениях
Слайд 10Электроотрицательность
- способность атомов одних химических элементов притягивать электроны в соединениях
от атомов других химических элементов
Δ א – разница электроотрицательностей:
Δ א
> 1,7 – ионная химическая связь;Например, NaCl
א(Na) = 1,01;
א (Cl) = 2,83;
Δ א = 2,83 – 1,01 = 1,82, т.е. ионная химическая связь
Слайд 11по составу
по заряду
простые:
Na+, Ca2+, Cl-
сложные:
OH-, SO42-, No3-
положительные: Ca2+, Na+
Ионы
отрицательные:
OH-, SO42-
Слайд 13Особенности (характеристики) ионной связи
2. ненасыщаемость.
Кристаллическая решетка ионных соединений представляет собой
трехмерную бесконечную решетку, в узлах которой находятся анионы и катионы
Кристаллическая
решетка NaClСлайд 14Домашнее задание
§6 (стр. 44-46), упр. 4 на стр. 56, распишите
механизм образования ионной связи в молекулах:
1 вариант - хлорида кальция;
2
вариант – бромида калия;3 вариант – нитриде натрия.