Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Избранные главы металлоорганической химии
Содержание
- 1. Избранные главы металлоорганической химии
- 2. Предмет металлоорганической химии:соединения со связью металл-углеродСчитается, что связь поляризована Mδ+−Cδ −
- 3. Электроотрицательность элементов по Полингу
- 4. Факторы, влияющие на электроотрицательность1) Гибридизация атома углерода:
- 5. 2) Степень окисления металла: EN(C)
- 6. 3) Групповая электроотрицательность:
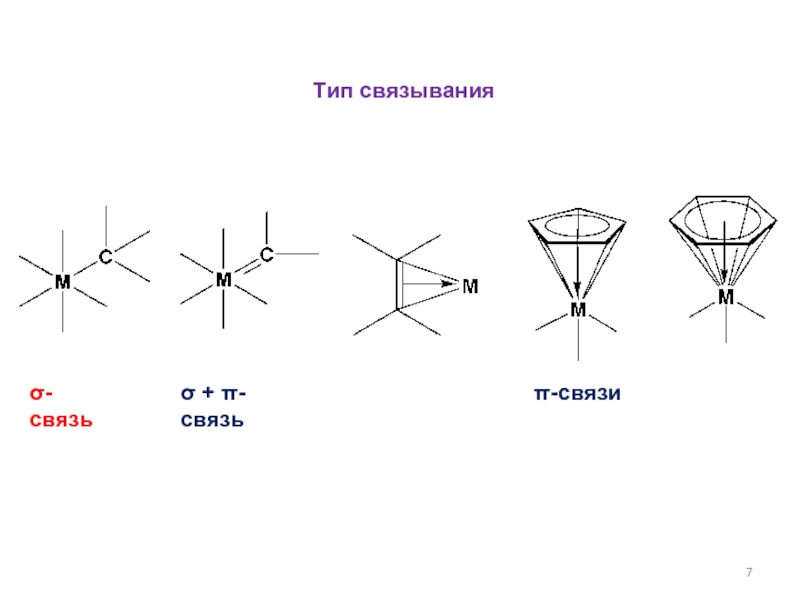
- 7. Тип связыванияσ-связьσ + π-связьπ-связи
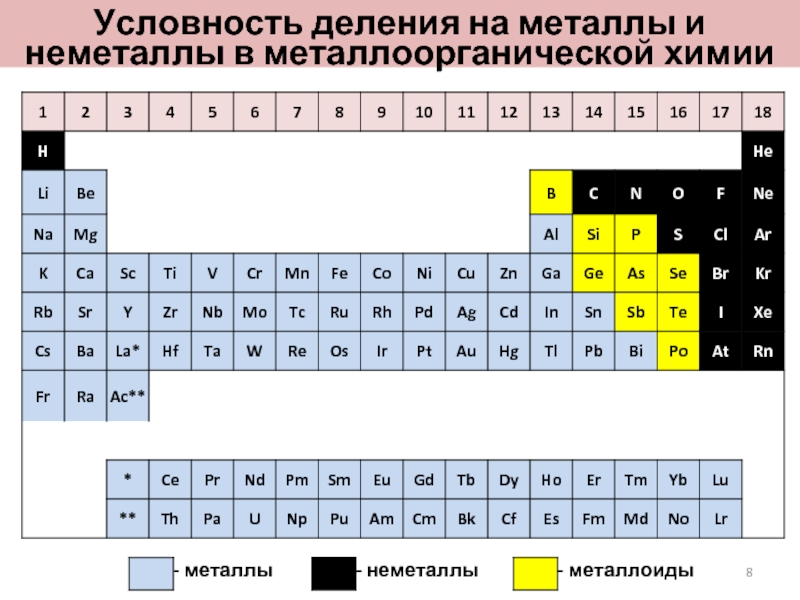
- 8. Условность деления на металлы и неметаллы в металлоорганической химии
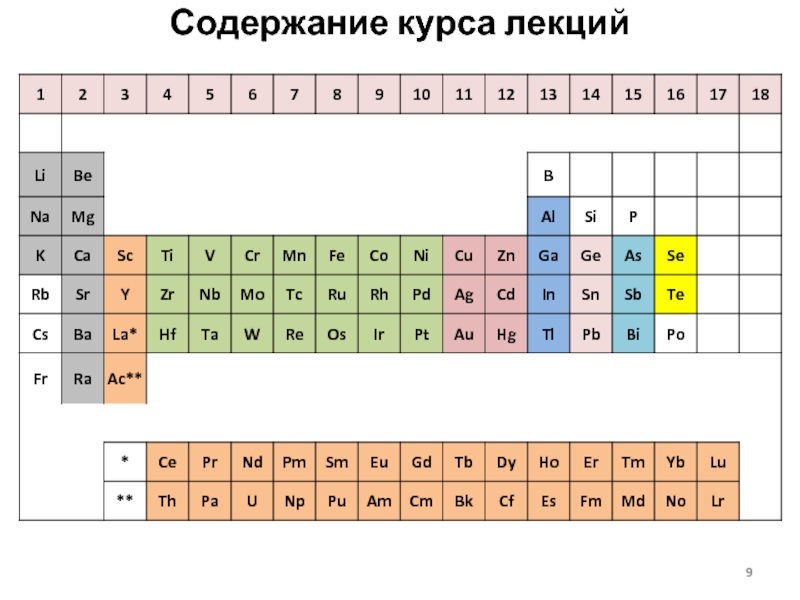
- 9. Содержание курса лекций
- 10. ЛитератураОсновнаяК. Эльшенбройх . Металлоорганическая химия. Пер. с
- 11. ЛитератураДополнительнаяComprehensive Organometallic Chemistry, 3-th ed., N. -Y.,
- 12. ЛитератураДополнительная Herrmann/Brauer , Synthetic Methods of Organometallic
- 13. Краткая история развития металлоорганической химии – основные события и люди
- 14. Dietmar Seyferth, «Cadet's Fuming Arsenical Liquid and
- 15. Первый олефиновый комплекс (1827 г.)William Christopher Zeise
- 16. Sir Edward Frankland (1825-1899) 2C2H5I + Zn2C2H5
- 17. В последующие годы R2Hg и R2Zn сыграли
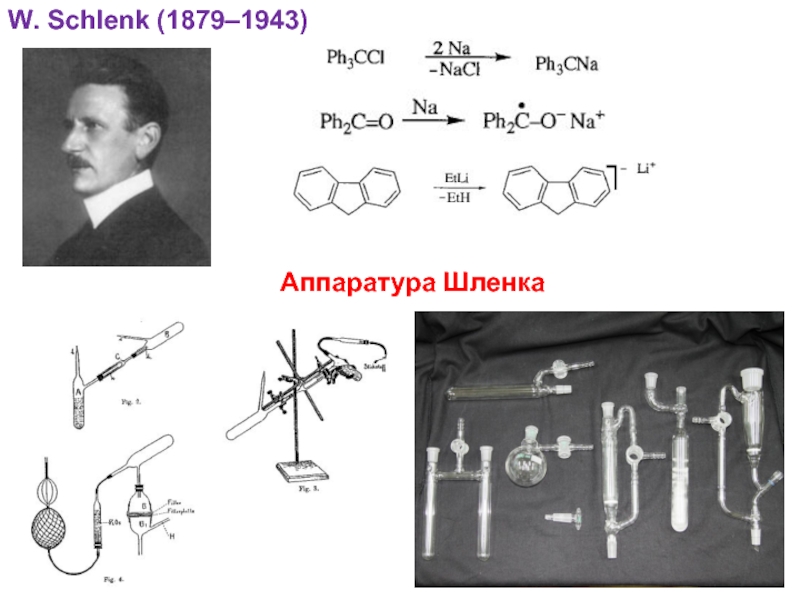
- 18. W. Schlenk (1879–1943)Аппаратура Шленка
- 19. Д.И. Менделеев (1834-1907) использовал знание о металлоорганических соединениях для предсказания новых элементов
- 20. P. Barbier (1848—1922) заменил цинк на магний
- 21. Реактивы Гриньяра нашли широкое применение в органическом
- 22. Развитие химии π-комплексовT. Kealy, P. Pauson (1951)1.
- 23. Развитие химии π-комплексов1959 г. R. Criegee (1902-1975) – синтез [(η4-C4Me4)NiCl2]21965 г. R. Petit – синтез [(C4H4)Fe(CO)3]2
- 24. Развитие химии π-комплексов1968 г. A. Streitwieser –
- 25. 1989 г. H. Schnöckel – разработка синтеза
- 26. Карбонильные комплексы1868 г. M.P. Schützenberger – синтез
- 27. Соединения с кратными связями M–C и M–M
- 28. Соединения с кратными связями M–C и M–M
- 29. Соединения с кратными связями M–C и M–M
- 30. 2004 г. E. Carmona – синтез первого
- 31. История прикладной элементоорганической химииКатализ1922 г. T. Midgley,
- 32. История прикладной элементоорганической химииКатализ(Нобелевская премия 1973 г.)1965
- 33. 1972 г. R.F. Heck – “palladium-catalyzed cross
- 34. История прикладной элементоорганической химииБиохимия/Медицина1909 г. P. Ehrlich
- 35. To be continued…
- 36. Скачать презентанцию
Слайды и текст этой презентации
Слайд 1ИЗБРАННЫЕ ГЛАВЫ МЕТАЛЛООРГАНИЧЕСКОЙ ХИМИИ
Сергей Николаевич Конченко
к. 408 (II), e-mail: konch@niic.nsc.ru
ftp://heap/incoming/KONCHENKO/Organometallics/Lectures
Слайд 2Предмет металлоорганической химии:
соединения со связью металл-углерод
Считается, что связь поляризована Mδ+−Cδ
−
Слайд 4Факторы, влияющие на электроотрицательность
1) Гибридизация атома углерода:
EN(C)
увеличивается с увеличением вклада s-орбитали в гибридные орбитали
EN(C(sp3)) = 2.5 EN(C(sp2)) = 2.7 EN(C(sp)) = 3.3сравнимо с: EN(S) = 2.6 EN(Cl) = 3.1
Коррелирует с увеличением кислотности в ряду:
C2H6 < C2H4 << C2H2
Слайд 52) Степень окисления металла:
EN(C) увеличивается с увеличением
степени окисления элемента
EN(Tl(I)) = 1.62
EN(Tl(III)) = 2.04
(по Полингу)
Факторы, влияющие
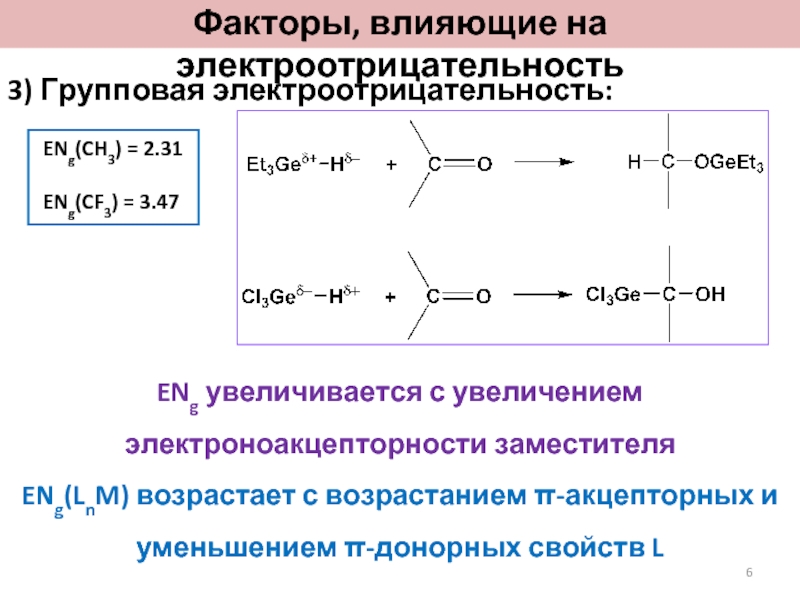
на электроотрицательностьСлайд 63) Групповая электроотрицательность:
ENg(CH3) = 2.31
ENg(CF3) = 3.47ENg увеличивается с увеличением электроноакцепторности заместителя
ENg(LnM) возрастает с возрастанием π-акцепторных и уменьшением π-донорных свойств L
Факторы, влияющие на электроотрицательность
Слайд 10Литература
Основная
К. Эльшенбройх . Металлоорганическая химия. Пер. с нем. Ю.Ф.Опруненко и
Д.С.Перекалина, Москва: БИНОМ. Лаборатория знаний, 2011. - 746 с. :
ил ISBN 978-5-9963-0203-1R.H. Crabtree. The Organometallic Chemistry of the Transition Metals, 5th Ed., Weinheim: Wiley-VCH, 2009.
Дж. Коллмен, Л. Хигедас, Дж. Нортон, Р. Финке. Металлоорганическая Химия Переходных Металлов. в 2-х томах, Москва: Мир, 1989.
Губин С.П., Шульпин Г.Б. Химия комплексов со связями металл-углерод. - Новосибирск: Наука, 1984. - 282 с
Слайд 11Литература
Дополнительная
Comprehensive Organometallic Chemistry, 3-th ed., N. -Y., 2006
Методы элементоорганической химии.
Т.В.
Талалаева, К. А. Кочешков. Литий, натрий, калий, рубидий, цезий.
С.
Т. Иоффе, А. Н. Несмеянов. Магний, бериллий, кальций, стронций, барий. Н. И. Шевердина, К. А. Кочешков. Цинк, кадмий.
Л. Г. Макарова, А. Н. Несмеянов. Ртуть.
А. Н. Несмеянов, Р. А. Соколик. Бор, алюминий, галлий, индий, таллий.
К. А. Андрианов. Кремний.
К. А. Кочешков, Н. Н. Землянский и др. Германий, олово, свинец.
P. X. Фрейдлина. Мышьяк.
А. П. Сколдинов, Н. Н. Землянский, К. А. Кочешков. Сурьма, висмут.
А. Н. Несмеянов, Э. Г, Перевалова и др. Химия переходных металлов.
М. И. Кабачник, Т. А. Мастрюкова и др. Фосфор.
Слайд 12Литература
Дополнительная
Herrmann/Brauer , Synthetic Methods of Organometallic and Inorganic Chemistry,
Ed. W.A. Herrmann, Thieme, in 10 v.
ftp://heap/incoming/KONCHENKO/Organometallics/Literature
Слайд 14Dietmar Seyferth, «Cadet's Fuming Arsenical Liquid and the Cacodyl Compounds
of Bunsen», Organometallics, 2001, V. 20, No. 8, P. 1488
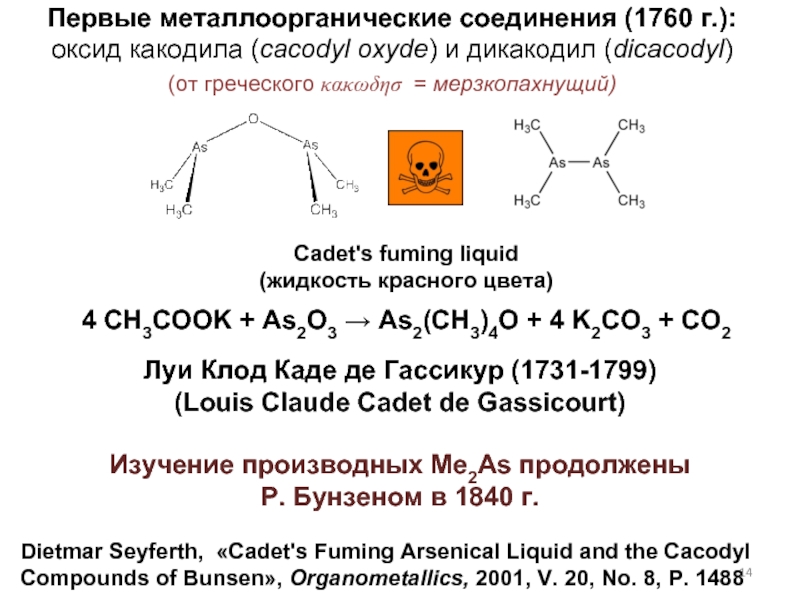
4 CH3COOK + As2O3 → As2(CH3)4O + 4 K2CO3 + CO2
Первые металлоорганические соединения (1760 г.):
оксид какодила (cacodyl oxyde) и дикакодил (dicacodyl)
Луи Клод Каде де Гассикур (1731-1799)
(Louis Claude Cadet de Gassicourt)
Cadet's fuming liquid (жидкость красного цвета)
(от греческого κακωδησ = мерзкопахнущий)
Изучение производных Me2As продолжены
Р. Бунзеном в 1840 г.
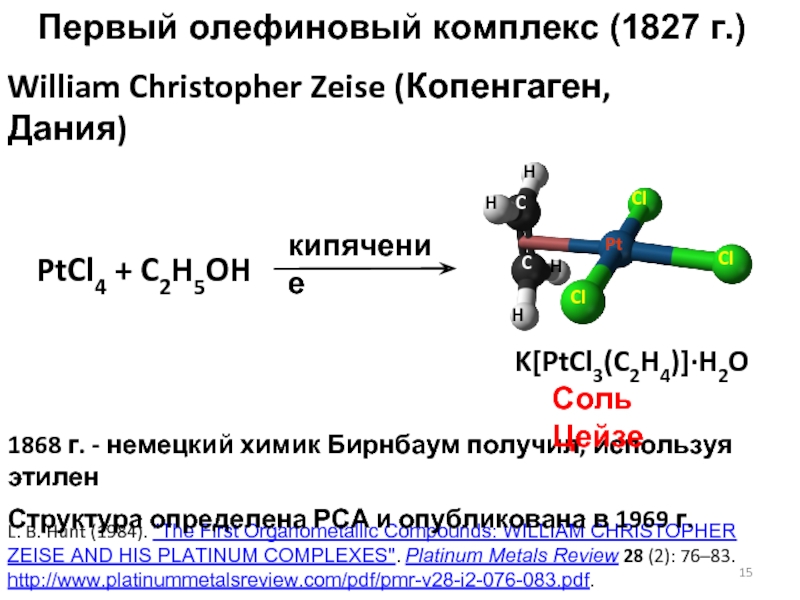
Слайд 15Первый олефиновый комплекс (1827 г.)
William Christopher Zeise (Копенгаген, Дания)
L.
B. Hunt (1984). "The First Organometallic Compounds: WILLIAM CHRISTOPHER ZEISE
AND HIS PLATINUM COMPLEXES". Platinum Metals Review 28 (2): 76–83. http://www.platinummetalsreview.com/pdf/pmr-v28-i2-076-083.pdf.1868 г. - немецкий химик Бирнбаум получил, используя этилен
Структура определена РСА и опубликована в 1969 г.
PtCl4 + C2H5OH
кипячение
Соль Цейзе
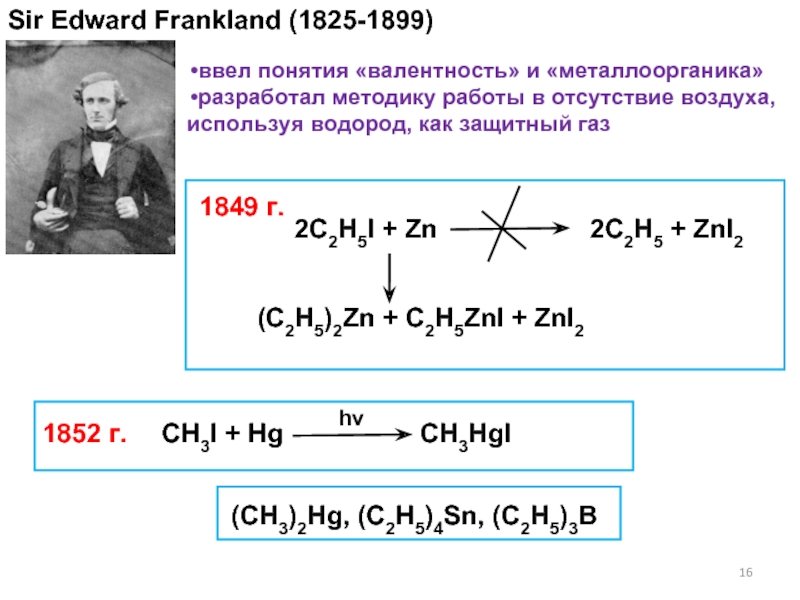
Слайд 16Sir Edward Frankland (1825-1899)
2C2H5I + Zn
2C2H5 + ZnI2
1849 г.
1852
г.
ввел понятия «валентность» и «металлоорганика»
разработал методику работы в отсутствие воздуха,
используя водород, как защитный газCH3I + Hg
CH3HgI
hν
(CH3)2Hg, (C2H5)4Sn, (C2H5)3B
Слайд 17В последующие годы R2Hg и R2Zn сыграли очень большую роль
в развитии металлоорганического синтеза
Например:
SiCl4 + m/2 ZnR2 → RmSiCl4-m +
m/2 ZnCl2 C. Friedel, J.M. Crafts (1863)
(C2H5)2Hg + Mg → (C2H5)2Mg + Hg
J.A. Wanklyn (1866)
R2Hg + 2Li → 2LiR + Hg
2C2H5Li + (CH3)2Hg → 2(CH3)Li + (C2H5)2Hg
трансалкилирование - W. Schlenk (1917)
Слайд 19Д.И. Менделеев (1834-1907)
использовал знание о металлоорганических соединениях для предсказания
новых элементов
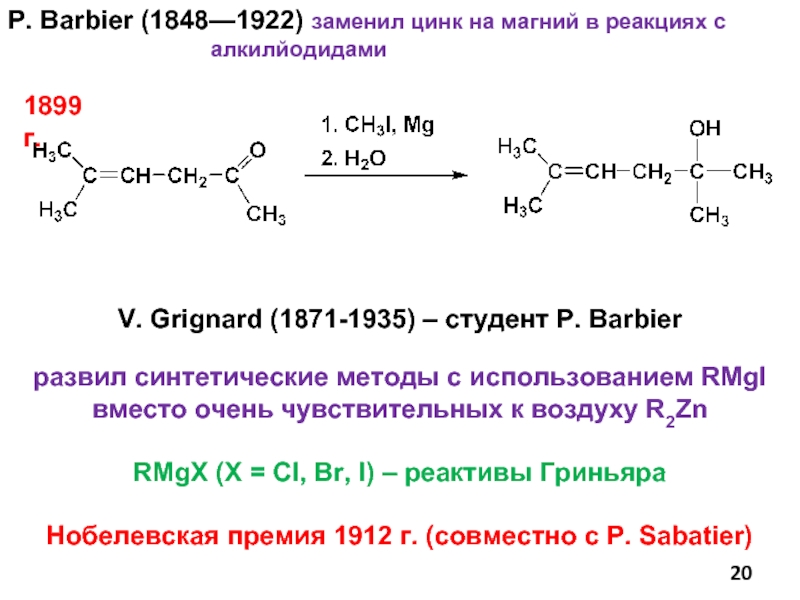
Слайд 20P. Barbier (1848—1922) заменил цинк на магний в реакциях с
алкилйодидами
V. Grignard (1871-1935) – студент P. Barbier
развил синтетические методы с использованием RMgI вместо очень чувствительных к воздуху R2Zn
RMgX (X = Cl, Br, I) – реактивы Гриньяра
Нобелевская премия 1912 г. (совместно с P. Sabatier)
1899 г.
Слайд 21Реактивы Гриньяра нашли широкое применение в органическом и металлоорганическом синтезе
Например:
PtI4
+ 3(CH3)MgI → (CH3)3PtI + 3MgI2
W.J. Pope (1909)
(C6H5)MgBr +
CrCl3 → «полифенилхромовые соединения»J.A. Wanklyn (1866)
в 1955, уже после открытия ферроцена E.O. Fischer разработал рациональный синтез дибензолхрома
CrCl3 + 2/3Al + 1/3AlCl3 + 2C6H6 → [Cr(C6H6)2]AlCl4 + 2/3AlCl3
[Cr(C6H6)2]AlCl4 + 1/2Na2S2O4 → [Cr(C6H6)2] + NaAlCl4 + SO2
сэндвичевое соединение дибензолхром
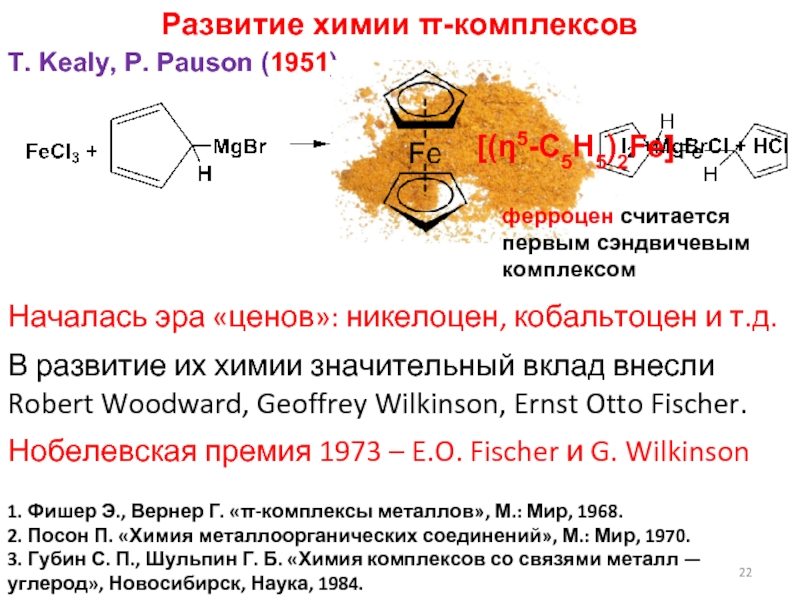
Слайд 22Развитие химии π-комплексов
T. Kealy, P. Pauson (1951)
1. Фишер Э., Вернер
Г. «π-комплексы металлов», М.: Мир, 1968.
2. Посон П. «Химия
металлоорганических соединений», М.: Мир, 1970. 3. Губин С. П., Шульпин Г. Б. «Химия комплексов со связями металл — углерод», Новосибирск, Наука, 1984.
Началась эра «ценов»: никелоцен, кобальтоцен и т.д.
В развитие их химии значительный вклад внесли Robert Woodward, Geoffrey Wilkinson, Ernst Otto Fischer.
Нобелевская премия 1973 – E.O. Fischer и G. Wilkinson
Слайд 23Развитие химии π-комплексов
1959 г. R. Criegee (1902-1975) – синтез [(η4-C4Me4)NiCl2]2
1965
г. R. Petit – синтез [(C4H4)Fe(CO)3]2
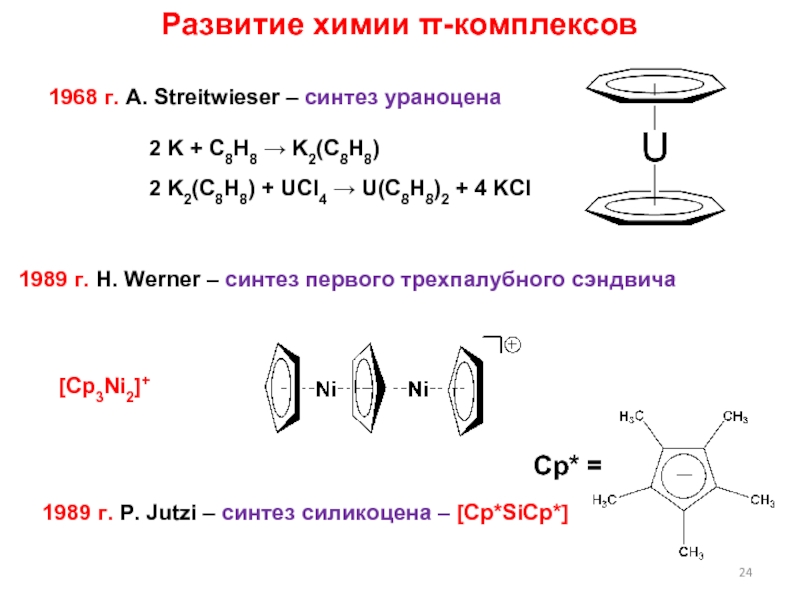
Слайд 24Развитие химии π-комплексов
1968 г. A. Streitwieser – синтез ураноцена
2 K
+ C8H8 → K2(C8H8)
2 K2(C8H8) + UCl4 → U(C8H8)2
+ 4 KCl1989 г. P. Jutzi – синтез силикоцена – [Cp*SiCp*]
Cp* =
1989 г. H. Werner – синтез первого трехпалубного сэндвича
[Cp3Ni2]+
Слайд 251989 г. H. Schnöckel – разработка синтеза AlCl(solv) и далее
– [Cp*Al]4
1994 г. S. Harder – синтез самого «легкого» сэндвича
[Cp2Li]–Развитие химии π-комплексов
Al(г) + HCl(г) → {AlCl(г)} + H2
{AlCl(г)} + толуол + эфир → {AlCl(solv)}
4{AlCl(solv)} + 2[Cp*2Mg] → [Cp*Al]4 + 2MgCl2
H. Schnöckel et al. Angew. Chem. Int. Ed. Engl. 1991, 30, 564.
H.W. Roesky et al. Angew. Chem. Int. Ed. Engl. 1993, 32, 1729.
A. Haaland, H. Schnöckel et al. Acta Chem. Scan. 1994, 48, 172.
S. Harder, M.H. Prosenc, Angew. Chem. Int. Ed. Engl., 33, No. 17, 1744
Слайд 26Карбонильные комплексы
1868 г. M.P. Schützenberger – синтез первого карбонильного
комплекса
[Pt(CO)Cl2]2
1890 г. L. Mond – синтез первого бинарного карбонильного
комплекса
[Ni(CO)4]1927 г. A. Job, A. Cassal – синтез [Cr(CO)6]
1928 г. W. Hieber начинает систематическое изучение химии карбонилов металлов
[Fe(CO)5] + En → [Fe(CO)3En] +2CO
[Fe(CO)5] + X2 → [Fe(CO)4X2] + CO (X = Cl, Br, I)
1931 г. W. Hieber – синтез первого карбонилгидрида [Fe(CO)4H2]
1999 г. A.H. Zewail – за изучение диссоциации связей M–M и M–C в [Mn2(CO)10] фемтосекундным импульсным лазером удостоен Нобелевской премии
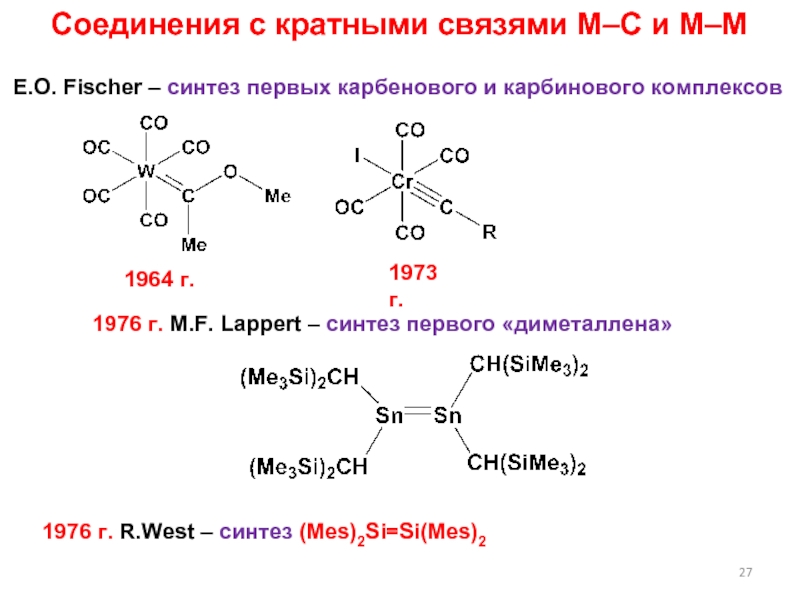
Слайд 27Соединения с кратными связями M–C и M–M
E.O. Fischer –
синтез первых карбенового и карбинового комплексов
1973 г.
1976 г. M.F. Lappert
– синтез первого «диметаллена»1964 г.
1976 г. R.West – синтез (Mes)2Si=Si(Mes)2
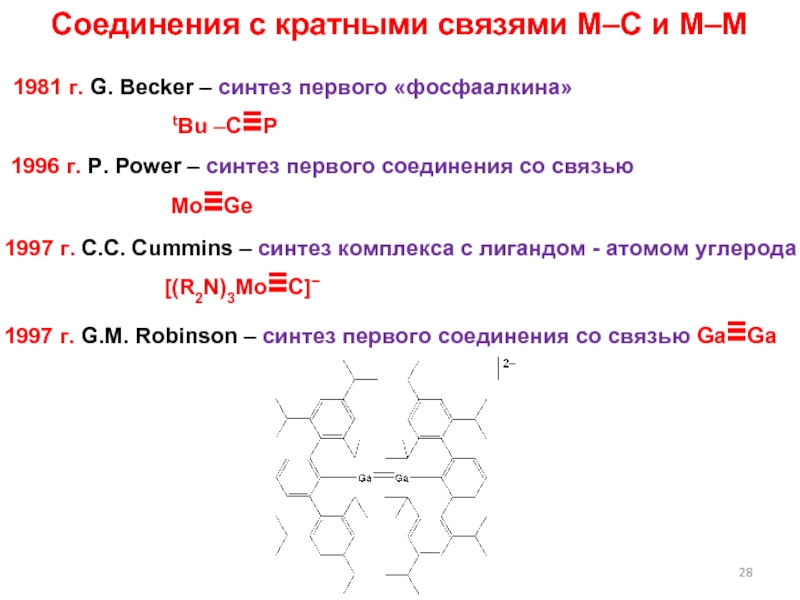
Слайд 28Соединения с кратными связями M–C и M–M
1981 г. G.
Becker – синтез первого «фосфаалкина»
tBu –C≡P
1996 г. P. Power
– синтез первого соединения со связьюMo≡Ge
1997 г. С.С. Cummins – синтез комплекса с лигандом - атомом углерода
[(R2N)3Mo≡C]−
1997 г. G.M. Robinson – синтез первого соединения со связью Ga≡Ga
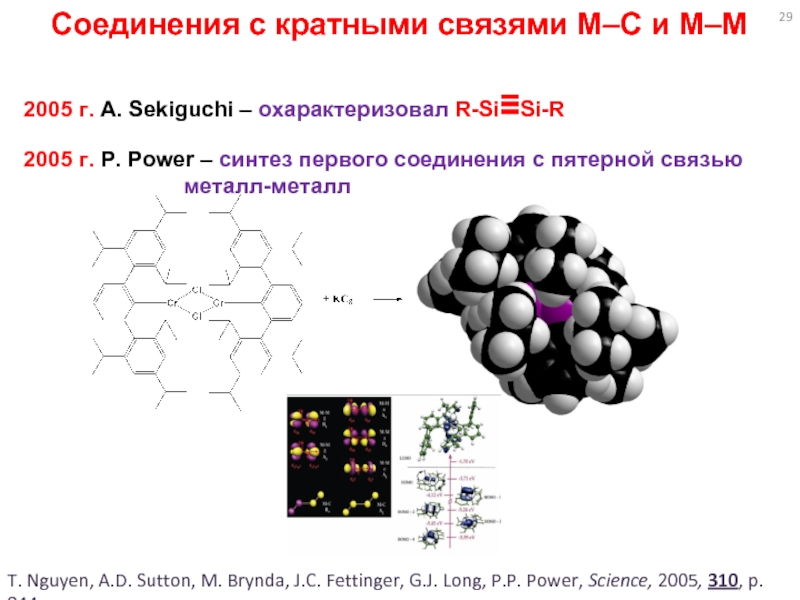
Слайд 29Соединения с кратными связями M–C и M–M
2005 г. A.
Sekiguchi – охарактеризовал R-Si≡Si-R
2005 г. P. Power – синтез первого
соединения с пятерной связьюметалл-металл
T. Nguyen, A.D. Sutton, M. Brynda, J.C. Fettinger, G.J. Long, P.P. Power, Science, 2005, 310, p. 844
Слайд 302004 г. E. Carmona – синтез первого соединения с пятерной
связью
металл-металл
Соединения с необычными связями M–M
I.Resa, E. Carmona, E.Gutierrez-Puebla, A.Monge
, Science, 2004, 305, p. 11362006 г. S.N. Konchenko, P.W. Roesky – синтез первых соединений
со связью Ln – Al
Gamer M. T., Roesky P. W., Konchenko S. N. e.a., Angew. Chem. Int. Ed. 2006, 45, 4447
2008 г. J. Arnold использовал этот подход для синтеза соединений
со связью U – Al и U – Ga
Minasian, S. G., Krinsky, J. L., Williams, V. A., Arnold, J. A JACS 2008, 130, 10086
Слайд 31История прикладной элементоорганической химии
Катализ
1922 г. T. Midgley, T.A. Boyd –
внедрили [Et4Pb] в качестве антидетонационной добавки в бензин
1938 г. O.
Roelen – открыл процесс гидроформилирования1939 г. W. Reppe – начинает цикл работ по каталитическим превращениям ацетиленов в коорд. сфере переходных металлов
1943 г. E.G. Rochow (Е.Г. Рохов) – разработал «прямой» метод синтеза хлорсиланов, позволивший получать их в промышленных масштабах
1955 г. K. Ziegler, G. Natta – разработали катализатор для получения изотактических полиалкенов:
“галогенид переходного металла + AlR3”
(Нобелевская премия 1963 г.)
Слайд 32История прикладной элементоорганической химии
Катализ
(Нобелевская премия 1973 г.)
1965 г. G. Wilkinson,
R.S. Coffey – установили, что [(Ph3P)3RhCl] выступает гомогенным катализатором в
реакциях гидрирования олефиновКатализатор Уилкинсона
1965 г. J. Tsuji – открыл активацию связи C–C на Pd
1969 г. А.Е. Шилов – открыл гомогенную активацию связи C–H алкенов на комплексах Pt(II) в растворе
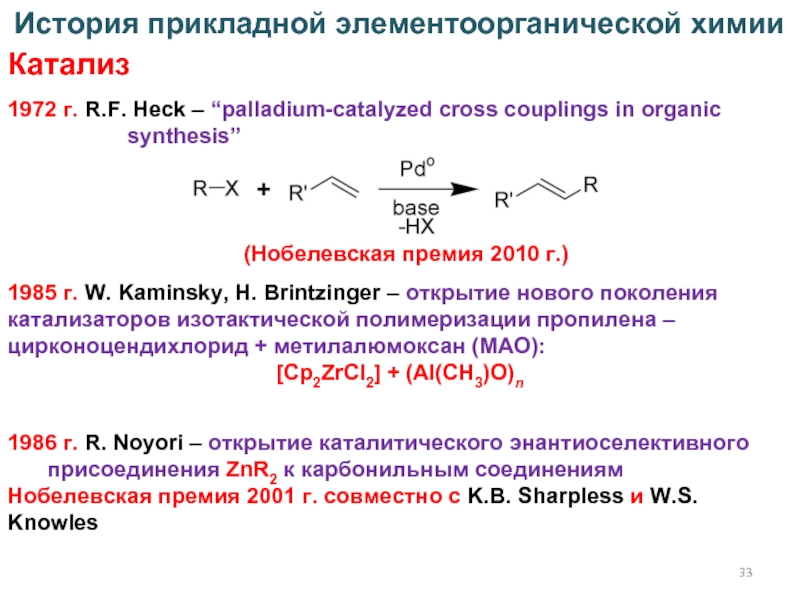
Слайд 331972 г. R.F. Heck – “palladium-catalyzed cross couplings in organic
synthesis”
История прикладной элементоорганической химии
Катализ
(Нобелевская премия 2010 г.)
1985 г. W. Kaminsky,
H. Brintzinger – открытие нового поколения катализаторов изотактической полимеризации пропилена – цирконоцендихлорид + метилалюмоксан (МАО):[Cp2ZrCl2] + (Al(CH3)O)n
1986 г. R. Noyori – открытие каталитического энантиоселективного присоединения ZnR2 к карбонильным соединениям
Нобелевская премия 2001 г. совместно с K.B. Sharpless и W.S. Knowles
Слайд 34История прикладной элементоорганической химии
Биохимия/Медицина
1909 г. P. Ehrlich – внедряет
Salvarsan как
лекарство от
сифилиса
(Нобелевская премия 1908
за развитие хемотерапии)
1979 г.
H. Kӧpf, P. Kӧpf-Maier – канцеростатическое действие
[Cp2TiCl2]
1961 г. D. Crowfoot Hodgkin
обнаруживает связь Co–C
в кобаламине с помощью РСА
(Нобелевская премия 1964 г.)











![Избранные главы металлоорганической химии Развитие химии π-комплексов1959 г. R. Criegee (1902-1975) – синтез [(η4-C4Me4)NiCl2]21965 г. R. Petit – синтез [(C4H4)Fe(CO)3]2 Развитие химии π-комплексов1959 г. R. Criegee (1902-1975) – синтез [(η4-C4Me4)NiCl2]21965 г. R. Petit – синтез [(C4H4)Fe(CO)3]2](/img/thumbs/e7a760914c567fa3f5d6b3b829014392-800x.jpg)
![Избранные главы металлоорганической химии 1989 г. H. Schnöckel – разработка синтеза AlCl(solv) и далее – 1989 г. H. Schnöckel – разработка синтеза AlCl(solv) и далее – [Cp*Al]41994 г. S. Harder – синтез](/img/thumbs/ef09700fc005ed61faf0517e722b5ff2-800x.jpg)
![Избранные главы металлоорганической химии Карбонильные комплексы1868 г. M.P. Schützenberger – синтез первого карбонильного комплекса [Pt(CO)Cl2]21890 Карбонильные комплексы1868 г. M.P. Schützenberger – синтез первого карбонильного комплекса [Pt(CO)Cl2]21890 г. L. Mond – синтез первого](/img/thumbs/cac07143efc182d9bfc9c9b54878e4ea-800x.jpg)

![Избранные главы металлоорганической химии История прикладной элементоорганической химииКатализ1922 г. T. Midgley, T.A. Boyd – внедрили История прикладной элементоорганической химииКатализ1922 г. T. Midgley, T.A. Boyd – внедрили [Et4Pb] в качестве антидетонационной добавки в](/img/thumbs/e052c735f1f48db324679e487c44b7a9-800x.jpg)
![Избранные главы металлоорганической химии История прикладной элементоорганической химииКатализ(Нобелевская премия 1973 г.)1965 г. G. Wilkinson, R.S. История прикладной элементоорганической химииКатализ(Нобелевская премия 1973 г.)1965 г. G. Wilkinson, R.S. Coffey – установили, что [(Ph3P)3RhCl] выступает](/img/thumbs/8072a6911da3103a7d1f9901c657a16e-800x.jpg)