Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Путешествие по стране карбонатов
Содержание
- 1. Путешествие по стране карбонатов
- 2. Кроссворд4АЙЫЛСИКЕЛГУ15ЗАМЛРО3АДСОРЯИЦБВОЛРНДИБ6КАРТНА7МЕЕРЫТЕ2Ч
- 3. Маршрутный лист ИНФОРМАЦИОННАЯЭКСПЕРИМЕНТАЛЬНАЯБИОЛОГО - ГЕОГРАФИЧЕСКАЯПРАКТИЧЕСКАЯКОНЕЧНАЯ
- 4. СТАНЦИЯ ИНФОРМАЦИОННАЯ
- 5. КАРБОНАТЫ – СОЛИ УГОЛЬНОЙ КИСЛОТЫСРЕДНИЕ КАРБОНАТЫ Na2CO3КИСЛЫЕ ГИДРОКАРБОНАТЫ NaHCO3
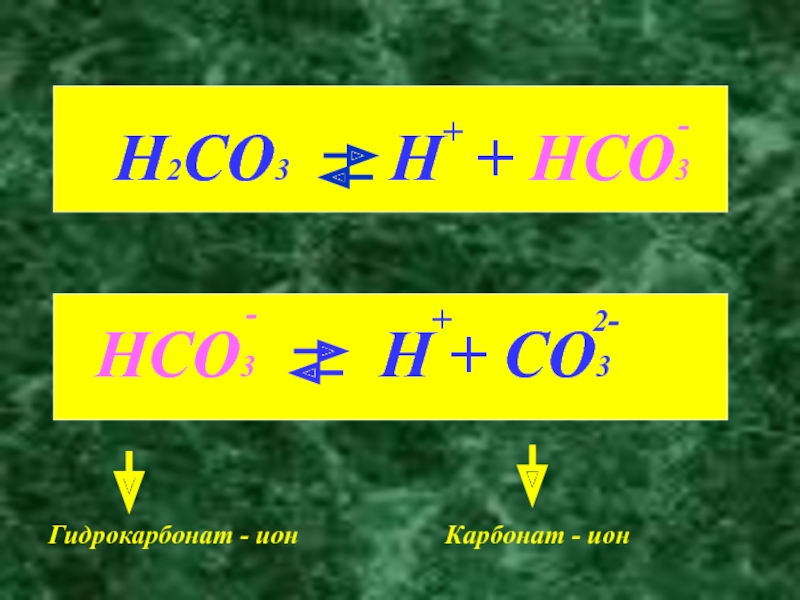
- 6. Гидрокарбонат - ионКарбонат - ион
- 7. КАРБОНАТЫ – СОЛИ УГОЛЬНОЙ КИСЛОТЫСРЕДНИЕ КАРБОНАТЫ Na2CO3КИСЛЫЕ ГИДРОКАРБОНАТЫ NaHCO3
- 8. СОСТАВИТЬ ФОРМУЛЫКАРБОНАТ ЦИНКАГИДРОКАРБОНАТ КАЛИЯКАРБОНАТ АММОНИЯГИДРОКАРБОНАТ МАГНИЯZnCO3KHCO3(NH4)2CO3Mg(HCO3)2
- 9. СТАНЦИЯ ЭКСПЕРИМЕНТАЛЬНАЯ
- 10. Взаимодействие с сильными кислотамиCaCO3+2HCl = CaCl2 +H2O+CO2Качественные реакции
- 11. Ca(OH)2+CO2
- 12. Превращение гидрокарбонатов в карбонатыа) при нагревании2NaHCO3
- 13. Na2 CO3+BaCl2 BaCO3 +2NaClВзаимодействие
- 14. ОСУЩЕСТВИТЕ ПРЕВРАЩЕНИЕ I. Ca(OH)2
- 15. РЕШЕНИЕ:I.1) Ca(OH)2 + CO2
- 16. СТАНЦИЯ БИОЛОГО - ГЕОГРАФИЧЕСКАЯ1,7% земной коры – карбонатные породы
- 17. КОРАЛЛОВЫЕ ПОЛИПЫ – CaCO3
- 18. CaCO3+CO2+H2O Ca(HCO3)2Ca(HCO3)2
- 19. СТАЛАКТИТЫСТАЛАГМИТЫ
- 20. СТАНЦИЯ ПРАКТИЧЕСКАЯ
- 21. ИЗВЕСТНЯК – CaCO3
- 22. МРАМОР – CaCO3
- 23. МРАМОРНЫЙ ДВОРЕЦ
- 24. Na HCO3 – ПИТЬЕВАЯ СОДАNaHCO3 + HCl = NaCl + CO2 + H2O
- 25. Слайд 25
- 26. СТАНЦИЯ КОНЕЧНАЯ
- 27. 1)Какие три брата из семейства карбонатов
- 28. 3) Что такое сталактиты? Каменные сосульки в
- 29. 5) Как еще называют гидрокарбонат натрия
- 30. Домашнее задание.Составить реакции к проведенному опыту.Конец.
- 31. Скачать презентанцию
Кроссворд4АЙЫЛСИКЕЛГУ15ЗАМЛРО3АДСОРЯИЦБВОЛРНДИБ6КАРТНА7МЕЕРЫТЕ2Ч
Слайды и текст этой презентации
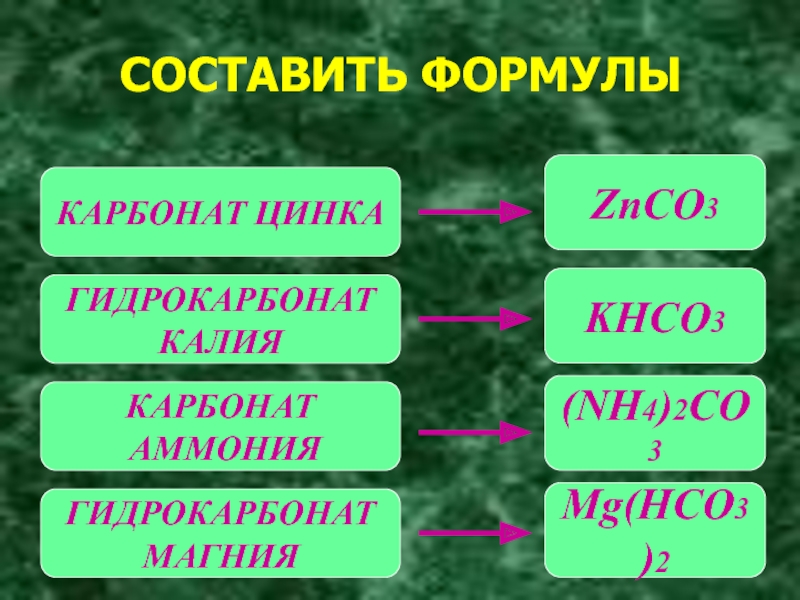
Слайд 8СОСТАВИТЬ ФОРМУЛЫ
КАРБОНАТ ЦИНКА
ГИДРОКАРБОНАТ
КАЛИЯ
КАРБОНАТ
АММОНИЯ
ГИДРОКАРБОНАТ
МАГНИЯ
ZnCO3
KHCO3
(NH4)2CO3
Mg(HCO3)2
Слайд 12Превращение гидрокарбонатов в карбонаты
а) при нагревании
2NaHCO3
Na2CO3 + H2O+CO2
б) при действии щёлочи
NaHCO3 + NaOH
Na2CO3 + H2OСлайд 13Na2 CO3+BaCl2 BaCO3 +2NaCl
Взаимодействие
с растворами солей
Разложение
карбонатов
MgCO3 MgO + CO2
Слайд 14
ОСУЩЕСТВИТЕ ПРЕВРАЩЕНИЕ
I. Ca(OH)2
CaCO3 Ca(HCO3)2
II. NaOH
Na2CO3 NaHCO3III. Na2CO3 BaCO3 CO2
Слайд 15РЕШЕНИЕ:
I.
1) Ca(OH)2 + CO2 CaCO3 + H2O
2)
CaCO3 + CO2 + H2O Ca(HCO3)2
II.
1) 2NaOH
+ CO2 Na2CO3 + H2O 2) Na2CO3+CO2+H2O 2NaHCO3
III.
1)Na2CO3+BaCl2 BaCO3+2NaCl
2) BaCO3 + 2HCl BaCl2 +CO2+ H2O
Слайд 271)Какие три брата из семейства
карбонатов живут на Земле?
Мрамор, известняк,
мел.
2) Зачем хозяйки добавляют
питьевую соду в тесто?
2NaHCO3
Na2CO3 + H2O+CO2 Углекислый газ делает
тесто пористым.
Слайд 283) Что такое сталактиты?
Каменные сосульки в пещерах
состоящие из
карбоната кальция.
4) Как химическим путем
очистить яйцо от скорлупы,
не
разбивая его?Растворить скорлупу с помощью
соляной кислоты.