Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Механизм реакций присоединения алкенов
Содержание
- 1. Механизм реакций присоединения алкенов
- 2. Оқыту мақсаттары:Learning Objectives: understand the terms ‘electrophile’
- 3. Активити:
- 4. MEET THE ATTACKERSВСТРЕЧА атакующихPress the space bar
- 5. MEET THE ATTACKERSI AM A NUCLEOPHILEI HAVE
- 6. MEET THE ATTACKERSPress the space bar
- 7. MEET THE ATTACKERSI AM AN ELECTROPHILEI HAVE
- 8. MEET THE ATTACKERSPress the space bar
- 9. MEET THE ATTACKERSAND I AM A FREE
- 10. Нуклеофил• Перевод: ядро любящий• Химическое значение: Реагирует
- 11. Электрофил• Перевод: Электронно-любящий• Химическая значение: Реагирует с
- 12. Активити:What am I?CH2=CH2,
- 13. Механизмы реакций в органической химииПо типу разрыва
- 14. Механизмы реакций в органической химииВ каждой органической
- 15. ActivityWHAT ATTACKS ALKENES?
- 16. ALKENES ARE MUCH MORE REACTIVE THAN ALKANESАлкены
- 17. CHEMICAL PROPERTIES OF ALKENESELECTROPHILIC ADDITION MECHANISMThe main
- 18. Основной реакцией алкенов является присоединение. Дополнительная электронная
- 19. CHEMICAL PROPERTIES OF ALKENESELECTROPHILIC ADDITION MECHANISMThe electrophile,
- 20. Химические свойства алкенов Электрофильный механизм присоединенияЭлектрофил, имеющий
- 21. CHEMICAL PROPERTIES OF ALKENESELECTROPHILIC ADDITION OF HYDROGEN BROMIDEANIMATED MECHANISM
- 22. CHEMICAL PROPERTIES OF ALKENESELECTROPHILIC ADDITION OF BROMINEReagent Bromine.
- 23. CHEMICAL PROPERTIES OF ALKENESELECTROPHILIC ADDITION MECHANISMReagent Hydrogen bromide...
- 24. CHEMICAL PROPERTIES OF ALKENESELECTROPHILIC ADDITION OF SULPHURIC
- 25. Activity:Напишите механизм реакции этена с серной кислотой
- 26. Слайд 26
- 27. Скачать презентанцию
Слайды и текст этой презентации
Слайд 2
Оқыту мақсаттары:
Learning Objectives:
understand the terms ‘electrophile’ and ‘nucleophile’ and
be able to classify reagents
know some examples and be able to apply the mechanism to new casesСлайд 5
MEET THE ATTACKERS
I AM A NUCLEOPHILE
I HAVE A LONE PAIR
WHICH I CAN USE TO FORM A NEW BOND.
I ATTACK
ELECTRON DEFICIENT AREAS (those with a + or δ+)Слайд 7
MEET THE ATTACKERS
I AM AN ELECTROPHILE
I HAVE A + CHARGE
or a δ+ CHARGE. I ATTACK ELECTRON RICH AREAS SUCH
AS C=C DOUBLE BONDS.Слайд 9
MEET THE ATTACKERS
AND I AM A FREE RADICAL
I HAVE AN
UNPAIRED ELECTRON WHICH I WANT TO PAIR UP. I AM
VERY REACTIVE AND DON’T MIND WHERE I ATTACK… WATCH OUT!Слайд 10Нуклеофил
• Перевод: ядро любящий
• Химическое значение: Реагирует с положительными зарядами(или
частично положительные) атомов
(электрофилы: электронно-любящий)
• Знание: Нуклеофильные атомы –это те атомы
у которых есть либо одинокие пары или пи связи, которые могут быть использованы для формирования новых связей в электрофиламиК нуклеофилам относятся отрицательно заряженные ионыК нуклеофилам относятся отрицательно заряженные ионы , нейтральныемолекулыК нуклеофилам относятся отрицательно заряженные ионы , нейтральныемолекулы, обладающие свободной паройК нуклеофилам относятся отрицательно заряженные ионы , нейтральныемолекулы, обладающие свободной парой электронов
Слайд 11Электрофил
• Перевод: Электронно-любящий
• Химическая значение: Реагирует с источниками
электронов (нуклеофилы: ядро
любящий)
• Технические характеристики: Электрофильные реагенты• Технические характеристики: Электрофильные реагенты, или электрофилы, при
образовании новой связи служат акцепторами пары• Технические характеристики: Электрофильные реагенты, или электрофилы, при образовании новой связи служат акцепторами пары электронов• Технические характеристики: Электрофильные реагенты, или электрофилы, при образовании новой связи служат акцепторами пары электронов и вытесняют уходящую группу в виде положительно заряженной частицы. К электрофилам относятся положительно заряженные ионы• Технические характеристики: Электрофильные реагенты, или электрофилы, при образовании новой связи служат акцепторами пары электронов и вытесняют уходящую группу в виде положительно заряженной частицы. К электрофилам относятся положительно заряженные ионы (нейтральные молекулы• Технические характеристики: Электрофильные реагенты, или электрофилы, при образовании новой связи служат акцепторами пары электронов и вытесняют уходящую группу в виде положительно заряженной частицы. К электрофилам относятся положительно заряженные ионы (нейтральные молекулы с электронным дефицитом, например , и сильно поляризованные молекулыСлайд 12Активити:
What am I?
CH2=CH2,
HO-
CH3+Br - , OH -, C N -
H-O-H, H3N, NO2 +
Cl2, I2, HCl, HOSO2OH
Слайд 13Механизмы реакций в органической химии
По типу разрыва химической связи органические
реакции подразделяют на радикальные и ионные.
При радикальных реакциях происходит гомолитический
разрыв общей электронной пары, образующей связь. При этом образуются свободные радикалы, имеющие неспаренный электрон.В ионных реакциях происходит гетеролитический разрыв связи. Образуются две частицы: нуклеофил (-) и электрофил (+).
Слайд 14Механизмы реакций в органической химии
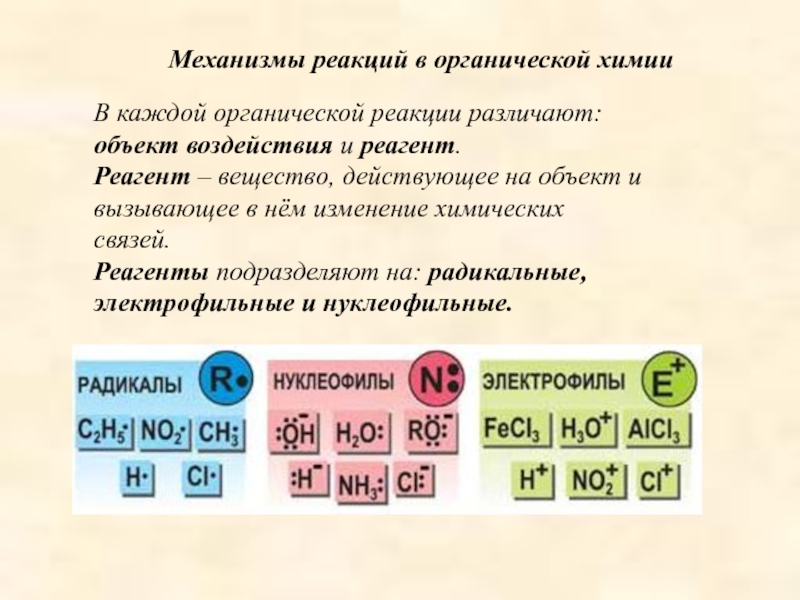
В каждой органической реакции различают: объект
воздействия и реагент.
Реагент – вещество, действующее на объект и вызывающее
в нём изменение химических связей.Реагенты подразделяют на: радикальные, электрофильные и нуклеофильные.
Слайд 16ALKENES ARE MUCH MORE REACTIVE THAN ALKANES
Алкены - более реактивные
чем АЛКАНЫ
ALKENES CONTAIN A C=C BOND
There will be twice as
many electrons between the carbon atoms as there are in a single bondВ алкенах в два раза больше электронов между атомами углерода, чем одинарная связь
WHAT ATTACKS ALKENES?
C=C bond is double – an electron rich area
Связи С = С двойной - богатая область электронами
Bonds are non-polar - no electron deficient areas
Связи неполярны - отсутствуют электронодефицитные зоны
ELECTROPHILIC ADDITION
Слайд 17CHEMICAL PROPERTIES OF ALKENES
ELECTROPHILIC ADDITION MECHANISM
The main reaction of alkenes
is addition
Because of the extra electron density in a C=C
double bond, alkenes are attacked by species which ‘like’ electrons.These species are called electrophiles; they
possess a positive or partial positive charge
somewhere in their structure.
Examples include... hydrogen halides
concentrated H2SO4
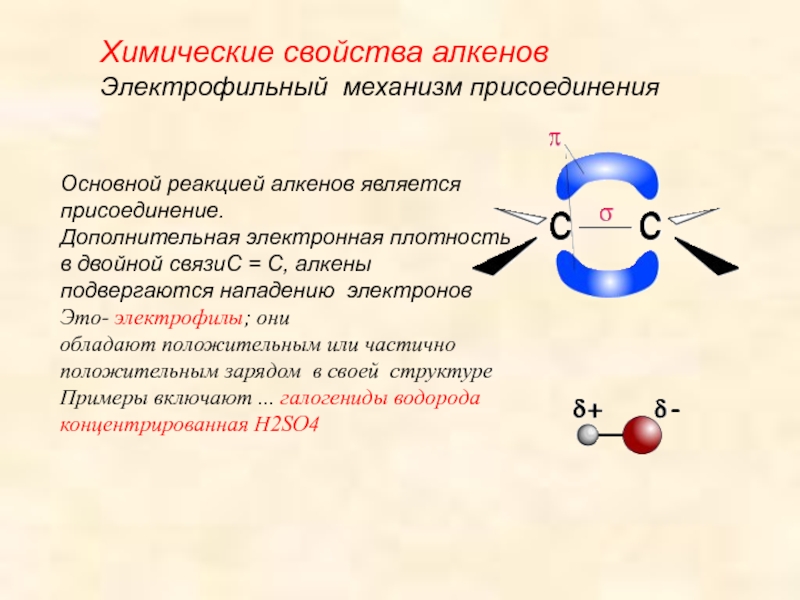
Слайд 18Основной реакцией алкенов является присоединение. Дополнительная электронная плотность в двойной связиС
= С, алкены подвергаются нападению электронов
Это- электрофилы; они
обладают положительным или
частично положительным зарядом в своей структуре
Примеры включают ... галогениды водорода
концентрированная H2SO4Химические свойства алкенов
Электрофильный механизм присоединения
Слайд 19CHEMICAL PROPERTIES OF ALKENES
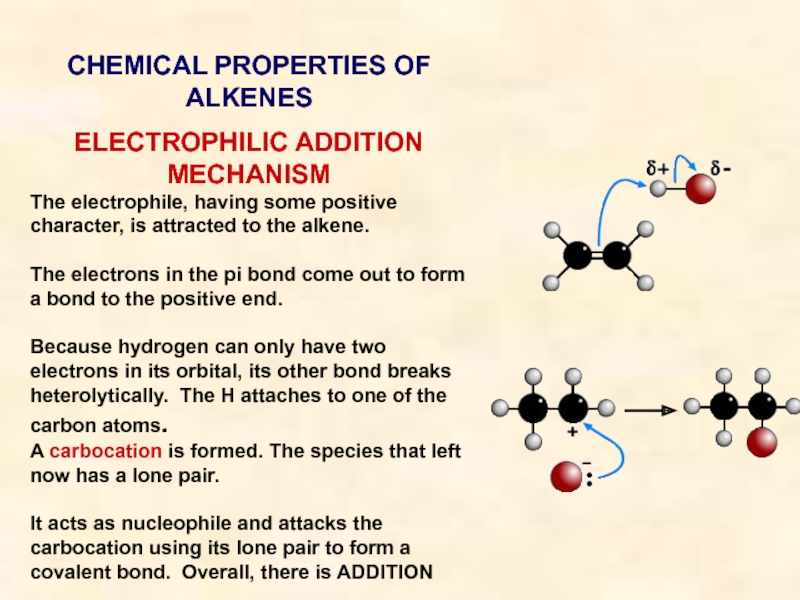
ELECTROPHILIC ADDITION MECHANISM
The electrophile, having some positive
character, is attracted to the alkene.
The electrons in the pi
bond come out to form a bond to the positive end.Because hydrogen can only have two electrons in its orbital, its other bond breaks heterolytically. The H attaches to one of the carbon atoms.
A carbocation is formed. The species that left now has a lone pair.
It acts as nucleophile and attacks the carbocation using its lone pair to form a covalent bond. Overall, there is ADDITION
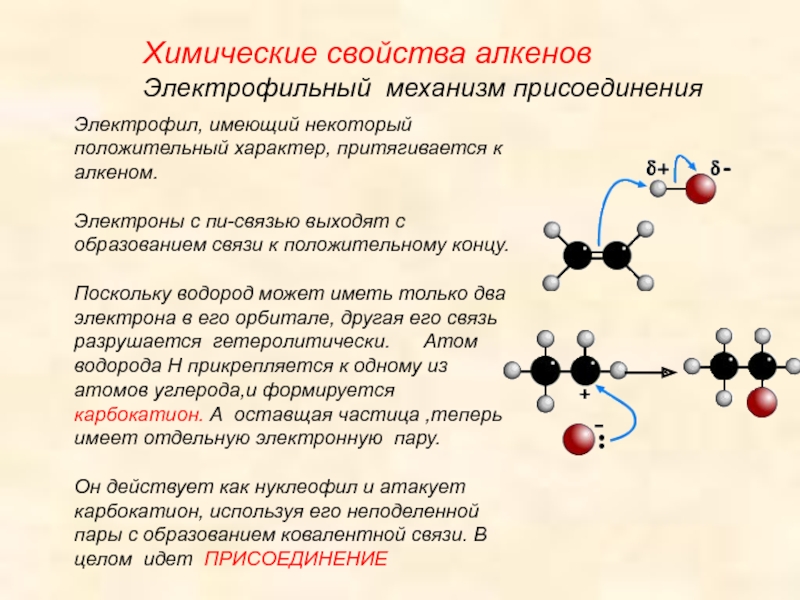
Слайд 20Химические свойства алкенов
Электрофильный механизм присоединения
Электрофил, имеющий некоторый положительный характер, притягивается
к алкеном. Электроны с пи-связью выходят с образованием связи к положительному
концу. Поскольку водород может иметь только два электрона в его орбитале, другая его связь разрушается гетеролитически. Атом водорода H прикрепляется к одному из атомов углерода,и формируется карбокатион. А оставщая частица ,теперь имеет отдельную электронную пару. Он действует как нуклеофил и атакует карбокатион, используя его неподеленной пары с образованием ковалентной связи. В целом идет ПРИСОЕДИНЕНИЕСлайд 22CHEMICAL PROPERTIES OF ALKENES
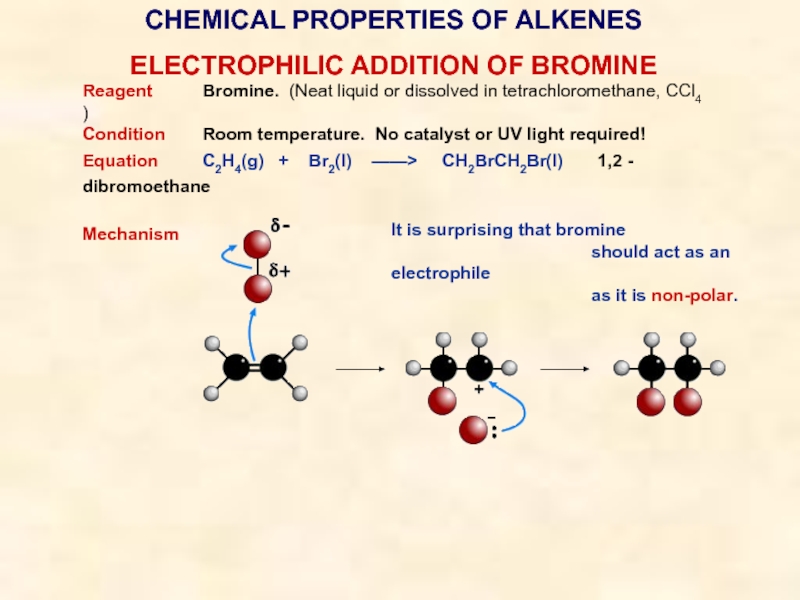
ELECTROPHILIC ADDITION OF BROMINE
Reagent Bromine. (Neat liquid or
dissolved in tetrachloromethane, CCl4 )
Condition Room temperature. No catalyst or UV
light required!Equation C2H4(g) + Br2(l) ——> CH2BrCH2Br(l) 1,2 - dibromoethane
Mechanism
It is surprising that bromine
should act as an electrophile
as it is non-polar.
Слайд 23CHEMICAL PROPERTIES OF ALKENES
ELECTROPHILIC ADDITION MECHANISM
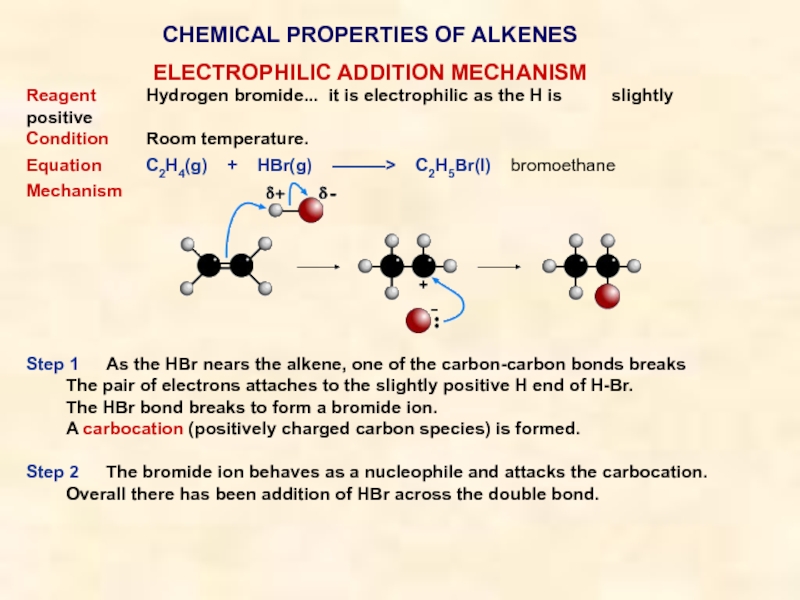
Reagent Hydrogen bromide... it is electrophilic
as the H is slightly positive
Condition Room
temperature.Equation C2H4(g) + HBr(g) ———> C2H5Br(l) bromoethane
Mechanism
Step 1 As the HBr nears the alkene, one of the carbon-carbon bonds breaks
The pair of electrons attaches to the slightly positive H end of H-Br.
The HBr bond breaks to form a bromide ion.
A carbocation (positively charged carbon species) is formed.
Step 2 The bromide ion behaves as a nucleophile and attacks the carbocation.
Overall there has been addition of HBr across the double bond.
Слайд 24CHEMICAL PROPERTIES OF ALKENES
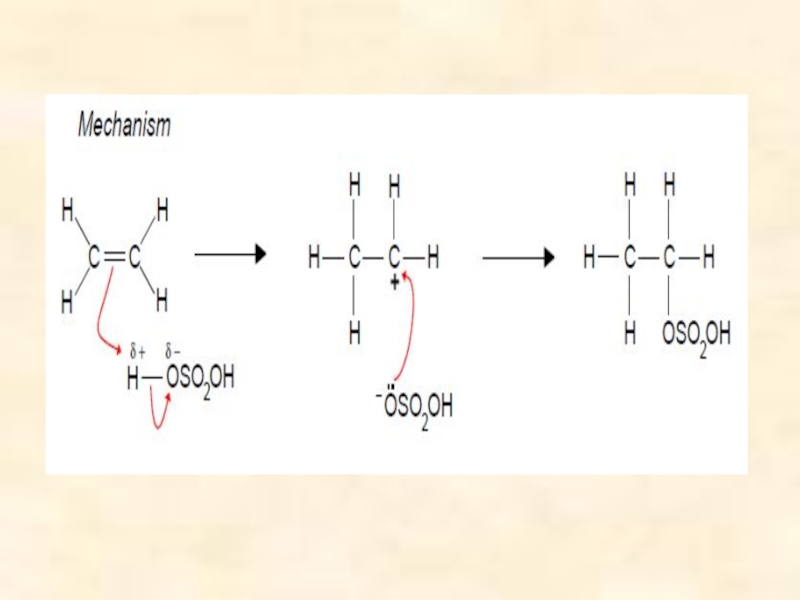
ELECTROPHILIC ADDITION OF SULPHURIC ACID
Reagent Concentrated sulphuric acid
(85%)
Conditions 0°C
Equation C2H4(g) + H2SO4(conc) ——> C2H5OSO2OH(aq)
ethyl hydrogensulphateHydrolysis the product can be converted to ethanol by boiling with water.
C2H5OSO2OH(aq) + H2O(l) ——> H2SO4(aq) + C2H5OH(l)
Industrial method(s) Phosphoric acid (H3PO4) and steam are used - see later
Ethanol can also be made by FERMENTATION