Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Обобщающий урок "Основные классы Неорганических соединений" 8 класс
Содержание
- 1. Обобщающий урок "Основные классы Неорганических соединений" 8 класс
- 2. Многообразие веществ
- 3. СоставСложные вещества, включающие в себя два химических
- 4. СоставСложные вещества, состоящие из атомов металлов, соединённых
- 5. Кислоты СоставСложные вещества, состоящие из одного или
- 6. Соли СоставСложные вещества, состоящие из атомов металла,
- 7. Проверим наши знания. Разнесите формулы из списка
- 8. Оксиды
- 9. От чего зависят свойства веществ?Чем обусловлено строение
- 10. Скачать презентанцию
Многообразие веществ
Слайды и текст этой презентации
Слайд 3Состав
Сложные вещества, включающие в себя два химических элемента, причём один
из них – кислород.
Примеры
Газы: CO2, SO2, NO2. Жидкости: H2O.
Твёрдые: SiO2, MgO.Классификация
Кислотные: CO2, SO3, N2O5…
Амфотерные: ZnO, Al2O3…
Основные: Na2O, CuO, MgO…
Оксиды
Слайд 4Состав
Сложные вещества, состоящие из атомов металлов, соединённых с одной или
несколькими гидроксильными группами.
Примеры
Все – твёрдые вещества: NaOH, Fe(OH)3, Cu(OH)2…
Классификация
Нерастворимые в
воде основания:Cu(OH)2, Al(OH)3, Fe(OH)2…
Щёлочи (растворимые в воде основания) :
NaOH, LiOH, Ca(OH)2, KOH …
Основания
Слайд 5Кислоты
Состав
Сложные вещества, состоящие из одного или нескольких атомов водорода,
соединённых с кислотным остатком
Примеры
HCl, HNO3, H2SO4, H3PO4, H2CO3
… Классификация
Слайд 6Соли
Состав
Сложные вещества, состоящие из атомов металла, соединённых с кислотными
остатками.
Примеры
Все – твёрдые вещества: NaCl, K2CO3, CaSO4, KMnO4 …
Классификация
Нейтральные: Na2CO3,
CuSO4, CaCO3 …Кислые : NaHCO3, KHSO4 …
Основные: СuOHCl, CaOHNO3 …
Слайд 7Проверим наши знания.
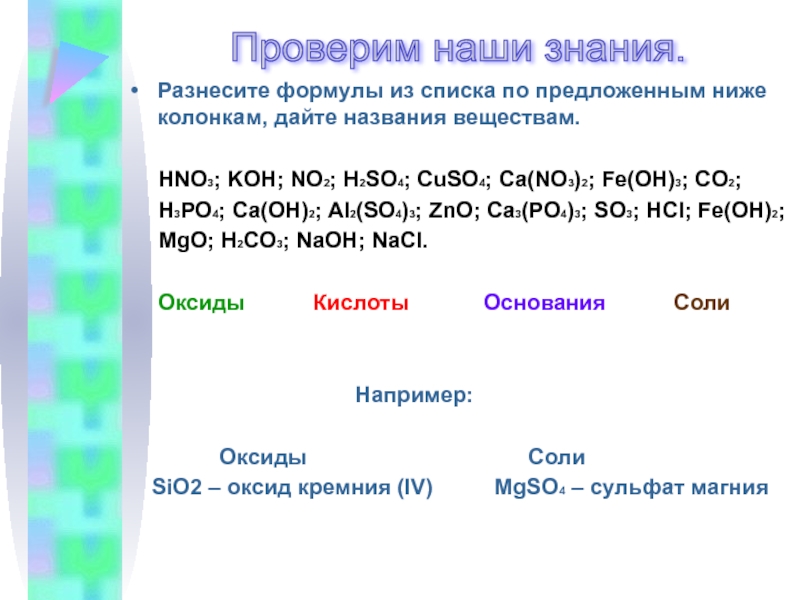
Разнесите формулы из списка по предложенным ниже
колонкам, дайте названия веществам.
HNO3; KOH; NO2; H2SO4;
CuSO4; Ca(NO3)2; Fe(OH)3; CO2; H3PO4; Ca(OH)2; Al2(SO4)3; ZnO; Ca3(PO4)3; SO3; HCl; Fe(OH)2;
MgO; H2CO3; NaOH; NaCl.
Оксиды Кислоты Основания Соли
Например:
Оксиды Соли
SiO2 – оксид кремния (IV) MgSO4 – сульфат магния
Слайд 8 Оксиды
Кислоты
NO2 – оксид азота (IV) HNO3 – азотная кислота
CO2 – Оксид углерода (IV) H2SO4 – серная кислота
ZnO – оксид цинка H3PO4 – фосфорная кислота
SO3 – оксид серы (VI) HCl – хлороводородная к – та
MgO – оксид магния H2CO3 – угольная кислота
Основания Соли
KOH – гидроксид калия CuSO4 – сульфат меди (II)
Fe(OH) 3 – гидроксид железа (III) Ca(NO3) 2 – нитрат кальция
Ca(OH) 2 – гидроксид кальция Al2(SO4)3 – сульфат алюминия
Fe(OH)2 – гидроксид железа (II) Ca3(PO4)2 – фосфат кальция
NaOH – гидроксид натрия Na2CO3 – карбонат натрия
Сравним ответы