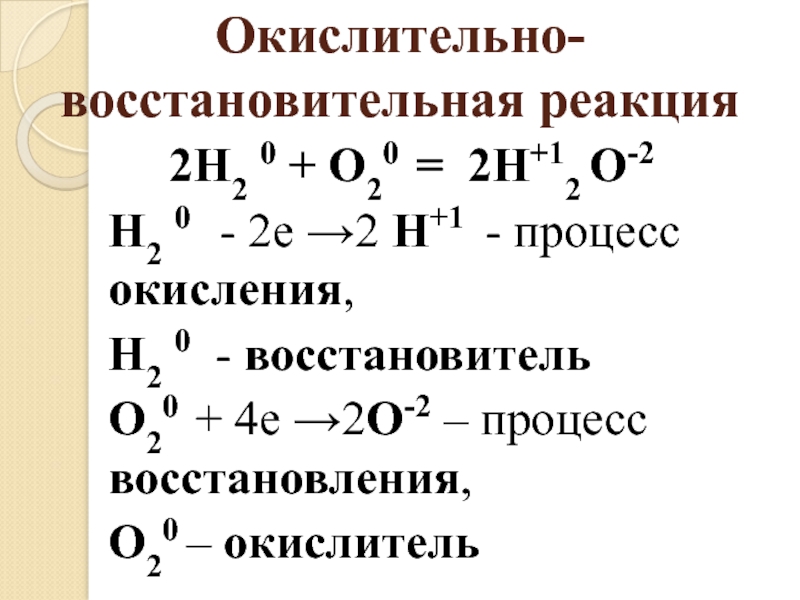Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Окислительно - восстановительные реакции
Содержание
- 1. Окислительно - восстановительные реакции
- 2. Признак классификации химической реакцииПо числу и составу реагирующих и образующихся веществПо тепловому эффекту???
- 3. Окислительно-восстановительная реакция 2Н2 0
- 4. С0 →
- 5. С0 → С-4 степень
- 6. Признак классификации химической реакцииПо числу и составу реагирующих и образующихся веществПо тепловому эффектуПо изменению степени окисления
- 7. Химические реакцииC(тв.) + O2 (г.) = CO2(г.)↑ CaCO3(тв.)=tCO2(г.)↑+ + СaO(тв.)
- 8. Химические реакции1) C0 + O02 = C+4O-22↑ окислительно-восстановительная реакция2) Ca+2C+4O-23 =t C+2O-22↑+Ca+2O-2 не окислительно-восстановительная реакция
- 9. Работа с терминамиОкислительВосстановительОкислениеВосстановлениеОкислительно-восстановительная реакция
- 10. Тестовое заданиеЗадание № 1.I вариантК окислительно-восстановительным реакциям
- 11. Тестовое заданиеЗадание № 2.I вариантВ каком соединении
- 12. Тестовое заданиеЗадание № 3.I вариантСхема Na0
- 13. Тестовое заданиеЗадание № 4.I вариантВосстановительные свойства простых
- 14. Ответы на тестовое заданиеI вариант1 - В2
- 15. Тема урока: Окислительно-восстановительные реакции 4Fe0 + 3O02 + 6H2O ? 4Fe+3(O-2H)3 КОРРОЗИЯ
- 16. Слайд 16
- 17. Скачать презентанцию
Слайды и текст этой презентации
Слайд 2Признак классификации химической реакции
По числу и составу реагирующих и образующихся
веществ
Слайд 3Окислительно-восстановительная реакция
2Н2 0 + O20 =
2Н+12 O-2
Н2 0 - 2е →2 Н+1 -
процесс окисления, Н2 0 - восстановитель
O20 + 4е →2О-2 – процесс восстановления,
O20 – окислитель
Слайд 6Признак классификации химической реакции
По числу и составу реагирующих и образующихся
веществ
По тепловому эффекту
По изменению степени окисления
Слайд 8Химические реакции
1) C0 + O02 = C+4O-22↑
окислительно-восстановительная реакция
2) Ca+2C+4O-23
=t C+2O-22↑+Ca+2O-2
не окислительно-восстановительная реакция
Слайд 9Работа с терминами
Окислитель
Восстановитель
Окисление
Восстановление
Окислительно-
восстановительная реакция
Слайд 10Тестовое задание
Задание № 1.
I вариант
К окислительно-
восстановительным
реакциям не относится
реакция,
представленная
схемой:
А) N2 + 3Н2 = 2NН3
Б) Mg +
2HCl = MgCl2 + + H2↑
В)MgCO3 = MgO + CO2 ↑
Г) 2CuO = 2Cu + O2↑
Задание № 1.
II вариант
К окислительно-
восстановительным
реакциям относится
реакция, представленная
схемой:
А) H2O + CaO = Ca(OH)2
Б) H2O + N2O5 = 2HNO3
В) Na2CO3 + 2HCl = 2NaCl + H2O + CO2
Г) CuO + H2 = Cu + H2O
Слайд 11Тестовое задание
Задание № 2.
I вариант
В каком соединении
степени окисления
элементов
равны -3 и +1
А) NF3 Б)
Cl2O3В) NH3 Г) AlCl3
Задание № 2.
II вариант
В каком соединении
степени окисления
элементов равны +3 и -2
А) NF3 Б) Cl2O3
В) NH3 Г) AlCl3
Слайд 12Тестовое задание
Задание № 3.
I вариант
Схема Na0 → Na+1
отражает процесс:
А) Окисления
Б) Восстановления
В) Нейтрализации
Г) Диссоциации
Задание № 3.
II
вариантСхема Сl0 → Сl-1
отражает процесс:
А) Окисления
Б) Восстановления
В) Нейтрализации
Г) Диссоциации
Слайд 13Тестовое задание
Задание № 4.
I вариант
Восстановительные свойства
простых веществ,
образованных элементами
второго периода, с
увеличением заряда ядра:
А) Уменьшаются
Б) Усиливаются
В)
Изменяются периодическиГ) Не изменяются
Задание № 4.
II вариант
Окислительные свойства
простых веществ,
образованных элементами
седьмой группы, главной
подгруппы с увеличением
заряда ядра:
А) Уменьшаются
Б) Усиливаются
В) Изменяются периодически
Г) Не изменяются