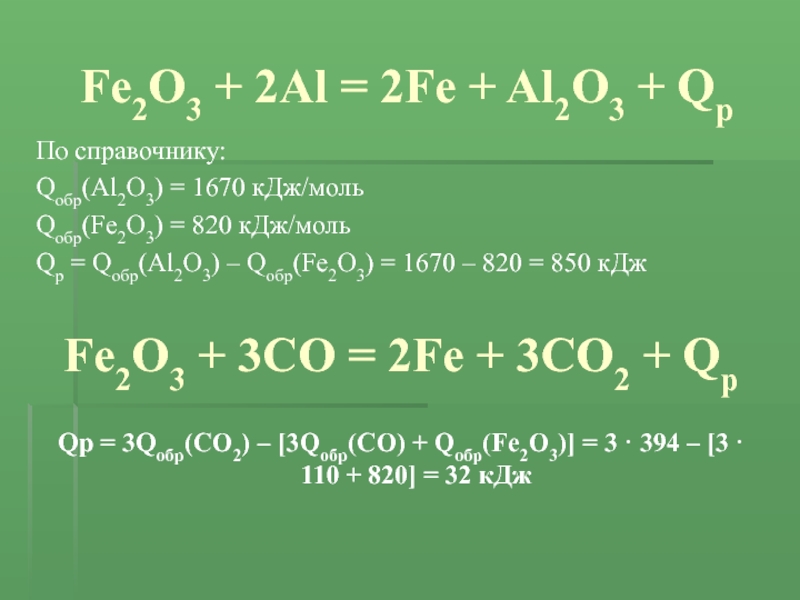Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Почему протекают химические реакции
Содержание
- 1. Почему протекают химические реакции
- 2. Первый закон термодинамики – закон сохранения энергииЭнергия
- 3. Энергия объектаКинетическая Потенциальная
- 4. Е реагентов > Е продуктовЭнергия выделяется в
- 5. Е реагентов < Е продуктовЭнергия поглощается из
- 6. Энергия, которая выделяется или поглощается в химической
- 7. Для расчета тепловых эффектов реакций используют значения
- 8. Закон Гесса (1840)Тепловой эффект химической реакции не
- 9. Следствие из закона ГессаТепловой эффект химической реакции
- 10. Fe2O3 + 2Al = 2Fe + Al2O3
- 11. Энтальпия (теплосодержание) – это величина, которая характеризует
- 12. Движущая сила реакцийДля экзотермических реакций – стремление
- 13. Слайд 13
- 14. ВыводыНаправление химической реакции определяется двумя факторами: стремлением
- 15. Возможность протекания реакций в зависимости от ΔH и ΔS
- 16. Энергия Гиббса (G)ΔG = ΔH – TΔST
- 17. Скачать презентанцию
Первый закон термодинамики – закон сохранения энергииЭнергия не возникает из ничего и не исчезает бесследно, а только переходит из одной формы в другую
Слайды и текст этой презентации
Слайд 1Почему протекают химические реакции
Начала термодинамики
Автор: Фельдман Людмила Валентиновна, учитель химии
МБОУ СОШ им. А.М.Горького г.Карачева Брянской обл.
Слайд 2Первый закон термодинамики – закон сохранения энергии
Энергия не возникает из
ничего и не исчезает бесследно, а только переходит из одной
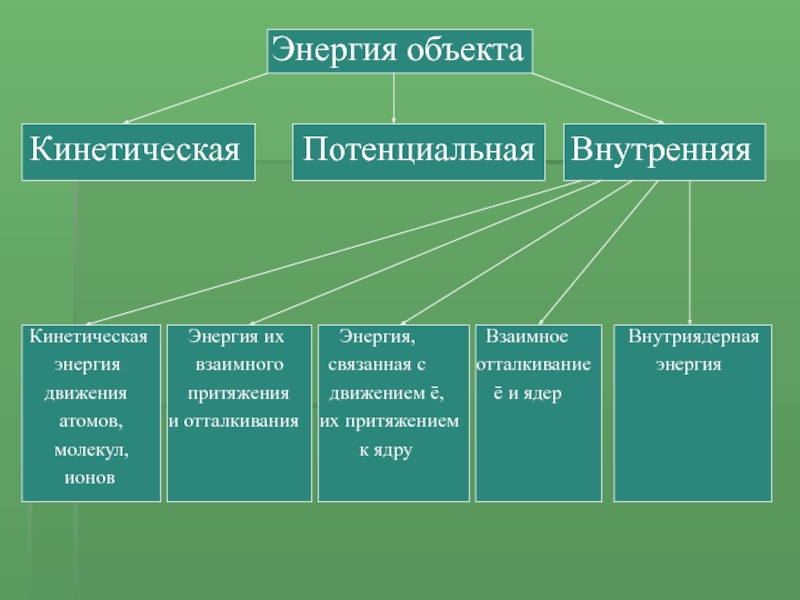
формы в другуюСлайд 3Энергия объекта
Кинетическая Потенциальная Внутренняя
Кинетическая
Энергия их
Энергия, Взаимное Внутриядернаяэнергия взаимного связанная с отталкивание энергия
движения притяжения движением ē, ē и ядер
атомов, и отталкивания их притяжением
молекул, к ядру
ионов
Слайд 4Е реагентов > Е продуктов
Энергия выделяется в окружающую среду
Реакции, при
которых выделяется энергия и нагревается окружающая среда, называются экзотермическими.
Слайд 5Е реагентов < Е продуктов
Энергия поглощается из окружающей среды, температура
системы понижается
Реакции, при протекании которых энергия поглощается из окружающей среды,
называется эндотермической.Слайд 6Энергия, которая выделяется или поглощается в химической реакции, называется тепловым
эффектом реакции.
Тепловой эффект реакции
выражается в кДж и его относят
к тем количествам веществ, которые определены уравнением.Уравнение, в котором указан тепловой эффект реакции, называется термохимическим.
2H2 + O2 = 2H2O + 484 кДж
Слайд 7Для расчета тепловых эффектов реакций используют значения величин теплот образования
исходных веществ и продуктов реакции
Теплота образования соединения (Qобр) – это
тепловой эффект реакции образования одного моля соединения из простых веществ, устойчивых в стандартных условиях (25°С, 1 атм)При таких условиях теплота образования простых веществ равна 0.
C + O2 = CO2 + 394 кДж
теплоты образования
0,5N2 + 0,5O2 = NO – 90 кДж
Слайд 8Закон Гесса (1840)
Тепловой эффект химической реакции не зависит от промежуточных
стадий (при условии, что исходные вещества и продукты реакции одинаковы).
С
+ O2 → CO2 + 394 кДж/моль (Q1)а) С + 0,5O2 → CO + ?(Q2)
б) CO + 0,5O2 → CO2 + 284 кДж/моль(Q3)
Q1 = Q2 + Q3
Q2 = Q1 – Q3 = 394 – 284 = 110 кДж
Слайд 9Следствие из закона Гесса
Тепловой эффект химической реакции равен сумме теплот
образования всех продуктов реакции минус сумма теплот образования всех реагентов
(с учетом коэффициентов в уравнении реакции):Qр = ΣQобр(продукты) – ΣQобр(реагенты)
Слайд 10Fe2O3 + 2Al = 2Fe + Al2O3 + Qр
По справочнику:
Qобр(Al2O3) = 1670 кДж/моль
Qобр(Fe2O3) = 820 кДж/моль
Qр = Qобр(Al2O3) –
Qобр(Fe2O3) = 1670 – 820 = 850 кДжFe2O3 + 3CO = 2Fe + 3CO2 + Qр
Qр = 3Qобр(CO2) – [3Qобр(CO) + Qобр(Fe2O3)] = 3 · 394 – [3 · 110 + 820] = 32 кДж
Слайд 11Энтальпия (теплосодержание) – это величина, которая характеризует запас энергии в
веществе.
ΔH = ΣHпродукты – ΣHреагенты
ΔH = -Qреакции
Для экзотермической реакции:
Q >
0, ΔH < 0Для эндотермической реакции
Q < 0, ΔH > 0
(ΔH обр – справочное значение)
Слайд 12Движущая сила реакций
Для экзотермических реакций – стремление системы к состоянию
с наименьшей внутренней энергией.
Для эндотермических реакций – стремление любой системы
в наиболее вероятному состоянию, которое характеризуется максимальным беспорядком, более высокой энтропией.Энтропия – мера хаоса.
Слайд 14Выводы
Направление химической реакции определяется двумя факторами: стремлением к уменьшению внутренней
энергии и стремлением к увеличению энтропии.
Эндотермическую реакцию можно активировать, если
она сопровождается увеличением энтропии.Энтропия увеличивается при повышении температуры и особенно при фазовых переходах.
Чем выше температура, при которой проводят реакцию, тем большее значение будет иметь энтропийный фактор по сравнению по сравнению с энергетическим.
Слайд 16Энергия Гиббса (G)
ΔG = ΔH – TΔS
T – абсолютная температура
ΔH
– изменение энтальпии системы
ΔS – изменение энтропии системы
Самопроизвольно протекают
лишь те процессы, в которых энергия Гиббса уменьшаетсяΔG < 0
Процессы, при которых ΔG > 0 – невозможны.
Если ΔG = 0, то есть ΔH = TΔS, значит в системе установилось равновесие.