Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Подгруппа углерода
Содержание
- 1. Подгруппа углерода
- 2. ХимияПодгруппа углеродаПоложение элементов подгруппы углерода в периодической
- 3. Общая характеристика. Углерод и кремний Подгруппа
- 4. Общая характеристика. Углерод и кремний На
- 5. Общая характеристика. Углерод и кремний При
- 6. Первый потенциал ионизации, сродство к электрону иэлектроотрицательность
- 7. Углерод в природе встречается в виде алмаза
- 8. В реакциях с металлами и менее активными
- 9. Кремний в природе встречается только в связанном
- 10. При разложении соляной кислотой силицида магния получается
- 11. Слайд 11
- 12. Слайд 12
- 13. Слайд 13
- 14. В 1867 г. Менделеев был назначен профессором
- 15. Скачать презентанцию
Слайды и текст этой презентации
Слайд 1
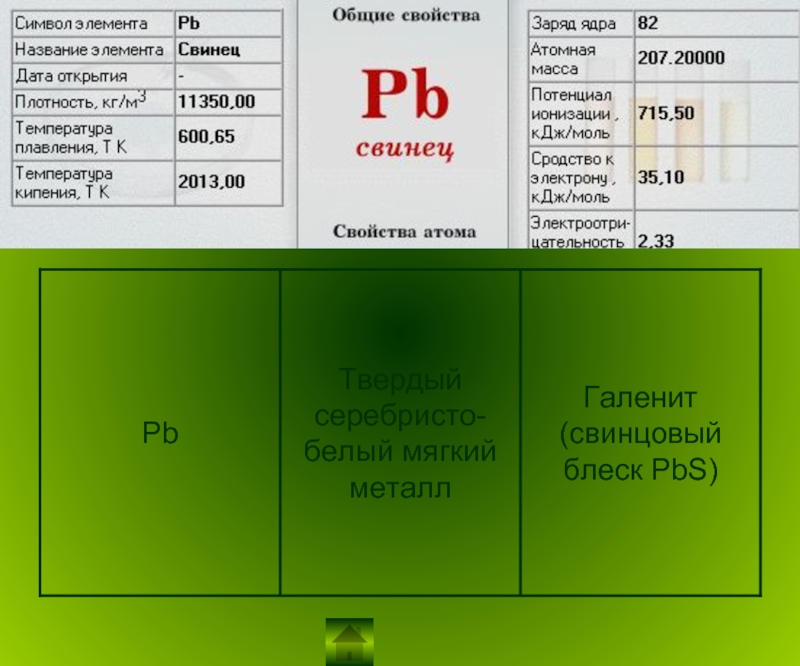
Подгруппа углерода.
Презентация на тему:
Выполнила Пивоварова Татьяна Николаевна учитель химии Рамонской
ОГ № 1.
Слайд 2Химия
Подгруппа углерода
Положение элементов подгруппы углерода
в периодической системе, строение их
атомов
C,
Si,
Ge,
Sn,
Pb
Общая характеристика.
Углерод и кремний
Дмитрий Иванович
Менделеев
Выход
Слайд 3
Общая характеристика.
Углерод и кремний
Подгруппа углерода, в которую входят
углерод, кремний, германий, олово и
свинец, является главной подгруппой 4
группы Периодической системы. История открытия химических элементов IVA группы.
Слайд 4
Общая характеристика.
Углерод и кремний
На внешней электронной оболочке атомов
этих элементов имеется 4 электрона и их электронную конфигурацию в
общем виде можно записать так: ns2np2, где n - это номерпериода, в котором расположен химический элемент. При переходе сверху вниз по группе неметаллические свойства ослабляются, а металлические возрастают, поэтому углерод и
кремний - это неметаллы, а олово и свинец проявляет свойства типичных металлов. Образуя ковалентные полярные связи с атомами водорода, C и Si проявляют формальную степень окисления -4, а с более активными неметаллами (N, O, S) и галогенами
проявляют степени окисления +2 и +4.
Слайд 5
Общая характеристика.
Углерод и кремний
При выяснениии механизма реакций иногда
используют изотоп углерода 13С (метод меченных атомов). Поэтому полезно знать,
что распространненость изотопов углерода: 12С - 98.89 % и 13С - 1.11 %. Если ограничиться перечислением изотопов, распространенность которых более 0.01 %, то у кремния таких изотопа 3, у германия - 5, у олова - 10, у свинца 4 стабильных изотопа. При обычных условиях углерод можетсуществовать в виде двух аллотропных
модификаций: алмаза и графита;
сверхчистый кристаллический кремний
- полупроводник.
Слайд 6Первый потенциал ионизации, сродство к электрону и
электроотрицательность по Полингу
атомов
элементов IVA группы. Из соединений элементов (Э) подгруппы углерода с
водородом рассмотрим соединения типа ЭН4. С увеличением заряда ядра атома Э стабильность гидридов уменьшается. При переходе от C к Pb устойчивость соединений со степенью окисления +4уменьшается, а с +2 - увеличивается. У оксидов ЭО2 уменьшается кислотный характер , а у оксидов ЭО
увеличивается основной характер.
Плотность, температура плавления,
температура кипения
простых веществ
элементов IVA группы.
Слайд 7
Углерод в природе встречается в виде алмаза и графита. В
ископаемых углях его содержится: от 92 % - в антраците,
до 80 % - в буром угле. В связном состоянии углерод встречается в карбидах: CaCO3 мел, известняк и мрамор, MgCO3·CaCO3 - доломит,MgCO3 - магнезит. В воздухе углерод содержится в виде углекислого газа (0.03 % по объему). Содержится углерод и в соединениях, растворенных в морской воде. Углерод входит в состав растений и животных, содержится в нефти и природном газе. В реакциях с активными неметаллами углерод легко окисляется:
C+O2=CO2
2C+O2=2CO
C+2S=CS2
C+2F2=CF4
Углерод может проявлять восстановительные свойства и при взаимодействии со сложными веществами:
C+2CuO=Cu+Co2
C+2H2SO4(конц.)=CO2+2SO2+H2O
2C+BaSO4=BaS+2CO2
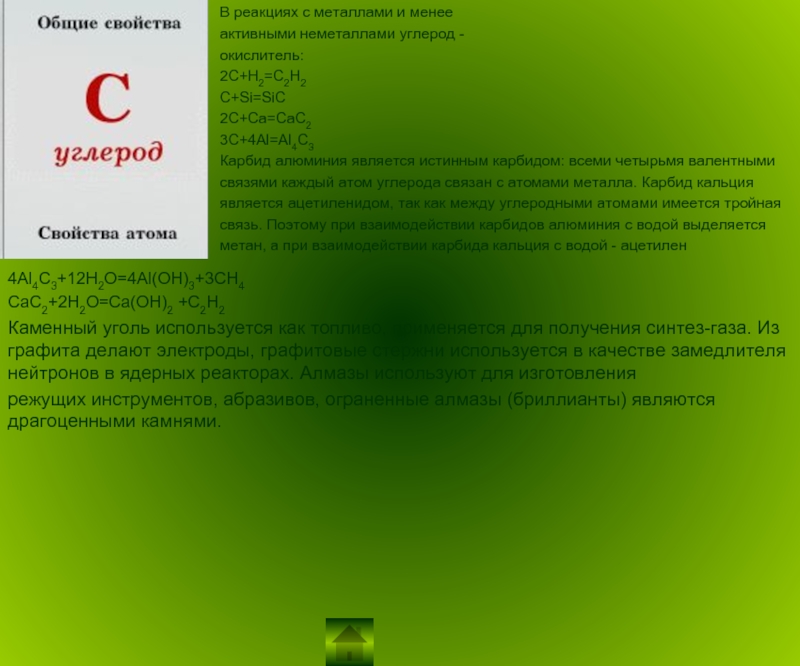
Слайд 8В реакциях с металлами и менее
активными неметаллами углерод -
окислитель:
2C+H2=C2H2
C+Si=SiC
2C+Ca=CaC2
3C+4Al=Al4C3
Карбид алюминия является истинным карбидом: всеми четырьмя валентными
связями каждый
атом углерода связан с атомами металла. Карбид кальция является ацетиленидом, так как между углеродными атомами имеется тройная
связь. Поэтому при взаимодействии карбидов алюминия с водой выделяется
метан, а при взаимодействии карбида кальция с водой - ацетилен
4Al4C3+12H2O=4Al(OH)3+3CH4
CaC2+2H2O=Ca(OH)2 +C2H2
Каменный уголь используется как топливо, применяется для получения синтез-газа. Из графита делают электроды, графитовые стержни используется в качестве замедлителя нейтронов в ядерных реакторах. Алмазы используют для изготовления
режущих инструментов, абразивов, ограненные алмазы (бриллианты) являются драгоценными камнями.
Слайд 9
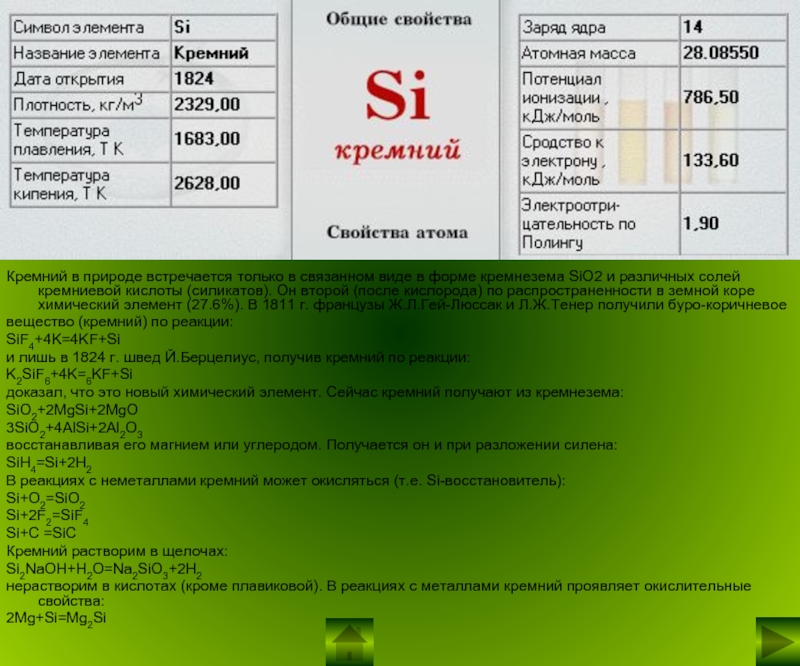
Кремний в природе встречается только в связанном виде в форме
кремнезема SiO2 и различных солей кремниевой кислоты (силикатов). Он второй
(после кислорода) по распространенности в земной коре химический элемент (27.6%). В 1811 г. французы Ж.Л.Гей-Люссак и Л.Ж.Тенер получили буро-коричневоевещество (кремний) по реакции:
SiF4+4K=4KF+Si
и лишь в 1824 г. швед Й.Берцелиус, получив кремний по реакции:
K2SiF6+4K=6KF+Si
доказал, что это новый химический элемент. Сейчас кремний получают из кремнезема:
SiO2+2MgSi+2MgO
3SiO2+4AlSi+2Al2O3
восстанавливая его магнием или углеродом. Получается он и при разложении силена:
SiH4=Si+2H2
В реакциях с неметаллами кремний может окисляться (т.е. Si-восстановитель):
Si+O2=SiO2
Si+2F2=SiF4
Si+C =SiC
Кремний растворим в щелочах:
Si2NaOH+H2O=Na2SiO3+2H2
нерастворим в кислотах (кроме плавиковой). В реакциях с металлами кремний проявляет окислительные свойства:
2Mg+Si=Mg2Si
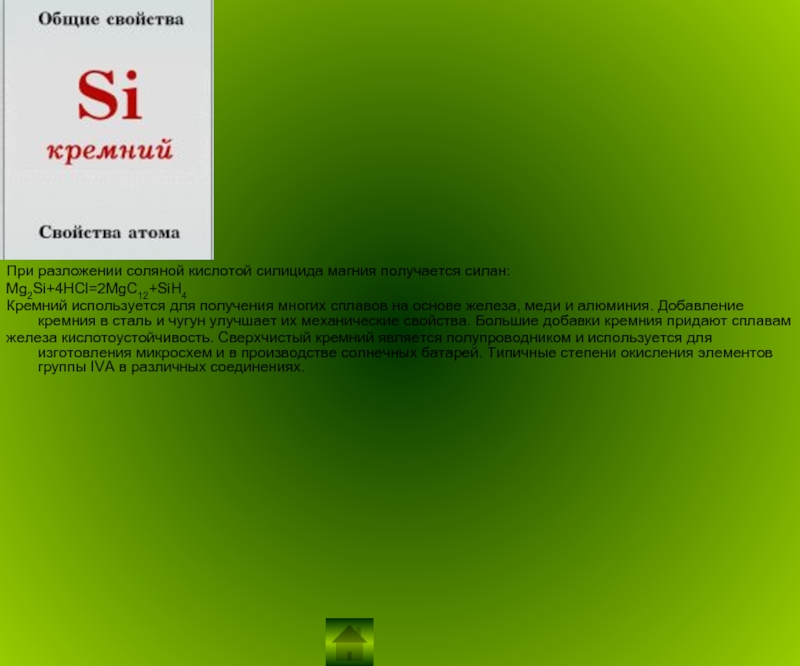
Слайд 10При разложении соляной кислотой силицида магния получается силан:
Mg2Si+4HCl=2MgC12+SiH4
Кремний используется для
получения многих сплавов на основе железа, меди и алюминия. Добавление
кремния в сталь и чугун улучшает их механические свойства. Большие добавки кремния придают сплавамжелеза кислотоустойчивость. Сверхчистый кремний является полупроводником и используется для изготовления микросхем и в производстве солнечных батарей. Типичные степени окисления элементов группы IVA в различных соединениях.
Слайд 14В 1867 г. Менделеев был назначен профессором химии Петербургского университета.
Заняв кафедру химии столичного университета, он стал главой университетских химиков
в России и инициатором создания Русского химического общества (1868 г.). В 1868 г. Менделеев начал работать над учебником "Основы химии". Он писал, что его цель - "познакомить учащихся с основными данными и выводами химии в общедоступном научном зложении, указать на значение этих выводов для понимания как природы вещества иявлений вокруг нас совершающихся, так и тех применений, которые получила химия в сельском хозяйстве, технике". В процессе работы над второй частью учебника в феврале 1869 г. Менделеев сформулировал Периодический закон и предложил наиболее совершенную форму его воплощения в виде таблицы, которую он назвал "Опыт системы элементов, основанной на их атомном весе и химическом сходстве". В течение двух
лет Менделеев работал над развитием и углублением открытого закона и готовил обобщающую статью "Естественная система элементов и применение ее к указанию свойств неоткрытых элементов". Менделеев
предсказал существование экаалюминия (был открыт в 1875 г. французом Лекоком де Буабодраном и назван галлием), экабора (был открыт в 1879 г. шведом Л.Ф.Нильсоном и назван скандием) и экасилиция (был открыт в 1886 г. немцем К.А.Винклером и назван германием). К середине 80-х годов XIX в. Периодический закон был признан всеми учеными и вошел в арсенал науки как один из важнейших законов природы. Изучая газы, Менделеев (в 1874 г.) уточнил уравнение состояния для идеальных газов (уравнение Клапейрона-Менделеева).В 1877 г. Менделеев высказал гипотезу о происхождении нефти из карбидов тяжелых металлов и предложил принцип дробной перегонки при переработке нефти, в 1888 г. - выдвинул идею о подземной газификации углей, в 1891 г. - разработал технологию изготовления нового типа бездымного пороха.
Дмитрий Иванович
Менделеев
(1834-1907)
Выдающийся русский химик, автор Периодического закона - родился в г. Тобольске, там же он закончил гимназию, а в 1850 г. был принят в Петербургский главный педагогический институт на физико-математический факультет. После защиты диссертации Менделеев в 1857 г. был назначен
приват-доцентом. В 1859 г. он уехал заграничную командировку в Германию
на два года, где работал в Гейдельберге у Бунзена, принял участие в работе Международного химического конгресса в Карлсруэ. После возвращения в Петербург Менделеев вел большую научную и преподавательскую деятельность, в 1865 г. защитил докторскую диссертацию, в которой была изложена его гидратная теория растворов и выдвинута идея о возможности
существования в растворах соединений переменного состава.