Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Презентация к уроку химии в 8 классе на тему: "Виды химической связи"
Содержание
- 1. Презентация к уроку химии в 8 классе на тему: "Виды химической связи"
- 2. Мотиватор к уроку
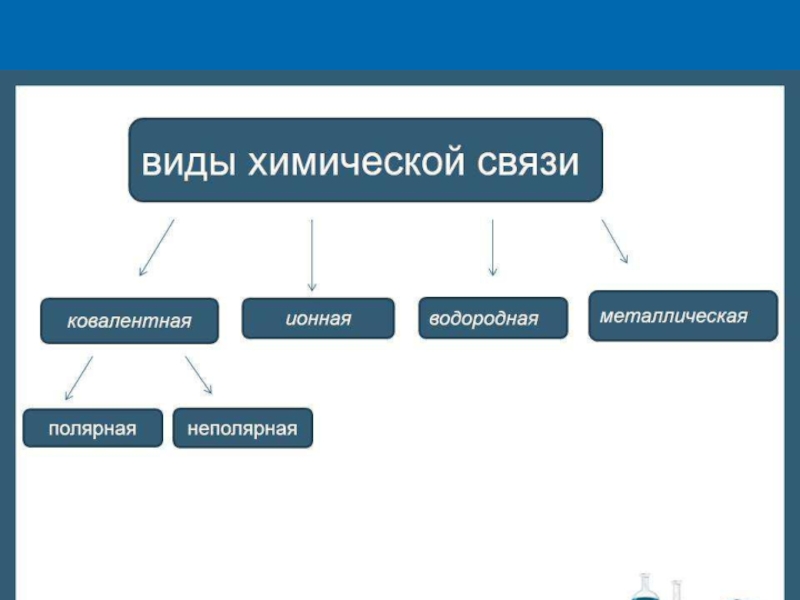
- 3. Цель урока:Изучить виды химической связи в неорганических веществах:Ковалентная связьКовалентная полярная связьКовалентная не полярная связьИонная связьМеталлическая связь
- 4. Слайд 4
- 5. Ковалентная связьОпределение :Связь,осуществляемая общими электронными парами
- 6. Ковалентная неполярная связьЭлектронное облако связи распределено в
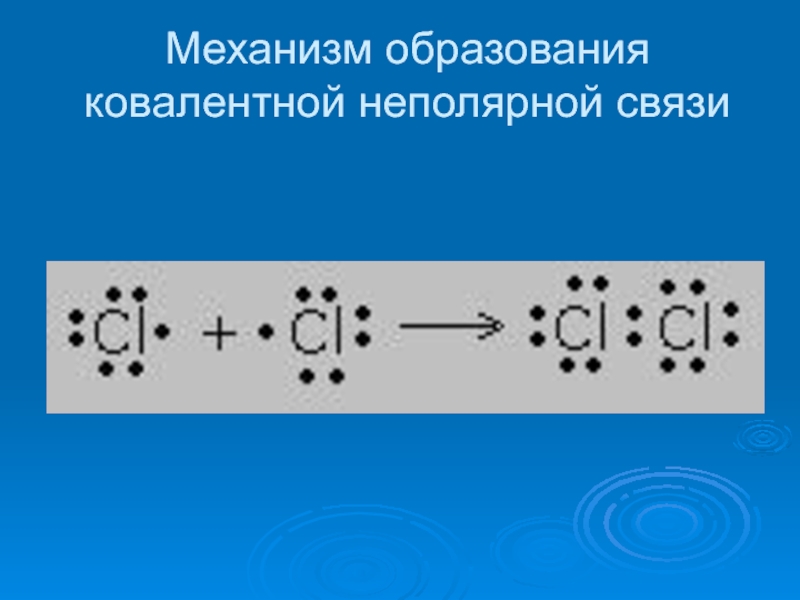
- 7. Механизм образования ковалентной неполярной связи
- 8. Ковалентная полярная связьЭлектронное облако связи смещено в
- 9. Механизм образования ковалентной полярной связиОбразование молекулы НСl можно
- 10. Ионная связьСвязь между ионами, осуществляемая посредством электростатического притяженияНапример NaCl BeF2 CuO
- 11. Металлическая связьСвязь между положительными ионами, осуществляемая за счет обобществленных электроновВсе металлы
- 12. Определить вид химической связи по формуламH2 O2
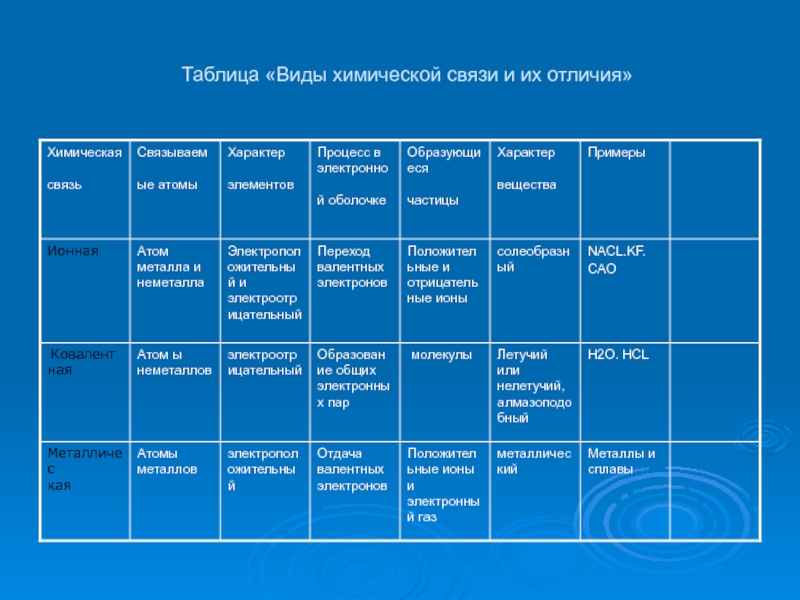
- 13. Таблица «Виды химической связи и их отличия»
- 14. Образование молекулы OF2
- 15. Образование ионной связи
- 16. Залание по проверке изученного на урокеКакой тип
- 17. Порядок построения молекулОпределить число не спаренных ē
- 18. Домашнее заданиеПараграф 62
- 19. Скачать презентанцию
Мотиватор к уроку
Слайды и текст этой презентации
Слайд 3Цель урока:
Изучить виды химической связи в неорганических веществах:
Ковалентная связь
Ковалентная полярная
связь
Ковалентная не полярная связь
Ионная связь
Металлическая связь
Слайд 6Ковалентная неполярная связь
Электронное облако связи распределено в пространстве симметрично относительно
обоих атомов
Например: O2 N2 Cl2 F2
Br2 Слайд 8Ковалентная полярная связь
Электронное облако связи смещено в сторону более электроотрицательного
атома
Например HCl H2O CO2
Слайд 9Механизм образования ковалентной полярной связи
Образование молекулы НСl можно представить схемой
Н.+ .Сl: = Н :Cl:
Слайд 10Ионная связь
Связь между ионами, осуществляемая
посредством электростатического притяжения
Например NaCl BeF2
CuO
Слайд 11Металлическая связь
Связь между положительными ионами, осуществляемая за счет обобществленных электронов
Все
металлы
Слайд 12Определить вид химической связи по формулам
H2 O2 K2O Fe H2O
H2S N2 Cu
F2 Ag HgO NaF
P4 NH3 SiO2 Br2KI PbO Zn Na O3 SO2 H2Se LiCl
Слайд 16Залание по проверке изученного на уроке
Какой тип связи в молекулах
веществ?
H2
H2O
NH3
Cl2
H2S
Напишите электронные формулы этих веществ.
Слайд 17Порядок построения молекул
Определить число не спаренных ē по формуле 8
– N. (N – номер группы)
Записать атомы, расположив их не
спаренными ē друг к другу.Составить электронную и структурную формулы.