Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Презентация про белки по химии
Содержание
- 1. Презентация про белки по химии
- 2. Цели урока. Образовательная.
- 3. План1. Биологические функции белков.2. Состав белков.3. Строение
- 4. Вопросы для повторения1. Какие органические вещества
- 5. «Жизнь есть способ существования белковых тел»
- 6. Биологические функции белков:1. Структурная. Белки являются обязательными
- 7. Определение Белки – это природные
- 8. Строение белковых молекул Первичная структура белка
- 9. Вторичная структура белка Это α-спираль,
- 10. Третичная структура белка Это пространственная конфигурация
- 11. Физические свойства Свойства белков также
- 12. Химические свойства1. Горение белков.
- 13. Химические свойста белков2. Денатурация белков(свёртывание): Белок
- 14. Превращение белков в организме
- 15. Успехи в изучении и синтезе белков
- 16. Вопросы для закрепления1. Что такое белки?2. Дайте
- 17. Домашнее задание § 11.3 стр. 221
- 18. Скачать презентанцию
Цели урока. Образовательная. Изучить состав, строение и свойства белков, их основные биологические функции; Развивающая. Уметь сравнивать состав, строение и свойства различных органических соединений; Воспитательная. Воспитывать
Слайды и текст этой презентации
Слайд 1«Белки»
Подготовила преподаватель химии - -
Дзагоева Фатима Борисовна
ГБПОУ
Владикавказский многопрофильный
техникум
Слайд 2Цели урока
.
Образовательная.
Изучить состав, строение и
свойства белков, их основные биологические функции;
Развивающая.
Уметь сравнивать состав,
строение и свойства различных органических соединений;
Воспитательная. Воспитывать у школьников потребность к изучению своего организма на примере изучения белков; осознание важности жизни.
Слайд 3План
1. Биологические функции белков.
2. Состав белков.
3. Строение белковых молекул.
4. Физические
свойства.
5. Химические свойства.
6. Превращения белков в организме.
7. Успехи в изучении
и синтезе белков.Слайд 4Вопросы для повторения
1. Какие органические вещества называются аминокислотами? Приведите
примеры формул и названий таких соединений. Можно ли их назвать
соединениями с двойными функциями?2. В чем проявляется амфотерный характер аминокислот? Напишите уравнения реакций аланина с соляной кислотой и гидроксидом калия.
3. Напишите уравнение реакции глицина с аланином.
4. Что такое пептидная связь, дипептид, полипептид?
5. В медицине для стимулирования работы головного мозга применяют глицин в таблетках. Рассчитайте массовую долю глицина в растворе, полученном растворением одной таблетки массой 0,2 г в 30 мл воды.
Слайд 5«Жизнь есть способ
существования белковых тел»
Ф.Энгельс
В 1838
г. для обозначения беков выдающийся шведский химик Й.Я.Берцелиус ввел термин
протеин (греч. Protos – первый).Белки – это природные полимеры, которые играют ключевую роль почти во всех структурах живых организмов и происходящих в них процессах.
Слайд 6Биологические функции белков:
1. Структурная. Белки являются обязательными компонентамивсех составных частей
растительных и животных клеток.
2. Транспортная. Белки накапливают и переносят по
организму важные вещества.3. Защитная. Антитела препятствуют проникновению в организм бактерий и ядовитых веществ, обеспечивают иммунитет.
4. Каталитическая. Все биологические катализаторы (ферменты) – это белки.
5. Двигательная. Мышечные ткани состоят из белковых молекул, способных сокращаться и скользить друг относительно друга.
6. Энергетическая. При окислении белков выделяется значительное количество энергии.
7. Регуляторная. Белки-гормоны регулируют многие процессы в организме.
Слайд 7Определение
Белки – это природные полимеры, образованные остатками
α-аминокислот, связанные пептидной связью.
Слайд 8Строение белковых молекул
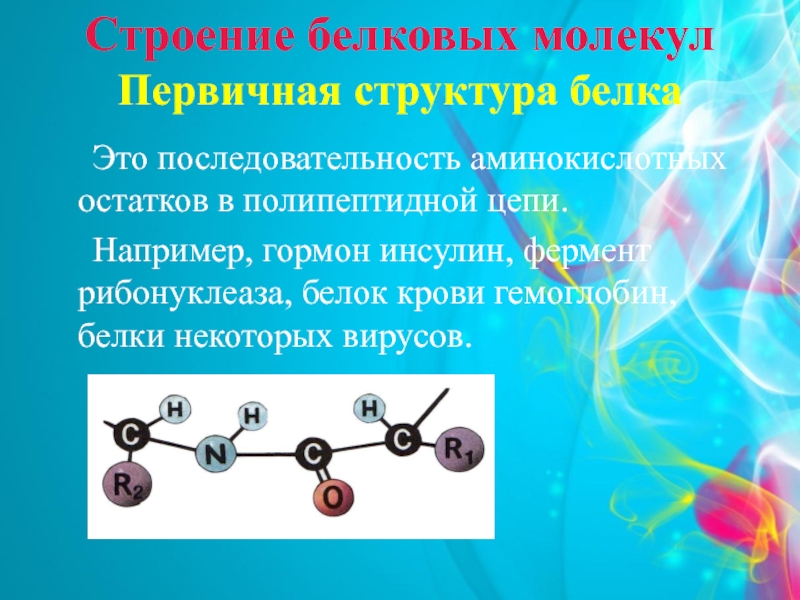
Первичная структура белка
Это последовательность аминокислотных
остатков в полипептидной цепи.
Например, гормон инсулин,
фермент рибонуклеаза, белок крови гемоглобин, белки некоторых вирусов. Слайд 9Вторичная структура белка
Это α-спираль, которая образуется в
результате скручивания полипептидной цепи за счет водородных связей между группами:
−CО− и −NН−Слайд 10Третичная структура белка
Это пространственная конфигурация спирали.
Образована
дисульфидными (- S - S -), гидрофобными и ионными связями.
Слайд 11Физические свойства
Свойства белков также разнообразны, как и
функции, которые они выполняют.
Одни белки растворяются
в воде, образуя, как правило, коллоидные растворы (например, белок яйца); другие растворяются в разбавленных растворах солей; третьи не растворимы (например, белки покровных тканей).Слайд 12Химические свойства
1. Горение белков.
Белки
горят с образованием азота, углекислого газа и воды, а также
некоторых других веществ. Горение сопровождается характерным запахом жжёных перьев2. Гидролиз белков:
Белки + Н2О → α- аминокислоты
Слайд 13Химические свойста белков
2. Денатурация белков(свёртывание):
Белок в растворе +
кислоты, щелочи, соли тяжелых металлов, t˚, УФ - лучи →
Белок с изменённой вторичной и третичной структурой.3. Цветные (качественные) реакции на белки:
а) Ксантопротеиновая реакция:
Белок + HNO3 → Жёлтое
окрашивание
б) Биуретовая реакция:
Белок + CuSO4 + NaOH →
Ярко-фиолетовое окрашивание
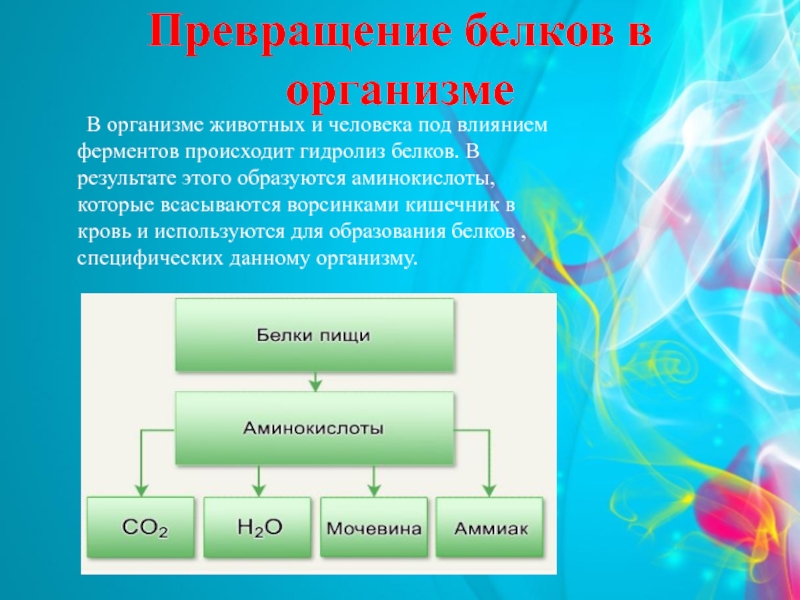
Слайд 14Превращение белков в организме
В организме животных
и человека под влиянием ферментов происходит гидролиз белков. В результате
этого образуются аминокислоты, которые всасываются ворсинками кишечник в кровь и используются для образования белков , специфических данному организму.Слайд 15Успехи в изучении и синтезе белков
Белки имеют
чрезвычайно сложное строение. Первый белок, у которого в 1954 г.
удалось расшифровать первичную структуру , был инсулин. Для этого потребовалось почти 10 лет.Синтез белков в условиях лабораторий и химических заводов – задача очень сложная. Решение её явится величайшей победой всего человечества.
Осуществится проблема биохимического и синтетического получения пищи. В настоящее время уже разработаны пути получения более 120 разных видов искусственных мясных и рыбных продуктов. Практическое осуществление этого ведется в двух направлениях:
1) использование белков растений, например сои;
2) использование белков продуктов, полученных микробиологическим путём из нефти.
Слайд 16Вопросы для закрепления
1. Что такое белки?
2. Дайте характеристику каждой из
трёх структур белковых молекул.
3. Охарактеризуйте биологическую роль белка
4. Опишите физические
и химические свойства белков.5. Что такое денатурация? Чем она может быть вызвана?
6. Что вы знаете о синдроме приобретённого иммунодефицита (СПИДе)? Как это заболевание связано с нарушением белкового обмена в организме?
7. В двух пробирках находятся растворы глицерина и белка. Как с помощью одного и того же реактива различить их?