Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Строение атома 11 класс
Содержание
- 1. Строение атома 11 класс
- 2. Первая гипотеза строения атома предложена английским учёным Томсоном(1904)-статическая или электронно-ионная теория
- 3. Для проверки гипотезы Томсона Резерфорд (1911) провёл
- 4. Планетарная модель атомаэлектрон+Общий заряд атома равен 0-3--
- 5. Слайд 5
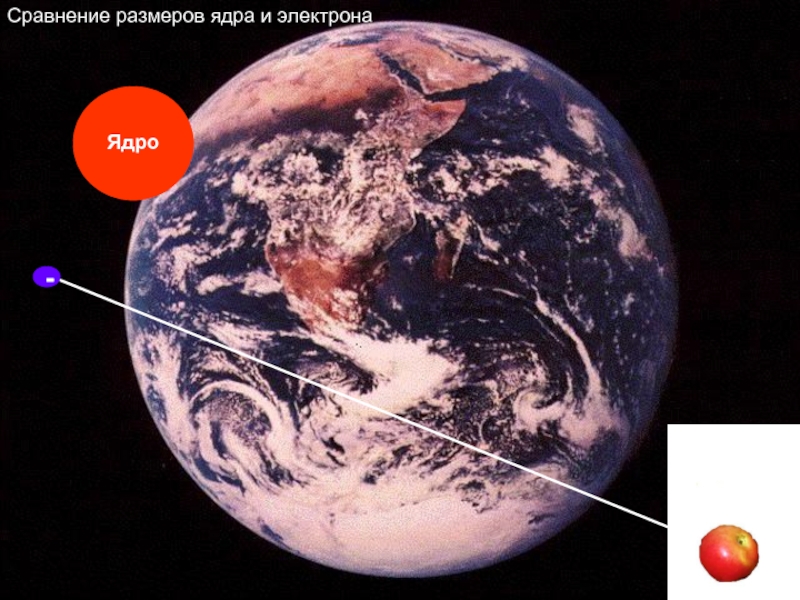
- 6. -Сравнение размеров ядра и электрона
- 7. Распределение электронов по электронным уровнямН+ 1Не+ 2Li+ 3+ 4BeB+ 5C+ 6N+ 7O+ 8F+ 9Ne+ 10Na+ 11
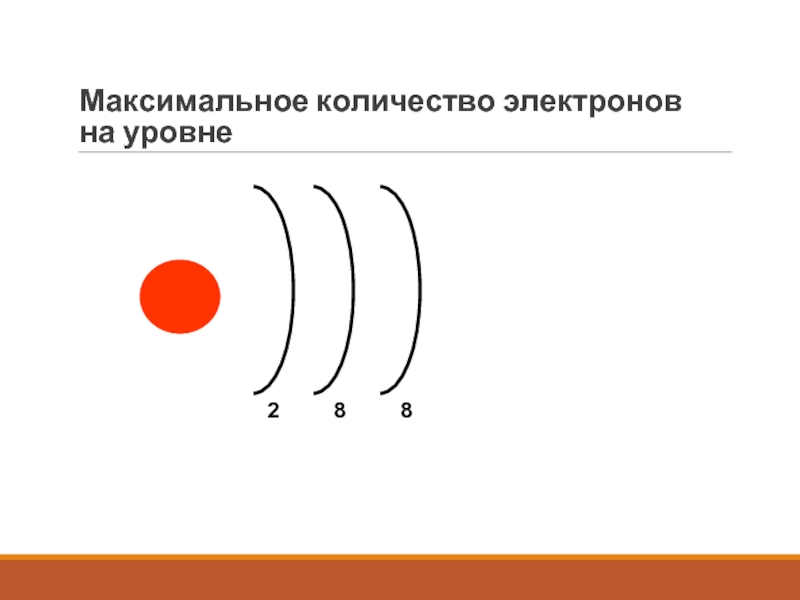
- 8. Максимальное количество электронов на уровне
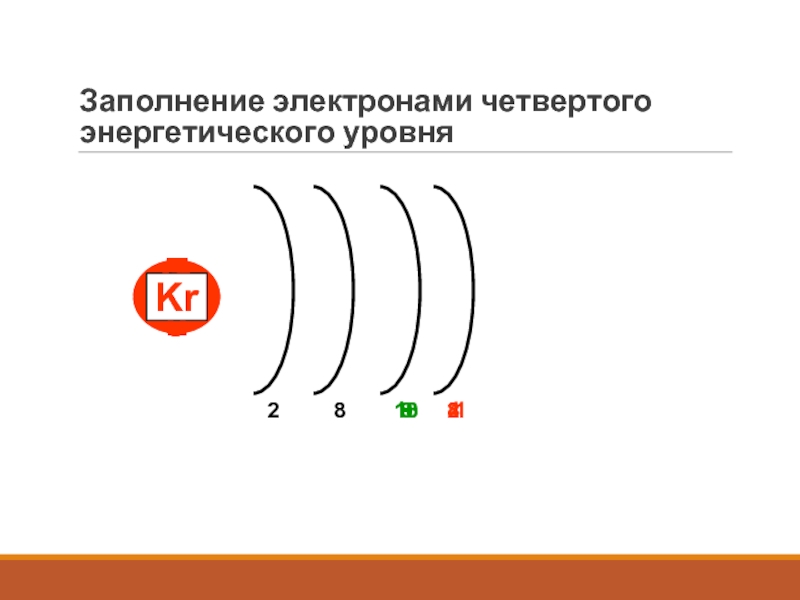
- 9. Заполнение электронами четвертого энергетического уровня81KCaScTi2910Zn18Ga3Ge4Kr8
- 10. ЭZАА- атомное число – относительная атомная массаZ-зарядное число- заряд ядра атома
- 11. Изотопы Изотопы − атомы с одинаковыми значениями
- 12. Строение ядраАr = 1Аr = 4Аr =
- 13. ИзотопыПротонДейтерийТритий1+3Разновидности атомов с одинаковым зарядом ядра, но разными относительными атомными массами называются изотопами
- 14. Электронное облако
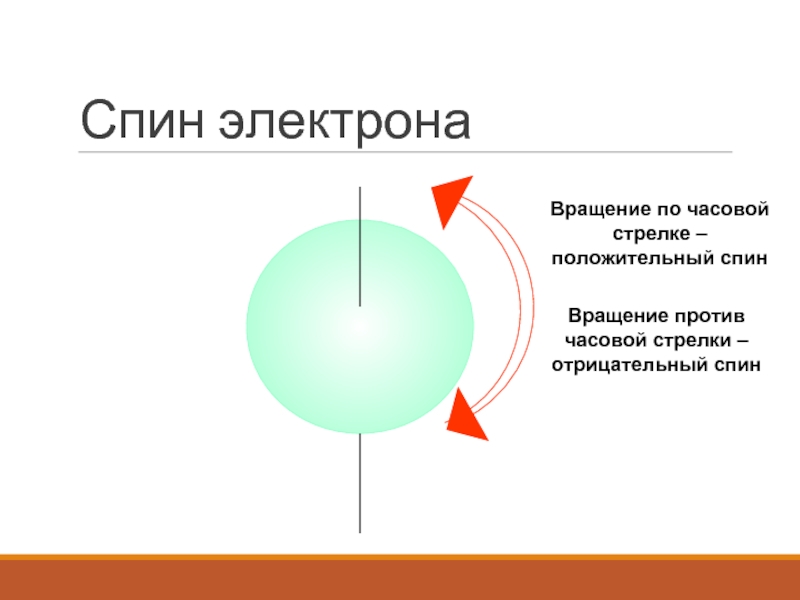
- 15. Спин электронаВращение по часовой стрелке – положительный спинВращение против часовой стрелки – отрицательный спин
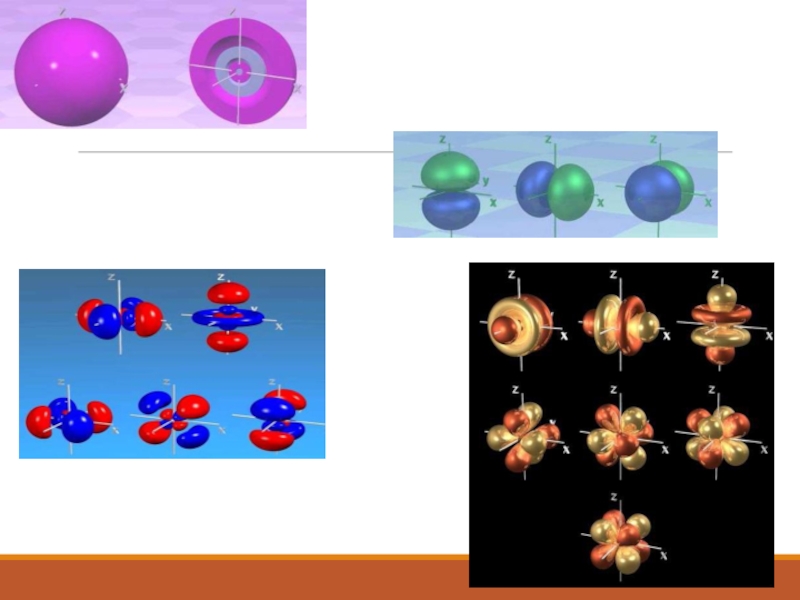
- 16. Формы электронных облаковСферическая форма (S - электронное
- 17. Слайд 17
- 18. Слайд 18
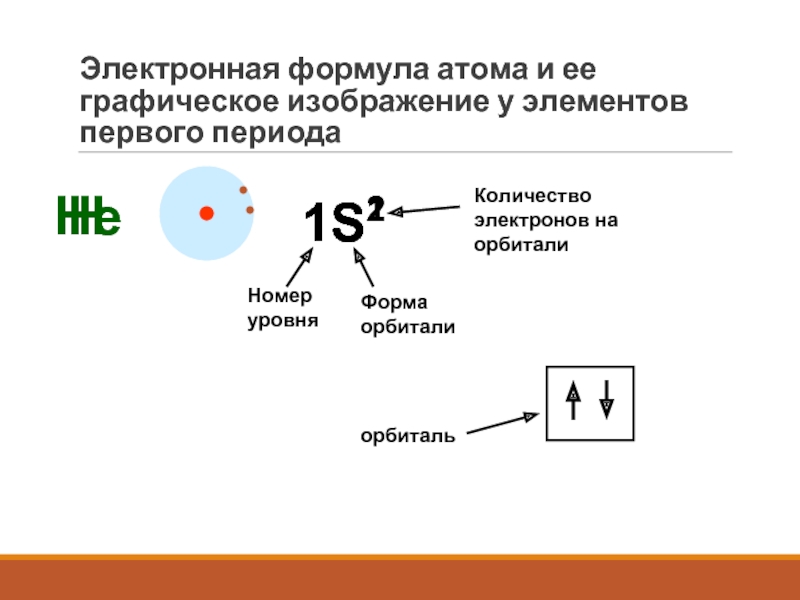
- 19. Электронная формула атома и ее графическое изображение у элементов первого периодаН1S1Номер уровняФорма орбиталиКоличество электронов на орбиталиНе1S2орбиталь
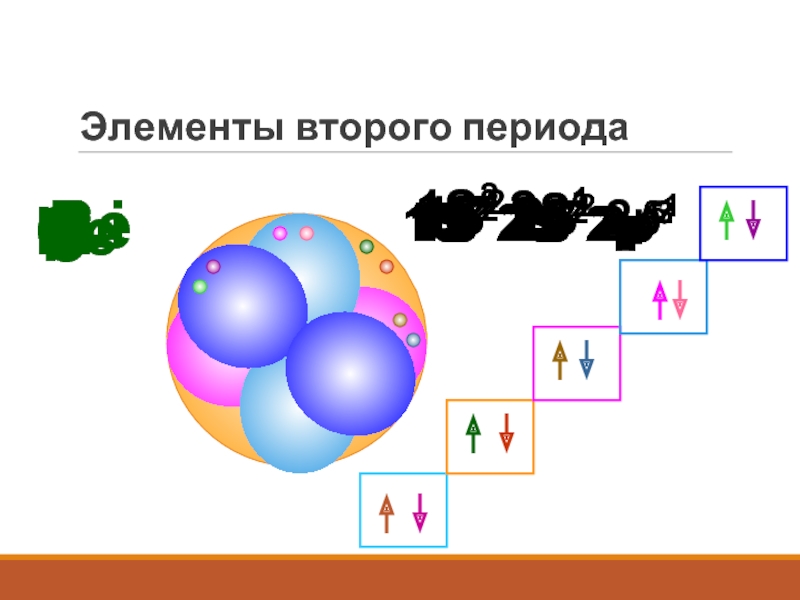
- 20. Элементы второго периодаLi1S2 2S1Be1S2 2S2B1S2 2S2 2p1C1S2
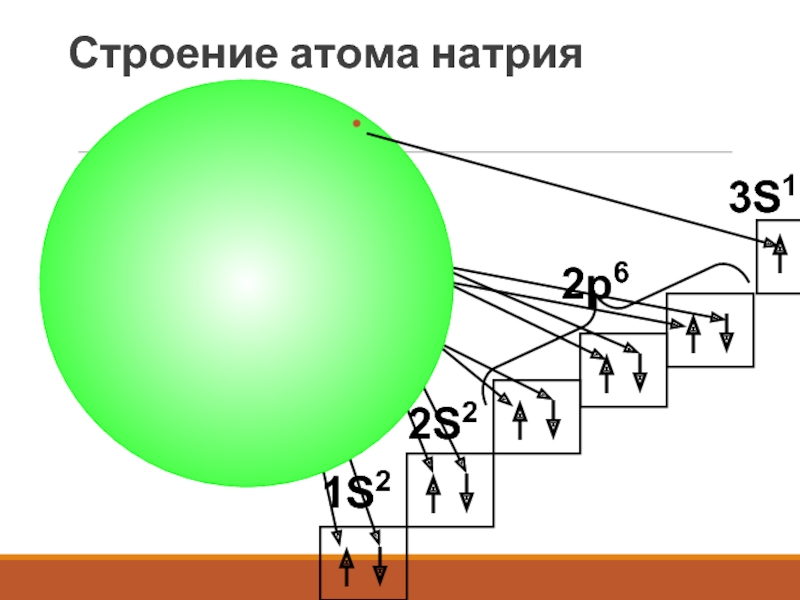
- 21. NaСтроение атома натрия2S22p63S11S2
- 22. Изменение внешнего электронного уровня у элементов третьего
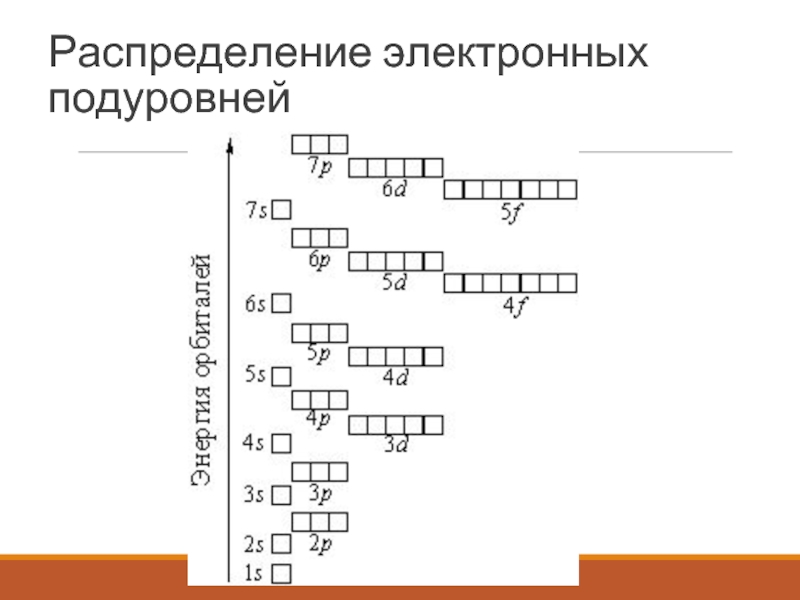
- 23. Распределение электронных подуровней
- 24. Электронная формула1s 2s 2p 3s 3p 4s
- 25. Валентные электроныS - 1s2 2s2 2p
- 26. Точный "адрес" электрона в оболочке определяется с
- 27. ℓ-орбитальное квантовое число, номер для подуровняℓ-изменяется от
- 28. Магнитное квантовое число ml определяет ориентацию электронного
- 29. Спиновое квантовое число ms характеризует собственное вращение
- 30. Принцип Паули или запрета :Никакие два электрона
- 31. Правило Хунда (Гунда) –суммарное значение спинового квантового числа электронов -должно быть максимальным.
- 32. Скачать презентанцию
Слайды и текст этой презентации
Слайд 2Первая гипотеза строения атома предложена английским учёным Томсоном(1904)-статическая или электронно-ионная
теория
Слайд 3Для проверки гипотезы Томсона Резерфорд (1911) провёл серию опытов по
рассеиванию альфа -частиц тонкими металлическими пластинами.
Слайд 7Распределение электронов по электронным уровням
Н
+ 1
Не
+ 2
Li
+ 3
+ 4
Be
B
+ 5
C
+
6
N
+ 7
O
+ 8
F
+ 9
Ne
+ 10
Na
+ 11
Слайд 11Изотопы
Изотопы − атомы с одинаковыми значениями Z, но различными
А то есть разное число нейтронов n0
Слайд 12Строение ядра
Аr = 1
Аr = 4
Аr = 7
Протон – масса
= 1, заряд = +1
Нейтрон – масса = 1, заряд
= 0+3
Слайд 13Изотопы
Протон
Дейтерий
Тритий
1+
3
Разновидности атомов с одинаковым зарядом ядра, но разными относительными атомными
массами называются изотопами
Слайд 15Спин электрона
Вращение по часовой стрелке – положительный спин
Вращение против часовой
стрелки – отрицательный спин
Слайд 16Формы электронных облаков
Сферическая форма
(S - электронное облако)
Форма объемной восьмерки
(p – электронное облако)
Перекрещенные объемные восьмерки
(d – электронное облако)
Слайд 19Электронная формула атома и ее графическое изображение у элементов первого
периода
Н
1S1
Номер уровня
Форма орбитали
Количество электронов на орбитали
Не
1S2
орбиталь
Слайд 20Элементы второго периода
Li
1S2 2S1
Be
1S2 2S2
B
1S2 2S2 2p1
C
1S2 2S2 2p2
N
1S2 2S2
2p3
O
1S2 2S2 2p4
F
1S2 2S2 2p5
Ne
1S2 2S2 2p6
Слайд 22Изменение внешнего электронного уровня у элементов третьего периода
Mg 3S2
Na 3S1
Al
3S2 3p1
Si 3S2 3p2
P 3S2 3p3
S 3S2
3p4Cl 3S2 3p5
Ar 3S2 3p6
Слайд 24Электронная формула
1s 2s 2p 3s 3p 4s 3d 4p 5s
4d 5p 4f 5d 5f……7f
Cu - 1s2 2s2 2p6
3s2 3p6 4s1 3d10S - 1s2 2s2 2p 6 3s2 3p4
Se - 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p4
Слайд 25Валентные электроны
S - 1s2 2s2 2p 6 3s 3p
2
4
Se
- 1s2 2s2 2p6 3s2 3p6 4s2 3d104p4
Na - 1s2
2s2 2p6 3s1Слайд 26Точный "адрес" электрона в оболочке определяется с помощью
квантовых чисел.
n-
главное квантового числа
принимать только целые значения- номер уровня
Слайд 27ℓ-орбитальное квантовое число, номер для подуровня
ℓ-изменяется от 0 до n-1
ℓ= 0 – это s-подуровень,
ℓ = 1 – это p-подуровень,
ℓ=
2 – это d-подуровень,ℓ = 3 – это f-подуровень
Слайд 28Магнитное квантовое число ml определяет ориентацию электронного облака в пространстве,
связано с ℓ
и может принимать целочисленные значения ℓ
от
–l до +l через 0.d электронов
ℓ = 2,
ml = –2, –1, 0, +1, +2.
Слайд 29Спиновое квантовое число ms характеризует собственное вращение электрона вокруг своей
оси.
Может принимать значения +½ и –½
ms = +1/2
ms = - 1/2
,
Слайд 30Принцип Паули или запрета :
Никакие два электрона в одном атоме
не могут характеризоваться одинаковым набором всех четырех квантовых чисел.
Правило Клечковского:
Энергия
уровней и подуровней возрастает в порядке увеличения суммы n + l, а при одном и том же значении этой суммы ниже располагаются уровни с меньшим n.