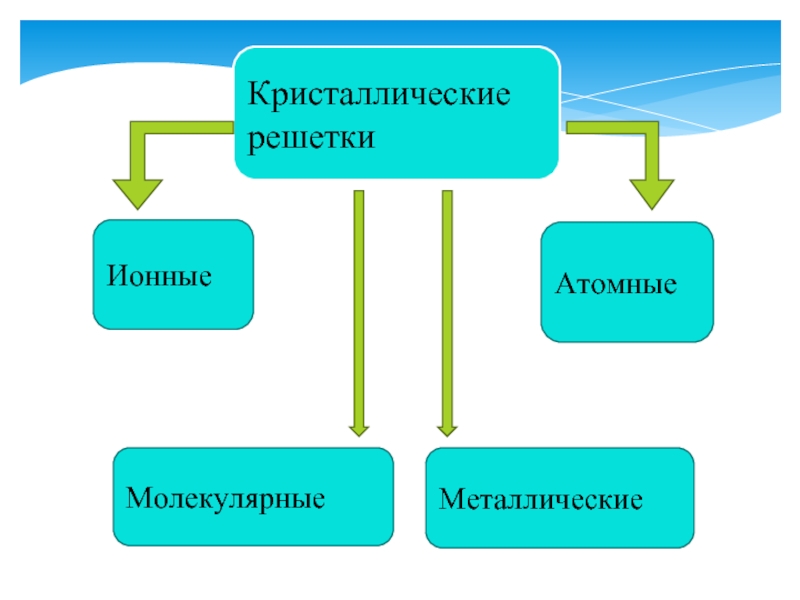
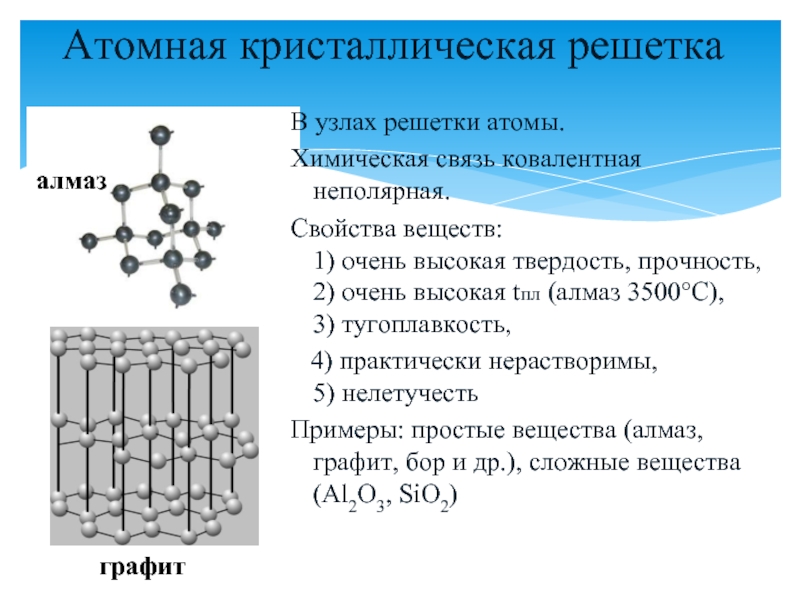
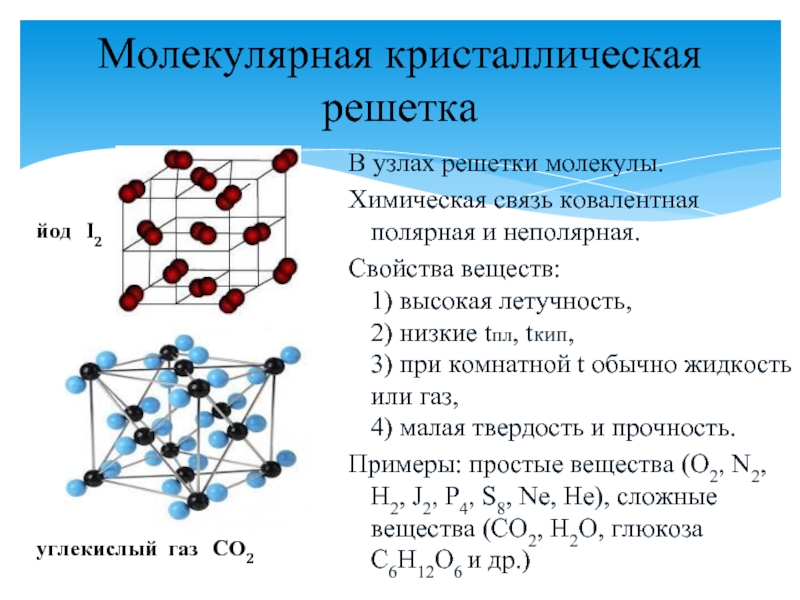
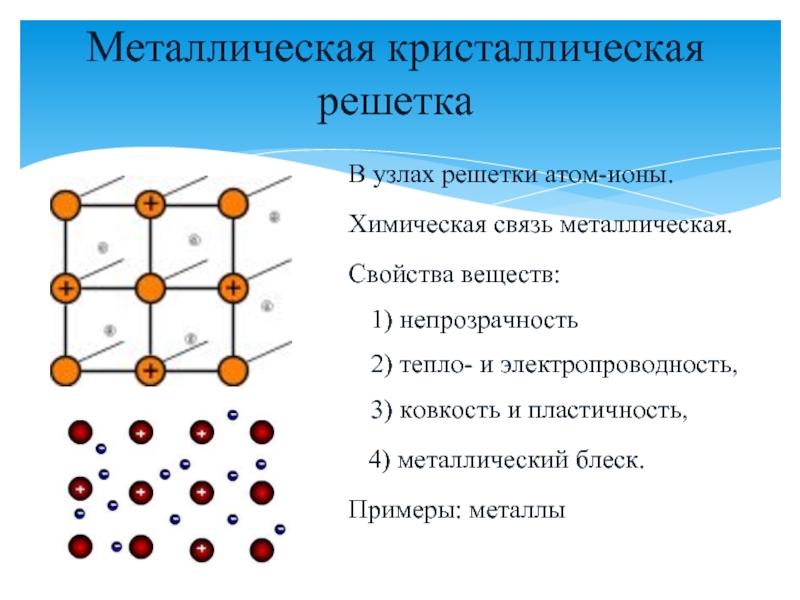
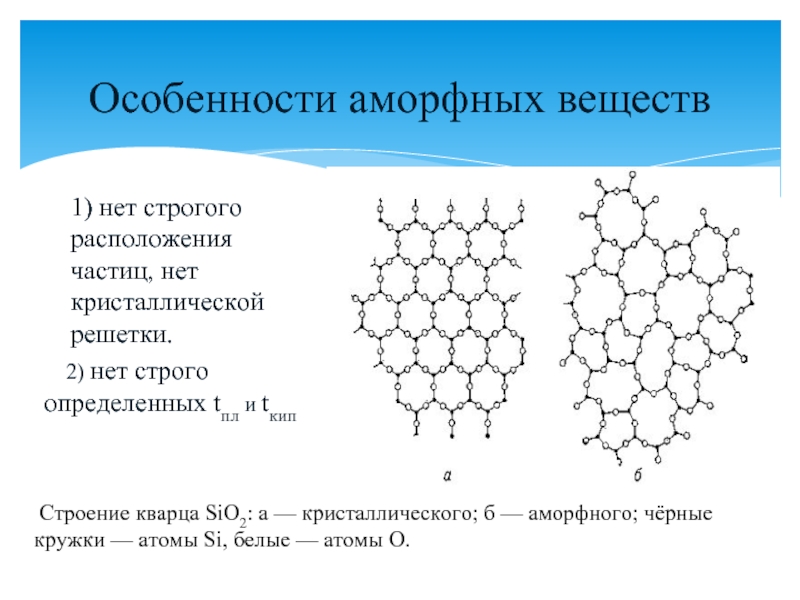
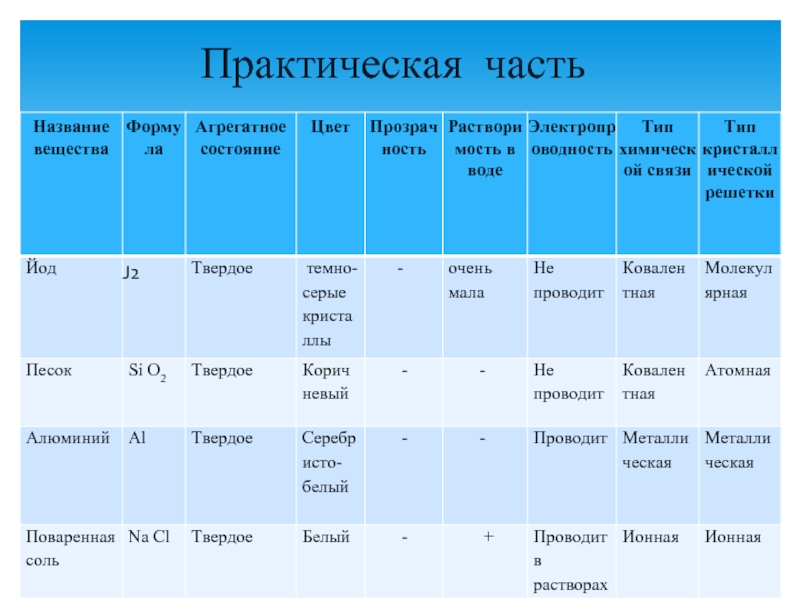
о типах кристаллических решеток
3)рассмотреть свойства веществ в зависимости от типа
кристаллических решеток;4)развивать познавательный интерес при выполнении теоретических и практических заданий.
Задачи урока: