Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Железо и его соединения
Содержание
- 1. Железо и его соединения
- 2. Цель урока в процессе исследования изучить физические и химические свойства железа и его соединений;
- 3. Другого ничего в природе нет Ни здесь,
- 4. Первая остановка “Космическая” (появление железа
- 5. 18 октября 1916 года вблизи с. Богуславки
- 6. Вторая остановка. “Составление визитки для железа»Порядковый номер:Период:Группа:Подгруппа:Электронная формула:
- 7. ЖелезоПорядковый номер: 26Период: 4Группа: VIIIПодгруппа: побочнаяЭлектронная формула: 1S2 2S2 2P6 3S2 3P6 3d6 4S2
- 8. . Третья остановка «Физические свойства»Цвет:Металлический блеск:Пластичность:Теплопроводность:Электропроводность:Плотность:Температура плавления:
- 9. Физические свойства железаЦвет: серебристо-белыйМеталлический блеск: имеетПластичность: имеется,
- 10. Четвёртая остановка. Экспериментальная. “Химические свойства железа”.
- 11. Химические свойства железаFe + S = FeS
- 12. Взаимодействие железа с водой в присутствии кислорода
- 13. Может вытеснять железо водород из воды?
- 14. Оксиды железаПри окислении железа в высокотемпературном режиме образуется железная окалина:
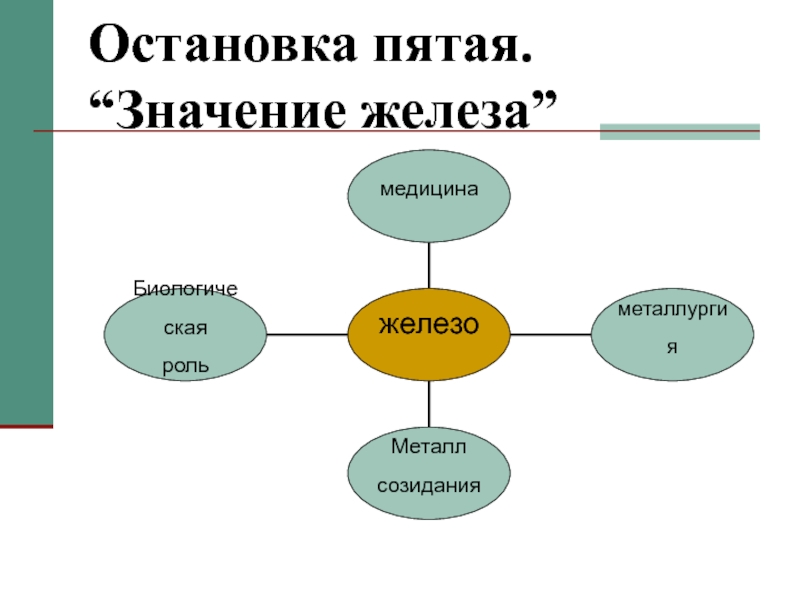
- 15. Остановка пятая. “Значение железа”
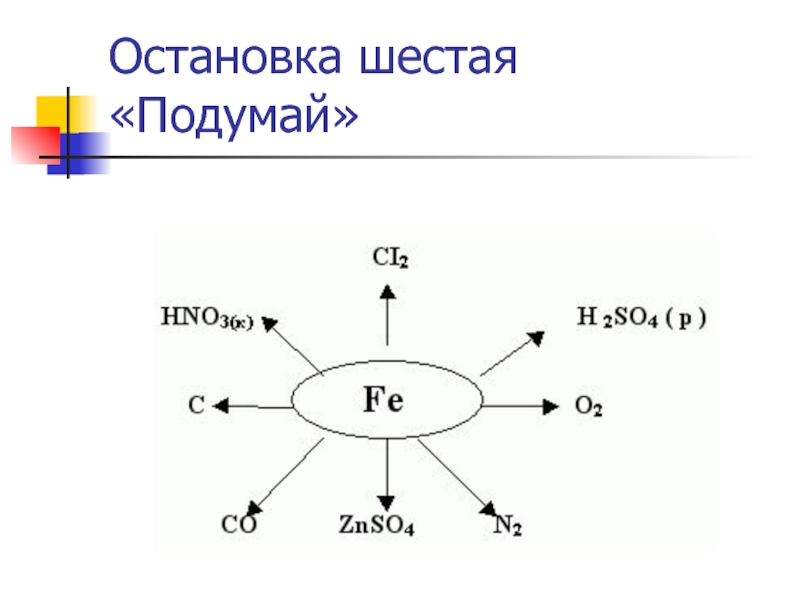
- 16. Остановка шестая «Подумай»
- 17. Скачать презентанцию
Цель урока в процессе исследования изучить физические и химические свойства железа и его соединений;
Слайды и текст этой презентации
Слайд 1Железо и его соединения
«Пришелец из космоса»
Подготовила учитель химии МОУ «СОШ
с.Березина Речка Саратовского района Саратовской области» Пономарева Т. Ю.
Слайд 2Цель урока
в процессе исследования изучить физические и химические
свойства железа и его соединений;
Слайд 3
Другого ничего в природе нет
Ни здесь, ни там, в космических
глубинах: Все от песчинок малых до планет - Из элементов состоит единых.
С. ЩипачевСлайд 4 Первая остановка “Космическая”
(появление железа на Земле).
Знакомство человека
с железом произошло в давние времена. Есть основания полагать, что
образцы железа, которые держали в руках первобытные люди, были неземного происхождения. Входя в состав некоторых метеоритов - вечных странников океана Вселенной, случайно нашедших приют на нашей планете, - метеоритное железо было тем материалом, из которого человек изготовил впервые железные изделия. Железо в самородном состоянии встречается на земле главным образом в виде метеоритного, “космического” железа.Слайд 518 октября 1916 года вблизи с. Богуславки Дальневосточного края наблюдали
падение метеорита, два его осколка весили по 256 кг. - 1920
год - Юго-Западная Африка, метеорит “Гоба” весом около 60 тонн. - 30 июня 1908 г. упал знаменитый Тунгусский метеорит весом 50 тыс. тонн.Слайд 6Вторая остановка.
“Составление визитки для железа»
Порядковый номер:
Период:
Группа:
Подгруппа:
Электронная формула:
Слайд 7Железо
Порядковый номер: 26
Период: 4
Группа: VIII
Подгруппа: побочная
Электронная формула:
1S2
2S2 2P6 3S2 3P6 3d6 4S2
Слайд 8. Третья остановка «Физические свойства»
Цвет:
Металлический блеск:
Пластичность:
Теплопроводность:
Электропроводность:
Плотность:
Температура плавления:
Слайд 9Физические свойства железа
Цвет: серебристо-белый
Металлический блеск: имеет
Пластичность: имеется, обладает ковкостью
Теплопроводность: высокая
Электропроводность:
высокая
Плотность: 7,87 г/см
Температура
плавления: 1539 ССлайд 10Четвёртая остановка. Экспериментальная. “Химические свойства железа”.
Составить уравнения химических
реакций
с серой,
соляной кислотой,
сульфатом меди,
Слайд 13Может вытеснять железо водород из воды?
может, но только
при сильном нагревании (запись на доске).
Fe + H2O = FeO
+H2Fe0 - 2e = Fe+2 - восстановитель - окисление
2H+ + 2е = Н2 - окислитель - восстановление