Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Углеводы-2
Содержание
- 1. Углеводы-2
- 2. Содержание 1.Пути обмена глюкозо-6 фосфата в тканях2.Анаэробное
- 3. Пути метаболизма глюкозы Гл + инсулинGLUTSGLTГл 6Ф ПВКлактат ГНГГликоген ПФПГАГАцетил-SКоАЦТК БОСО2Н2О
- 4. Гликолиз
- 5. гликогенФн Гл-1-фглюкоза 2 Гл-6-фАТФАДФ 11.Гексокиназа /глюкокиназа 2. фосфоглюкомутаза гликолиз
- 6. ГликолизЦентральный путь энергетичекого обмена.В анаэробных условиях –гликолиз
- 7. Слайд 7
- 8. ГК реакция
- 9. ГК реакция (прод.)Первая реакция гликолиза - активация
- 10. В печени, почках, поджелудочной железе есть глюкокиназа,
- 11. 2.
- 12. 3-я реакция - получение симметричной
- 13. ФФК реакция
- 14. Регуляция активности ФФК и скорости гликолиза Км
- 15. Регуляция активности ФФК и скорости гликолиза (прод) ФФК
- 16. 4
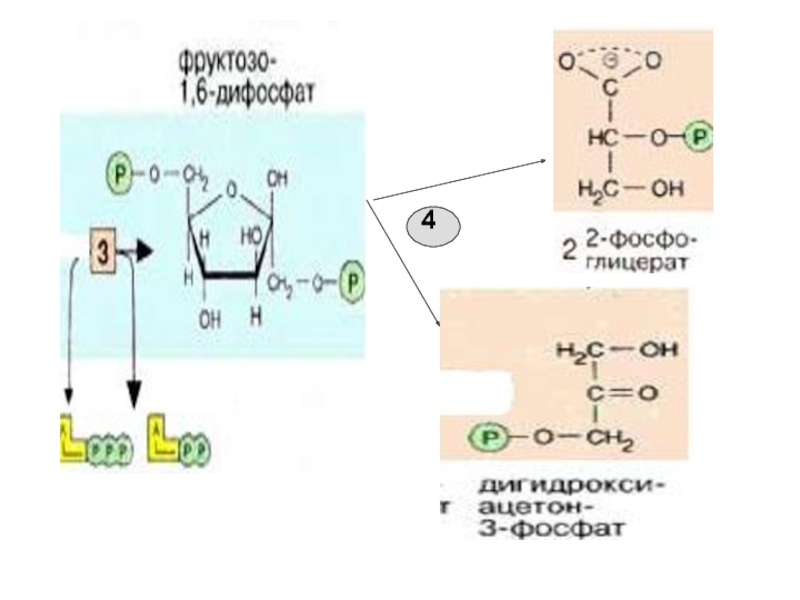
- 17. 4-я реакция. Фермент-альдолаза (лиаза). Разрыв связи происходит
- 18. Характеристика альдолазы (см. учебник) Определение активности альдолазы используют
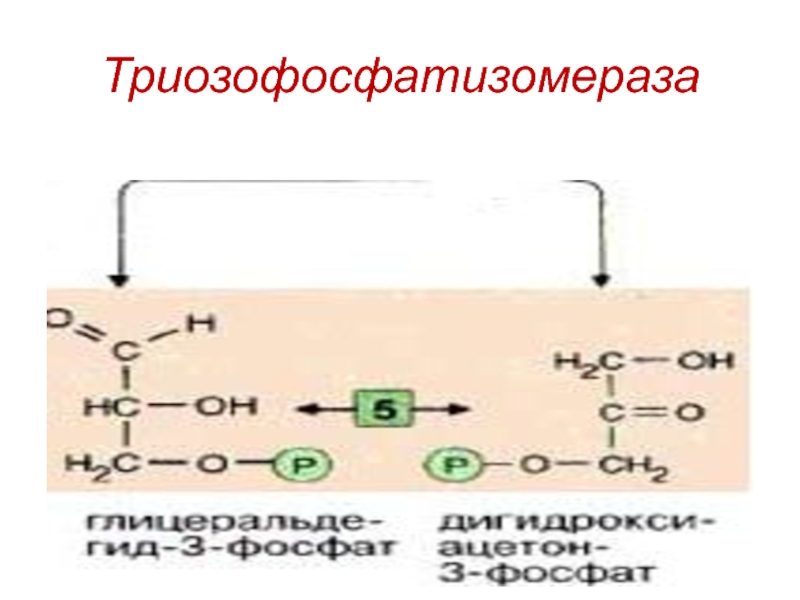
- 19. Триозофосфатизомераза
- 20. Эти триозы — глицеральдегид-3-фосфат (3ФГА) и дигидроксиацетонфосфат
- 21. 3ФГА затем окисляется глицеральдегид-З-фосфатдегидрогеназой [6] с образованием
- 22. Слайд 22
- 23. На следующей стадии (катализируемой фосфоглицераткиназой [7]) перенос фосфата этого соединения сопряжен с образованием АТФ.
- 24. Слайд 24
- 25. Слайд 25
- 26. Следующие реакции:изомеризации 3-ФГК, полученного в результате реакции
- 27. Слайд 27
- 28. На предпоследней необратимой стадии, которая катализируется пируваткиназой
- 29. Слайд 29
- 30. ЛДГЗавершающий стадией гликолиза является ЛДГ реакция:Стадия регенерации
- 31. При гликолизе на активацию одной молекулы глюкозы
- 32. Ферменты гликолиза
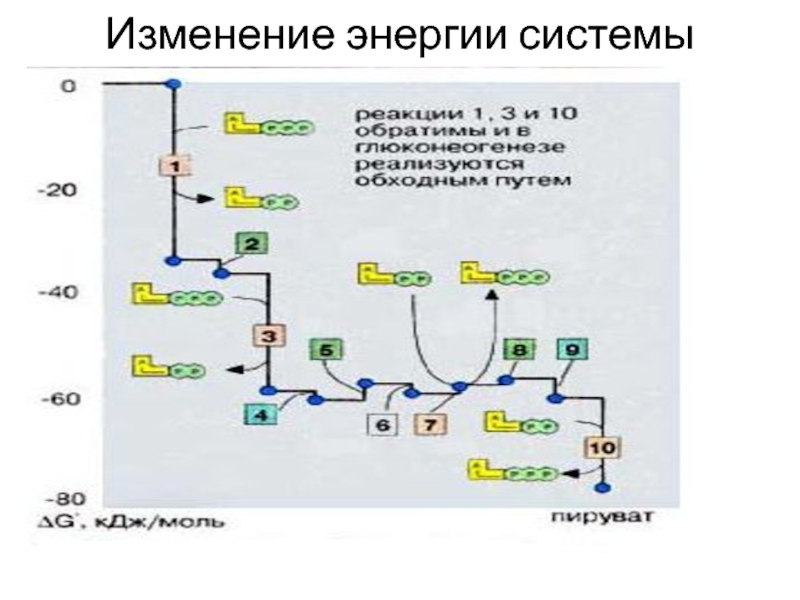
- 33. Изменение энергии системы
- 34. Спиртовое брожениеАнаэробный распад глюкозы с образованием этанолаВсе
- 35. Метаболизм этанолаНебольшая амфифильная молекула (R ≈0.43нм), хорошо
- 36. Метаболизм этанола (прод.)3 пути метаболизма:Алкоголь ДГ –
- 37. Метаболизм этанола (прод.)2. МЭОС – микросомальная этанолокисляющая
- 38. Метаболизм этанола (прод.)3. Минорный каталазный путь (до
- 39. Метаболизм ацетальдегида (Ац)Ац подвергается окислению до ацетата
- 40. Метаболические эффекты этанола (100-150 г.)Увеличение в цит
- 41. Метаболические механизмы формирования зависимостиКатехоламиновая эйфорияУвеличение продукции эндогенного
- 42. Слайд 42
- 43. Скачать презентанцию
Содержание 1.Пути обмена глюкозо-6 фосфата в тканях2.Анаэробное расщепление глюкозы3.Спиртовое брожение4. Метаболизм этанола5.Регуляция гликолиза и гликогенолиза6.Энергетический баланс окисления углеводов.
Слайды и текст этой презентации
Слайд 2Содержание
1.Пути обмена глюкозо-6 фосфата в тканях
2.Анаэробное расщепление глюкозы
3.Спиртовое брожение
4.
Метаболизм этанола
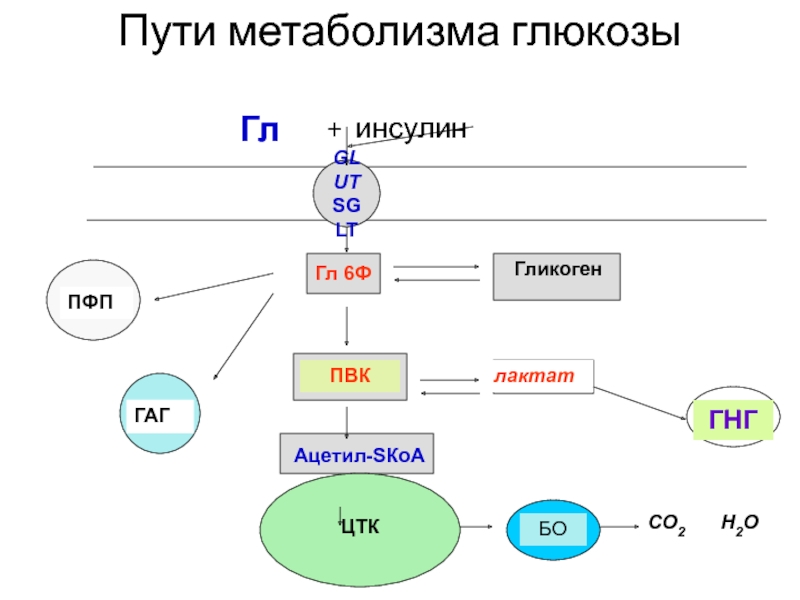
Слайд 3Пути метаболизма глюкозы
Гл + инсулин
GLUT
SGLT
Гл 6Ф
ПВК
лактат
ГНГ
Гликоген
ПФП
ГАГ
Ацетил-SКоА
ЦТК
БО
СО2
Н2О
Слайд 4 Гликолиз и гликогенолиз
Гликолиз (греч.
glykys-сладкий, lysis-распад)-процесс распада глюкоз (аэробный или анаэробный)
Брожение – анаэробный гликолиз
с образованием АТФ и различных в-в (спирта, лактата, ацетата, пропионата, бутирата) Гликогенолиз- процесс распада гликогена
В фосфоглюкомутазной реакции образуется Г-6ф, после чего пути гликолиза и гликогенолиза полностью совпадают
В процессе гликогенолиза образуется 3 молекулы АТФ, а не 2, (образование Г-6ф происходит без затраты АТФ)
Во время синтеза гликогена расходуется АТФ, поэтому гликогенолиз и гликолиз энергетически равноценны
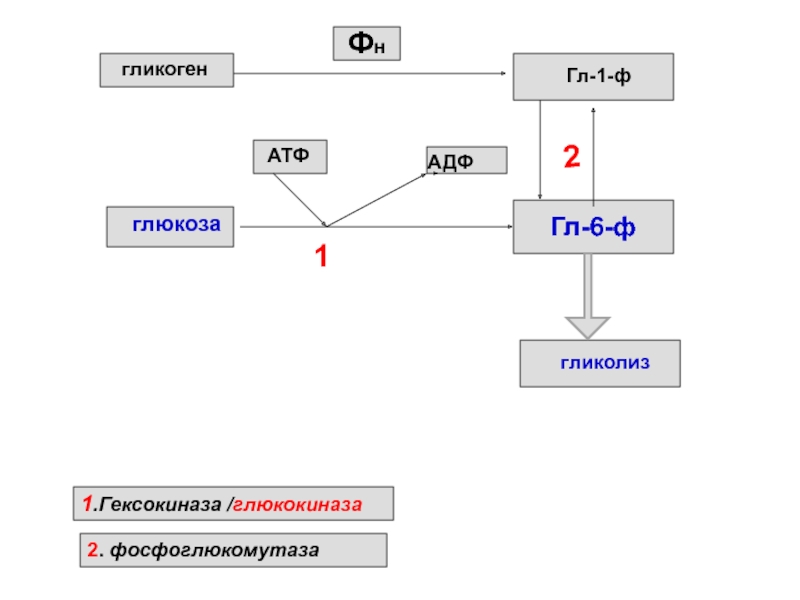
Слайд 5
гликоген
Фн
Гл-1-ф
глюкоза
2
Гл-6-ф
АТФ
АДФ
1
1.Гексокиназа /глюкокиназа
2. фосфоглюкомутаза
гликолиз
Слайд 6Гликолиз
Центральный путь энергетичекого обмена.
В анаэробных условиях –гликолиз единственный путь производства
энергии
Протекает практически во всех тканях
Активность зависит от уровня
кровоснабжения ткани, т.е. ее аэрации и оксигенацииИмеет две стадии
– энергозатратная (подготовительная) и
– энергопродуцирующая
Слайд 9ГК реакция (прод.)
Первая реакция гликолиза - активация (фосфорилирование) Гл.
фермент Гексокиназа
(фосфотрансфераза),
может фосфорилировать фруктозу и маннозу.
Реакции необратима, т.к. происходит
диссипация большей части энергии. ГК- аллостерический фермент и ингибируется Гл-6-ф и высокими конц АТФ.
ГК есть во всех клетках организма Км 0.01- 0.1 мМ/л
Слайд 10В печени, почках, поджелудочной железе есть глюкокиназа, которая фосфорилирует только
глюкозу.
Она не ингибируется Гл-6-ф
имеет высокую (10 мМ/л) Км
для глюкозы т.е. «работает» при высоких конц. глюкозы.2-я реакция - обратимая изомеризация Гл-6-ф с образованием более симметричной молекулы Фр6ф
Фермент - фосфогексоизомераза
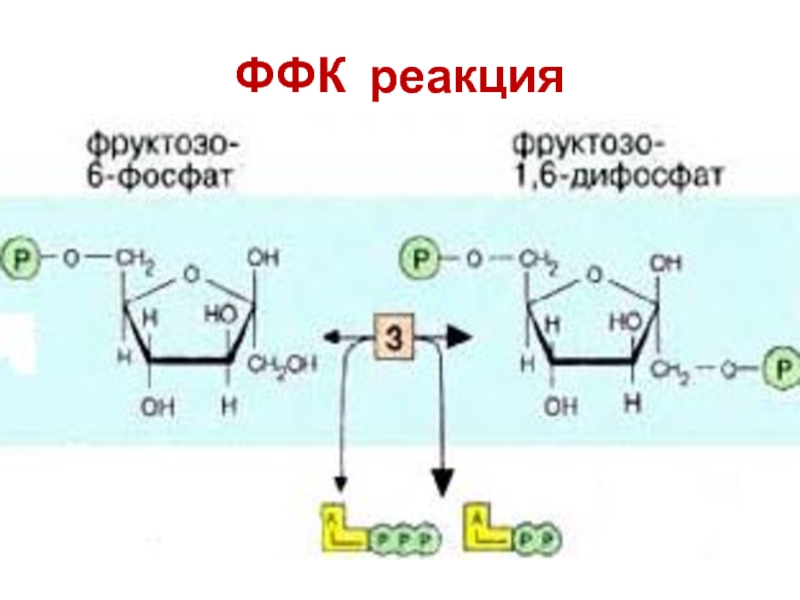
Слайд 12 3-я реакция - получение симметричной молекулы
Фермент - Фосфофруктокиназа
(ФФК) катализирует лимитирующую стадию, определяющую скорость гликолиза в целом
ФФК
- аллостерический фермент, ингибируется АТФ и стимулируется АДФ и АМФАТФ в разных (субстратных или регуляторных) концентрациях является субстратом или аллостерическим ингибитором, тормозящим гликолиз
Слайд 14Регуляция активности ФФК и скорости гликолиза
Км для субстратного и
регуляторного центров различны, фермент «отслеживает» уровень АТФ и зависимости от
[АТФ] активируется или ингибируетсяПри накоплении [АТФ] отношение АТФ/АДФ активность ФФК и гликолиза снижается, например, в неработающей мышце
При снижении [АТФ] - обратная реакция
Слайд 15Регуляция активности ФФК и скорости гликолиза (прод)
ФФК и гликолиз:
ингибируется цитратом,
ЖК и их ацил-КоА. При АТФ/АДФ, скорость ЦТК
снижается → [цитрат], который ингибирует гликолизактивируется ионами Са++ - вторичный мессенджер (активатор многих функций клетки) например при мышечном сокращении
Слайд 174-я реакция. Фермент-альдолаза (лиаза). Разрыв связи происходит в результате ослабления
связи между атомами С3 и С4 , за счет смещения
е плотности на периферию.Равновесие реакции сдвинуто в сторону распада Ф1,6-ф, т.к. образующийся 3-ФГА расходуется в реакциях гликолиза.
Т. О. завершается первый этап гликолиза, связанный с расходом энергии 2 мол. АТФ на активацию субстратов.
Слайд 18Характеристика альдолазы (см. учебник)
Определение активности альдолазы используют в энзимодиагностике при
заболеваниях, связанных с повреждением или гибелью клеток при:
остром гепатите активность
этого фермента может увеличиваться в 5-20 раз, инфаркте миокарда – в 3-10 раз,
миодистрофии – в 4-10 раз.
Слайд 20
Эти триозы — глицеральдегид-3-фосфат (3ФГА) и дигидроксиацетонфосфат (ФДА)— превращаются один
в другой триозофосфатизомеразой [5].
В дальнейший метаболизм вступает 2 мол.
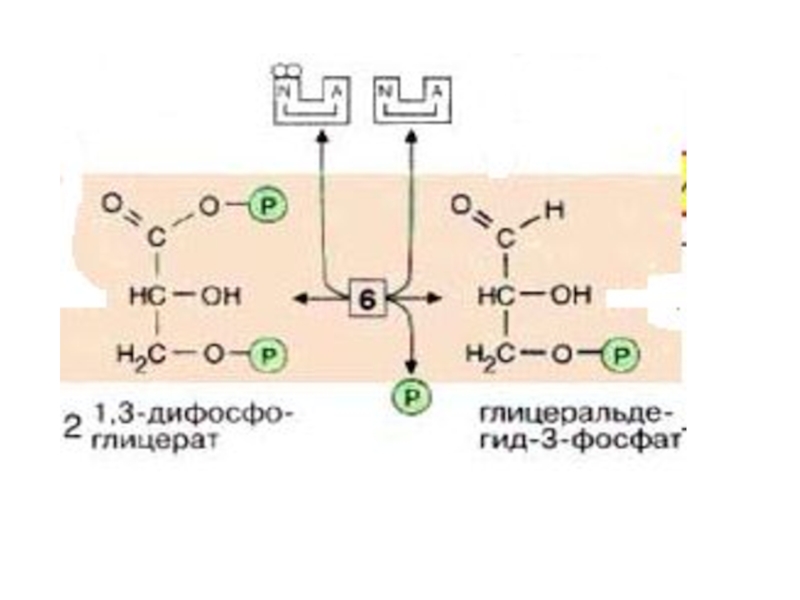
3ФГАСлайд 213ФГА затем окисляется глицеральдегид-З-фосфатдегидрогеназой [6] с образованием NADH + H+
Процесс
называется гликолитической оксидоредукцией
В этой обратимой реакции в молекулу включается
Фн (для последующего «субстратного фосфорилирования»,) с образованием 1,3-диФГК. 1,3-диФГК содержит фосфо~ангидридную связь, расщепление которой сопряжено с образованием АТФ
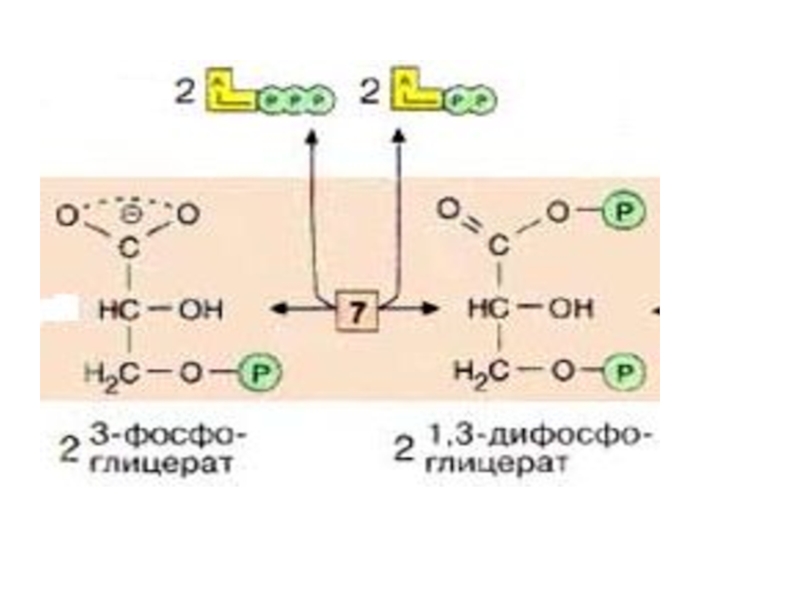
Слайд 23На следующей стадии (катализируемой фосфоглицераткиназой [7]) перенос фосфата этого соединения
сопряжен с образованием АТФ.
Слайд 26Следующие реакции:
изомеризации 3-ФГК, полученного в результате реакции [7], в 2-фосфоглицерат
(фермент: фосфоглицератмутаза [8])
и последующего отщепления воды (фермент: енолаза -
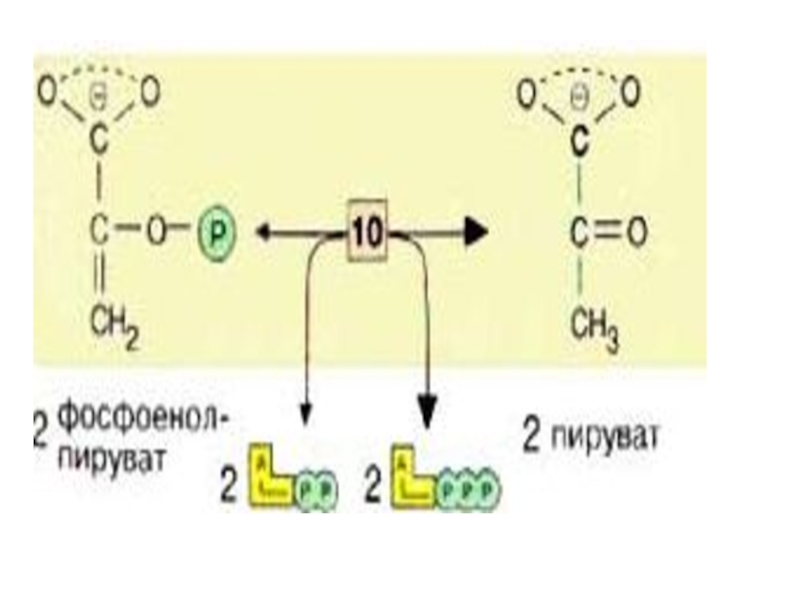
лиаза[9]). Продукт представляет собой сложный эфир фосфорной кислоты и енольной формы пирувата и потому называется фосфоенолпируватом (ФЕП). Слайд 28На предпоследней необратимой стадии, которая катализируется пируваткиназой [10], образуются ПВК
и АТФ.
Это вторая энергодающая реакция гликолиза (синтеза АТФ) –
вторая реакция субстратного фосфорилированияФермент активируется Ф1,6диФ, и ингибируется АТФ и ацетил-КоА
Слайд 30ЛДГ
Завершающий стадией гликолиза является ЛДГ реакция:
Стадия регенерации NAD+ и образования
лактата
ПВК + NADH+H+ лактат +NAD+
Слайд 31При гликолизе на активацию одной молекулы глюкозы потребляется 2 молекулы
АТФ. В то же время при метаболическом превращении каждого С3-фрагмента
образуются 2 молекулы АТФ. В результате выигрыш энергии составляет 2 моля АТФ на моль глюкозыСлайд 34Спиртовое брожение
Анаэробный распад глюкозы с образованием этанола
Все стадии до образования
ПВК идентичны гликолизу
Различие:
ПВК 1 ----> Ацетальдегид 2 ----> Этанол
1. ПВК
декарбоксилаза (IV) кофермент ТПФ2. Алкоголь ДГ кофермент NADH
Слайд 35Метаболизм этанола
Небольшая амфифильная молекула (R ≈0.43нм), хорошо растворима в водной
и гидрофобной фазах
В организме образуется эндогенный этанол – 20-200
мкМ/л (0.0004 – 0.001 г/л) – буфер ацетальдегида – мощного регулятора О-В процессовУ животных с низким содержанием эндогенного этанола его метаболизм и выведение повышены
Вероятно у человека потребность в экзогенном этаноле м.б. отчасти объяснена снижением его эндогенного содержания при стрессе, старении, голодании, авитаминозах и т.д.
Слайд 36Метаболизм этанола (прод.)
3 пути метаболизма:
Алкоголь ДГ – низкоспецифичный NAD-завис. фермент
цитоплазмы (до 80% экз. этанола)
Этанол +NAD+
Ац-альдегид + NADH + H+ ≈ 80% монголоидов и 5-20% европеоидов имеют АДГ2 2-1 (β2β1) и АДГ2 2(β2β2) с высокой активностью (быстрый токсич. эффект)
Слайд 37Метаболизм этанола (прод.)
2. МЭОС – микросомальная этанолокисляющая система (10-20% экз.
этанола)
Этанол + О2 + NADPH+H+
Ац +NADP+ + 2Н2ОИндуцибельная система действием спиртов, и др. ксенобиотиков
У алкоголиков до 50-70% экз. этанола, причем одновременно метаболизируют и др. ксенобиотики (причина толерантности к алкоголю)
Более высокая Км чем у АДГ
Попутно образуются АФК, повреждающие различніе ткани – печень миокард, ЖКТ и др
Слайд 38Метаболизм этанола (прод.)
3. Минорный каталазный путь (до 2%)
Этанол +
Н2О2 каталаза Ац + 2 Н2О
Наиболее
активен в мозге и пероксисомах печени
Слайд 39Метаболизм ацетальдегида (Ац)
Ац подвергается окислению до ацетата 2 путями
минорный
альдегдоксидазный:
Ац + О2 + FADH2
+ Н2О2+ FAD при этом обр различные АФК, вызывающие пероксидный стресс и поражение внутренних органов
2. АцДГ обнаружена в разных органах (печень до 40%, почки, ЖКТ, эритроциты):
Ац + Н2О +NAD+ ацетат +NADH+H+
Слайд 40Метаболические эффекты этанола (100-150 г.)
Увеличение в цит и Мх [Ац],
[NADH+H+ ]
Ингибирование NAD-зависимых ДГ (ЦТК, ДЦ, окисление ЖК), что еще
более увеличивает [NADH+H+] – лактат-ацидозТорможение окисления ЖК и синтез эндогенных ТГ – жировая инфильтрация и дегенерация внутр. органов (жировая печень, тигровое сердце и др.)
Активация продукции и окисления эндогенного сукцината
Снижение скорости ТД и ОФ – потребления О2 (низкоэнергетическое состояние)
Метаболизм этанола и высокая [NADH+H+ ] инициирует образование АФК и пероксидный стресс, ПОЛ – изменение вязкости мембран их повреждение, а также белков, ДНК и др.
Апоптоз, дегенеративные повреждение внутр. органов
Слайд 41Метаболические механизмы формирования зависимости
Катехоламиновая эйфория
Увеличение продукции эндогенного этанола
Снижение скорости потребления
О2 – (низкоэнергетическое состояние) - образование в ГМ медиаторов торможения
ГАМК, ГОМКВзаимодействие Ац и биогенных аминов и образование морфиноподобных в-в (сальсолинол, бета-карболины, тетрагидропапаверолины)
Истощение и нарушение обмена дофамин →норадрена- лин причина депрессий между приемами этанола
Гипогликемия из-за алиментарных нарушений и торможения ГНГ
Снижение продукции половых гормонов (депрессия)














![Углеводы-2 Эти триозы — глицеральдегид-3-фосфат (3ФГА) и дигидроксиацетонфосфат (ФДА)— превращаются один в Эти триозы — глицеральдегид-3-фосфат (3ФГА) и дигидроксиацетонфосфат (ФДА)— превращаются один в другой триозофосфатизомеразой [5]. В дальнейший метаболизм](/img/thumbs/5b3b987097232c165f10434838f3baf8-800x.jpg)
![Углеводы-2 3ФГА затем окисляется глицеральдегид-З-фосфатдегидрогеназой [6] с образованием NADH + H+Процесс называется 3ФГА затем окисляется глицеральдегид-З-фосфатдегидрогеназой [6] с образованием NADH + H+Процесс называется гликолитической оксидоредукцией В этой обратимой реакции](/img/thumbs/2390daa6b3716977469b6620029ae261-800x.jpg)
![Углеводы-2 На следующей стадии (катализируемой фосфоглицераткиназой [7]) перенос фосфата этого соединения сопряжен с образованием АТФ. На следующей стадии (катализируемой фосфоглицераткиназой [7]) перенос фосфата этого соединения сопряжен с образованием АТФ.](/img/thumbs/37596258d56715013cff16ec64671e9b-800x.jpg)

![Углеводы-2 Следующие реакции:изомеризации 3-ФГК, полученного в результате реакции [7], в 2-фосфоглицерат (фермент: Следующие реакции:изомеризации 3-ФГК, полученного в результате реакции [7], в 2-фосфоглицерат (фермент: фосфоглицератмутаза [8]) и последующего отщепления воды](/img/thumbs/a57521fd5f21024644743133f4662511-800x.jpg)

![Углеводы-2 На предпоследней необратимой стадии, которая катализируется пируваткиназой [10], образуются ПВК и На предпоследней необратимой стадии, которая катализируется пируваткиназой [10], образуются ПВК и АТФ. Это вторая энергодающая реакция гликолиза](/img/thumbs/b10ea913330df375009b07179cd875b9-800x.jpg)









![Углеводы-2 Метаболические эффекты этанола (100-150 г.)Увеличение в цит и Мх [Ац], [NADH+H+ Метаболические эффекты этанола (100-150 г.)Увеличение в цит и Мх [Ац], [NADH+H+ ]Ингибирование NAD-зависимых ДГ (ЦТК, ДЦ, окисление](/img/thumbs/3b6418a0064302a26a1dec70af384061-800x.jpg)