Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
1_Sily_BMM.ppt
Содержание
- 1. 1_Sily_BMM.ppt
- 2. ПРЕДМЕТ МОЛЕКУЛЯРНОЙ БИОФИЗИКИРАСКРЫТЬ ПРИРОДУ ВЗАИМОДЕЙСТВИЯ АТОМАРНЫХ ГРУПП,
- 3. СПЕЦИФИКА БИОМАКРОМОЛЕКУЛСТАТИСТИЧЕСКИЙ ХАРАКТЕР ПОВЕДЕНИЯ, Т.К. БИОМАКРОМОЛЕКУЛЫ СОСТОЯТ
- 4. МЕТОДЫ ИССЛЕДОВАНИЯ БИОМАКРОМОЛЕКУЛ (обзор)
- 5. В 1953 Дж. Уотсон и Ф.Крик предложили
- 6. РЕНТГЕНОГРАММА ДНК, ПОЛУЧЕННАЯ РОЗАЛИНДОЙ ФРАНКЛИНРозалинда Франклин (1920–1958)
- 7. Первые рентгенограммы белков получены еще в 30-х годах (У.Астбюри, Л.Полинг, Р.Кори).Л.Полинг1901 - 1994
- 8. РЕНТГЕНОСТРУКТУРНЫЙ АНАЛИЗ ПРЯМОЙ МЕТОД ИССЛЕДОВАНИЯПОЗВОЛЯЕТ ОПРЕДЕЛИТЬ РАСПОЛОЖЕНИЕ ВСЕХ АТОМОВ В ТРЕХМЕРНОМ ПРОСТРАНСТВЕИМЕЕТ ОГРАНИЧЕНИЯМЕТОДЫ ИССЛЕДОВАНИЯ БИОМАКРОМОЛЕКУЛ
- 9. Рентгеновский структурный анализ Взаимодействие рентгеновского излучения с
- 10. Принципиальная схема : исследуемый объект помещают в
- 11. Основные положения1. Пучок рентгеновских лучей является плоской
- 12. Кристаллический образец (1) рентгеновские лучи (2). Рентгеновские
- 13. 1.Из данных рентгенограммы получают карту распределения электронной
- 14. 2.На основании карты распределения электронной плотности определяют
- 15. Основные этапы определения структуры белкаВыделение, очисткаКристаллизацияРентгеновский эксперимент, обработка результатов
- 16. РЕНТГЕНОГРАММА БАКТЕРИАЛЬНОГО БЕЛКА
- 17. Схематичная модель молекулы гемоглобина (М.Ф.Перутц, 1960 г.) Структура фермента дуоденазы с молекулой субстрата
- 18. Рентгеноструктурный анализ белковой молекулы позволяет установитьПоследовательность аминокислотных остатков в цепиЗакономерности конфигурации белковой молекулы
- 19. ОГРАНИЧЕНИЕ МЕТОДА: С ПОМОЩЬЮ РЕНГГЕНОВСКИХ ЛУЧЕЙ МОЖНО
- 20. МЕТОДЫ ИССЛЕДОВАНИЯ БИОМАКРОМОЛЕКУЛДЛЯ ОПРЕДЕЛЕНИЯ МАССЫ, РАЗМЕРОВ, ГИБКОСТИ БИОМАКРОМОЛЕКУЛ ИСПОЛЬЗУЮТСЯЭЛЕКТРОФОРЕЗВИСКОЗИМЕТРИЯСЕДИМЕНТАЦИОННЫЙ АНАЛИЗКВАЗИУПРУГОЕ РАССЕЯНИЕ СВЕТАЭЛЕКТРОННАЯ МИКРОСКОПИЯ
- 21. МЕТОДЫ ИССЛЕДОВАНИЯ БИОМАКРОМОЛЕКУЛДЛЯ ИЗУЧЕНИЯ ВТОРИЧНОЙ СТРУКТУРЫ ИСПОЛЬЗУЮТСЯСПЕКТРОФОТОМЕТРИЯИНФРАКРАСНАЯ СПЕКТРОСКОПИЯКРУГОВОЙ ДИХРОИЗМДИСПЕРСИЯ ОПТИЧЕСКОГО ВРАЩЕНИЯ
- 22. ДЛЯ ИССЛЕДОВАНИЯ ДИНАМИКИ БИОМАКРОМОЛЕКУЛ ИСПОЛЬЗУЮТСЯФЛУОРЕСЦЕНТНАЯ СПЕКТРОСКОПИЯЯМРЭПРМЕТОДЫ ИССЛЕДОВАНИЯ БИОМАКРОМОЛЕКУЛ
- 23. КОНФОРМАЦИИ БИОМАКРОМОЛЕКУЛ
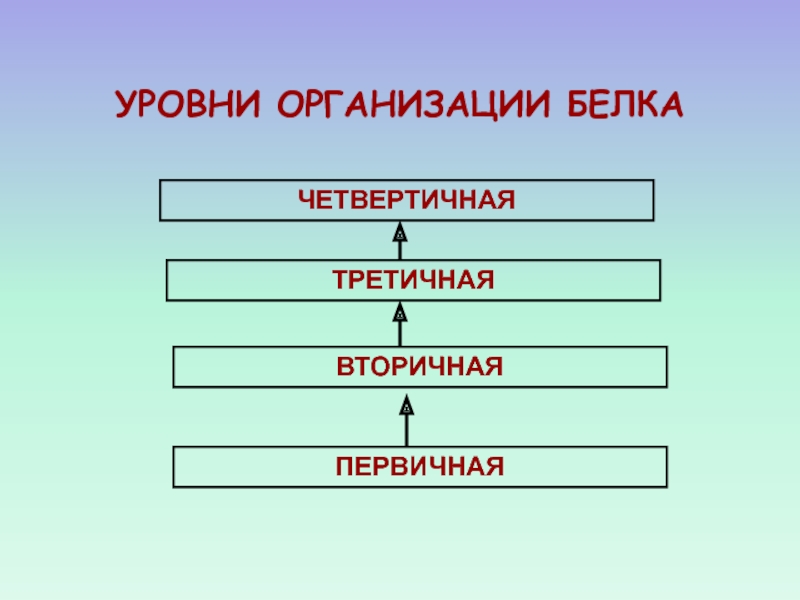
- 24. УРОВНИ ОРГАНИЗАЦИИ БЕЛКАЧЕТВЕРТИЧНАЯТРЕТИЧНАЯВТОРИЧНАЯПЕРВИЧНАЯ
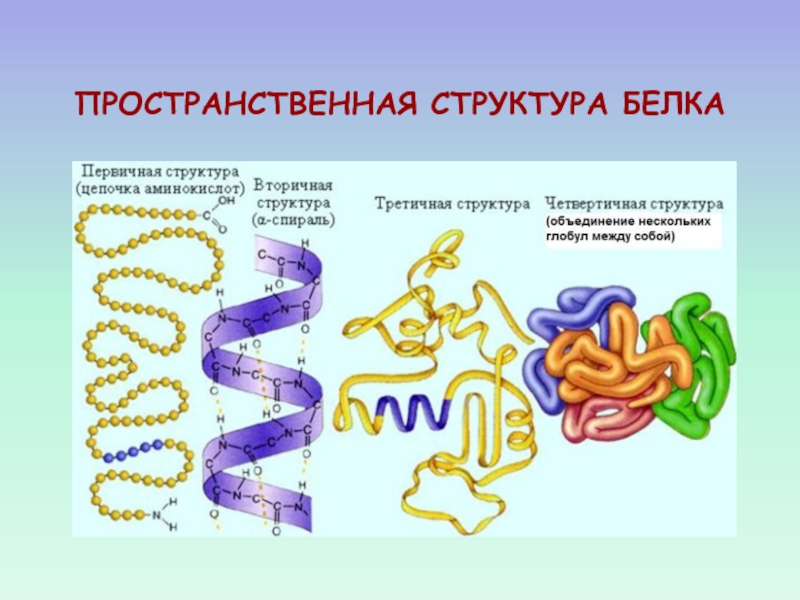
- 25. ПРОСТРАНСТВЕННАЯ СТРУКТУРА БЕЛКА
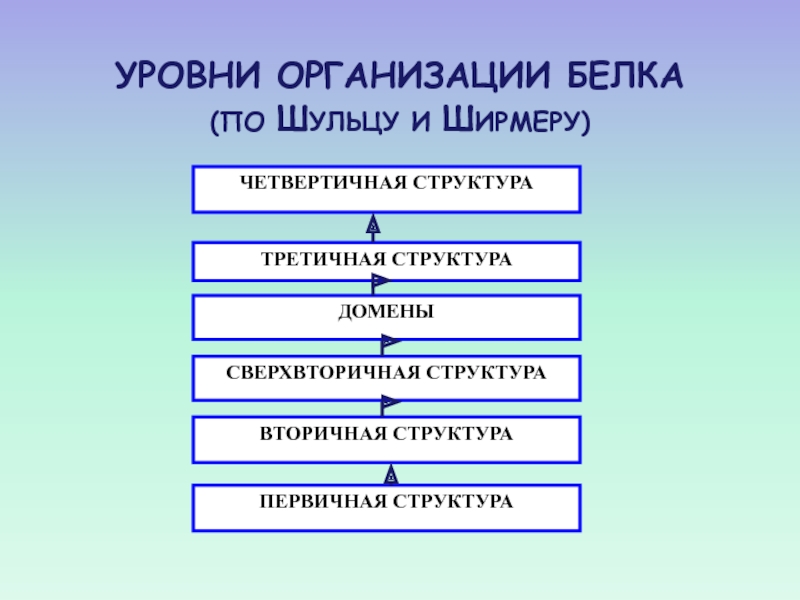
- 26. УРОВНИ ОРГАНИЗАЦИИ БЕЛКА (ПО ШУЛЬЦУ И ШИРМЕРУ)
- 27. СИЛЫ, СТАБИЛИЗИРУЮШИЕ СТРУКТУРУ БИОМАКРОМОЛЕКУЛ
- 28. ВЗАИМОДЕЙСТВИЯ, СТАБИЛИЗИРУЮЩИЕ СТРУКТУРУ БИОМАКРОМОЛЕКУЛСИЛЬНЫЕ СВЯЗИКОВАЛЕНТНЫЕИОННЫЕСЛАБЫЕ СВЯЗИВАН-ДЕР-ВААЛЬСОВЫГИДРОФОБНЫЕПРОМЕЖУТОЧНЫЕ СВЯЗИВОДОРОДНЫЕ
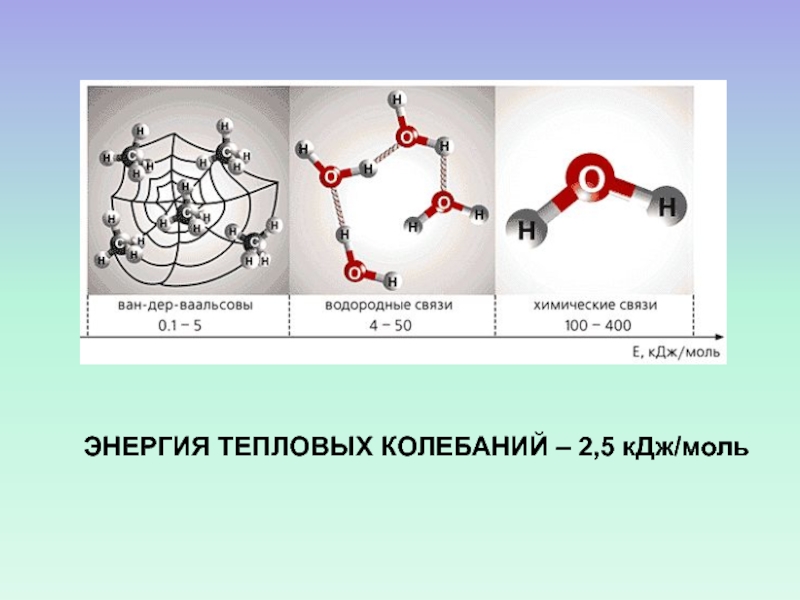
- 29. ЭНЕРГИЯ ТЕПЛОВЫХ КОЛЕБАНИЙ – 2,5 кДж/моль
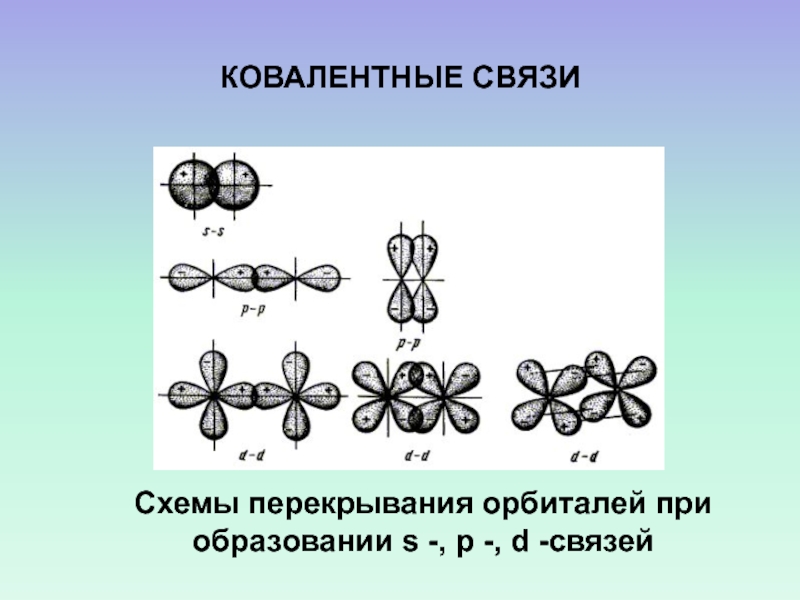
- 30. Схемы перекрывания орбиталей при образовании s -, p -, d -связейКОВАЛЕНТНЫЕ СВЯЗИ
- 31. Ионная связь – взаимодействие двух нейтральных атомов
- 32. 1231 – ЭЛЕКТРОСТАТИЧЕСКИЕ СИЛЫ 4 – ВАН-ДЕР-ВААЛЬСОВЫ СИЛЫ2 – ВОДОРОДНАЯ СВЯЗЬ3 – ГИДРОФОБНЫЕ ВЗАИМОДЕЙСТВИЯ4
- 33. ЭНЕРГИЯ ЭЛЕКТРОСТАТИЧЕСКОГО ВЗАИМОДЕЙСТВИЯ ЗАВИСИТ ОТ ВЕЛИЧИНЫ ЗАРЯДОВ
- 34. ВАН-ДЕР-ВААЛЬСОВЫ ВЗАИМОДЕЙСТВИЯЯн-Дидерик ВАН-ДЕР-ВААЛЬС(1837 - 1923)
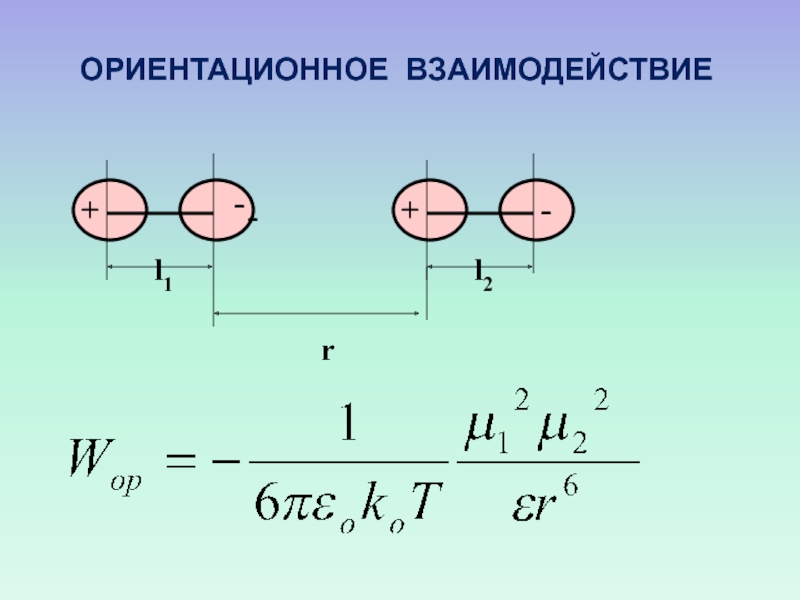
- 35. l1l2r-+--+ОРИЕНТАЦИОННОЕ ВЗАИМОДЕЙСТВИЕ
- 36. Схема взаимодействия между полярными молекулами
- 37. ИНДУКЦИОННОЕ ВЗАИМОДЕЙСТВИЕ- поляризуемость, μ - дипольный момент
- 38. ДИСПЕРСИОННОЕ ВЗАИМОДЕЙСТВИЕI1 I2 - потенциалы ионизацииα1 и α2 – поляризуемость групп
- 39. ВОДОРОДНАЯ СВЯЗЬ
- 40. ВОДОРОДНЫЕ СВЯЗИ ВОДОРОД ХИМИЧЕСКИ СВЯЗАН С ОДНИМ
- 41. АНОМАЛЬНЫЕ СВОЙСТВА ВОДЫ:ВЫСОКАЯ ТЕМПЕРАТУРА КИПЕНИЯ (373К) И
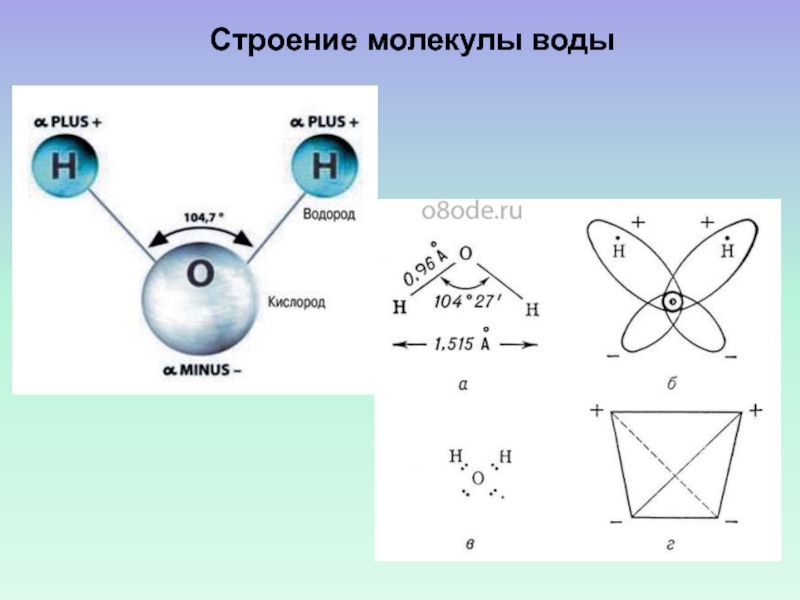
- 42. Строение молекулы воды
- 43. Распределение зарядов и электронной плотности в молекуле
- 44. Слайд 44
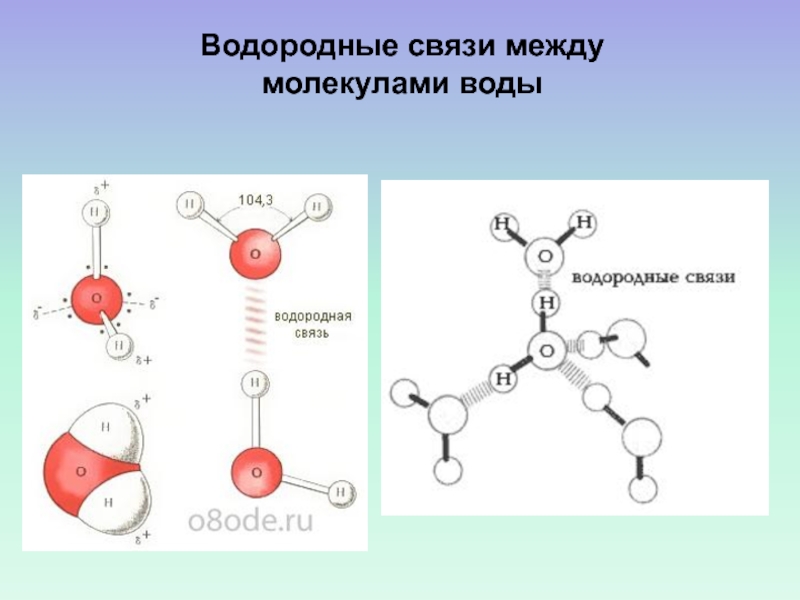
- 45. Водородные связи между молекулами воды
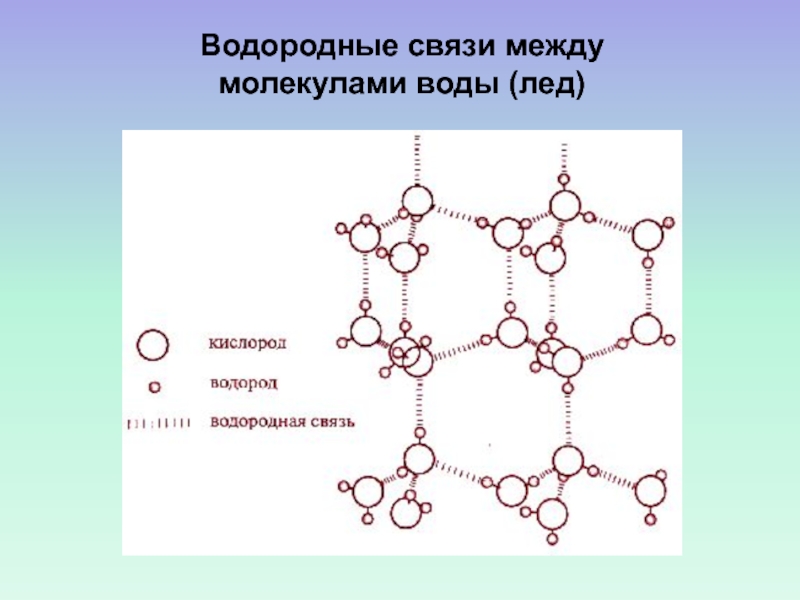
- 46. Водородные связи между молекулами воды (лед)
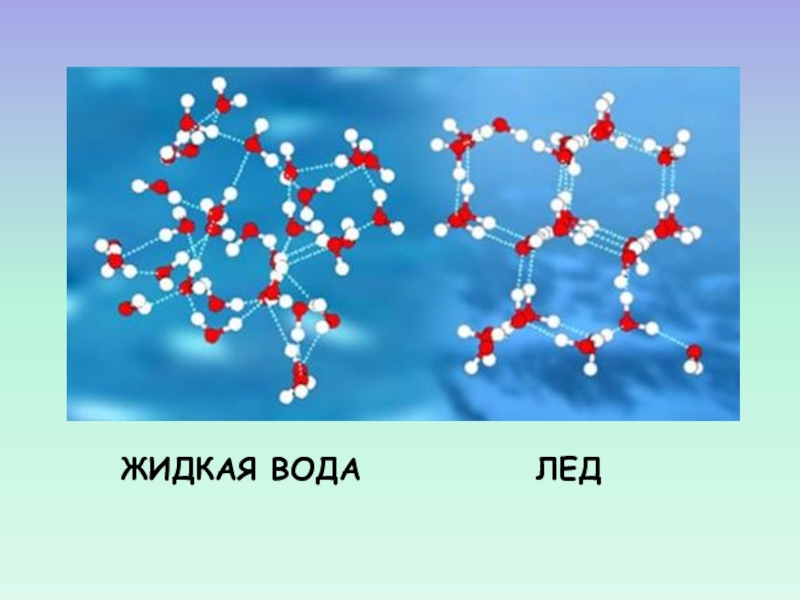
- 47. ЖИДКАЯ ВОДА ЛЕД
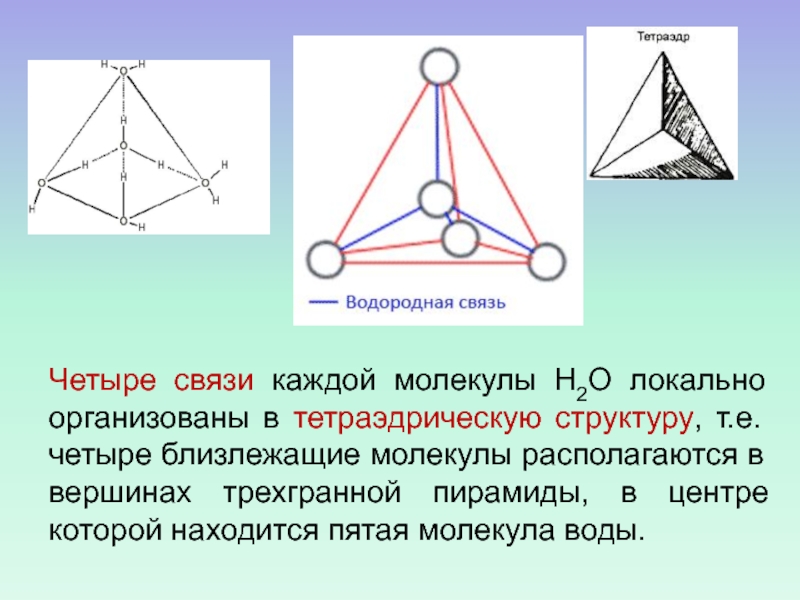
- 48. Четыре связи каждой молекулы Н2О локально организованы
- 49. ТЕОРИИ СТРУКТУРЫ ВОДЫВпервые идея о том, что
- 50. Модель непрерывной структуры воды (континуальная модель).
- 51. КЛАСТЕРНЫЕ МОДЕЛИВОДА В ВИДЕ КЛАСТЕРОВ ИЗ МОЛЕКУЛ,
- 52. Модель мерцающих кластеров, Фрэк и Уэн, 1957
- 53. КЛАТРАТНАЯ МОДЕЛЬ ВОДЫВОДА ОБРАЗУЕТ НЕПРЕРЫВНУЮ СЕТКУ (КАРКАС)
- 54. В 1993 году американский химик Кен Джордан
- 55. Структура жидкой воды. В воде кластеры периодически разрушаются и образуются снова. Время перескока составляет 10-12 секунд.
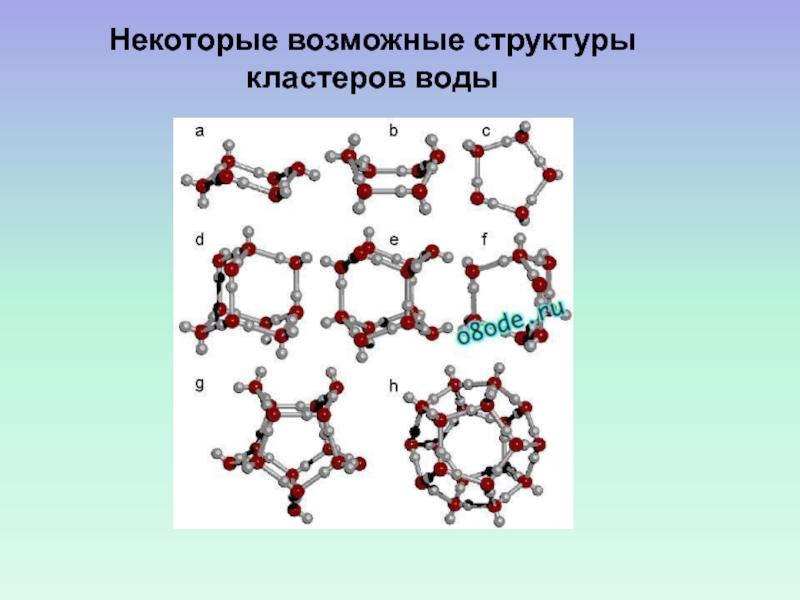
- 56. Некоторые возможные структуры кластеров воды
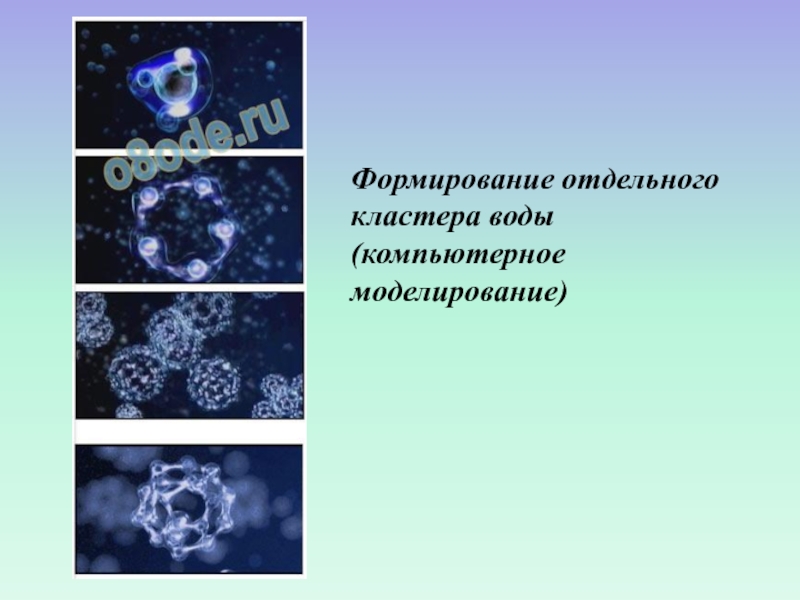
- 57. Формирование отдельного кластера воды (компьютерное моделирование)
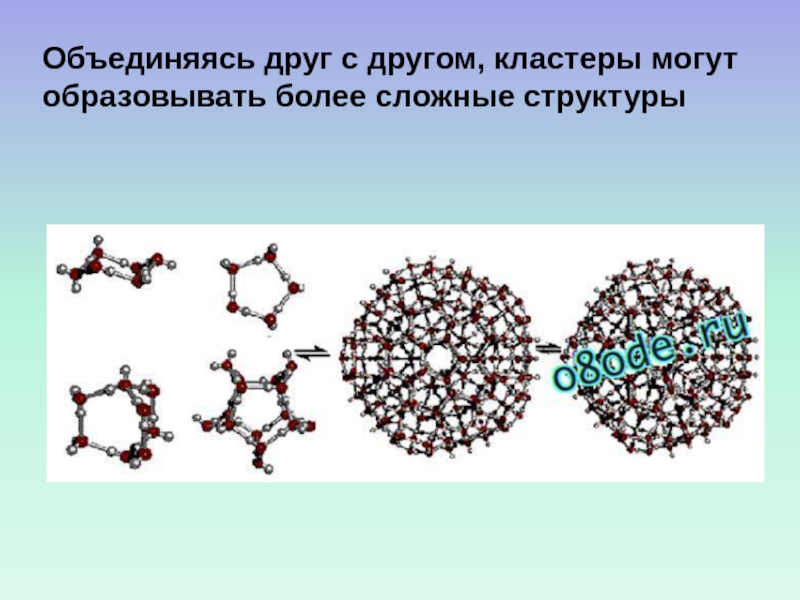
- 58. Объединяясь друг с другом, кластеры могут образовывать более сложные структуры
- 59. ГИДРОФОБНЫЕ ВЗАИМОДЕЙСТВИЯ
- 60. ЭНТРОПИЙНАЯ ПРИРОДА ГИДРОФОБНЫХ ВЗАИМОДЕЙСТВИЙСНИЖЕНИЕ ЭНТРОПИИ ВЫЗЫВАЕТ УВЕЛИЧЕНИЕ СВОБОДНОЙ ЭНЕРГИИ, НО ЭТО КОМПЕНСИРУЕТСЯ СНИЖЕНИЕМ ЭНТАЛЬПИИ
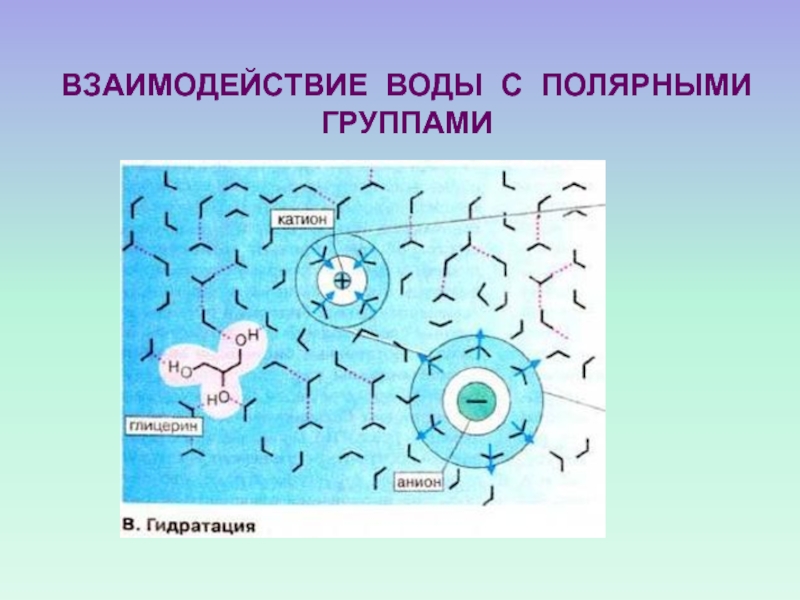
- 61. ВЗАИМОДЕЙСТВИЕ ВОДЫ С ПОЛЯРНЫМИ ГРУППАМИ
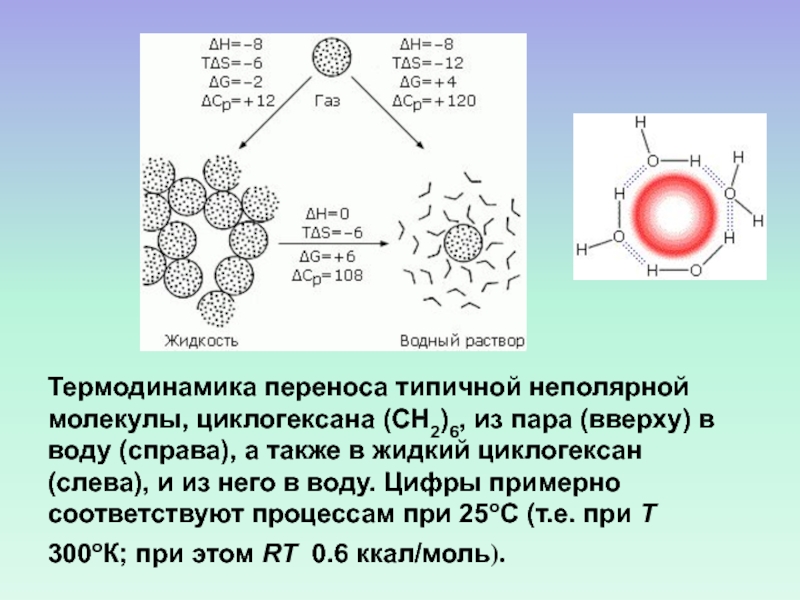
- 62. Термодинамика переноса типичной неполярной молекулы, циклогексана (СН2)6,
- 63. ИЗМЕНЕНИЕ СВОБОДНОЙ ЭНЕРГИИ ПРИ РАСТВОРЕНИИ НЕПОЛЯРНЫХ ВЕЩЕСТВРЕЗУЛЬТАТ:
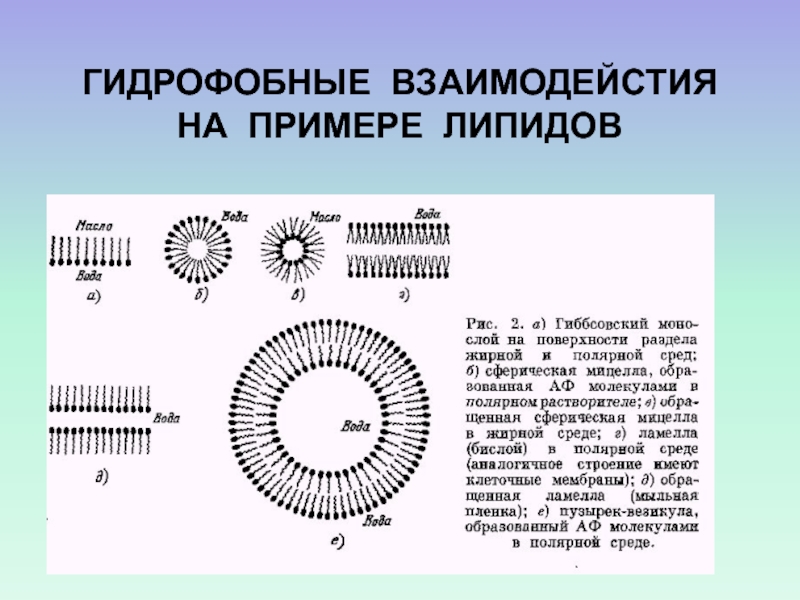
- 64. ГИДРОФОБНЫЕ ВЗАИМОДЕЙСТИЯ НА ПРИМЕРЕ ЛИПИДОВ
- 65. Скачать презентанцию
Слайды и текст этой презентации
Слайд 1ВВЕДЕНИЕ В МОЛЕКУЛЯРНУЮ БИОФИЗИКУ
Предмет молекулярной биофизики
Специфика биомакромолекул
Обзор методов, используемых для
изучения биомакромолекул. Рентгеноструктурный анализ
Слайд 2ПРЕДМЕТ МОЛЕКУЛЯРНОЙ БИОФИЗИКИ
РАСКРЫТЬ ПРИРОДУ ВЗАИМОДЕЙСТВИЯ АТОМАРНЫХ ГРУПП, ОПРЕДЕЛЯЮЩИХ КОНФОРМАЦИИ БИОМАКРОМОЛЕКУЛ,
ВЫЯВИТЬ МЕХАНИЗМЫ ЭЛЕКТРОННЫХ И КОНФОРМАЦИОННЫХ ПЕРЕХОДОВ,
РАСКРЫТЬ МЕХАНИЗМ ФУНКЦИОНИРОВАНИЯ БИОМАКРОМОЛЕКУЛ
В ЖИВЫХ СИСТЕМАХСлайд 3СПЕЦИФИКА БИОМАКРОМОЛЕКУЛ
СТАТИСТИЧЕСКИЙ ХАРАКТЕР ПОВЕДЕНИЯ, Т.К. БИОМАКРОМОЛЕКУЛЫ СОСТОЯТ ИЗ БОЛЬШОГО ЧИСЛА
ОДНОТИПНЫХ ЗВЕНЬЕВ – МОНОМЕРОВ.
НАЛИЧИЕ НЕ ТОЛЬКО ХИМИЧЕСКИХ СВЯЗЕЙ, НО И
ДРУГИХ ВЗАИМОДЕЙСТВИЙ РАЗНОГО ТИПА, ЧТО ОГРАНИЧИВАЕТ ЧИСЛО ВОЗМОЖНЫХ КОНФОРМАЦИЙ.Слайд 5В 1953 Дж. Уотсон и Ф.Крик предложили модель молекулы ДНК,
которая хорошо согласовалась с результатами рентгенографических исследований ДНК, полученными М.Уилкинсом
и Р. Франклин.Слайд 7Первые рентгенограммы белков получены еще в 30-х годах (У.Астбюри, Л.Полинг,
Р.Кори).
Л.Полинг
1901 - 1994
Слайд 8РЕНТГЕНОСТРУКТУРНЫЙ АНАЛИЗ
ПРЯМОЙ МЕТОД ИССЛЕДОВАНИЯ
ПОЗВОЛЯЕТ ОПРЕДЕЛИТЬ РАСПОЛОЖЕНИЕ ВСЕХ АТОМОВ В
ТРЕХМЕРНОМ ПРОСТРАНСТВЕ
ИМЕЕТ ОГРАНИЧЕНИЯ
МЕТОДЫ ИССЛЕДОВАНИЯ БИОМАКРОМОЛЕКУЛ
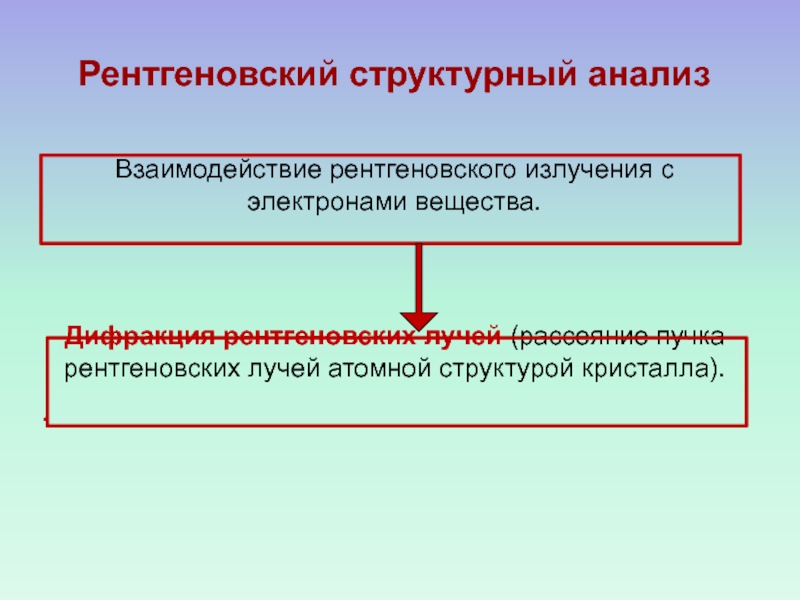
Слайд 9Рентгеновский структурный анализ
Взаимодействие рентгеновского излучения с электронами вещества.
Дифракция рентгеновских
лучей (рассеяние пучка рентгеновских лучей атомной структурой кристалла).
.
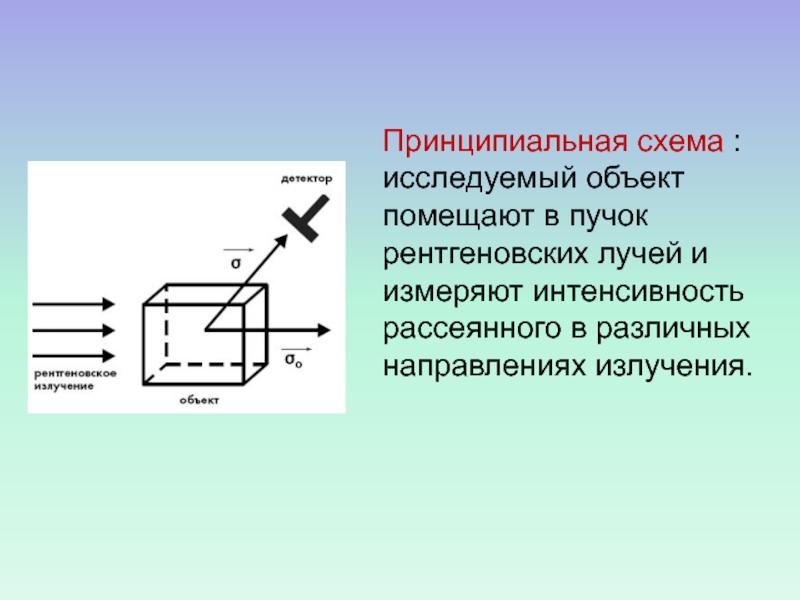
Слайд 10Принципиальная схема : исследуемый объект помещают в пучок рентгеновских лучей
и измеряют интенсивность рассеянного в различных направлениях излучения.
Слайд 11Основные положения
1. Пучок рентгеновских лучей является плоской монохроматической электромагнитной волной.
2.
Под воздействием этой электромагнитной волны каждый электрон образца приходит в
движение.3. Движущийся электрон - источник новой рассеянной сферической электромагнитной волны, распространяющейся во всех направлениях.
4. Эти новые волны суммируются и определяют интенсивность излучения в интересующем нас направлении.
Слайд 12Кристаллический образец (1) рентгеновские лучи (2).
Рентгеновские лучи образуются при
бомбардировке вольфрамового анода (3) электронами в вакууме (4).
Прорезь (5)
фокусирует лучи на кристалле. Расстояние между плоскостями атомов в кристалле либо усиливает (6), либо ослабляет (7) рентгеновские лучи.
Когда луч усиливается, возникающий луч (8) создает пятно (9) на фотопленке. Рисунок пятен служит для установления точной структуры молекулы
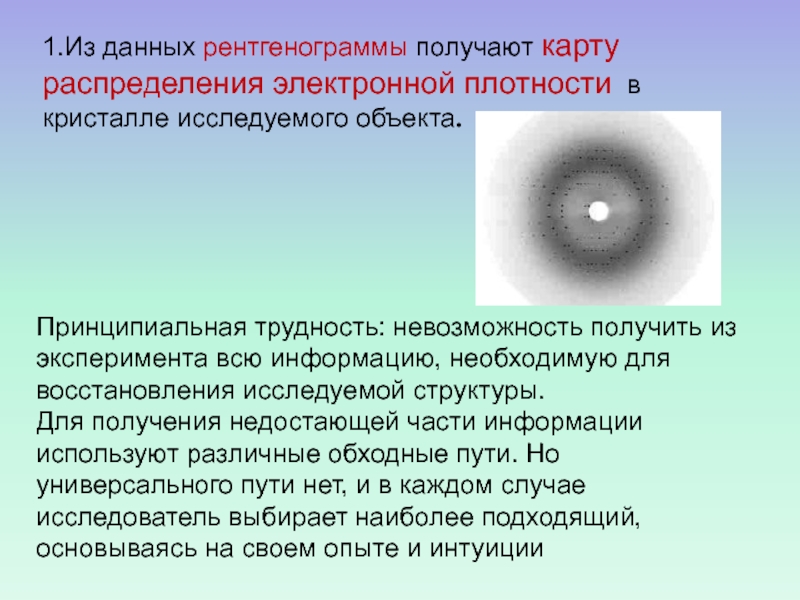
Слайд 131.Из данных рентгенограммы получают карту распределения электронной плотности в кристалле
исследуемого объекта.
Принципиальная трудность: невозможность получить из эксперимента всю информацию,
необходимую для восстановления исследуемой структуры. Для получения недостающей части информации используют различные обходные пути. Но универсального пути нет, и в каждом случае исследователь выбирает наиболее подходящий, основываясь на своем опыте и интуиции
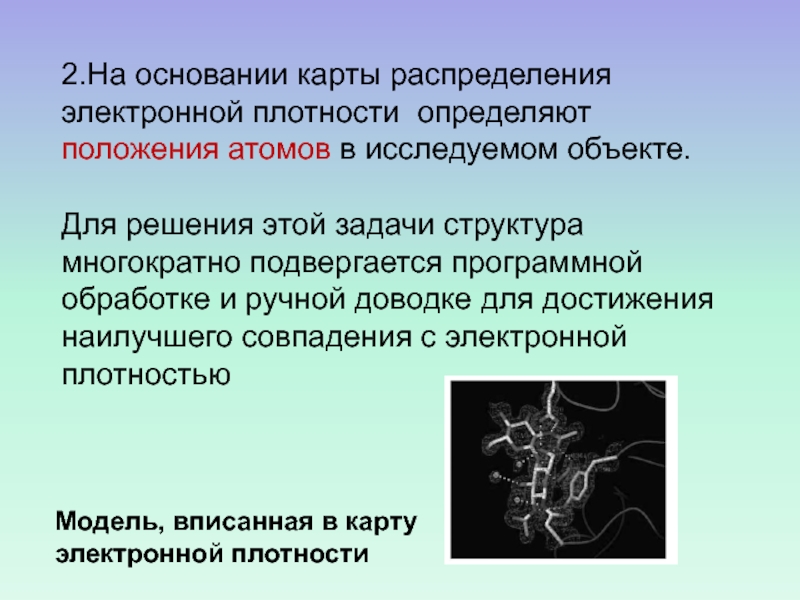
Слайд 142.На основании карты распределения электронной плотности определяют положения атомов в
исследуемом объекте.
Для решения этой задачи структура многократно подвергается программной
обработке и ручной доводке для достижения наилучшего совпадения с электронной плотностьюМодель, вписанная в карту электронной плотности
Слайд 15Основные этапы определения структуры белка
Выделение, очистка
Кристаллизация
Рентгеновский эксперимент, обработка результатов
Слайд 17
Схематичная модель молекулы гемоглобина
(М.Ф.Перутц, 1960 г.)
Структура фермента дуоденазы
с молекулой субстрата
Слайд 18Рентгеноструктурный анализ белковой молекулы позволяет установить
Последовательность аминокислотных остатков в цепи
Закономерности
конфигурации белковой молекулы
Слайд 19ОГРАНИЧЕНИЕ МЕТОДА:
С ПОМОЩЬЮ РЕНГГЕНОВСКИХ ЛУЧЕЙ МОЖНО ИССЛЕДОВАТЬ ТОЛЬКО ТЕ
БЕЛКИ, КОТОРЫЕ КРИСТАЛЛИЗУЮТСЯ.
ЭТО СУЖАЕТ ОБЛАСТЬ ПРИМЕНИМОСТИ МЕТОДА РЕНТГЕНСТРУКТУРНОГО АНАЛИЗА.
ПРИЧИНА: кристаллы
обладают строгой периодичностью строения и представляют собой природную дифракционную решётку для рентгеновских лучей.Слайд 20МЕТОДЫ ИССЛЕДОВАНИЯ БИОМАКРОМОЛЕКУЛ
ДЛЯ ОПРЕДЕЛЕНИЯ МАССЫ, РАЗМЕРОВ, ГИБКОСТИ БИОМАКРОМОЛЕКУЛ ИСПОЛЬЗУЮТСЯ
ЭЛЕКТРОФОРЕЗ
ВИСКОЗИМЕТРИЯ
СЕДИМЕНТАЦИОННЫЙ АНАЛИЗ
КВАЗИУПРУГОЕ
РАССЕЯНИЕ СВЕТА
ЭЛЕКТРОННАЯ МИКРОСКОПИЯ
Слайд 21МЕТОДЫ ИССЛЕДОВАНИЯ БИОМАКРОМОЛЕКУЛ
ДЛЯ ИЗУЧЕНИЯ ВТОРИЧНОЙ СТРУКТУРЫ ИСПОЛЬЗУЮТСЯ
СПЕКТРОФОТОМЕТРИЯ
ИНФРАКРАСНАЯ СПЕКТРОСКОПИЯ
КРУГОВОЙ ДИХРОИЗМ
ДИСПЕРСИЯ ОПТИЧЕСКОГО
ВРАЩЕНИЯ
Слайд 22ДЛЯ ИССЛЕДОВАНИЯ ДИНАМИКИ БИОМАКРОМОЛЕКУЛ ИСПОЛЬЗУЮТСЯ
ФЛУОРЕСЦЕНТНАЯ СПЕКТРОСКОПИЯ
ЯМР
ЭПР
МЕТОДЫ ИССЛЕДОВАНИЯ БИОМАКРОМОЛЕКУЛ
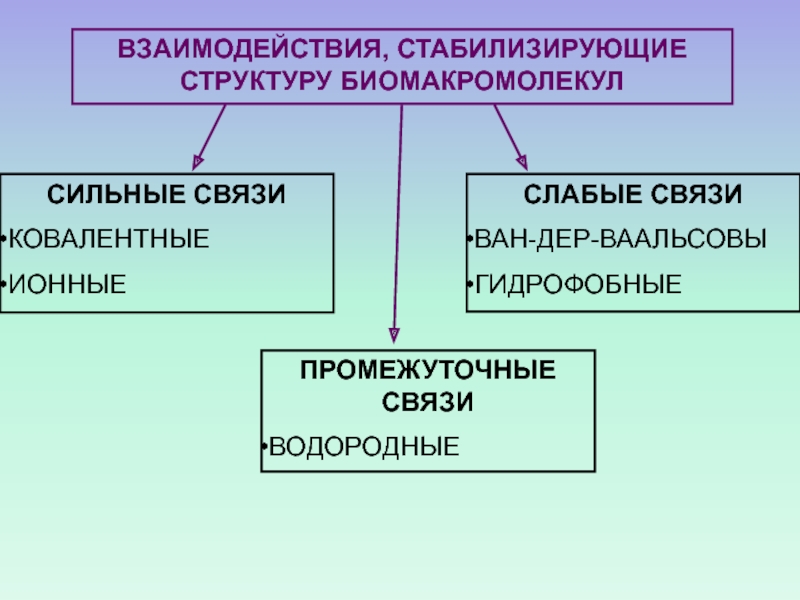
Слайд 28ВЗАИМОДЕЙСТВИЯ, СТАБИЛИЗИРУЮЩИЕ СТРУКТУРУ БИОМАКРОМОЛЕКУЛ
СИЛЬНЫЕ СВЯЗИ
КОВАЛЕНТНЫЕ
ИОННЫЕ
СЛАБЫЕ СВЯЗИ
ВАН-ДЕР-ВААЛЬСОВЫ
ГИДРОФОБНЫЕ
ПРОМЕЖУТОЧНЫЕ СВЯЗИ
ВОДОРОДНЫЕ
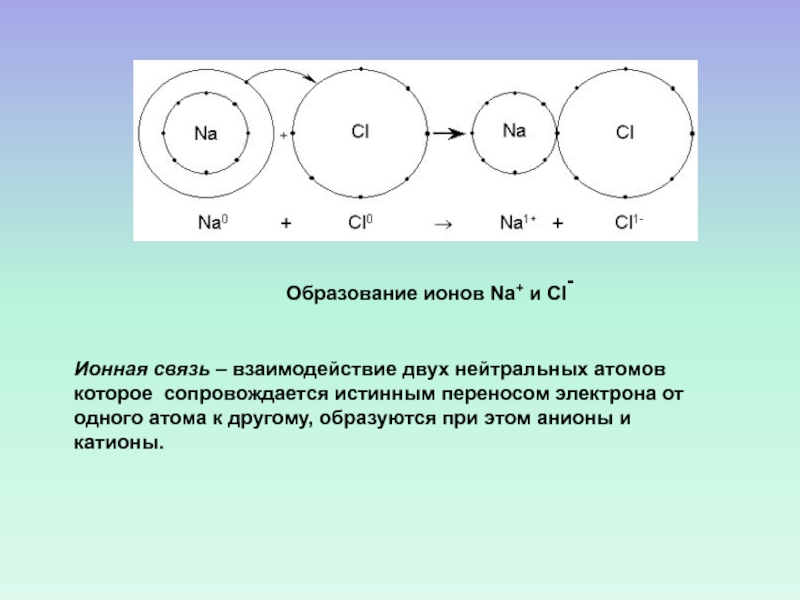
Слайд 31Ионная связь – взаимодействие двух нейтральных атомов которое сопровождается истинным
переносом электрона от одного атома к другому, образуются при этом
анионы и катионы.Образование ионов Na+ и Cl-
Слайд 321
2
3
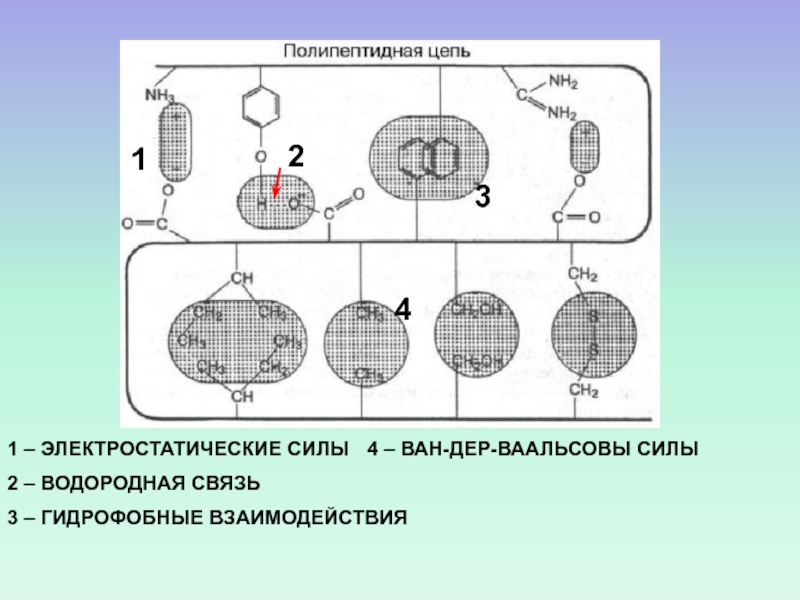
1 – ЭЛЕКТРОСТАТИЧЕСКИЕ СИЛЫ 4 – ВАН-ДЕР-ВААЛЬСОВЫ СИЛЫ
2 – ВОДОРОДНАЯ СВЯЗЬ
3
– ГИДРОФОБНЫЕ ВЗАИМОДЕЙСТВИЯ
4
Слайд 33
ЭНЕРГИЯ ЭЛЕКТРОСТАТИЧЕСКОГО ВЗАИМОДЕЙСТВИЯ ЗАВИСИТ ОТ ВЕЛИЧИНЫ ЗАРЯДОВ ЧАСТИЦ И РАССТОЯНИЯ
МЕЖДУ НИМИ
q1 и q2 – электрические заряды; ε - диэлектрическая
проницаемость; εо – электрическая постоянная (8,85·10-12Кл/В ·м )ЭЛЕКТРОСТАТИЧЕСКОЕ ВЗАИМОДЕЙСТВИЕ
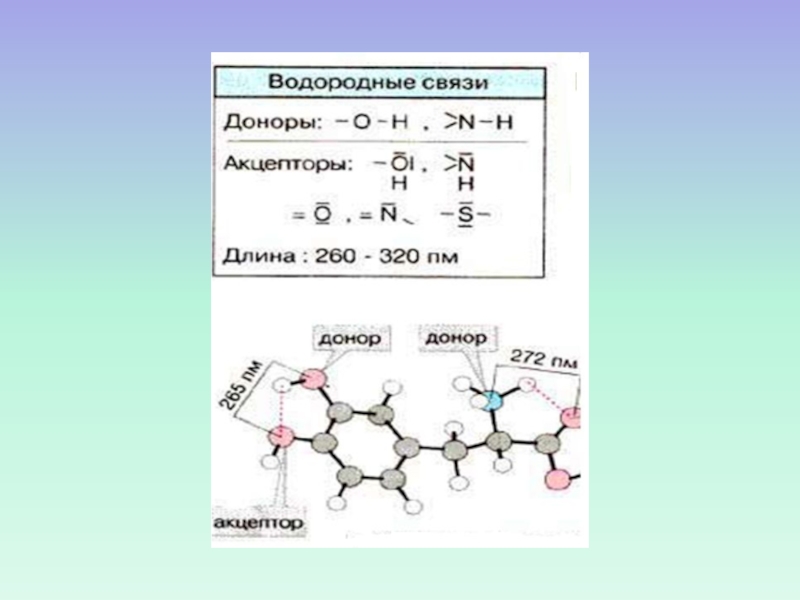
Слайд 40ВОДОРОДНЫЕ СВЯЗИ
ВОДОРОД ХИМИЧЕСКИ СВЯЗАН С ОДНИМ ЭЛЕКТРООТРИЦАТЕЛЬНЫМ АТОМОМ
И ПРИ ЭТОМ ПРИБЛИЖАЕТСЯ К ДРУГОМУ ЭЛЕКТРООТРИЦАТЕЛЬНОМУ АТОМУ.
Слайд 41АНОМАЛЬНЫЕ СВОЙСТВА ВОДЫ:
ВЫСОКАЯ ТЕМПЕРАТУРА КИПЕНИЯ (373К) И
ТЕМПЕРАТУРА ЗАМЕРЗАНИЯ (273К)
ДЛЯ ЕЕ МАЛОГО МОЛЕКУЛЯРНОГО ВЕСА.
ДЛЯ СРАВНЕНИЯ: О2 КИПИТ ПРИ 90К
И ЗАМЕРЗАЕТ ПРИ 54К.ПРИЧИНА АНОМАЛЬНЫХ СВОЙСТВ ВОДЫ – НАЛИЧИЕ ВОДОРОДНЫХ СВЯЗЕЙ.
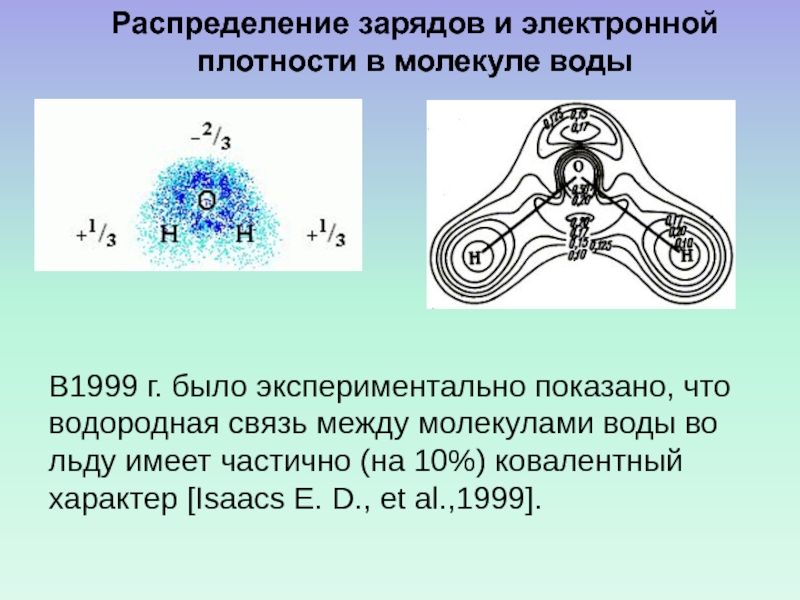
Слайд 43
Распределение зарядов и электронной плотности в молекуле воды
В1999 г.
было экспериментально показано, что водородная связь между молекулами воды во
льду имеет частично (на 10%) ковалентный характер [Isaacs E. D., et al.,1999].Слайд 48Четыре связи каждой молекулы Н2О локально организованы в тетраэдрическую структуру,
т.е. четыре близлежащие молекулы располагаются в вершинах трехгранной пирамиды, в
центре которой находится пятая молекула воды.Слайд 49ТЕОРИИ СТРУКТУРЫ ВОДЫ
Впервые идея о том, что вода имеет сложную
структуру появилась в конце XIX века.
20-е годы XX века: установлена
структура льда.30-е годы XX века: предположение, что подобная трехмерная сетка присутствует и в жидкой воде.
1951 г: Дж. ПОПЛ создает модель непрерывной структуры воды (континуальная модель).
2-я половина XX века: 2 группы «смешанных» моделей – кластерная и клатратная.
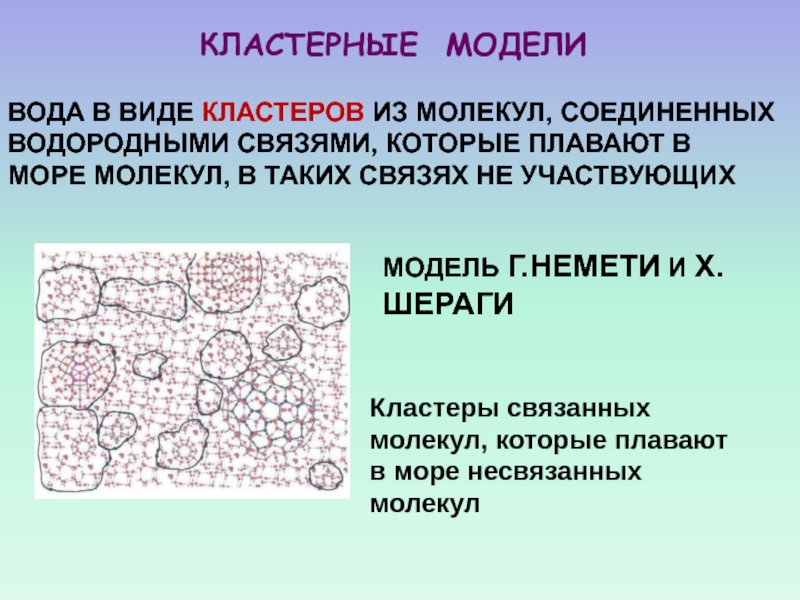
Слайд 51КЛАСТЕРНЫЕ МОДЕЛИ
ВОДА В ВИДЕ КЛАСТЕРОВ ИЗ МОЛЕКУЛ, СОЕДИНЕННЫХ ВОДОРОДНЫМИ СВЯЗЯМИ,
КОТОРЫЕ ПЛАВАЮТ В МОРЕ МОЛЕКУЛ, В ТАКИХ СВЯЗЯХ НЕ УЧАСТВУЮЩИХ
МОДЕЛЬ
Г.НЕМЕТИ И Х. ШЕРАГИКластеры связанных молекул, которые плавают в море несвязанных молекул
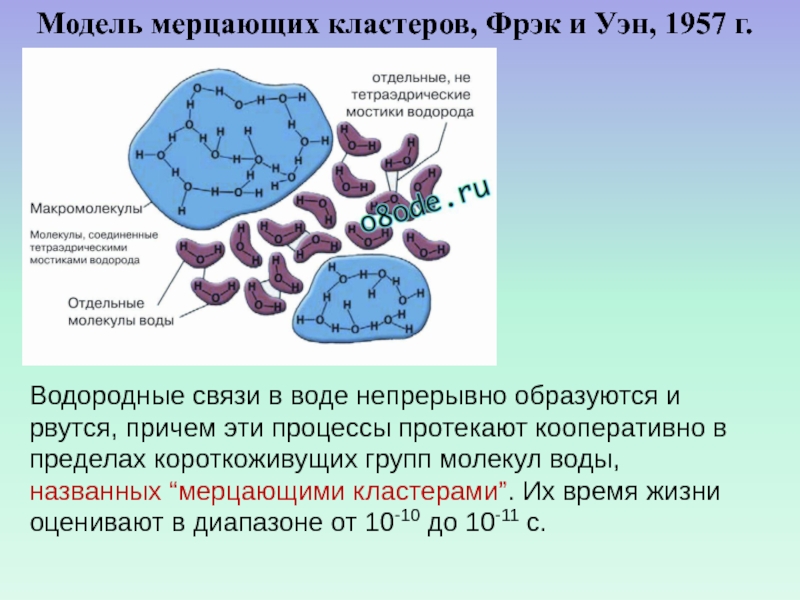
Слайд 52Модель мерцающих кластеров, Фрэк и Уэн, 1957 г.
Водородные связи
в воде непрерывно образуются и рвутся, причем эти процессы протекают
кооперативно в пределах короткоживущих групп молекул воды, названных “мерцающими кластерами”. Их время жизни оценивают в диапазоне от 10-10 до 10-11 с.Слайд 53КЛАТРАТНАЯ МОДЕЛЬ ВОДЫ
ВОДА ОБРАЗУЕТ НЕПРЕРЫВНУЮ СЕТКУ (КАРКАС) БЛАГОДАРЯ ВОДОРОДНЫМ СВЯЗЯМ,
НО СОДЕРЖИТ ПУСТОТЫ. В НИХ РАЗМЕЩАЮТСЯ МОЛЕКУЛЫ ВОДЫ, НЕ ОБРАЗУЮЩИЕ
СВЯЗЕЙ С МОЛЕКУЛАМИ КАРКАСА.АВТОРЫ ПЕРВЫХ ТЕОРИЙ – О.Я.САМОЙЛОВ, Л. ПОЛИНГ
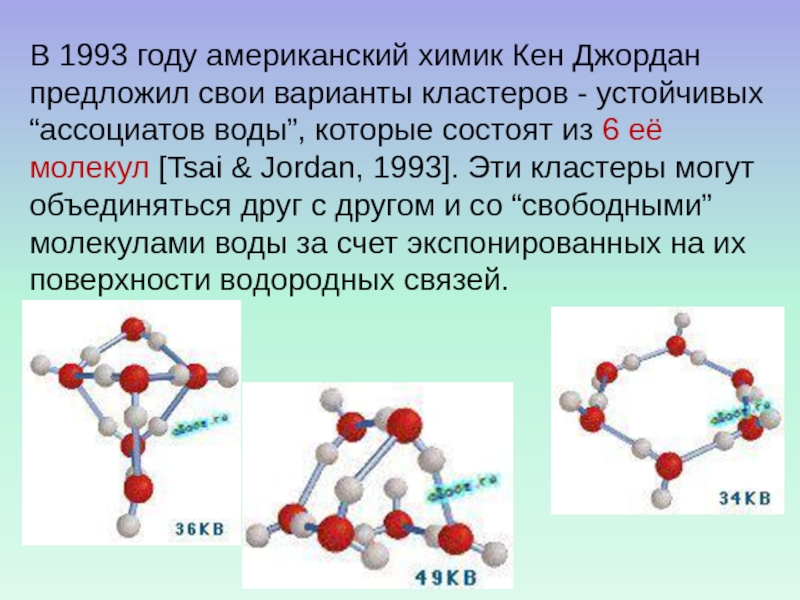
Слайд 54В 1993 году американский химик Кен Джордан предложил свои варианты
кластеров - устойчивых “ассоциатов воды”, которые состоят из 6 её
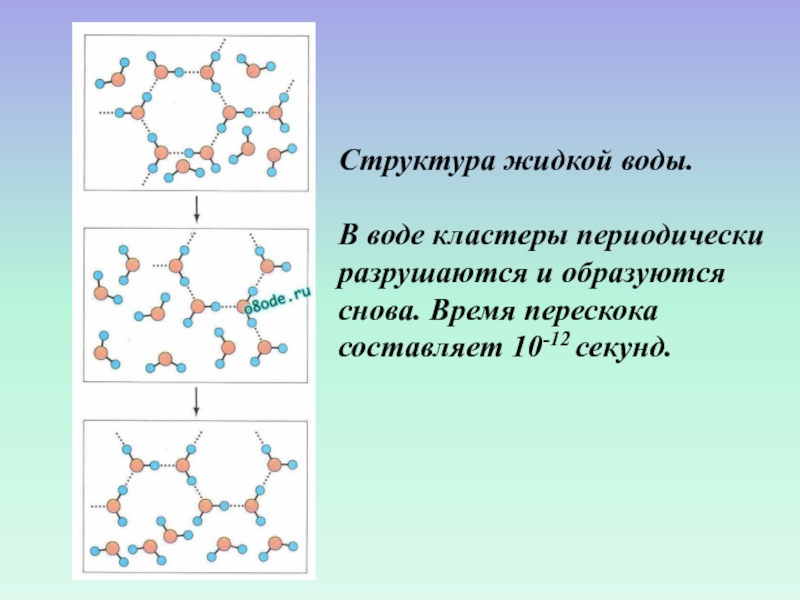
молекул [Tsai & Jordan, 1993]. Эти кластеры могут объединяться друг с другом и со “свободными” молекулами воды за счет экспонированных на их поверхности водородных связей.Слайд 55Структура жидкой воды.
В воде кластеры периодически разрушаются и образуются
снова. Время перескока составляет 10-12 секунд.
Слайд 60ЭНТРОПИЙНАЯ ПРИРОДА ГИДРОФОБНЫХ ВЗАИМОДЕЙСТВИЙ
СНИЖЕНИЕ ЭНТРОПИИ ВЫЗЫВАЕТ УВЕЛИЧЕНИЕ СВОБОДНОЙ ЭНЕРГИИ, НО
ЭТО КОМПЕНСИРУЕТСЯ СНИЖЕНИЕМ ЭНТАЛЬПИИ
Слайд 62
Термодинамика переноса типичной неполярной молекулы, циклогексана (СН2)6, из пара (вверху)
в воду (справа), а также в жидкий циклогексан (слева), и
из него в воду. Цифры примерно соответствуют процессам при 25оС (т.е. при Т 300оК; при этом RT 0.6 ккал/моль).