Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
2.1.1 Температура и ее измерение. 2.1.2 Абсолютный нуль температуры и
Содержание
- 1. 2.1.1 Температура и ее измерение. 2.1.2 Абсолютный нуль температуры и
- 2. Величины, характеризующие состояние макроскопических тел без учета
- 3. Распространённые в быту термометры – ртутные, спиртовые
- 4. По шкале Цельсия, при градуировке термометра берется
- 5. Поэтому для работы с физическими величинами необходима
- 6. Обозначение температуры: ТЕдиница измерения: К, «кельвин»Перевод к
- 7. Температура является мерой средней кинетической энергией поступательного движения.
- 8. Слайд 8
- 9. Слайд 9
- 10. Слайд 10
- 11. Слайд 11
- 12. Количественные зависимости между двумя параметрами газа называю
- 13. Изотермический процесс – процесс перехода идеального газа из
- 14. При увеличении объёма наблюдается уменьшение давления, и
- 15. Слайд 15
- 16. При увеличении температуры наблюдается увеличение объёма, и
- 17. Слайд 17
- 18. При увеличении температуры наблюдается увеличение давления, и
- 19. Слайд 19
- 20. Скачать презентанцию
Величины, характеризующие состояние макроскопических тел без учета их молекулярного строения (V, p, t), называют макроскопическими параметрами.Тепловое равновесие – такое состояние тела, при котором его макроскопические параметры не меняются длительное время.Температура – мера теплового
Слайды и текст этой презентации
Слайд 12.1.1 Температура и ее измерение.
2.1.2 Абсолютный нуль температуры и
термодинамическая шкала.
Слайд 2Величины, характеризующие состояние макроскопических тел без учета их молекулярного строения
(V, p, t), называют макроскопическими параметрами.
Тепловое равновесие – такое состояние тела,
при котором его макроскопические параметры не меняются длительное время.Температура – мера теплового равновесия тела или системы тел. И сведения о температурах двух тел дают нам представление о направлении перехода тепла – от более нагретого тела к менее нагретому.
Слайд 3Распространённые в быту термометры – ртутные, спиртовые и т.д. – не
отвечают физическим стандартам измерения температур.
Причины:
Различные термометры используют различные вещества в
качестве индикатора, поэтому на одно и то же изменение температуры в зависимости от свойств конкретного вещества термометры реагируют по-разному;Произвольность выбора начала отсчёта шкалы температур.
Слайд 4По шкале Цельсия, при градуировке термометра берется за 0 температура
тающего льда, а за 100 - температуру кипения воды и
затем делят шкалу на 100 равных частей, называемых градусами.Т.к различные жидкости расширяются при нагревании не одинаково, то и градусы спиртового и ртутного термометров будут отличаться.
Слайд 5Поэтому для работы с физическими величинами необходима абсолютная шкала.
Эту шкалу
ввёл в 1848 г английский физик лорд Кельвин. Зная, что
при росте температур скорость движения молекул и атомов тоже растёт, нетрудно установить, что при уменьшении температур скорость будет падать и при определённой температуре рано или поздно станет нулём, как и давление (исходя и основного уравнения МКТ). Эту температуру и выбрали за начало отсчёта. Температура не может достигнуть значения меньше этого значения, поэтому оно получило название «абсолютный ноль температур».Слайд 6Обозначение температуры: Т
Единица измерения: К, «кельвин»
Перевод к шкале Кельвина: 1К=
1⸰С+273
Абсолютный ноль температур – это температура Т=0К=-273 ⸰С
Слайд 12Количественные зависимости между двумя параметрами газа называю газовыми законами.
Процессы, протекающие
при неизменном значении одного из параметров, называют изопроцессами.
Изопроцесс – идеализированная
модель реального процесса, которая только приближенно отражает действительность. Слайд 13Изотермический процесс – процесс перехода идеального газа из одного состояния в
другое без изменения температуры. Закон, описывающий связь меду параметрами газа
при таком процессе, называется закон Бойля-Мариотта в честь двух учёных, практически одновременно выведших его: англичанина Роберта Бойля и француза Эдма Мариотта.PV=const при T=const
Для газа данной массы при постоянной температуре произведение давления на его объём постоянно.
Слайд 14При увеличении объёма наблюдается уменьшение давления, и наоборот.
График зависимости
давления газа от объёма при постоянной температуре называется изотермой.
Изотерма газа
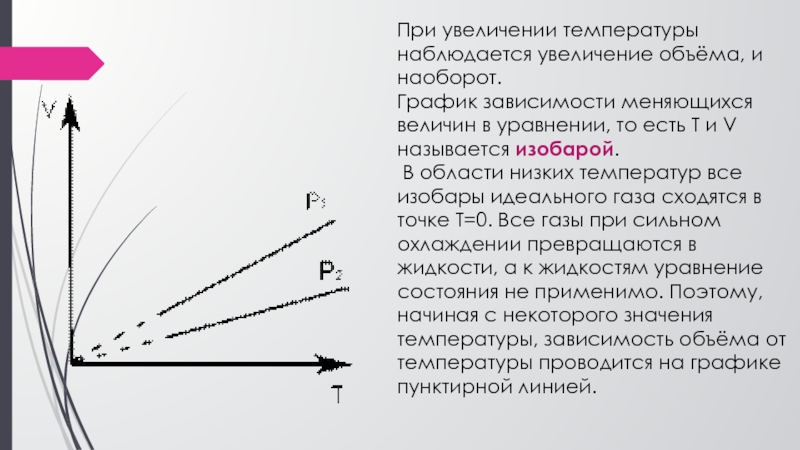
изображает обратно пропорциональную зависимость между давлением и объёмом.Слайд 16При увеличении температуры наблюдается увеличение объёма, и наоборот.
График зависимости
меняющихся величин в уравнении, то есть T и V называется
изобарой.В области низких температур все изобары идеального газа сходятся в точке Т=0. Все газы при сильном охлаждении превращаются в жидкости, а к жидкостям уравнение состояния не применимо. Поэтому, начиная с некоторого значения температуры, зависимость объёма от температуры проводится на графике пунктирной линией.
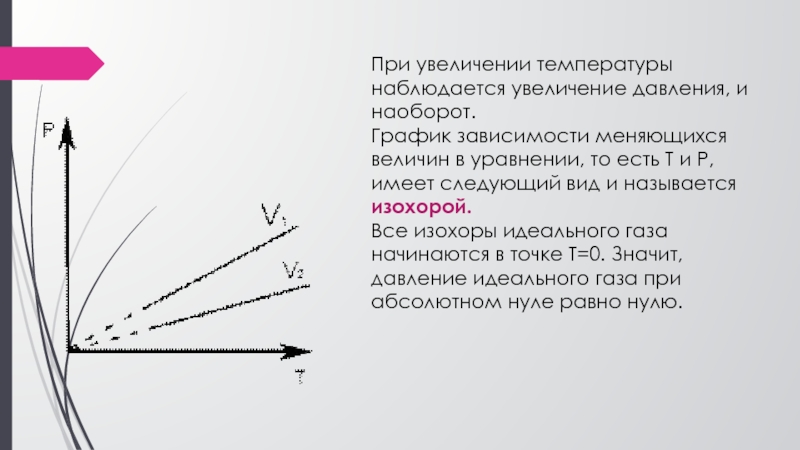
Слайд 18При увеличении температуры наблюдается увеличение давления, и наоборот.
График зависимости меняющихся
величин в уравнении, то есть T и P, имеет следующий
вид и называется изохорой.Все изохоры идеального газа начинаются в точке Т=0. Значит, давление идеального газа при абсолютном нуле равно нулю.