может являться не только следствием стремления системы к минимуму энергии.
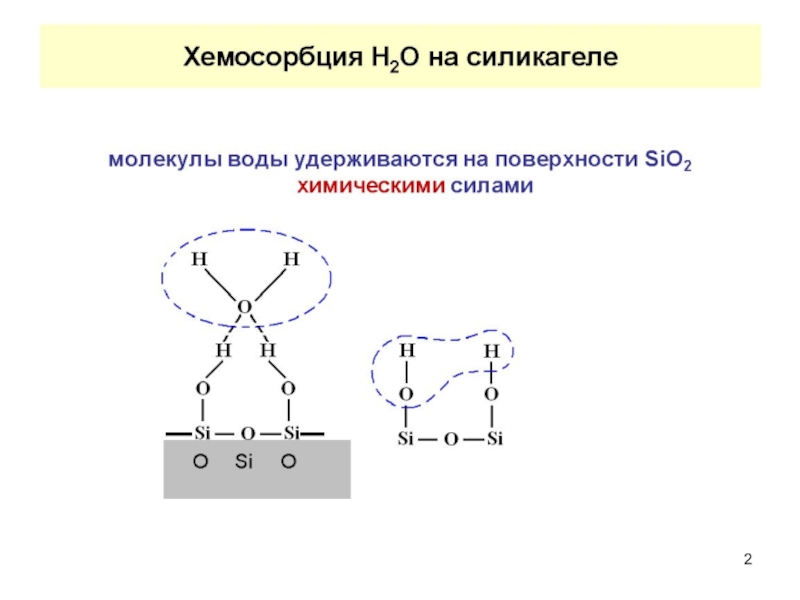
Он также может быть результатом взаимодействия компонентов раствора и поверхностного слоя. Это явление называется химической адсорбцией или хемосорбцией.Не всегда можно провести четкую грань между физической и химической адсорбцией. Физическая адсорбция, как правило, предшествует химической. Обычно переход от физической адсорбции к химической происходит при повышении температуры. Однако этот переход к хемосорбции наблюдается не всегда.
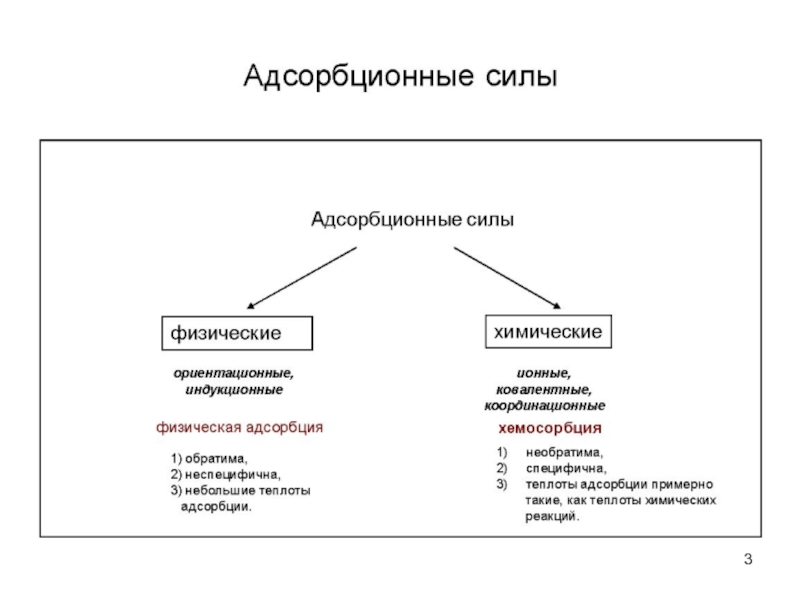
Можно выделить несколько основных критериев различия физической и химической адсорбции:
1) величина химической адсорбции, как правило, выше физической;
2) физическая адсорбция всегда обратима, а хемосорбция необратима, хотя имеются случаи обратимости химической адсорбции;
3) теплота химической адсорбции примерно на порядок выше, чем физической и достигает
400 кДж/моль, в то время как теплота физической адсорбции всего 10–40 кДж/моль;
4) для физической адсорбции не нужна энергия активации, а для химической она необходима, хотя имеются и исключения; если перед адсорбцией молекуле необходима переориентация, то для этого процесса нужна энергия активации, и она может сопровождать физическую адсорбцию;
5) при физической адсорбции молекулы сохраняют свою индивидуальность, а при хемосорбции часто имеет место перенос заряда от адсорбата к адсорбенту с образованием поверхностного соединения.
Мы будем рассматривать только физическую адсорбцию.