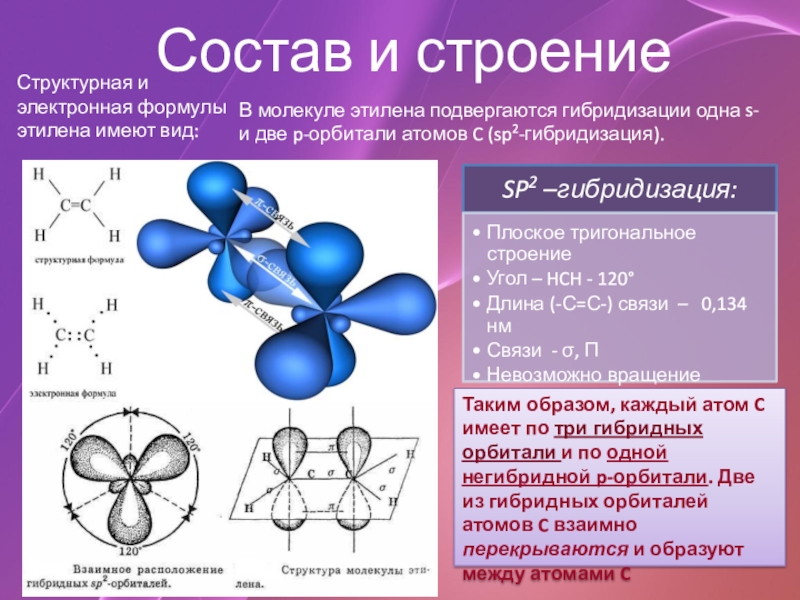
CnH2n.
Впервые этилен был получен в 1669 году немецким химиком и врачом Бехером действием серной кислоты на этиловый
спирт. Ученый установил, что его «воздух» более химически активен, чем метан, однако, идентифицировать полученный газ он не смог и названия ему не присвоил.Александр Михайлович Бутлеров
Иоганн Иоахим Бехер
Жан-Батист Андре Дюма
Ю́стус фон Ли́бих
Йёнс Якоб Берце́лиус