Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Алюміній
Содержание
- 1. Алюміній
- 2. Найпоширеніший серед металів 6,6 ат. %
- 3. Добування 3Na2CO3 + 2Al(OH)3 + 12HF
- 4. К(-) Al3+ + 3e → Al
- 5. Слайд 5
- 6. 1-катод; 2-розплавленний алюміній; 3-теплова ізоляція;
- 7. Сріблясто-білий, легкий, досить твердий метал. Пластичний, характеризується
- 8. 3s23p13d00Al+1AlГAl2Oсполуки не утворюються за звичайних умов лише за t понад 10000С+3AlCl3Al2O3Al(OH)3
- 9. За нагрівання Al реагує з усіма неметалами,
- 10. 2Al + 6H+ → 2Al3+ + 3H2↑2Al
- 11. 2Al + 4H2SO4(конц.) → Al2(SO4)3 + S
- 12. AlH3 + 3H2O → Al(OH)3 + 3H2↑AlH3
- 13. 4Al + 3O2 → 2Al2O3Al2O3 (глинозем) –
- 14. α – Al2O3 хімічно інертний Не розчиняється
- 15. Υ -Al2O3 не розчиняється у воді, але
- 16. Al2(SO4)3 + 6NaOH → 2Al(OH)3↓ + Na2SO4Al3+
- 17. [Al(H2O)6]3+ ⇄ [Al (OH)3(H2O)3] ⇄ [Al(OH)6]3-Кислотні й
- 18. Al2(SO4)3 + 3Na2CO3 + 3H2O →
- 19. Al2(SO4)3 + 6NH4OH → 2AlO(OH)↓ +
- 20. Слайд 20
- 21. Гідроліз Al2(SO4)3 Al3+ + H2O →
- 22. [Al(H2O)6]3+ + H2O ⇆ [AlOH(H2O)5]2+ + H3O+
- 23. [Al(H2O)6]3+ + H2O⇆ [AlOH(H2O)5]2+ +
- 24. З галогенами Al взаємодіє дуже бурхливо з
- 25. Al2O3 + 3C + 3Cl2 → 2AlCl3↑
- 26. Слайд 26
- 27. Слайд 27
- 28. Сполуки з іншими неметалами2NH3 + 2Al →
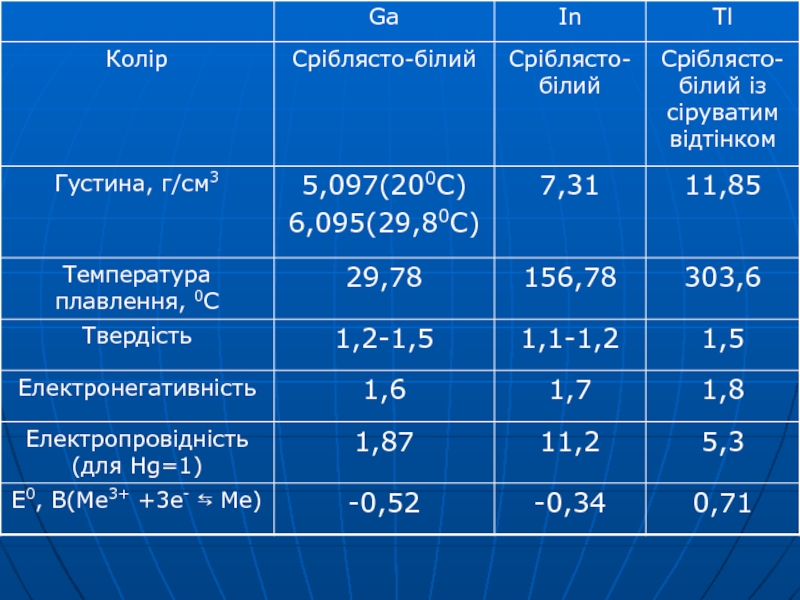
- 29. Ga In Tl
- 30. Слайд 30
- 31. Хімічні властивостіНа повітрі Ga та In зберігають
- 32. In + 6HNO3 → In(NO3)3 + 3NO2
- 33. За нагрівання усі три метали бурхливо взаємодіють
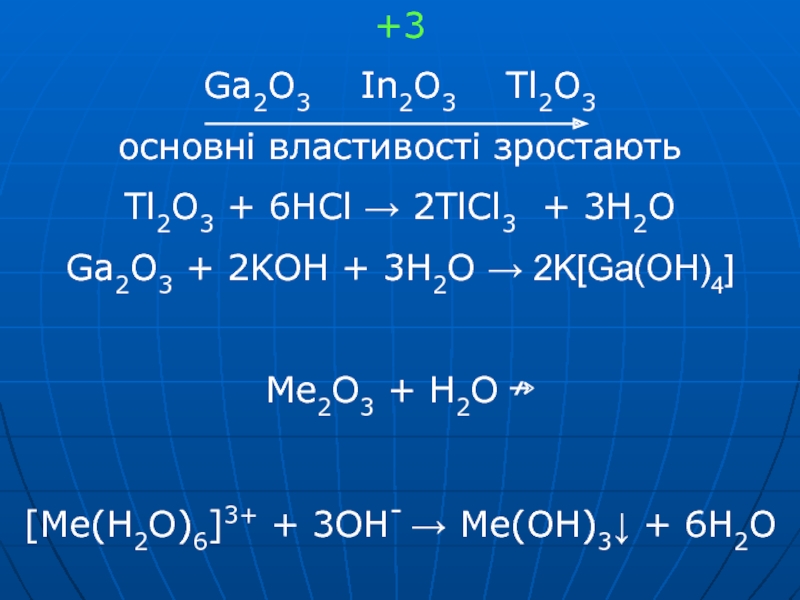
- 34. +3Ga2O3 In2O3 Tl2O3основні властивості зростаютьTl2O3
- 35. Tl2SO4 + 2NaOH + 2H2O2 → 2Tl(OH)3↓
- 36. Сполуки з гідрогеном4LiH + MeCl3 → Li[MeH4]
- 37. +1Ga In
- 38. 2TlOH + CO2 → Tl2CO3 + H2OTl2CO3
- 39. ЗастосуванняСеред металів Al посідає друге місце після
- 40. Al застосовують в алюмотермії для добування металів
- 41. Слайд 41
- 42. Серед сполук алюмінію найширше використовують сульфат алюмінію:
- 43. α – Al2O3 у вигляді корунду використовують
- 44. Ga, In і Tl поки що не
- 45. Індій – для створення антикорозійних покритьСполуки InSb,
- 46. Скачать презентанцию
Слайды и текст этой презентации
Слайд 2Найпоширеніший серед металів 6,6 ат. % 250 мінералів Al2O3·2SiO2·2H2O Al2O3 – корунд (рубін, сапфір) Na2O(K2O)·Al2O3·2SiO2 –
нефелін
Al2O3·xH2O – боксит
Na3[AlF6] – кріоліт (поклади вже вичерпані)
Слайд 3Добування 3Na2CO3 + 2Al(OH)3 + 12HF → 2Na3[AlF6] + 3CO2 +
9H2O Al2O3 tпл = 20450С Al2O3 + Na3[AlF6]
tпл = 6600С tпроцесу ~ 9600С Al2O3 → Al + AlO33-
t
3+
Слайд 4К(-) Al3+ + 3e → Al A(+) 4AlO3 – 12e → 2Al2O3
+ 3O2 K(-) та А(+) графітові С + О2 → суміш СО2
+ СО При добуванні 1 т алюмінію згоряє 0,7 т графіту Обсяги виробництва Fe – l Al - ll3-
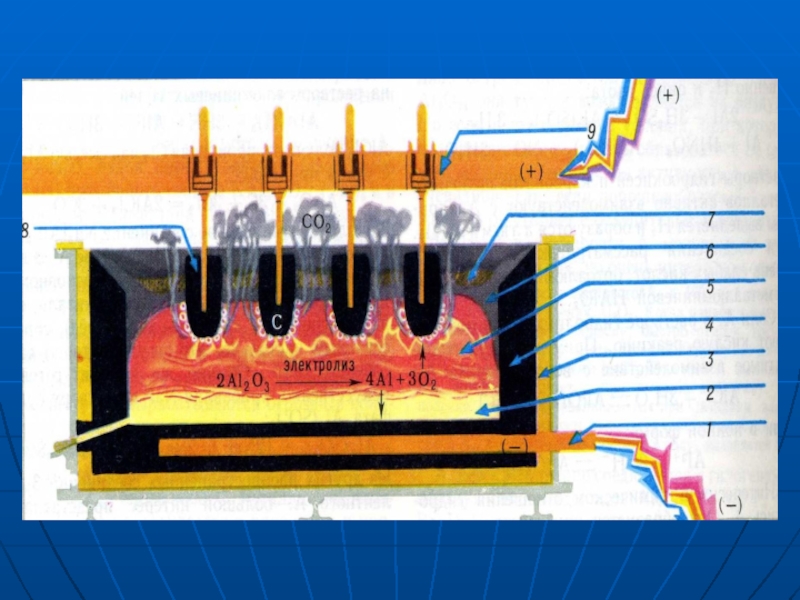
Слайд 61-катод; 2-розплавленний алюміній;
3-теплова ізоляція; 4-вугільна
обкладка;
5-розплавлений електроліт;
7-шар Al2O3; 8-вугільні аноди.
Електроліт для
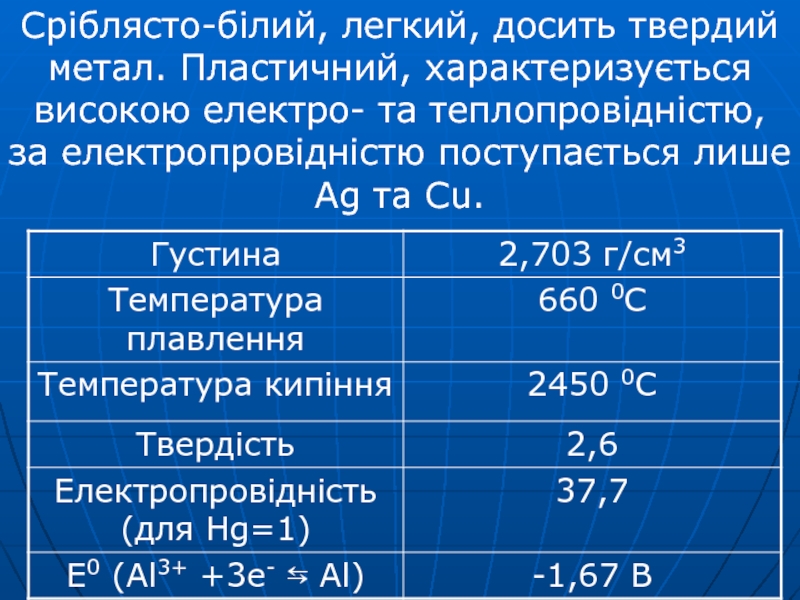
добування алюмінію складається з розплаву кріоліту Na3[AlF6] і оксиду алюмінію Al2O3. Електроди виготовляють з нафтового коксу, який складається майже з чистого вуглецю. Блоки з коксу, які вкривають дно і стінки ванни, відіграють роль катода. Аноди закріплюються на підвісній рамі і автоматично опускаються в залежності від того, як згоряють. Рідкий алюміній збирається на дні ванни, з якої його періодично випускають через похилий канал, який закривається глиняною пробкою. Процес іде безперервно.Слайд 7Сріблясто-білий, легкий, досить твердий метал. Пластичний, характеризується високою електро- та
теплопровідністю, за електропровідністю поступається лише Ag та Cu.
Слайд 83s23p13d0
0
Al
+1
AlГ
Al2O
сполуки не утворюються за звичайних умов лише за t понад
10000С
+3
AlCl3
Al2O3
Al(OH)3
Слайд 9За нагрівання Al реагує з усіма неметалами, крім водню
2Al +
3Г2 → 2AlГ3 (Г – F, Cl, Br, I)
4Al
+ 3O2 → 2Al2O3Поверхнева оксидна плівка легко руйнується ртутю
2Al + 3HgCl2 → 2AlCl3 + 3Hg
xAl + yHg → AlxHgy
2Al + 6H2O → 2Al(OH)3↓ + 3H2↑
Слайд 102Al + 6H+ → 2Al3+ + 3H2↑
2Al + 12OH- +
3H2O → 2[Al(OH)6]3- + 3H2↑
8Al + 30HNO3(розв.) →
→ 8Al(NO3)3 + 3N2O +15H2OAl + 6HNO3(конц.) → Al(NO3)3 + 3NO2 +
+ 3H2O
(N2 , NH4NO3)
Слайд 112Al + 4H2SO4(конц.) → Al2(SO4)3 + S + 4H2O
8Al +
3Fe3O4 → 9Fe + 4Al2O3
Al + H2 ↛
AlCl3 + 3LiH
→ AlH3 + 3LiCl2AlH3 → 2Al + 3H2
t
біла аморфна речовина складу (AlH3)x
>100 0C
Слайд 12AlH3 + 3H2O → Al(OH)3 + 3H2↑
AlH3 реагує з гідридами
лужних металів (за рахунок вакнтної р-орбіталі на валентному підрівні), утворюючи
комплексні тетрагідриди Ме[AlH4] (Me – Li, Na, K), які легко руйнуються водою і є сильними відновникамиLi[AlH4] + 4H2O → LiOH + Al(OH)3 +4H2↑
3LiAlH4 + 4CO2 + 8H2O → 4CH3OH + 3Al(OH)3 + 3LiOH
Слайд 134Al + 3O2 → 2Al2O3
Al2O3 (глинозем) – біла тугоплавка не
розчинна у воді речовина
Відомі дві кристалічні форми
α – Al2O3
і Υ -Al2O3Al(OH)3 → Υ -Al2O3 → α – Al2O3
α – Al2O3 у природі зустрічається у вигляді мінералу корунду
450-600 0C
- H2O
> 950 0C
Слайд 14α – Al2O3 хімічно інертний
Не розчиняється у воді, розчинах
кислот і лугів
Перевести α – Al2O3 у розчинний стан
можна сплавлянням з піросульфатом Na2S2O7, содою або лугамиAl2O3 + 3Na2S2O7 → Al2(SO4)3 + 3Na2SO4
Al2O3 + Na2CO3 → 2NaAlO2 + CO2
Al2O3 + 2NaOH → 2NaAlO2 + H2O
Na2SO4·SO3
t
t
t
Слайд 15Υ -Al2O3 не розчиняється у воді, але розчиняється у розчинах
кислот та лугів
Al2O3 + 6NaOH + 3H2O → 2Na3[Al(OH)6]
Al2O3 +
6HCl + 3H2O → 2[Al(H2O)6]Cl3Слайд 16Al2(SO4)3 + 6NaOH → 2Al(OH)3↓ + Na2SO4
Al3+ + 3OH- →
Al(OH)3↓
Al(OH)3 – амфотерна сполука
Al(OH)3 + 3Н+ + 3H2O
→ [Al(H2O)6]3+Al(OH)3 + 3OH- → [Al(OH)6]3-
Слайд 17
[Al(H2O)6]3+ ⇄ [Al (OH)3(H2O)3] ⇄ [Al(OH)6]3-
Кислотні й основні властивості Al(OH)3
виражені слабко:
HAlO2 ⇆ H+ + AlO2
K = 4·10-13Al(OH)3 ⇆ Al3+ + 3OH- K = 1·10-9
[Al(OH)3]·3H2O
3OH-
3H3O+
3OH-
3H3O+
-
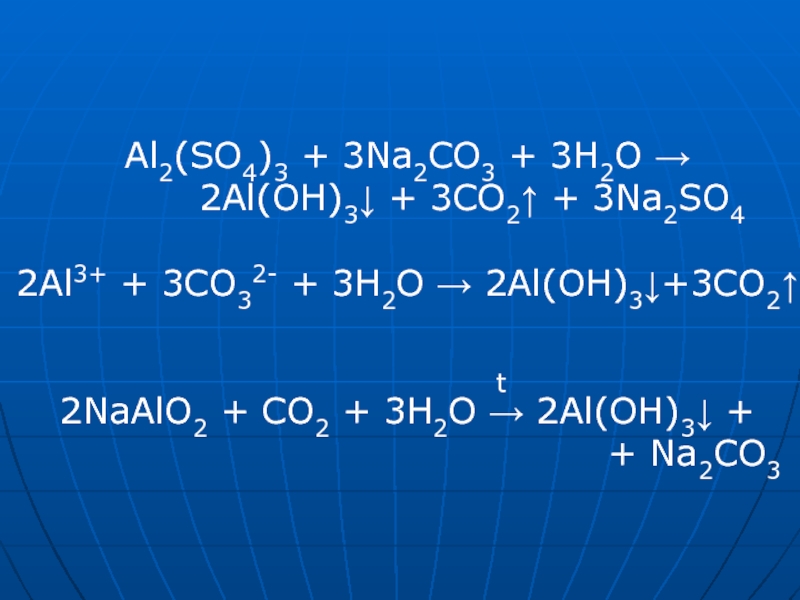
Слайд 18Al2(SO4)3 + 3Na2CO3 + 3H2O → 2Al(OH)3↓ +
3CO2↑ + 3Na2SO4 2Al3+ + 3CO32- + 3H2O → 2Al(OH)3↓+3CO2↑ 2NaAlO2
+ CO2 + 3H2O → 2Al(OH)3↓ + + Na2CO3t
Слайд 19Al2(SO4)3 + 6NH4OH → 2AlO(OH)↓ +
+ 3(NH4)2SO4 + 2H2O
“старіння”
[Al(OH)3]n → [AlO(OH)]n + nH2O
[AlO(OH)]n → 0,5nAl2O3 + 0,5nH2O
Слайд 23[Al(H2O)6]3+ + H2O⇆ [AlOH(H2O)5]2+ +
H3O+
K = 1·10-5
[AlOH(H2O)5]2+ + H2O ⇆ [Al(OH)2(H2O)4]+
+ H3O+
[Al(OH)2(H2O)4]+ + H2O ⇆ [Al(OH)3(H2O)3]
+ H3O+
Слайд 24З галогенами Al взаємодіє дуже бурхливо з утворенням галогенідів AlГ3
2Al
+ 3Г2 → 2AlГ3 (Г – F, Cl, Br, I)
AlF3
не розчинний у воді і має високу температуру плавлення (1040 0С) AlF3 + 3NaF → Na3[AlF6]
t
Слайд 25Al2O3 + 3C + 3Cl2 → 2AlCl3↑ + 3CO↑
AlCl3 +
3H2O → Al(OH)3 + 3HCl
AlCl3·6H2O → Al(OH)3 + 3H2O +
3HCl↑t
Слайд 28Сполуки з іншими неметалами
2NH3 + 2Al → 2AlN + 3H2↑
AlN
+ 3H2O → Al(OH)3 + NH3↑
Al2S3 + 6H2O → 2Al(OH)3
+ 3H2S↑Al4C3 + 12H2O → 4Al(OH)3 + 3CH4↑
Слайд 31Хімічні властивості
На повітрі Ga та In зберігають блиск, а Tl
на свіжому розрізі тьмяніє
Ga та In по відношенню до води
стійкі, а Tl за наявості повітря поступово нею руйнуєтьсяGa та In пасивуються нітратною кислотою
3Tl + 4HNO3 → 3TlNO3 + NO + 2H2O
Слайд 32In + 6HNO3 → In(NO3)3 + 3NO2 + 3H2O
2Ga +
3H2SO4 → Ga2(SO4)3 + 3H2↑
2Ga + 2NaOH + 6H2O →
2Na[Ga(OH)4] + 3H2↑t
Слайд 33За нагрівання усі три метали бурхливо взаємодіють з киснем
Me +
O2 → Me2O3
2Tl + 3/2O2(г.) → Tl2O3(т.)
2Tl + 1/2O2(г.)
→ Tl2O(т.)Tl2O3 → Tl2O + O2
Ga2O3
білий
In2O3
жовтий
Tl2O3
чорний
t
Слайд 34+3
Ga2O3 In2O3 Tl2O3
основні властивості зростають
Tl2O3 + 6HCl →
2TlCl3 + 3H2O
Ga2O3 + 2KOH + 3H2O → 2K[Ga(OH)4]
Me2O3 +
H2O ↛[Me(H2O)6]3+ + 3OH- → Me(OH)3↓ + 6H2O
Слайд 35Tl2SO4 + 2NaOH + 2H2O2 → 2Tl(OH)3↓ +
2Tl(OH)3 → Tl2O3 + 3H2O
Усі розчинні солі гідролізують
[Me(H2O)6]3+ + H2O ⇆ [Me(OH)(H2O)5]2+ +
+ H3O+
Слайд 37+1
Ga In
Tl
стійкість збільшується
Найхарактерніша для талію
4Tl + O2 → 2Tl2O
Гідрооксид Tl(I) –
жовта, кристалічна речовина, добре розчиняється у водіTl2O + H2O → 2TlOH
Слайд 38
2TlOH + CO2 → Tl2CO3 + H2O
Tl2CO3 + CO2 +
H2O → 2Tl(HCO3)
Більшість солей Tl(I) розчинні у воді і
нагадують солі лужних металів2TlOH → Tl2O + H2O
TlCl + KCl → K[TlCl2]
TlCl + 2KCl → K2[TlCl3]
t
Слайд 39Застосування
Серед металів Al посідає друге місце після заліза за обсягами
використання. Світове виробицтво алюмінію сягає багатьох мільйонів тонн
Металічний алюміній використовують
для виробництва широкого асортименту електричного дроту для заміни(в міру можливості) дорогої мідіСлайд 40Al застосовують в алюмотермії для добування металів і виготовлення фольги
для конденсаторів, у харчовій промисловості
Порошок алюмінію є основою алюмінієвої фарби
Сплави
алюмінію застосовують у ракетній техніці, авіа-, авто-, судно-, приладобудуванні, залізничному транспорті, хімічому апаратобудуванніСлайд 42Серед сполук алюмінію найширше використовують сульфат алюмінію: для проклеювання паперу,
“білого” дублення шкіри, протравлювання тканин перед фарбуванням, очищення води
3Ca(HCO3)2 +
Al2(SO4)3 → 2Al(OH)3 + + 3CaSO4 + 6CO2↑
Сорбент
Малорозчинна сіль
Слайд 43α – Al2O3 у вигляді корунду використовують як абразив, а
Υ -Al2O3 – як ефективний сорбент та каталізатор
Рубіни широко використовуються
у лазерній техніці, виробництві годинників, ювелірній справіСлайд 44
Ga, In і Tl поки що не знаходять широкого застосування
внаслідок їх малої доступності і великої вартоcті
Ga запропоновано використовувати у
високотемпературних термометрахВін може замінити ртуть у дифузійних вакуумних насосах
Галієві оптичні дзеркала мають велику відбивну здатність


![Алюміній Добування 3Na2CO3 + 2Al(OH)3 + 12HF → 2Na3[AlF6] + 3CO2 + Добування 3Na2CO3 + 2Al(OH)3 + 12HF → 2Na3[AlF6] + 3CO2 + 9H2O Al2O3](/img/thumbs/ae3fdb24cc0d7c176a98eeb731eb4ec3-800x.jpg)




![Алюміній 2Al + 6H+ → 2Al3+ + 3H2↑2Al + 12OH- + 3H2O 2Al + 6H+ → 2Al3+ + 3H2↑2Al + 12OH- + 3H2O → 2[Al(OH)6]3- + 3H2↑8Al + 30HNO3(розв.)](/img/thumbs/6c8d4ad71006c830122f1dd4a6c5ce52-800x.jpg)






![Алюміній [Al(H2O)6]3+ ⇄ [Al (OH)3(H2O)3] ⇄ [Al(OH)6]3-Кислотні й основні властивості Al(OH)3 виражені [Al(H2O)6]3+ ⇄ [Al (OH)3(H2O)3] ⇄ [Al(OH)6]3-Кислотні й основні властивості Al(OH)3 виражені слабко:HAlO2 ⇆ H+ + AlO2](/img/tmb/3/213648/7ef801486a79d4cbb45123c88da1280f-800x.jpg)


![Алюміній [Al(H2O)6]3+ + H2O ⇆ [AlOH(H2O)5]2+ + H3O+ [Al(H2O)6]3+ + H2O ⇆ [AlOH(H2O)5]2+ + H3O+](/img/thumbs/3d6f31d38de5137fa9000c3635a7dece-800x.jpg)
![Алюміній [Al(H2O)6]3+ + H2O⇆ [AlOH(H2O)5]2+ + [Al(H2O)6]3+ + H2O⇆ [AlOH(H2O)5]2+ +](/img/tmb/3/213648/21ec0524cad87f8e67406d340f605a19-800x.jpg)










![Алюміній Сполуки з гідрогеном4LiH + MeCl3 → Li[MeH4] + 3LiClGaH4 Сполуки з гідрогеном4LiH + MeCl3 → Li[MeH4] + 3LiClGaH4 InH4](/img/thumbs/48567416674935c2a4fb3256a4c91ba3-800x.jpg)




























