Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Аналитическая химия II. Инструментальные методы анализа Майстренко
Содержание
- 1. Аналитическая химия II. Инструментальные методы анализа Майстренко
- 2. Аналитическая химия – наука обопределении химического состававеществи
- 3. Инструментальные методы анализа — методы
- 4. Рекомендуемые учебники
- 5. ДефиницияАналитический сигналy = f(x)y"Контроль объекта аналитический. Термины
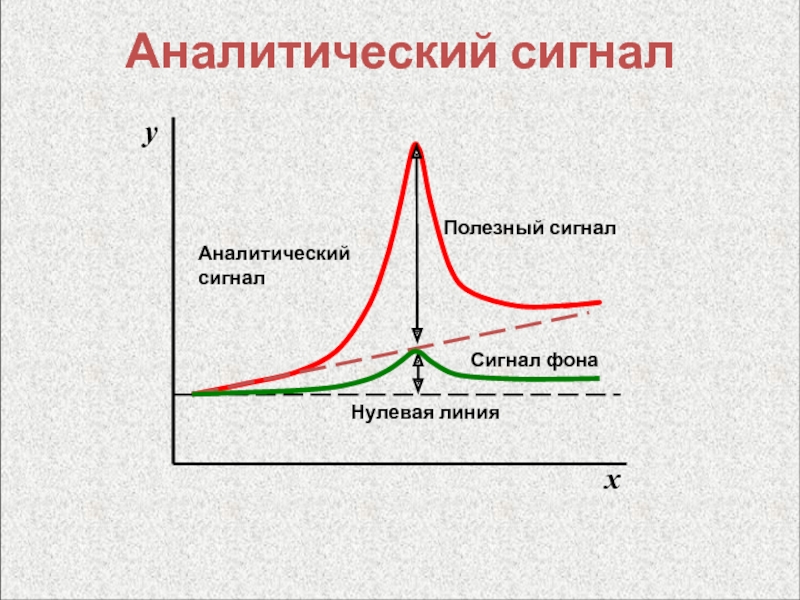
- 6. Аналитический сигналАналитическийсигналСигнал фонаПолезный сигналНулевая линияyx
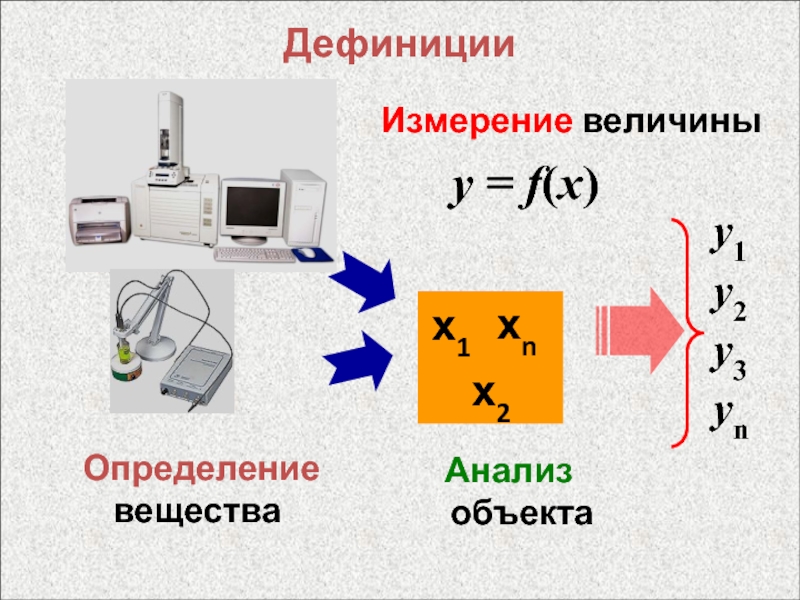
- 7. Дефиниции Измерение величиныОпределение веществаy = f(x) Анализ объектах1х2хny1y2y3yn
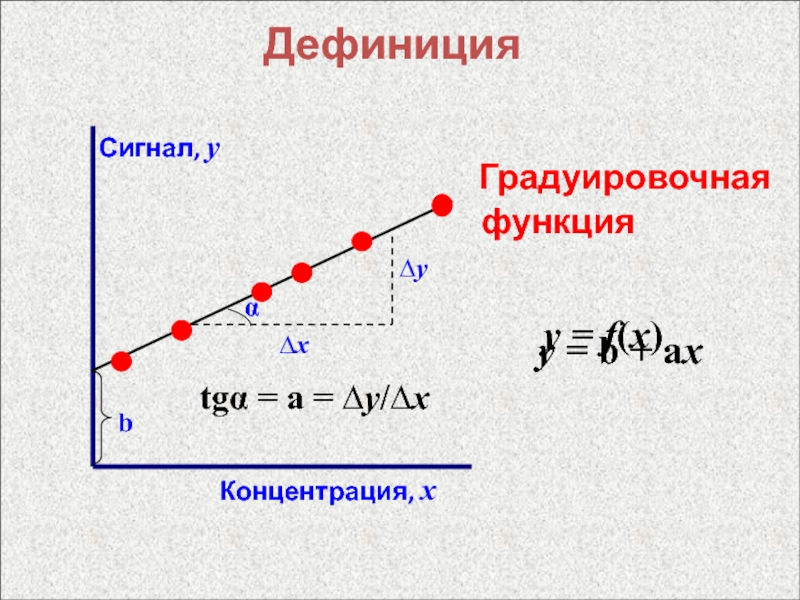
- 8. Градуировочная функция y = b + аx Дефиницияy = f(x)
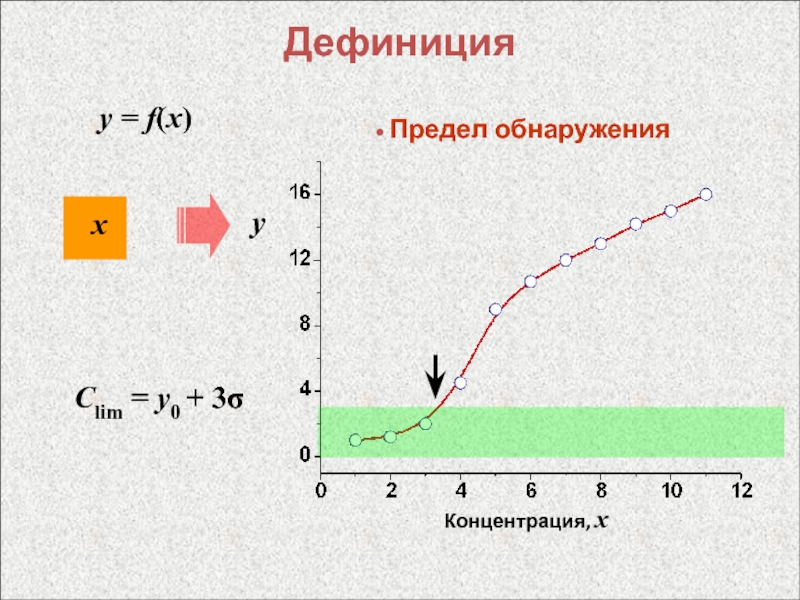
- 9. Дефиницияy = f(x)хy Предел обнаружения Сlim = y0 + 3σКонцентрация, x
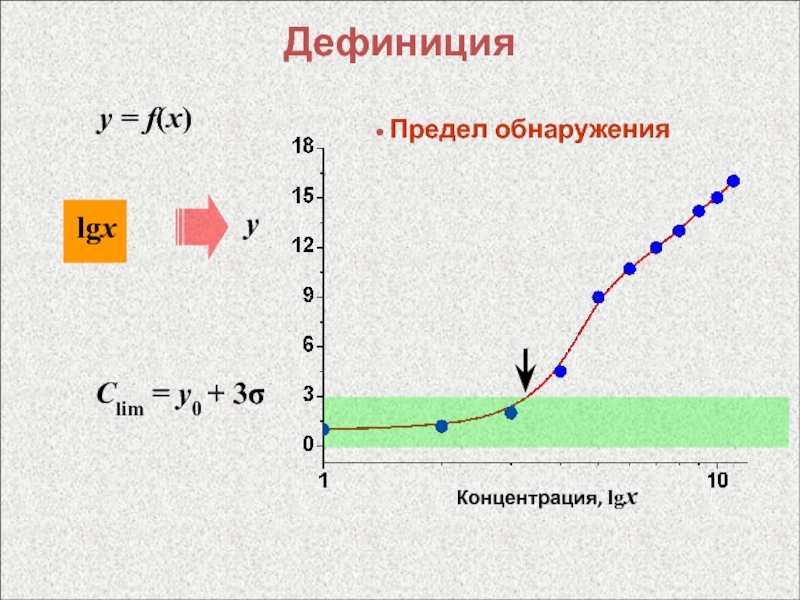
- 10. Дефиницияy = f(x)lgхy Предел обнаружения Сlim = y0 + 3σКонцентрация, lgx
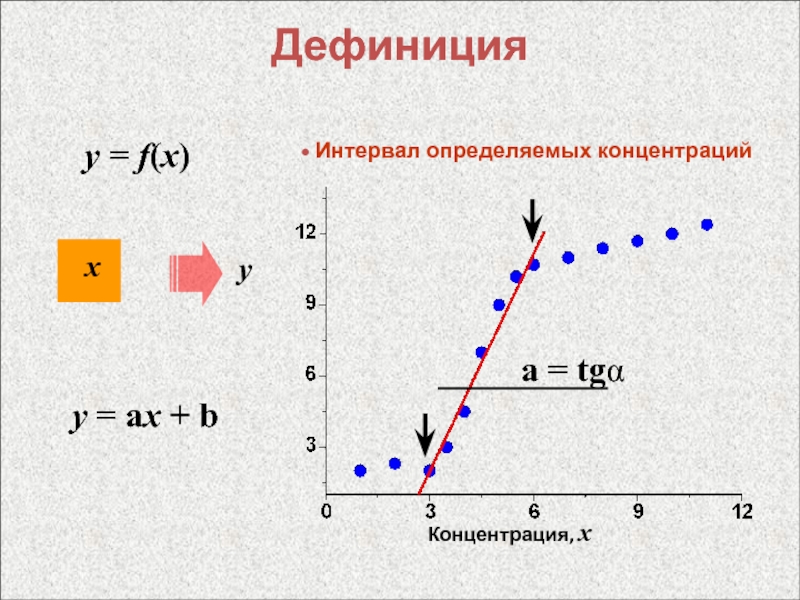
- 11. Дефиницияy = f(x)хy Интервал определяемых концентрацийy = ax + ba = tgαКонцентрация, x
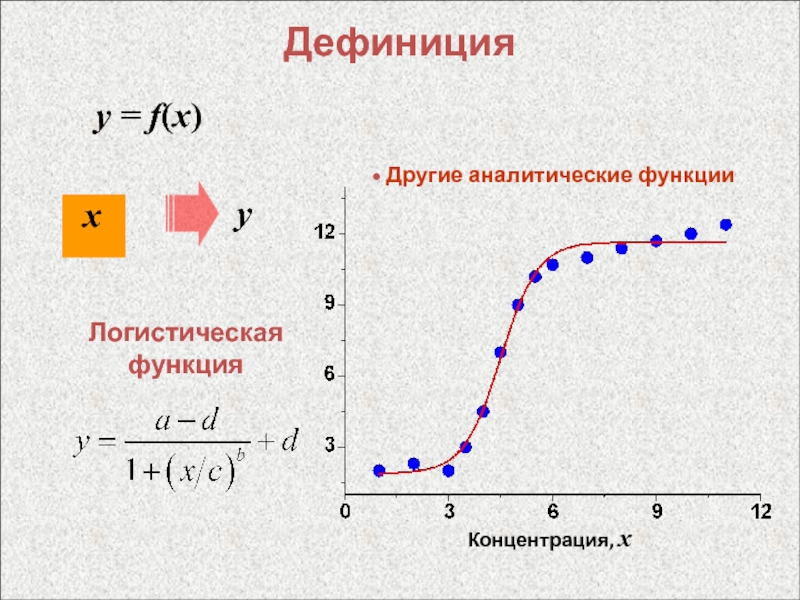
- 12. Дефиницияy = f(x)хy Другие аналитические функцииЛогистическая функцияКонцентрация, x
- 13. Метод и методика анализа"Контроль объекта аналитический. Термины
- 14. Методы аналитической химииМетоды отбора проб (пробоотбора)Методы разложения пробМетоды разделения компонентовМетоды концентрированияМетоды обнаружения (идентификации)Методы определения
- 15. Проба – или образец – предмет исследования
- 16. В зависимости от способа получения: разовая,
- 17. Абсолютные и относительные методы анализа Абсолютные
- 18. Одномерные и многомерные методы Одномерные методы
- 19. Классификация методов анализа по способу регистрации по способу измерения по объекту общая классификация
- 20. Классификация методов анализа Общая классификация качественный /
- 21. Классификация методов анализа По способу регистрации сигнала
- 22. Классификация методов анализа По способу регистрации сигнала
- 23. Классификация методов анализа По способу регистрации сигнала
- 24. Классификация методов анализа По способу регистрации сигнала
- 25. Спектроскопия Молекулярная Атомная ЯдернаяЭлектрохимические методы Вольтамперометрия
- 26. Слайд 26
- 27. По объекту анализаКлассификациях по агрегатному состоянию
- 28. Распределительный анализАнализ распределения элемента по поверхностиАнализ распределения
- 29. Критерии сравненияАналитические характеристикиМетрологические характеристикиТребования к пробоподготовкеОсобенности приборного оснащенияСпециальные требования, связанные с природой объекта контроляЭкономические характеристики
- 30. ЛитератураОсновы аналитической химии. Кн. 2. Методы химического
- 31. Инструментальные методы анализа:
- 32. В арсенале современной
- 33. Спектр солнечного света
- 34. История атомного спектрального
- 35. Окрашивание пламени горелки при внесении соли металла
- 36. Эксперимент Бунзена-Кирхгофа А – сигарный ящик, B
- 37. Историческая справкаКачественный и полу-количественный анализМетоды количест-венного анализаСередина
- 38. Атомы химических элементов
- 39. Сплошной спектрСпектр испускания (эмиссионный)Спектр поглощения (абсорбционный)
- 40. Слайд 40
- 41. Электрическая и магнитная составляющие электромагнитного излучения = с /
- 42. Спектральные линии характеризуют
- 43. Энергетические переходыЕ3Е2Е1Е0Возбужденные состоянияОсновное состояние
- 44. Спектр Совокупность спектральных линий, принадлежащих данной
- 45. Атомные спектрыЛайманБальмерПашенЕ0Е1Е2БрэкеттЕ3
- 46. Спектры атомов с
- 47. Спектральные термы Серия Лаймана n = 1
- 48. Эмиссионный спектр атома водородаУФvisИК
- 49. Спектральные термы многоэлектронных атомов Учет заряда ядра:
- 50. Слайд 50
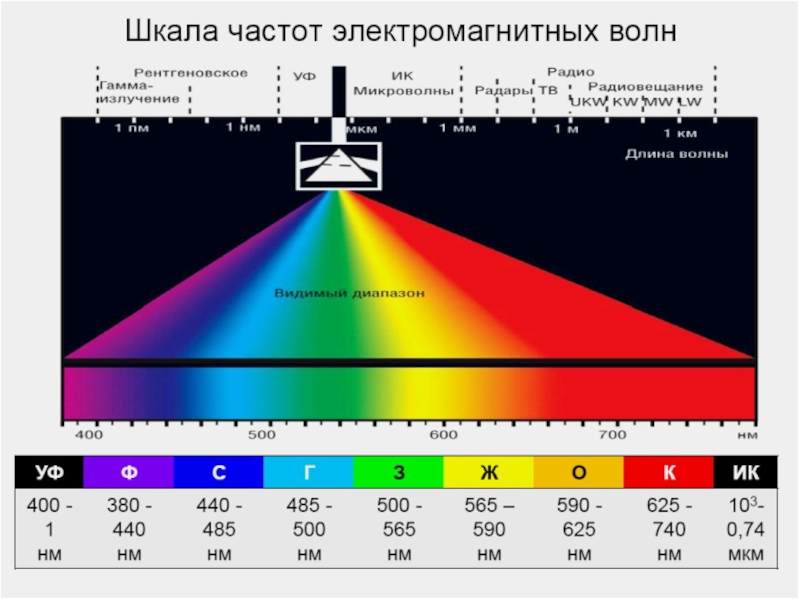
- 51. Длины волн электромагнитного излучения
- 52. Интенсивность спектральных линий Энергия, поглощаемая, излучаемая
- 53. Ширина спектральных линийестественная тепловое движение (допплеровское
- 54. МОЛЕКУЛЯРНЫЕ СПЕКТРЫ - спектры
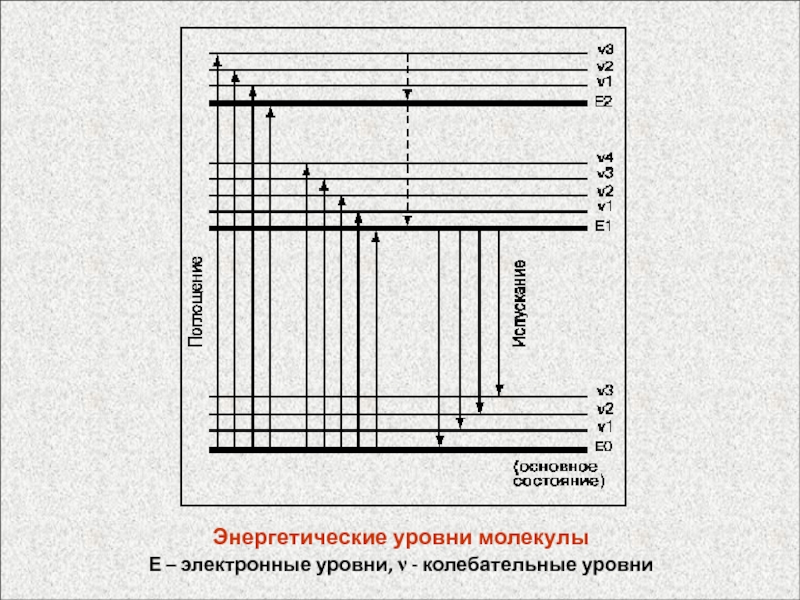
- 55. Энергетические уровни молекулыЕ – электронные уровни, - колебательные уровни
- 56. Молекулярные спектры веществ: а – гладкий контур,
- 57. Электронные спектры молекулЭлектронные спектры обусловлены переходами между
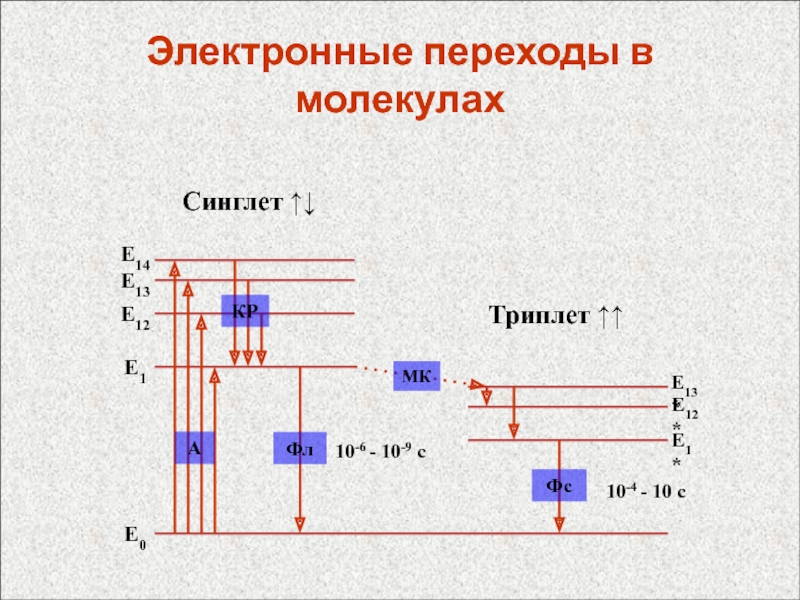
- 58. Электронные переходы в молекулах10-6 - 10-9 с10-4 - 10 cЕ1*Е12*Е13*
- 59. Природа электронных переходов или связывающиемолекулярныеорбиталиs или pатомныеорбитали* или * разрыхляющиемолекулярныеорбиталинесвязывающиеорбитали
- 60. УФ-спектры кодеина и норэфедринаКодеинНорэфедрин
- 61. Слайд 61
- 62. Энергетические уровни молекулыЕ – электронные уровни, v - колебательные уровни
- 63. Колебательные молекулярные спектры
- 64. Существуют два основных вида
- 65. Нормальные колебания молекулы водыN = 3n-6 =
- 66. Частота колебаний зависит от массы атомов (легче
- 67. Типичные частоты колебаний функциональных групп, см-1
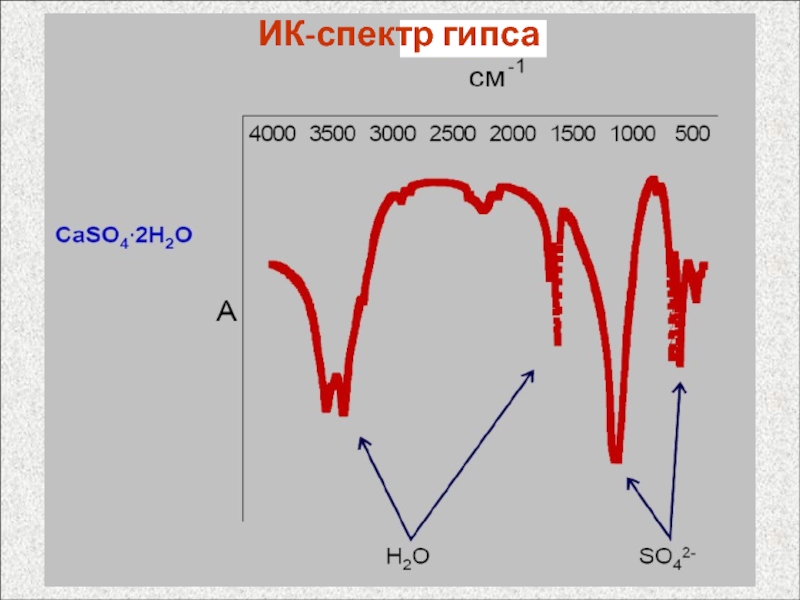
- 68. ИК-спектр гипса
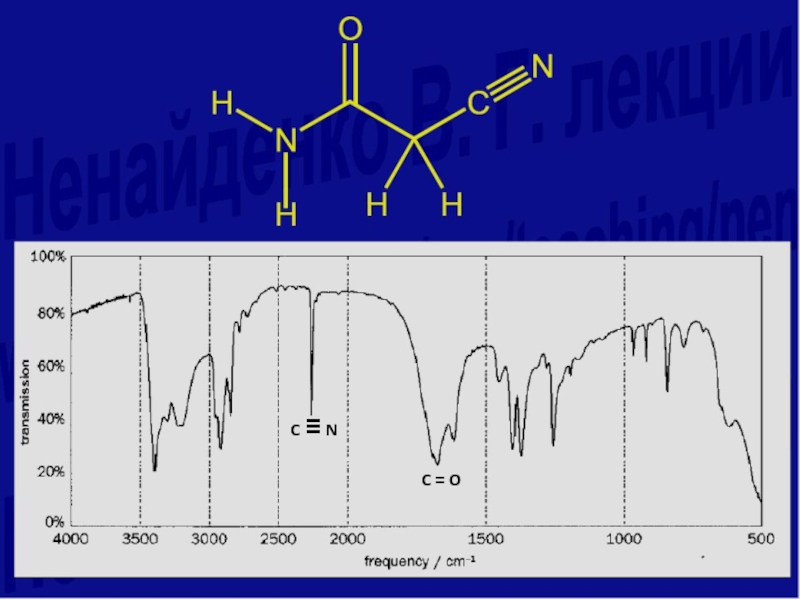
- 69. C NC = O
- 70. ЛитератураОсновы аналитической химии. Кн. 2. Методы химического
- 71. Спасибо!
- 72. Скачать презентанцию
Слайды и текст этой презентации
Слайд 1Аналитическая химия
II. Инструментальные методы анализа
Майстренко В.Н.
Башкирский государственный университет
Кафедра аналитической химии
V_maystrenko@mail.ru
Тел:
229-97-12
Слайд 2Аналитическая химия – наука об
определении химического состава
веществ
и отчасти их химического
строения
Химические методы анализа
Физико-химические методы анализа
Физические методы анализа
Инструментальные методы анализа
Слайд 3 Инструментальные методы анализа — методы аналитической химии, для
выполнения которых требуется электрохимическая, оптическая, радио-химическая и иная аппаратура. К
инструментальным методам анализа относятся: электрохимические методы - потенциометрия (ионометрия), кулонометрия, вольтамперометрия, кондуктометрия и др.;
методы, основанные на испускании или погло-щении электромагнитного излучения – эмиссионная, абсорбционная, флуоресцентная атомная и молеку-лярная спектроскопия, фотометрические методы, рентгеноспектральный анализ и др.;
масс-спектральный анализ;
ЯМР, ЭПР, методы, основанные на измерении радиоактивности и др.
Слайд 5Дефиниция
Аналитический сигнал
y = f(x)
y
"Контроль объекта аналитический. Термины и определения." ГОСТ
Р 52361–2005.
Сигнал, содержащий количественную информацию о величине, функционально
связанной с содержанием определяемого компонента, и регистрируемый в ходе анализа вещества или материалах
Слайд 13Метод и методика анализа
"Контроль объекта аналитический. Термины и определения." ГОСТ
Р 52361–2005.
Метод анализа – достаточно универсальный и теоретически обоснованный
способ определения состава безотносительно к определяемому компоненту и (обычно) к анализируемому объекту. Методика анализа – подробное описание анализа данного объекта с использованием выбранного метода.
Слайд 14Методы аналитической химии
Методы отбора проб (пробоотбора)
Методы разложения проб
Методы разделения компонентов
Методы
концентрирования
Методы обнаружения (идентификации)
Методы определения
Слайд 15Проба – или образец – предмет исследования аналитика, объект, взятый
для анализа.
По ГОСТ: проба - часть вещества (материала), являющегося
объектом аналитического контроля, отобранная для анализа и/или исследования его структуры, и/или определе-ния свойств, отражающая его химический состав и/или структуру, и/или свойства. Представительная проба вещества или материала - объекта аналитического контроля – проба, которая по химическому составу и/или свойствам, и/или структуре идентична объекту аналитического контроля, от которого она отобрана.
Проба
Слайд 16В зависимости от способа получения:
разовая,
точечная (единичная, частная),
мгновенная,
суточная и
т. п. Классификация проб
В зависимости от стадии первичной обработки:
исходная,
промежуточная,
объединенная,
средняя,
сокращенная,
лабораторная,
аналитическая и др.
В зависимости от назначения:
контрольная,
рабочая,
резервная,
арбитражная и др.
Слайд 17Абсолютные и относительные методы анализа
Абсолютные методы – не
требуют градуировки и стандартных образцов (гравиметрия, кулонометрия и т.
д.). Относительные методы – параметры градуировочной функции определяют экспериментально (потенциометрия, вольтамперометрия и т. д.) с использованием стандартных образцов.
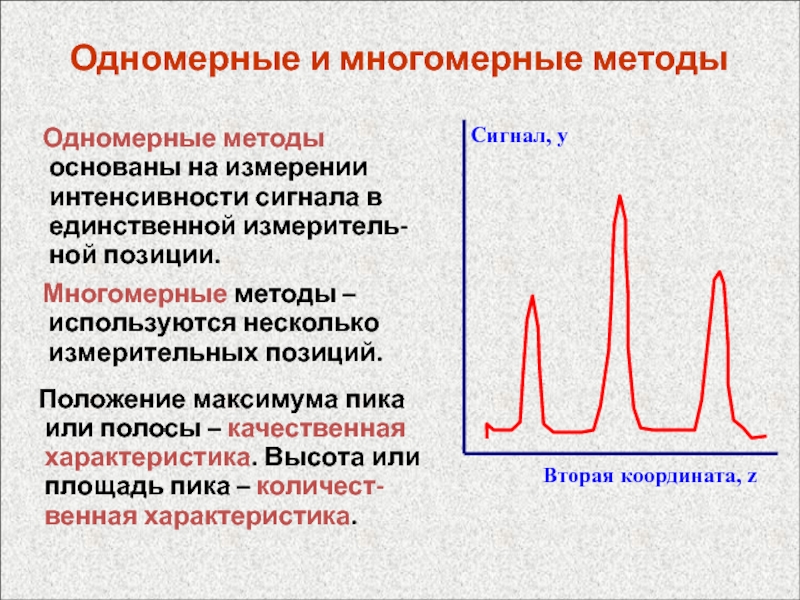
Слайд 18Одномерные и многомерные методы
Одномерные методы основаны на измерении
интенсивности сигнала в единственной измеритель-ной позиции.
Многомерные методы –
используются несколько измерительных позиций. Положение максимума пика или полосы – качественная характеристика. Высота или площадь пика – количест-венная характеристика.
Слайд 19Классификация методов анализа
по способу регистрации
по способу измерения
по объекту
общая классификация
Слайд 20Классификация методов анализа
Общая классификация
качественный / количественный
элементный
/ изотопный / молекулярный / структурно-групповой
валовый / распределительный
(локальный) / вещественный / фазовыйконтактный / дистанционный
деструктивный / недеструктив-ный
макро- / полумикро- / микро- / ультрамикро- / субмикро-
макро- > 0.1 г
полумикро- 0.1 - 0.01 г
микро- 0.01 – 0.001 г
ультрамикро- 10-6 г
субмикро- 10-9 г
Слайд 21Классификация методов анализа
По способу регистрации сигнала
Химические
Гравиметрия
Титриметрия
Электрохимические
Биохимические
Химические (погрешность < 0.1 -
0.2 %) Физические (погрешность 2 - 5 %)
Биологические
Слайд 22Классификация методов анализа
По способу регистрации сигнала
Физические
Спектральные
Масс-спектральные
Основанные на измерении
радиоактивности
Термический анализ
Химические
(погрешность < 0.1 - 0.2 %) Физические (погрешность 2 - 5 %)
Биологические
Слайд 23Классификация методов анализа
По способу регистрации сигнала
Биологические
Биотестирование
Биоиндикация
Микробиологический анализ
Биосенсоры
Химические (погрешность < 0.1
- 0.2 %) Физические (погрешность 2 - 5 %)
Биологические
Слайд 24Классификация методов анализа
По способу регистрации сигнала
Химические
Физические
Биологические
Физико-химические
Спектроскопические
Масс-спектральные
Основанные на радиоактивности
Электрохимические
БиохимическиеТермические
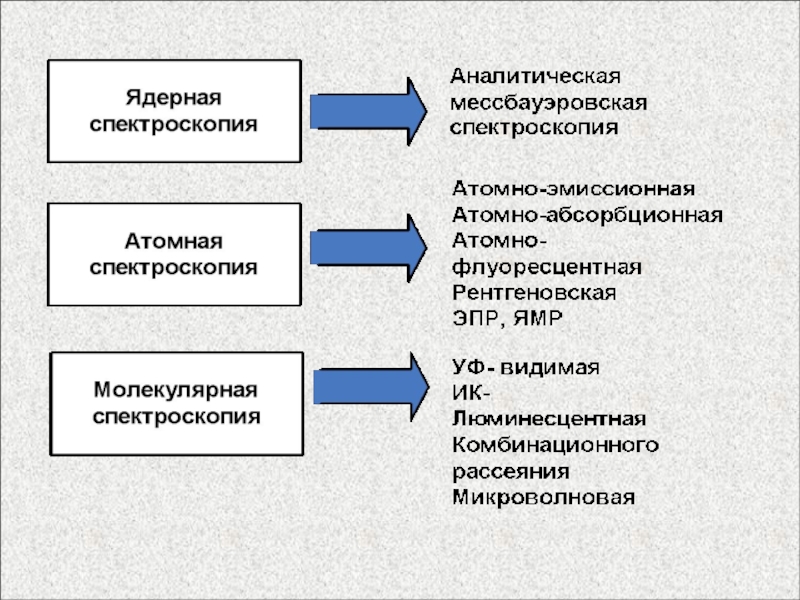
Слайд 25Спектроскопия
Молекулярная
Атомная
Ядерная
Электрохимические методы
Вольтамперометрия
Потенциометрия
Кондуктометрия
Кулонометрия
Хронопотенциометрия,
хроноамперометрия
По способу измерения сигнала
Слайд 27 По объекту анализа
Классификация
х
по агрегатному состоянию
по химической природе
по происхождению объекта
по степени распространенности
и важности
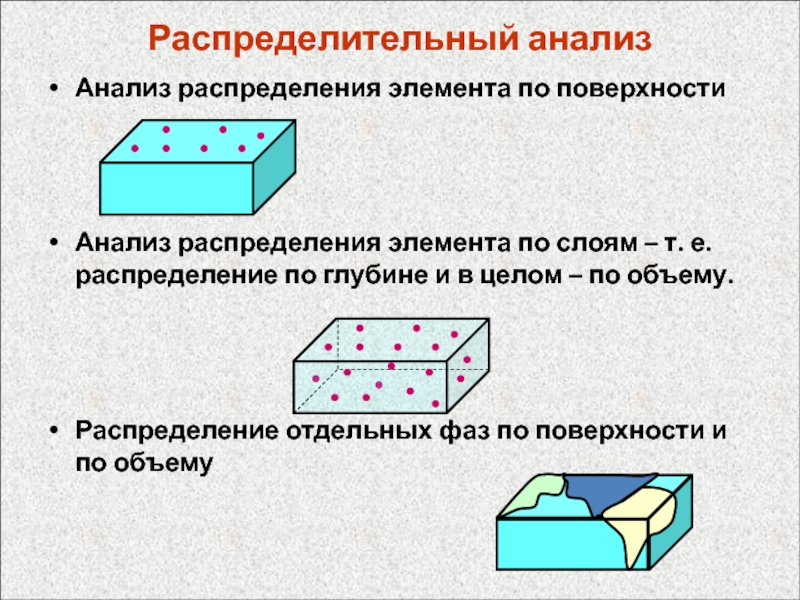
по степени чистотыСлайд 28Распределительный анализ
Анализ распределения элемента по поверхности
Анализ распределения элемента по слоям
– т. е. распределение по глубине и в целом –
по объему.Распределение отдельных фаз по поверхности и по объему
Слайд 29Критерии сравнения
Аналитические характеристики
Метрологические характеристики
Требования к пробоподготовке
Особенности приборного оснащения
Специальные требования, связанные
с природой объекта контроля
Экономические характеристики
Слайд 30Литература
Основы аналитической химии. Кн. 2. Методы химического анализа.
/ Под ред. Ю. А. Золотова. 2-е изд. М.:
Высшая школа, 2004.Аналитическая химия. Физические и физико-химические методы анализа. Под ред. О. М. Петрухина. М.: Химия, 2001.
Васильев В. П. Аналитическая химия. Кн. 2. Физико-химические
методы анализа. М.: Дрофа, 2004.
Дополнительная литература
Кристиан Г. Аналитическая химия. В 2-х т. М.: БИНОМ, 2009.
Аналитическая химия. Проблемы и подходы: В 2-х т. / Под ред. Р. Кельнера, Ж-М. Мерме, М. Отто, Н. Видмера. М.: Мир, 2004.
Отто М. Современные методы аналитической химии. В 2 т. М.: Техносфера, 2003.
Слайд 31Инструментальные методы анализа:
спектры атомов и молекул
Майстренко В.Н.
Башкирский государственный университет
Кафедра аналитической химии
V_maystrenko@mail.ru
Тел: 229-97-12
Слайд 32 В арсенале современной аналитической химии важнейшее
место занимают методы атомной оптической спектроскопии, основанные на измерении интенсивности
электромагнитного излучения, испускаемого или поглощаемого атомами элементов, которые находятся в газо- или парообразном состоянии. Эти методы являются многоэлементными и широко используются для установления состава различных объектов – сплавов, минералов, руд, пищевых продуктов, объектов окружающей среды и др.Слайд 34 История атомного спектрального анализа началась с
опытов Исаака Ньютона (1666 г) по разложению света в спектр.
Первые атомные спектры наблюдали в начале XIX века в ходе астрономических исследований. Возникновение спектрального анализа как метода определения химичес-кого состава вещества относят к 1859 г., когда немецкие ученые Г. Кирхгоф и Р. Бунзен, исследуя поведение солей металлов в пламени, наблюдали появление линий в спектрах элементов.Густав Кирхгоф (слева)
и Роберт Бунзен (справа)
Спектроскоп Кирхгофа и Бунзена
Слайд 36Эксперимент Бунзена-Кирхгофа
А – сигарный ящик, B – часть подзорной
трубы, С – подзорная труба, D – газовая горелка Бунзена,
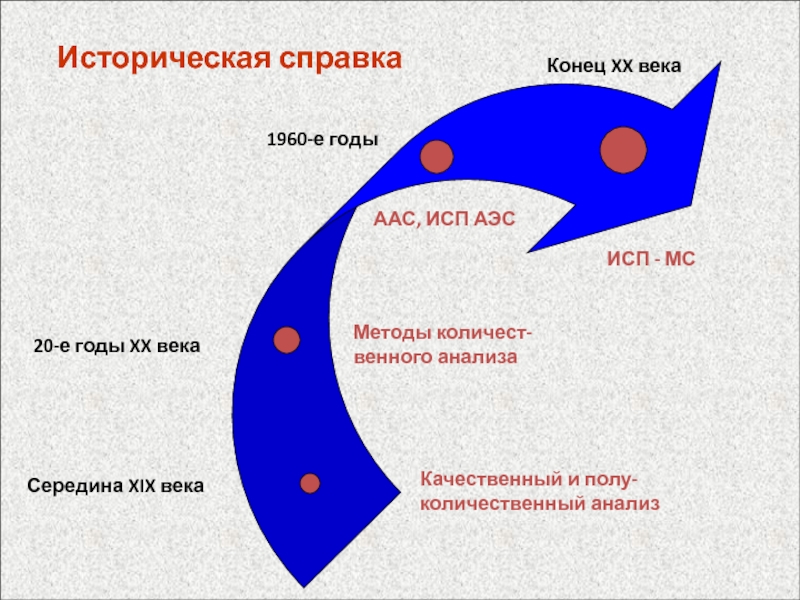
E – штатив с солью натрия, F – призма из стекла с CS2, G – зеркало, H – поворотное устройствоСлайд 37Историческая справка
Качественный и полу-количественный анализ
Методы количест-венного анализа
Середина XIX века
20-е годы
XX века
1960-е годы
ААС, ИСП АЭС
Конец XX века
ИСП - МС
Слайд 38 Атомы химических элементов имеют строго определённые
частоты, на которых они излучают или поглощают свет. При этом
на спектрах элементов наблюдаются светлые или темные линии в определённых местах, характерные для каждого элемента.Атомарные спектры получают переведением веществ в парообраз-ное состояние путём нагревания до 1000—10000 °C. В качестве источни-ков возбуждения атомов применяют искру, дугу переменного тока, пламя или плазму различных газов, лазеры и др.
Спектры поглощения и испускания атомов натрия
Спектры атомов
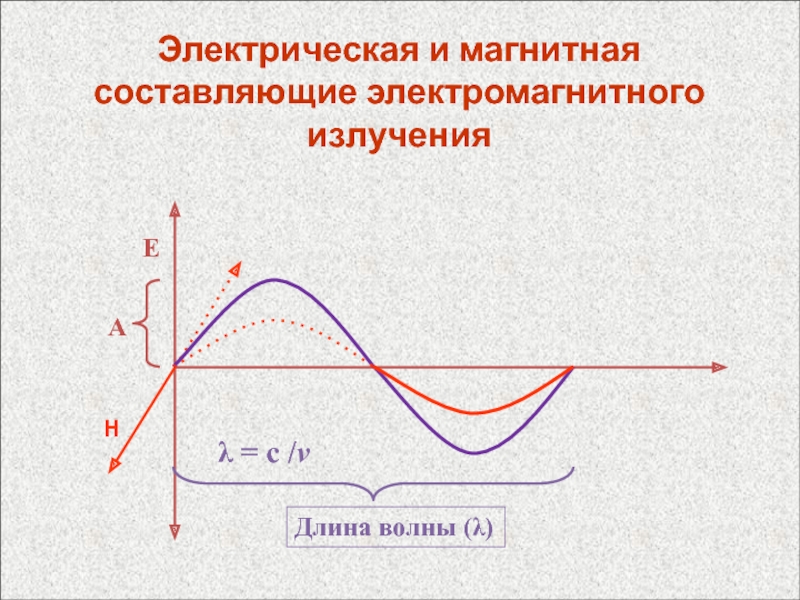
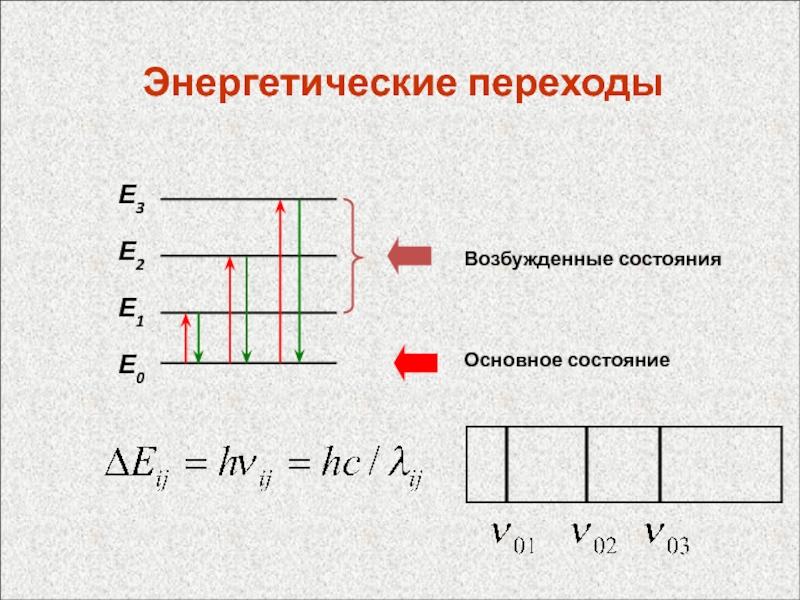
Слайд 42 Спектральные линии характеризуют частотой излучения ,
которая соответствует квантовому переходу между уровнями энергии Еi и Еk
атома согласно соотношениюh = Еi - Еk ,
где h – постоянная Планка, а также длиной волны = с / (с – скорость света), волновым числом ’ = 1/ и энергией фотона h. Частоты спектральных линий выражают в обратных секундах (с-1), длины волн – в нм, мкм и ангстремах, волновые числа – в обратных сантиметрах (см-1), энергию фотонов в электрон-вольтах (эВ).
Спектры испускания (эмиссионные) получают при возбуждении атомов различными способами. Время жизни возбужденного состояния 10-7 – 10-8 с. В течение этого времени атом испускает квант электро-магнитного излучения и переходит в состояние с более низкой энергией.
Спектры поглощения (абсорбционные) наблюдаются при прохож-дении электромагнитного излучения, имеющего непрерывный спектр, через пары или газы атомов.
Возникновение оптических спектров и их характер определяет система электронов атома, которые характеризуются четыремя квантовыми числами: главным квантовым числом (уровни K, L, M, N…Q), орбитальным квантовым числом (подуровни s, p, d, f…), магнитным и спиновым квантовыми числами.
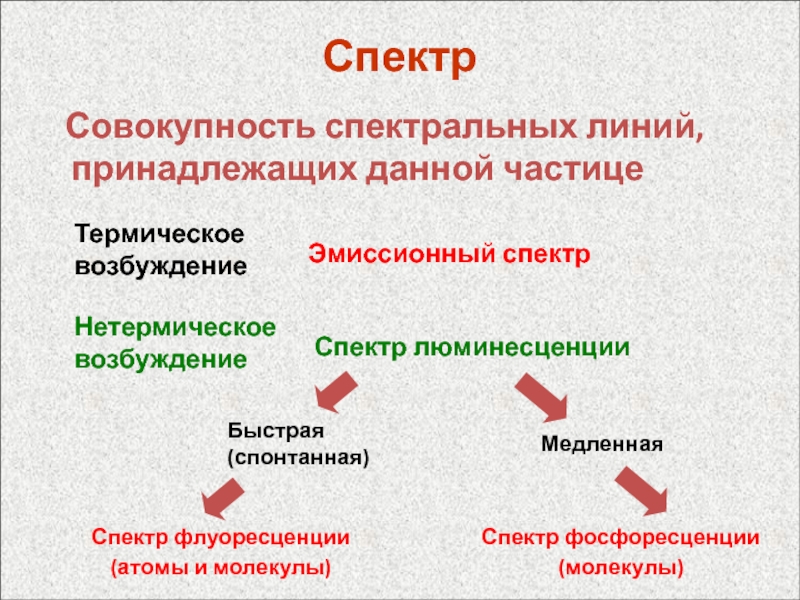
Слайд 44Спектр
Совокупность спектральных линий, принадлежащих данной частице
Термическое возбуждение
Нетермическое возбуждение
Эмиссионный
спектр
Спектр люминесценции
Быстрая (спонтанная)
Медленная
Спектр флуоресценции
(атомы и молекулы)
Спектр фосфоресценции
(молекулы)
Слайд 46 Спектры атомов с малым числом валентных
электронов (щелочные металлы, водород) имеют относительно мало линий (менее 100)
в диапазоне 200 - 800 нм. Атомы с более сложными электронными оболочками (элементы побочных групп) имеют спектры с большим числом линий ( Cu – более 500, Fe – более 3000, U – несколько тысяч). Линии, обусловленные переходом электронов на основной энергетический уровень, называются резонансными. Вследствие высокой интенсивности они обеспечивают наибольшую чувствитель-ность определений и используются для аналитических целей.
Для возбуждения резонансных линий щелочных металлов необхо-дима небольшая энергия, тогда как для неметаллов она высокая и спектры из видимой области смещаются в труднодоступную ультра-фиолетовую область: для Na – 589 нм, Mg – 285 нм, Si – 251 нм, P – 176 нм.
Основная область применения атомной спектроскопии – опреде-ление элементов с металлическими и полуметаллическими свойствами.
Для получения количественной информации измеряют интенсив-ность одной из спектральных линий определяемого элемента.
Процессы, происходящие с атомом при поглощении или испускании фотона, описывают с помощью спектральных термов, характеризующих энергетическое состояние поглощающего или испускающего атома. Спектральные термы получают путем векторного сложения орбитальных моментов и спинов всех электронов атома.
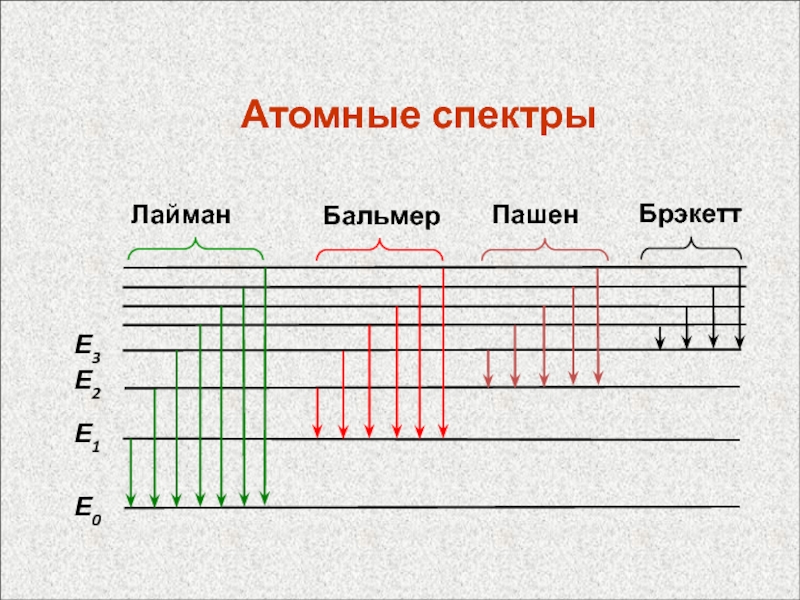
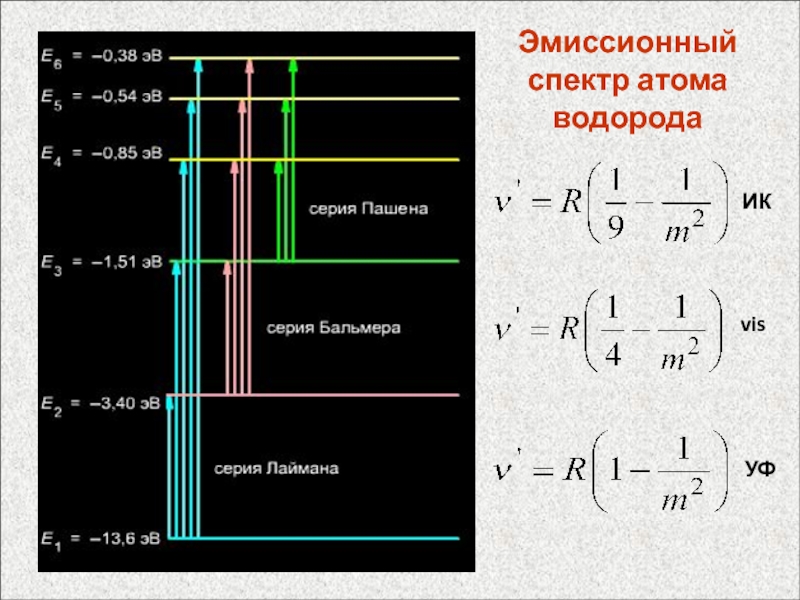
Слайд 47Спектральные термы
Серия Лаймана n = 1
Серия Бальмера: n
= 2
Серия Пашена: n = 3
Серия Брэкетта: n
= 4Спектральный терм:
R = 109 677 см−1 – постоянная Ридберга,
m – целые числа.
(m > n)
Терм:
Формула Бальмера
Слайд 49Спектральные термы многоэлектронных атомов
Учет заряда ядра:
He+, Li2+, Be3+
Учет суммарного орбитального момента и суммарного спина
Слайд 52Интенсивность спектральных линий
Энергия, поглощаемая, излучаемая или рассеиваемая в
единицу времени
Спектр испускания:
Спектр поглощения:
Рентгеновская спектроскопия, АЭС, АФС
ААС, UV-Vis, ИК, микроволновая
и радиочастотная спектроскопия Слайд 53Ширина спектральных линий
естественная
тепловое движение (допплеровское уширение)
соударение
частиц (лоренцево уширение)
расщепление энергетических уровней в магнитном поле
(эффект Зеемана)УФ: 10-5 нм
УФ: 10-3-10-2 нм
Слайд 54 МОЛЕКУЛЯРНЫЕ СПЕКТРЫ - спектры поглощения, испускания или
рассеяния, возникающие при квантовых переходах молекул из одного энергетического состояния
в другое. Молекулярные спектры определяются составом молекул, их структурой, характером химических связей и взаимодействием с окружающими атомами и молекулами. Наиболее характерными являются молекулярные спектры молекул разреженных газов, которые состоят из узких линий. Молекулярные спектры состоят из электронных, колебательных и вращательных спектров и лежат в диапазоне электромагнитных волн от радиочастот до рентгеновской области спектра. Частоты переходов между вращательными уровнями энергии обычно попадают в микроволновую область, частоты переходов между колебательными уровнями - в ИК-область, а частоты переходов между электронными уровнями - в видимую и УФ-области спектра.
Часто вращательные переходы попадают в ИК-область, колебательные - в видимую область, электронные - в ИК-область. Электронные переходы сопровождаются изменением колебательной энергии молекул, а при колебательных переходах изменяется вращательная энергия. Поэтому электронные спектры обычно представляют собой электронно-колебательные полосы. При высоком разрешении обнаруживается и вращательная структура.
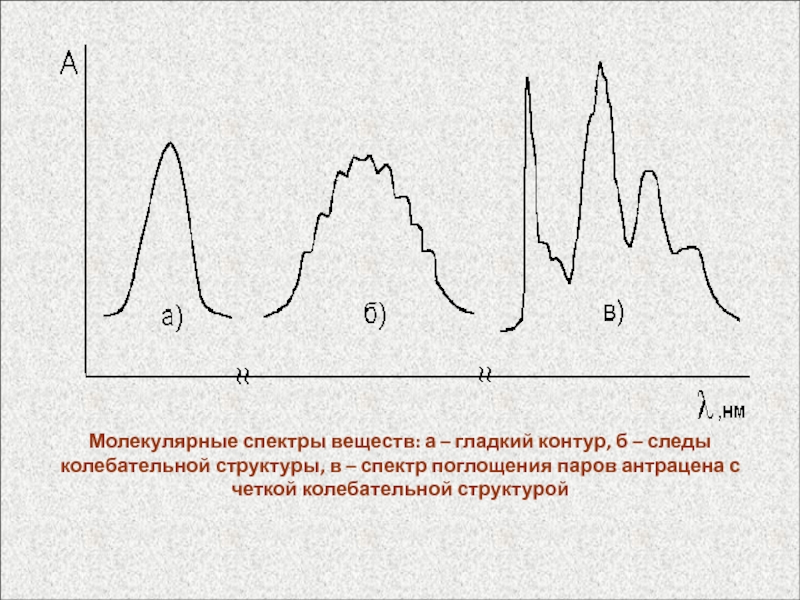
Слайд 56Молекулярные спектры веществ: а – гладкий контур, б – следы
колебательной структуры, в – спектр поглощения паров антрацена с четкой
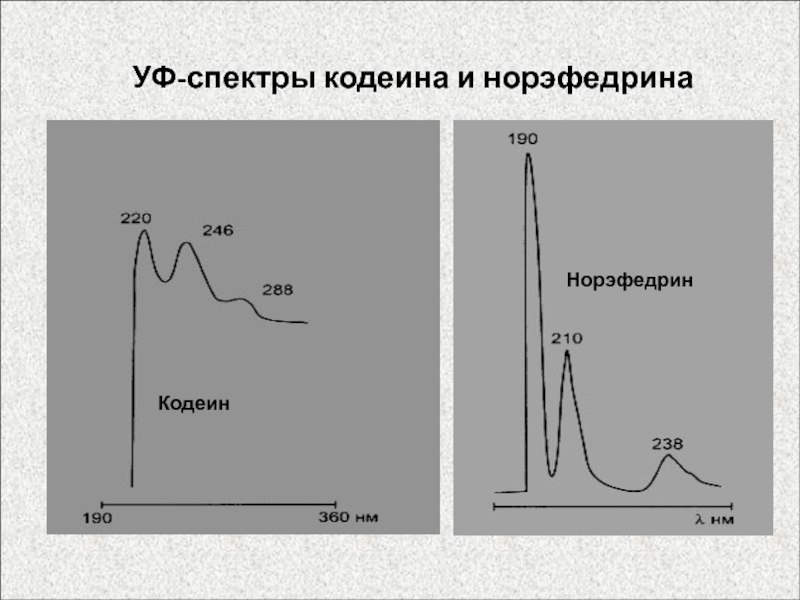
колебательной структуройСлайд 57Электронные спектры молекул
Электронные спектры обусловлены переходами между электронными энергетическими уровнями.
Чем
определяются электронные спектры?
Для атомов
электронной конфигурацией атомов
Для молекул
электронной конфигурацией
молекул Электронные переходы в молекулах, как правило, имеют энергию, соответствующую УФ- и видимой областям электромагнитного спектра.
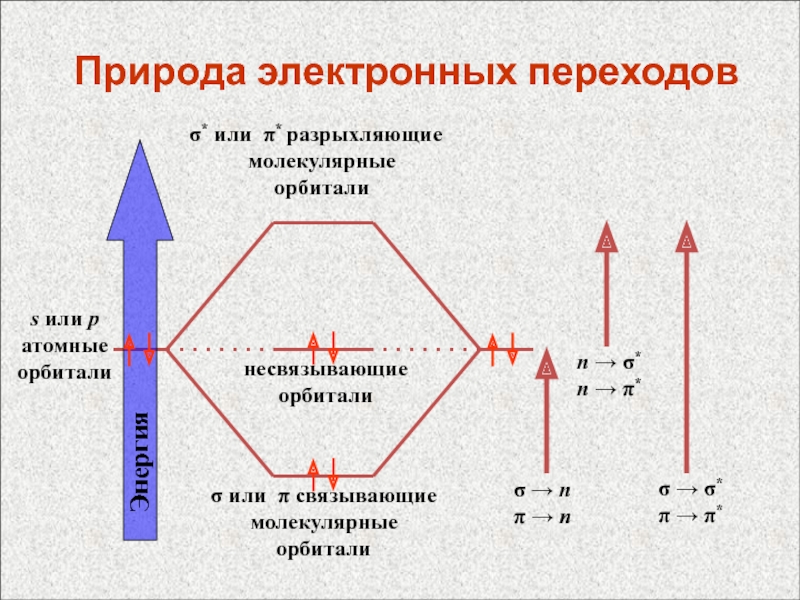
Слайд 59Природа электронных переходов
или связывающие
молекулярные
орбитали
s или p
атомные
орбитали
* или *
разрыхляющие
молекулярные
орбитали
несвязывающие
орбитали
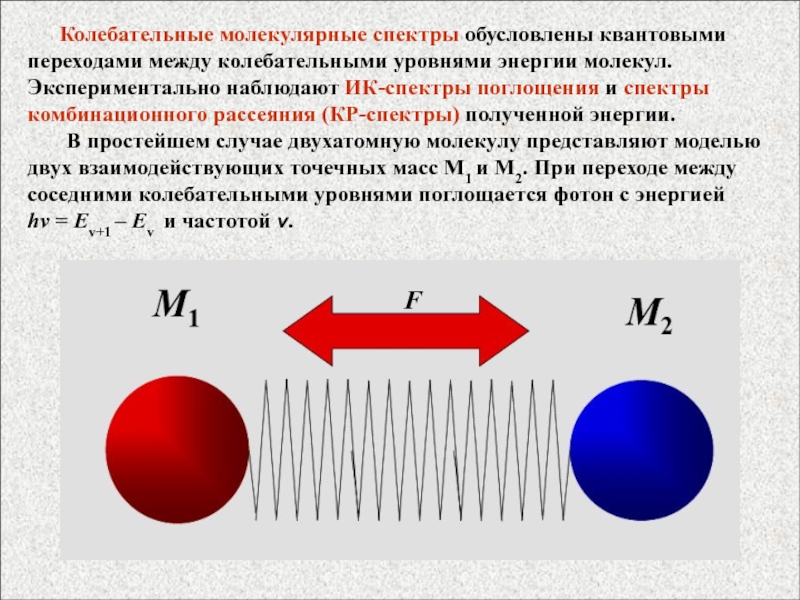
Слайд 63 Колебательные молекулярные спектры обусловлены квантовыми переходами
между колебательными уровнями энергии молекул. Экспериментально наблюдают ИК-спектры поглощения и
спектры комбинационного рассеяния (КР-спектры) полученной энергии.В простейшем случае двухатомную молекулу представляют моделью двух взаимодействующих точечных масс M1 и M2. При переходе между соседними колебательными уровнями поглощается фотон с энергией h = Ev+1 – Ev и частотой .
F
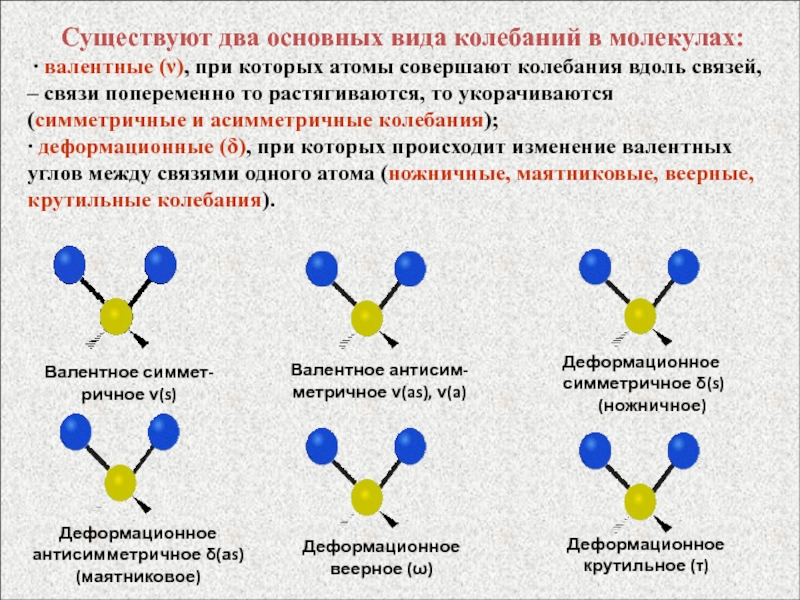
Слайд 64 Существуют два основных вида колебаний в молекулах:
валентные (), при которых атомы совершают колебания вдоль связей,
– связи попеременно то растягиваются, то укорачиваются (симметричные и асимметричные колебания); деформационные (), при которых происходит изменение валентных углов между связями одного атома (ножничные, маятниковые, веерные, крутильные колебания).
Валентное симмет-ричное (s)
Валентное антисим-метричное (as), (a)
Деформационное симметричное (s)
(ножничное)
Деформационное антисимметричное (аs)
(маятниковое)
Деформационное веерное ()
Деформационное крутильное ()
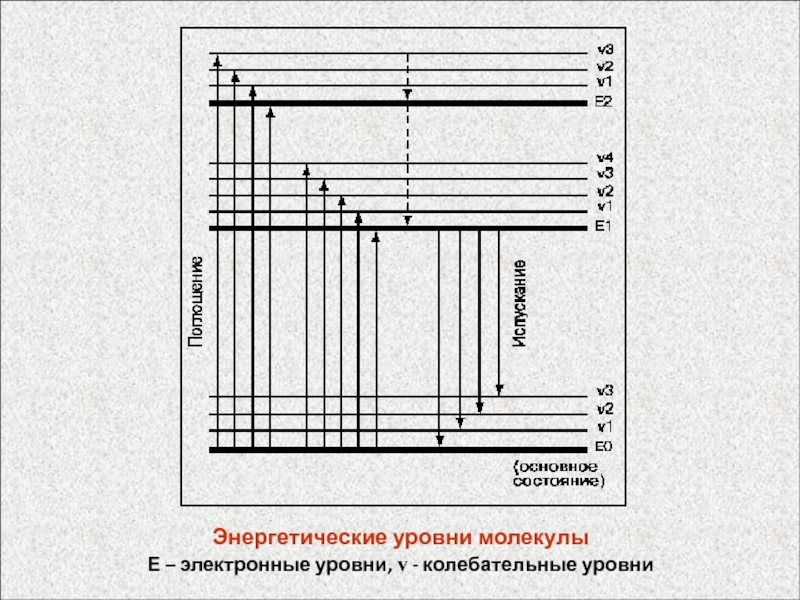
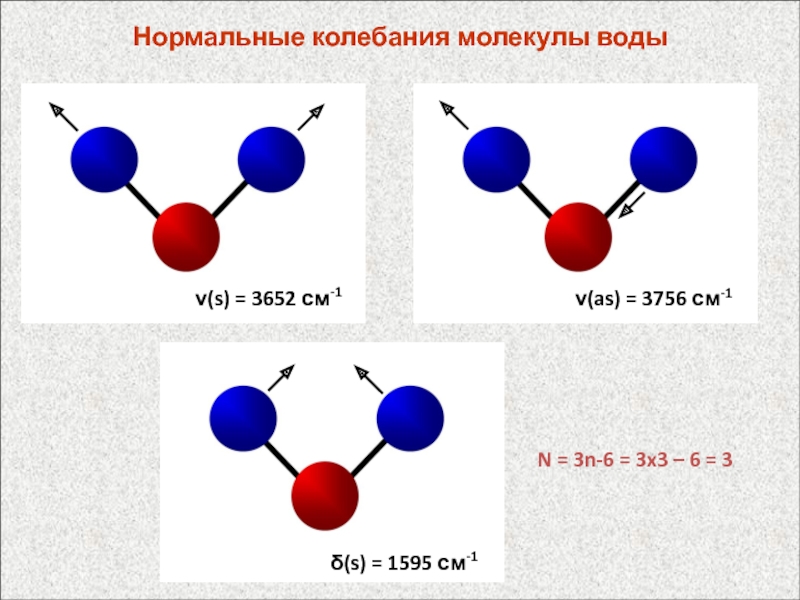
Слайд 65Нормальные колебания молекулы воды
N = 3n-6 = 3x3 – 6
= 3
(s) = 3652 см-1
(s) = 1595 см-1
(as) =
3756 см-1Слайд 66Частота колебаний зависит от массы атомов (легче атом – выше
частота)
C – H
3000 см-1
C – D
2200 см-1
C – O
1100 см-1
C – Cl
700 см-1
Частота колебаний зависит от энергии связи (связь прочнее – выше частота)
C С
2143 см-1
C = O
1715 см-1
C – O
1100 см-1
Слайд 70Литература
Основы аналитической химии. Кн. 2. Методы химического анализа.
/ Под ред. Ю. А. Золотова. 2-е изд. М.:
Высшая школа, 2004.Аналитическая химия. Физические и физико-химические методы анализа. Под ред. О. М. Петрухина. М.: Химия, 2001.
Васильев В. П. Аналитическая химия. Кн. 2. Физико-химические
методы анализа. М.: Дрофа, 2004.
Дополнительная литература
Кристиан Г. Аналитическая химия. В 2-х т. М.: БИНОМ, 2009.
Аналитическая химия. Проблемы и подходы: В 2 т. / Под ред. Р. Кельнера, Ж-М. Мерме, М. Отто, Н. Видмера. М.: Мир, 2004.
Отто М. Современные методы аналитической химии. В 2 т. М.: Техносфера, 2003.
Кузяков Ю. Я., Семененко К. А., Зоров Н. Б. Методы спектрального анализа. М.: МГУ, 1990.
Казицына Л. А., Куплетская Н. Б. Применение УФ-, ИК- и ЯМР- спектроскопии в органической химии. М.: Высшая школа, 1971.