Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Арены (общая характеристика)
Содержание
- 1. Арены (общая характеристика)
- 2. Слайд 2
- 3. Структура бензола
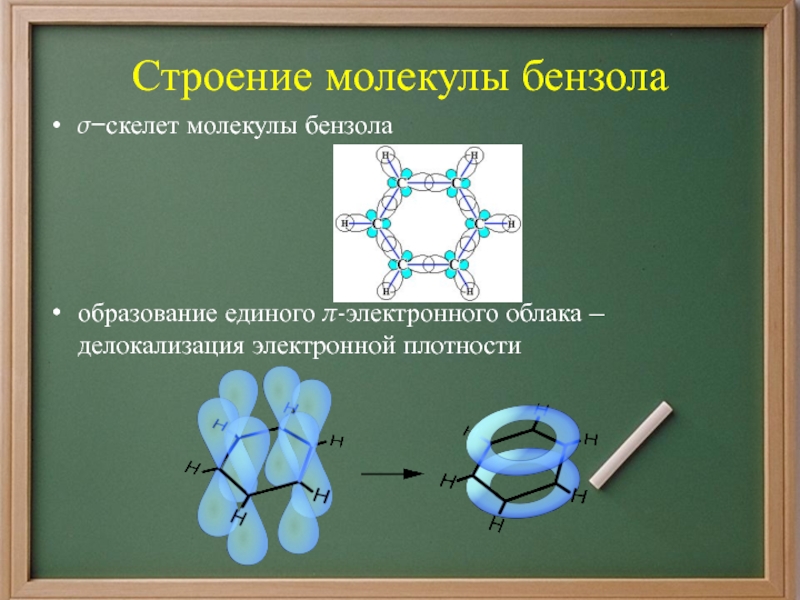
- 4. Строение молекулы бензолаσ−скелет молекулы бензолаобразование единого π-электронного облака – делокализация электронной плотности
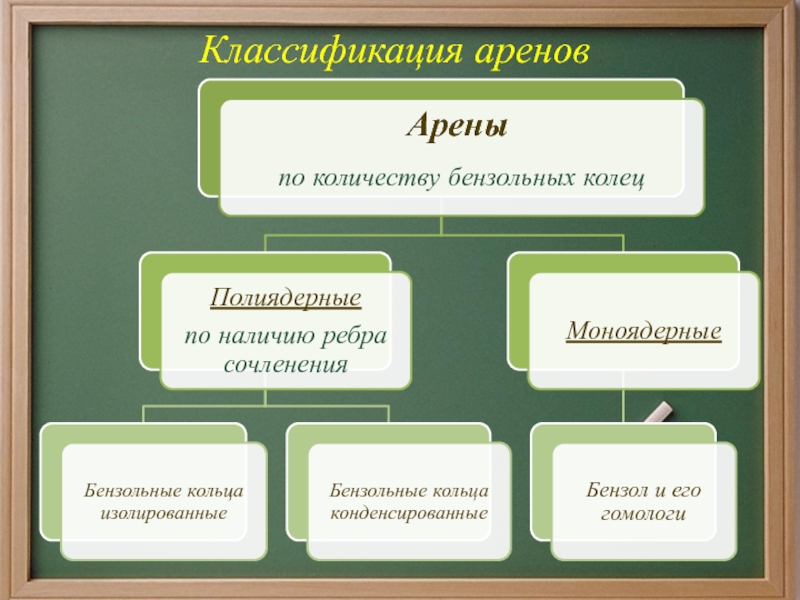
- 5. Классификация ареновАрены
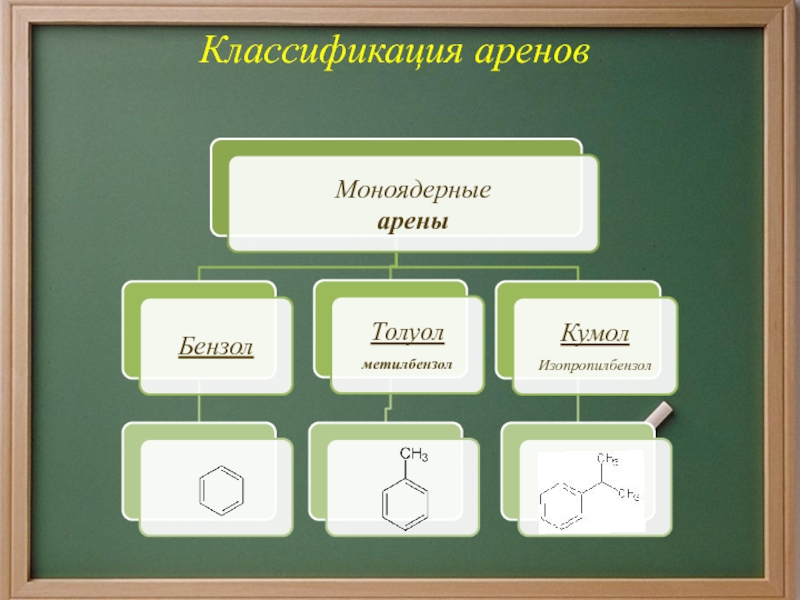
- 6. Классификация аренов
- 7. Классификация ареновДифенилДифенилметан
- 8. Классификация ареновАнтраценФенантренНафталин
- 9. Общая характеристика ареновОбщая формула аренов: CnH2n−6, где
- 10. Основные характеристики ароматических соединений склонность к
- 11. Ароматические радикалы фенил
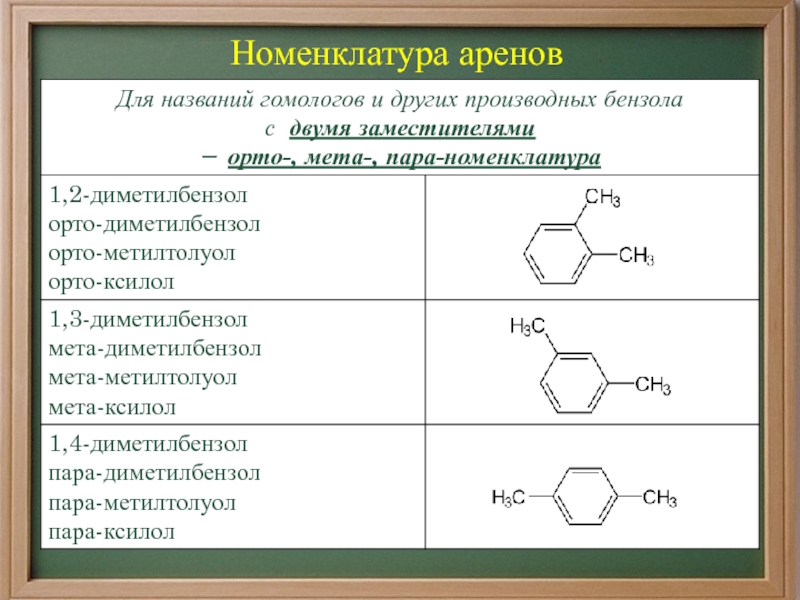
- 12. Номенклатура аренов
- 13. Номенклатура аренов
- 14. Изомерия, гомология ареновI. Структурная изомерия1. Изомерия углеродного
- 15. Изомерия, номенклатура, гомологияСтруктурная изомерия2. (б) Изомерия положения
- 16. Изомерия, номенклатура, гомологияПространственная изомерияГеометрическая изомерия (цис-транс-изомерия) для аренов невозможна
- 17. Методы получения ароматических углеводородов Алкилирование бензола и
- 18. Методы получения ароматических углеводородов5. Дегидроциклизация (ароматизация) алканов*
- 19. Скачать презентанцию
Структура бензола
Слайды и текст этой презентации
Слайд 1Арены (общая характеристика)
Ароматические углеводороды – циклические углеводороды,
в молекуле которых
Слайд 4Строение молекулы бензола
σ−скелет молекулы бензола
образование единого π-электронного облака – делокализация
электронной плотности
Слайд 9Общая характеристика аренов
Общая формула аренов: CnH2n−6, где n ≥6;
Простейший представитель
– бензол С6Н6;
Атомы углерода в молекуле бензола –
атомы sp2−C;
Валентный
угол (∠НСС и ∠ССС) равен 120°;Длина С−С связи 0,140 нм; С−Н связи 0,108 нм;
Направленность σ−связей −
плоскостно-тригональная;
σ−скелет молекулы бензола − плоский
Слайд 10Основные характеристики ароматических соединений
склонность к реакциям замещения,
а
не присоединения;
выигрыш в энергии по сравнении с
системой несопряженных двойных связей – энергия сопряжения Eсопряжения бензола = 150 кДж/моль;наличие плоскости, в которой лежат все атомы образующие ароматическую систему,
единое π-электронное облако, образующееся
при сопряжении, лежит над и под плоскостью ароматической системы.
правило Хюккеля: ароматичной может
быть лишь система, содержащая (в кольце)
4n+2 электронов (где n = 0, 1, 2, …).
Слайд 11Ароматические радикалы
фенил
или ─С6Н5
бензил
СН2─ или С6Н5─СН2 ─орто-толил СН3
\
мета-толил
СН3
/
пара-толил ─ СН3
Слайд 14Изомерия, гомология аренов
I. Структурная изомерия
1. Изомерия углеродного скелета боковой цепи
(С9Н12)
Пропилбензол Изопропилбензол
1-фенилпропан 2-фенилпропан или кумол
СН2−СН2−СН3 СН3−СН−СН3
2.
(а) Изомерия числа или количества заместителей в цикле (С8Н10)а) этилбензол 1,2-диметилбензол
Слайд 15Изомерия, номенклатура, гомология
Структурная изомерия
2. (б) Изомерия положения заместителей в цикле
(С8Н10)
б)
пара-ксилол мета-ксилол орто-ксилол
3. Межклассовая изомерия
Как правило, не приводят межклассовые изомеры
аренов, хотя существует не один класс углеводородов, которые являются межклассовыми изомерами аренов, например:для бензола С6Н6
гексадиин-1,5 СН≡С─СН2─СН2─С≡СН
гексадиен-1,5-ин-3 или дивинилацетилен
СН2=СН−С≡С−СН=СН2
Слайд 16Изомерия, номенклатура, гомология
Пространственная изомерия
Геометрическая изомерия (цис-транс-изомерия)
для аренов невозможна
Слайд 17Методы получения ароматических углеводородов
Алкилирование бензола и его гомологов по
Фриделю-Крафтсу – метод получения гомологов бензола (химическое свойство).
Алкилирование бензола и
его гомологов алкенами – метод получения гомологов бензола (химическое свойство)*.
Восстановление ароматических кетонов –
метод получения гомологов бензола,
в молекуле которых содержится α−метиленовое звено
(α−СН2−звено).
Реакция Вюрца−Фиттига –
метод получения гомологов бензола,
модифицированная реакция Вюрца*.
Слайд 18Методы получения ароматических углеводородов
5. Дегидроциклизация (ароматизация) алканов* − метод получения
бензола и его гомологов.
6. Дегидрирование циклогексана и его гомологов* −
метод получения бензола и его гомологов.7. Щелочное декарбоксилирование солей ароматических карбоновых кислот* − метод получения бензола и его гомологов.
8. Синтез Зелинского – циклическая тримеризация низших алкинов* − метод получения бензола и его симметричных полизамещенных гомологов,
например: 1,3,5-триметилбензола.