Слайд 1БИОХИМИЯ
КРОВИ
Метаболизм эритроцитов.
Синтез и распад гемоглобина.
Слайд 2Эритроциты –
безъядерные клетки, в них нет митохондрий, рибосом, наполнены гемоглобином.
Состав
эритроцита:
65% - вода,
33% - гемоглобин,
2% - негемоглобиновые белки, липиды, глутатион,
метаболиты (2,3-дифосфоглицерат).
Ферменты эритроцитов:
все ферменты гликолиза и пентозного цикла,
аденилатциклаза,
СОД,
кислая фосфатаза,
аденозиндезаминаза,
АЛТ,
каталаза.
Слайд 3Обмен в эритроцитах:
направлен на обеспечение их функции как переносчиков кислорода
и на выполнении роли посредников при переносе углекислого газа.
Гликолиз –
90% окисления глюкозы до лактата → 2 АТФ, используется на работу K/Na-АТФ-азы (работу K-Na канала, поддержания структуры эритроцита).
2,3-дифосфоглицерат → регулирует сродство Нв к О2.
Пентозный цикл – 10% глюкозы → НАДФН2, используется на восстановление глутатиона → защита мембраны (липидов) от действия окислителей; поддержание Fe в двухвалентном состоянии (чтобы железо могло связывать кислород).
Слайд 4Эритроцитарные энзимопатии -
врожденные наследственные заболевания, которые развиваются из-за нарушения синтеза
какого-либо фермента гликолиза или пентозного цикла в эритроцитах.
Дефицит Г-6-ФДГ наследуется
как сцепленный с Х-хромосомой признак, поэтому среди заболевших лиц преобладают мужчины (блокируется реакция окисления Гл-6-Ф в пентозо-фосфатном цикле, уменьшается образование восстановленной формы глутатиона).
В результате снижается осмотическая стойкость эритроцитов, у больного приступы гемолитической анемии.
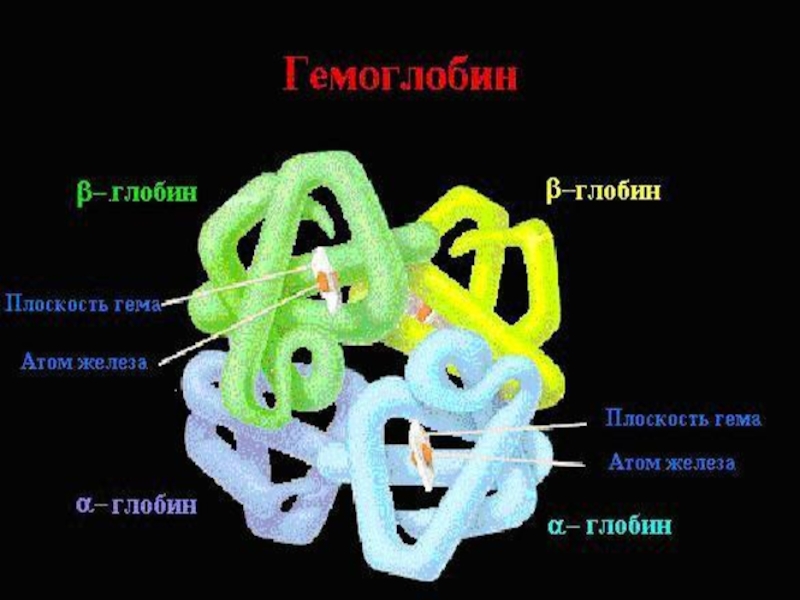
Слайд 5Структура гемоглобина
Гемоглобин – глобулярный белок, железосодержащий хромопротеин, М.м. Нв
≈ 64500.
Гемоглобин состоит из 4 цепей белка глобина и четырёх
гемов.
Глобины – α, β, γ, δ, ε и др. (синтезируются в нормобластах).
Гем – всегда одинаков.
Структура глобина:
1° - Много гистидина (связан с гемом), 2 ° - На 70% α-спираль, 3 ° - Всегда глобула, 4 ° - 4 цепи уложены в пространстве относительно друг друга. Молекула гема связана с каждой из 4-х цепей глобина.
Слайд 7Виды гемоглобина
Различны:
по АМК составу,
по электрофоретической подвижности,
по физико-химическим свойствам.
Hb A1≈
98% у взрослых (2α-цепи по 141 АМК, 2β-цепи по 146
АМК)
Hb A2 ≈ 2% от общего Hb (2α-цепи, 2δ-цепи),
Hb F ≈ менее 1% у взрослых (2α-цепи, 2γ-цепи) – высокое сродство к О2, но менее устойчив к действию окислителей; 80% у новорожденных, к концу 1 года заменяется на HbA1.
Hb Р (эмбриональный) (2α-цепи, 2ε-цепи - Говар II) - синтезируется в первые 3 месяца внутриутробного развития.
Слайд 8Гемоглобины крови
НвО2 (оксигемоглобин) – связан с кислородом,
НвСО2 (карбгемоглобин) – связан
с углекислым газом,
НвСО (карбоксигемоглобин) – связан с окисью углерода,
МетНв (метгемоглобин)
– железо в 3-х валентном состоянии, не связывает кислород.
Слайд 9Гемоглобинозы
Наследственные нарушения первичной структуры и функций глобина (более 200):
1. Гемоглобинопатии
– изменение структуры глобина.
НвS – серповидно-клеточная анемия – в β-цепи
ГЛУ заменена на ВАЛ (эритроциты в форме полумесяца, не переносят кислород)
М-гемоглобины – гистидин, участвующий в связывании Fe замещен другими аминокислотами (восстановление в 2-х вал. состояние затруднено или не происходит)
2. Талассемии – нарушен синтез α-, β- цепей, уменьшение физиологических видов гемоглобина (Нв А). Микроцитоз, гипохромия, гемолитическая анемия.
Слайд 10СИТНЕЗ ГЕМА
Гем - это соединение циклического тетрапиррола (порфирина) с
железом.
Является составной частью О2-связывающих белков и коферментом различных оксидоредуктаз.
Атом железа
имеет 6 связей:
четыре – с атомами азота пиррольных колец,
пятая – с гистидином глобина,
шестая – для связывания с кислородом.
Почти на 85% биосинтез гема происходит в костном мозге и лишь небольшая часть — в печени.
Синтез гема протекает в митохондрии и цитоплазме.
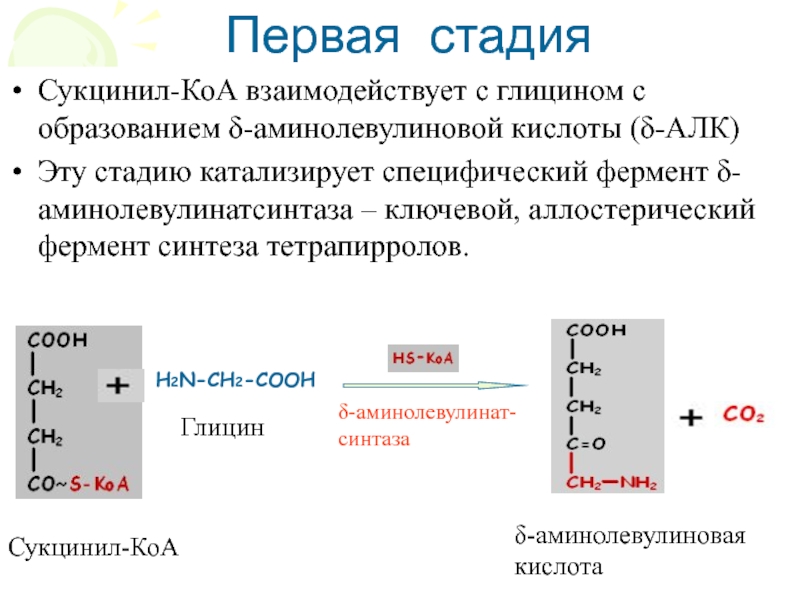
Слайд 11Сукцинил-КоА взаимодействует с глицином с образованием δ-аминолевулиновой кислоты (δ-АЛК)
Эту стадию
катализирует специфический фермент δ-аминолевулинатсинтаза – ключевой, аллостерический фермент синтеза тетрапирролов.
Первая
стадия
H2N-CH2-COOH
δ-аминолевулиновая
кислота
Глицин
Сукцинил-КоА
δ-аминолевулинат-
синтаза
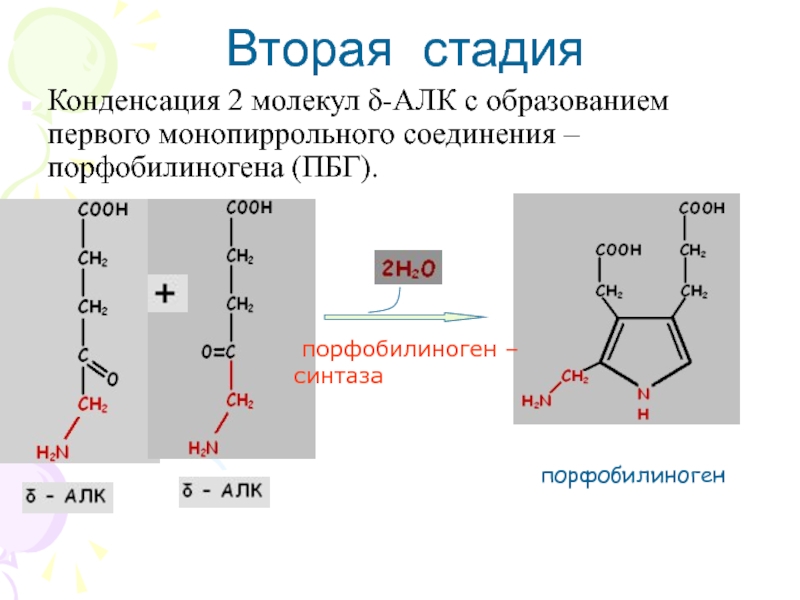
Слайд 12Конденсация 2 молекул δ-АЛК с образованием первого монопиррольного соединения –
порфобилиногена (ПБГ).
Вторая стадия
порфобилиноген
порфобилиноген –
синтаза
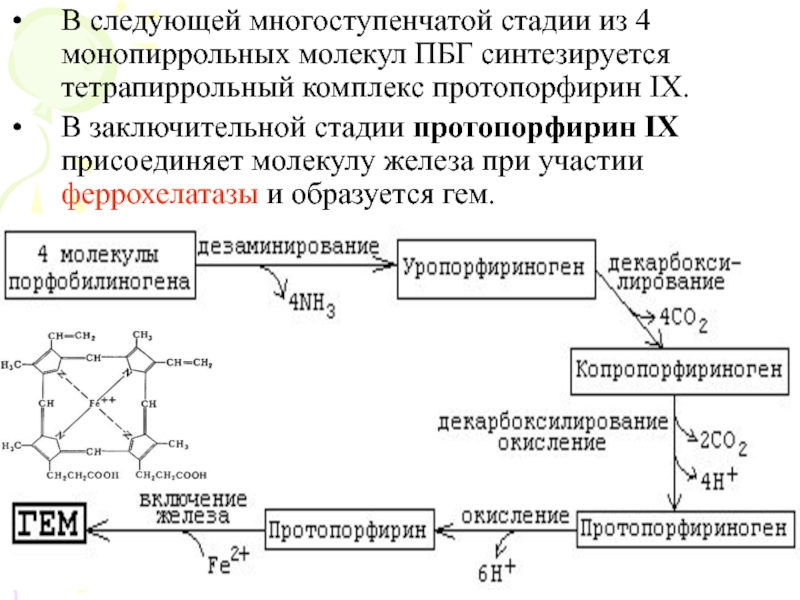
Слайд 13В следующей многоступенчатой стадии из 4 монопиррольных молекул ПБГ синтезируется
тетрапиррольный комплекс протопорфирин IХ.
В заключительной стадии протопорфирин IХ присоединяет молекулу
железа при участии феррохелатазы и образуется гем.
Слайд 14Синтез гема - энергозависимый процесс.
Стимуляторы синтеза:
ионы железа (из
трансферрина),
ионы меди (способствуют включению Fe в структуру гема),
витамин В12, ТГФК
(ВС).
δ-Аминолевулинатсинтаза - ингибируется гемом, активируется стероидами.
Эритропоэтин (синтезируется в мозговом слое почек) стимулирует синтез ферментов образования гема.
Регуляция синтеза гема
Слайд 15Порфирии
Ряд заболеваний, вызванных нарушениями порфиринового синтеза. Характерно повышение порфирина в
тканях, крови и моче.
Первичные – генетический дефект ферментов. Некоторые из
них протекают очень тяжело. Многие из этих заболеваний приводят к выделению предшественников гема с калом или мочой, которая вследствие этого может быть окрашена в темно-красный цвет.
Также наблюдается отложение порфиринов в коже. При воздействии света это приводит к образованию трудноизлечимых волдырей. При порфириях часты также неврологические нарушения.
Слайд 16Болезнь Гюнтера – врождённая порфирия (или порфиринурия): блок синтеза гема,
активность фермента увеличивается, накапливается δ-АЛК и порфирины. С мочой выделяются
уро- и копропорфирины. Клиника: фотодерматоз, розовые зубы, красная моча, нейро-психические расстройства, гепатосленомегалия.
Вторичные порфирии возникают при:
поражении печени (гепатит, цирроз)
отравлении свинцом
приеме сульфаниламидов, барбитуратов, стероидов
Аллергии
В период полового созревания, когда идет выброс стероидов (повышенная активность δ-АЛК-синтетазы).
Слайд 17Распад гемоглобина
Срок жизни эритроцита ≈ 120 дней
Распад гемоглобина происходит
в микросомальной фракции ретикулоэндотелиальных клеток печени, селезенки и костного мозга.
В
сутки у человека обновляется ≈ 6 г Нb.
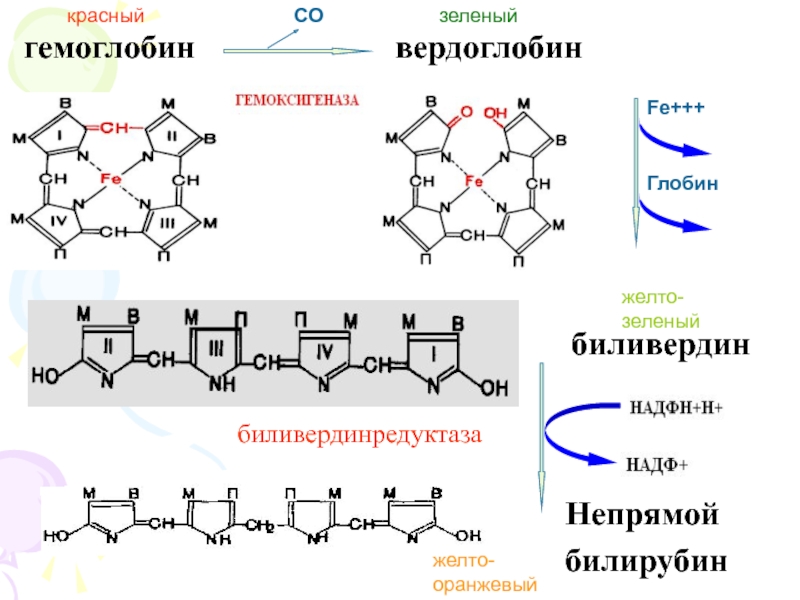
Слайд 18гемоглобин
вердоглобин
биливердин
Непрямой
билирубин
биливердинредуктаза
Fe+++
Глобин
красный
желто-зеленый
зеленый
желто-оранжевый
СО
Слайд 19Непрямой (свободный, неконъюгированный) билирубин
нерастворим в воде, в мочу не
выделяется
растворим в липидах,
токсичен,
проникает через ГЭБ
даёт непрямую
реакцию с диазореактивом Эрлиха (после обработки сыворотки крови спиртом),
транспортируется с альбуминами.
Слайд 20Токсичность непрямого билирубина:
снижает потребление кислорода,
повреждает мембраны,
снижает активность
дегидрогеназ,
замедляет пробег электронов в дыхательной цепи,
разобщитель тканевого дыхания
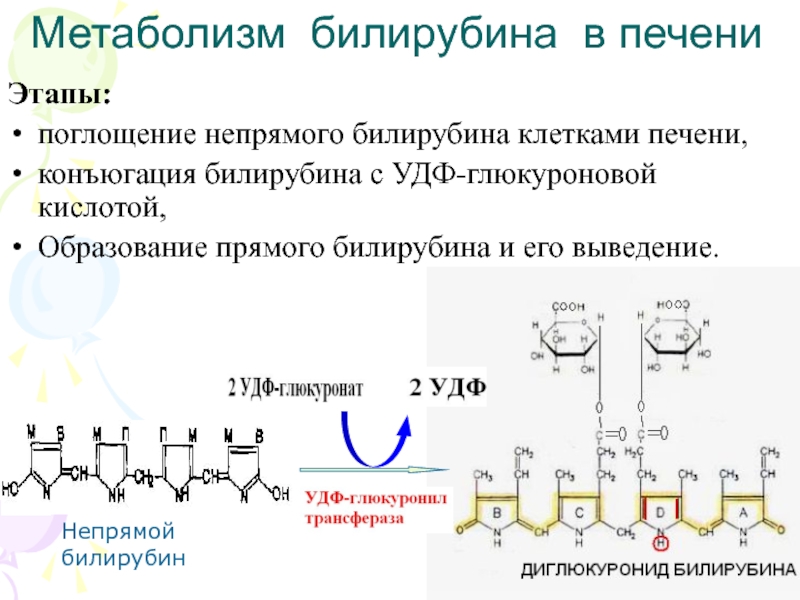
Слайд 21Метаболизм билирубина в печени
Этапы:
поглощение непрямого билирубина клетками печени,
конъюгация билирубина с
УДФ-глюкуроновой кислотой,
Образование прямого билирубина и его выведение.
Непрямой билирубин
Слайд 22Прямой (связанный, конъюгированный) билирубин
поступает из печени в желчный пузырь,
растворим в
воде,
нетоксичен,
реагирует с диазореактивом напрямую,
выделяется с мочой,
легко проходит через мембраны.
Слайд 23Секреция прямого билирубина в желчь идёт с помощью механизма активного
транспорта.
Часть прямого билирубина из печени всасывается в кровь
В норме содержание
общего билирубина в крови
1,7 - 20,5 мкмоль/л:
75% от общего билирубина составляет непрямой билирубин (1,7 - 17,1 мкмоль/л).
25% от общего билирубина в крови приходится на прямой билирубин (0,96 - 5,1 мкмоль/л).
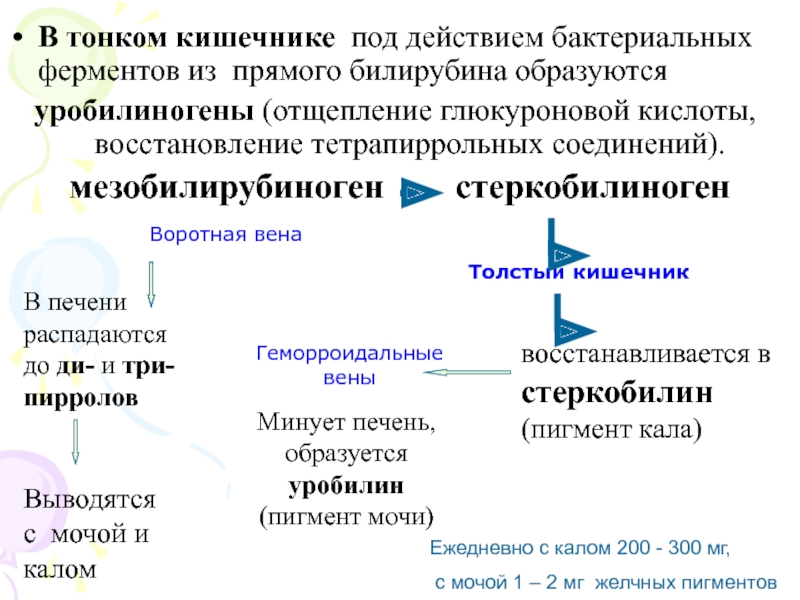
Слайд 24В тонком кишечнике под действием бактериальных ферментов из прямого билирубина
образуются
уробилиногены (отщепление глюкуроновой кислоты, восстановление тетрапиррольных соединений).
мезобилирубиноген
стеркобилиноген
В печени распадаются
до ди- и три- пирролов
восстанавливается в стеркобилин (пигмент кала)
Минует печень, образуется уробилин
(пигмент мочи)
Выводятся
с мочой и калом
Толстый кишечник
Геморроидальные вены
Воротная вена
Ежедневно с калом 200 - 300 мг,
с мочой 1 – 2 мг желчных пигментов
Слайд 25Классификация желтух. Диагностическое значение определения прямого и непрямого билирубина.
При гипербилирубинемии
более 34 мкмоль/л желчные пигменты придают желтую окраску коже и
слизистым – симптом желтухи.
3 вида желтух:
Гемолитическая
Механическая (обтурационная)
Паренхиматозная (печеночная)
Слайд 26Гемолитическая желтуха
Возникает при ускоренном распаде (гемолизе) эритроцитов:
Врождённые и приобретённые гемолитические
анемии,
Интоксикации ядами, фосфором, лекарствами,
Переливание несовместимой крови,
Резус-конфликт матери и плода
Слайд 27В крови увеличен общий билирубин за счет непрямого билирубина
Положительная реакция
на уробилиноген (за счет повышенного попадания в кровь и мочу
стеркобилиногена, а в тяжелых случаях – и за счет мезобилиногена, не утилизирующегося печенью);
В моче много уробилина, цвет насыщенный желтый.
Билирубина в моче нет (непрямой билирубин не фильтруется почками),
Кал темный, интенсивно окрашен (много стеркобилина).
Слайд 28Механическая желтуха
Возникает при нарушении оттока желчи:
опухоль головки поджелудочной железы,
желчнокаменная болезнь,
глистная
инвазия
атрезия желчевыводящих путей
Печень увеличена из-за застоя желчи, увеличивается давление →
боли в правом подреберье, элементы желчи (билирубин, холестерин, желчные кислоты) попадают в кровь.
Слайд 29В крови увеличивается общий билирубин за счет прямого билирубина
Кожный зуд
(желчные кислоты выделяются через кожу, раздражение нервных окончаний)
В моче билирубин
(прямой) – темная моча (цвета пива)
Уробилина в моче нет
В кале нет стеркобилина (стул серо-белый с жирным блеском - стеаторея)
Увеличена ЩФ (выделяется эндотелием желчных путей), холестерин
Слайд 30Паренхиматозная желтуха
Возникает при:
вирусных гепатитах,
токсических гепатитах (гепатотропные яды) ,
циррозах,
паразитарных заболеваниях печени.
развиваются
воспалительно-деструктивные процессы в печени, цитолиз гепатоцитов, нарушение функций.
Слайд 31В крови увеличивается общий билирубин за счет прямого и непрямого
билирубина
Прямой → клетка воспалена, отек, повышенная проницаемость. Непрямой → пораженные
гепатоциты слабо захватывают билирубин из крови
В моче билирубин (темная моча, цвета пива)
Уробилин в моче,
Стеркобилина в кале мало (светлый стул)
В крови увеличены печеночные ферменты (АЛТ, АСТ, ЛДГ4-5, Аргиназа, …);
диспротеинемия (↓ альбуминов, ↑ глобулинов);
положительная реакция на уробилиноген
Слайд 32Роль печени
в углеводном обмене
Поддержание физиологического уровня глюкозы в крови.
Поступление с пищей →
1. синтез гликогена (10-15%),
2. окислительный
распад (более 60%),
3. синтез ЖК (до 30%). При избыточном поступлении синтез гликогена увеличивается - роль фермента глюкокиназы (поступление глюкозы в печень).
Слайд 33При гипогликемии – распад гликогена.
1. Образование глюкозы, поступление ее
в кровоток.
2. Пентозно-фосфатный путь (НАДФН2 → процессы синтеза ЖК,
холестерина в печени)
Глюконеогенез. Основные предшественники глюкозы:
лактат и аланин – из мышц,
глицерол – из жировой ткани,
глюкогенные аминокислоты – с пищей.
Изомеризация моносахаров (галактоза, фруктоза) в глюкозу.
Слайд 34Главная роль в метаболизме липидов.
При дефиците глюкозы ускоряется окисление ЖК
При
избытке глюкозы используются ЖК для синтеза ФЛ, ТАГ.
Избыточное образование
Ац-КоА стимулирует липогенез, синтез холестрола, образование кетоновых тел
Синтез желчных кислот
Депо жирорастворимых витаминов
Активация витаминов (провитамин → витамин)
Образование ЛПОНП и ЛПВП
Роль печени
в липидном обмене
Слайд 35Биосинтез белков крови (90%)
Биосинтез ферментов
Обмен аминокислот: трансаминирование, дезаминирование
Обмен хромопротеинов
Синтез БАВ
из аминокислот
Синтез пуриновых и пиримидиновых оснований
Обезвреживание аммиака (синтез мочевины)
Образование мочевой
кислоты
Синтез холина и креатина
Роль печени
в белковом обмене
Слайд 36Токсические вещества образуются в процессе метаболизма организма, а также поступают
извне (ксенобиотики).
Токсические вещества могут блокировать или разрушать структуру рецепторов, что
изменяет клеточный метаболизм.
Детоксикация – химическая модификация (метаболические превращения веществ) – биотрансформация → превращение в менее токсичные или индифферентные вещества.
Обезвреживание токсических соединений в печени
Слайд 37 Цель – повышение гидрофильности, что облегчает выведение. Обезвреживание с помощью
двух фаз или любой из них.
2 фазы биотрансформации:
1. окисление,
восстановление, гидролиз → с образованием полярных группы (-ОН, -СООН, -SН, -NН2), что облегчает их выведение.
Микросомальные ферментные системы (ключевой фермент цитохром Р-450, имеющий огромное количество изоферментов)
Слайд 38 2. конъюгация – присоединение к полярным группам донаторов:
Глюкуроновой кислоты (УДФ-глюкоронат)
-образование глюкуронидов,
Серной кислоты (ФАФС) - сульфирование,
Ацетила (АцКоА) -
ацетилирование,
Метильной группы - метилирование,
присоединение глутамина, глицина (на место АцКоА).
Выведение продуктов обезвреживания в основном с желчью или мочей.
Слайд 39 Обезвреживание нормальных метаболитов:
Билирубин, аммиак,
инактивация гормонов (инсулиназа → до 80%
инсулина; стероидные гормоны – конъюгация с ФАФС и УДФ-глюкоронатом; тироксин
– трансаминирование → кетопроизводное)
Катехоламины → дезаминирование, метилирование, конъюгация.
Обезвреживание продуктов гниения аминокислот.
Слайд 40Чужеродные соединения (ксенобиотики):
Чем ниже растворимость чужеродного вещества, тем большая часть
его метаболизируется.
Индивидуальные различия в способности метаболизировать ксенобиотики (чувствительность к алкоголю,
лекарственным препаратам) – различный набор изоферментов.