Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
ЭКСПРЕСС-МЕТОДЫ РЕШЕНИЯ ЗАДАЧ ПО ХИМИИ
Содержание
- 1. ЭКСПРЕСС-МЕТОДЫ РЕШЕНИЯ ЗАДАЧ ПО ХИМИИ
- 2. ТИПЫ ЗАДАЧСвязь физико-химических величин (ФХВ) для
- 3. ТИПЫ ЗАДАЧКомбинированные задачи - зима Нестандартные задачи - весна
- 4. МАТЕМАТИЧЕСКИЕ АСПЕКТЫ РЕШЕНИЯ ЗАДАЧ ПО ХИМИИ
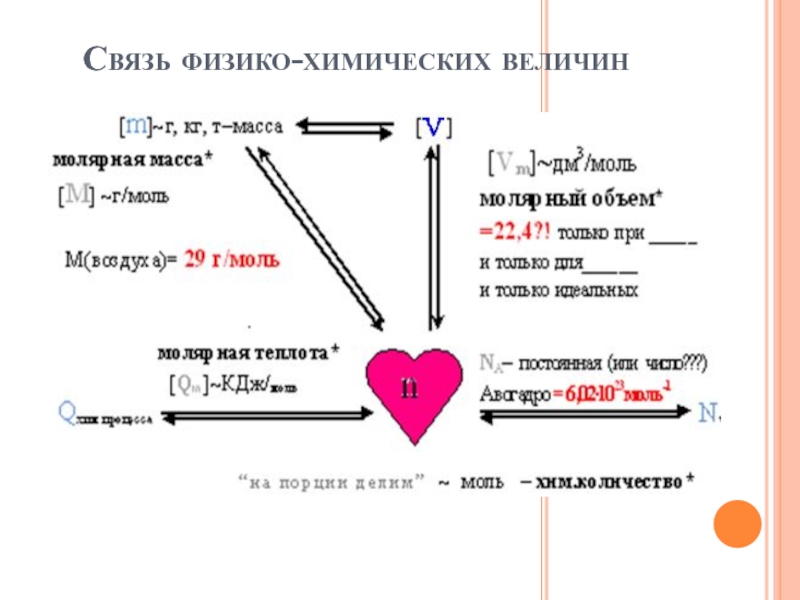
- 5. Связь физико-химических величин
- 6. P ∙ V = n ∙ R
- 7. НИ ДНЯ БЕЗ РЕШЁННОЙ ЗАДАЧИ!!! ?2 Какое
- 8. Расчеты по уравнениям, стехиометрическим схемамСтараемся уравнение упростить до стехиометрической схемы
- 9. ПЗ 1.Какая масса осадка выпадет при взаимодействии
- 10. ПЗ 4. Молярная теплота сгорания водорода -142,2
- 11. ПЗ 6. Какова массовая доля серной кислоты,
- 12. СубботаВведение в химию 15 сентября в 12-00
- 13. СОСТАВ РАСТВОРА
- 14. РАСТВОРЫ приготовление, смешение, выпадение осадка при охлажденииСколько
- 15. Какую массу кристаллической соды необходимо растворить в
- 16. Смешали 300 г 50%-ного раствора гироксида натрия
- 17. В каком соотношении масс необходимо взять 10%-ный
- 18. Определите концентрацию раствора фосфорной кислоты, полученного сливанием
- 19. Какая масса осадка образуется при охлаждении 250
- 20. Приготовили 200 г насыщенного при 60 0С
- 21. СПАСИБО ЗА ВНИМАНИЕ!!!
- 22. Скачать презентанцию
ТИПЫ ЗАДАЧСвязь физико-химических величин (ФХВ) для 1 компонента − через количество вещества; доли.Расчеты по стехиометрическим соотношениям связь нескольких объектов через количества веществ
Слайды и текст этой презентации
Слайд 1ЭКСПРЕСС-МЕТОДЫ РЕШЕНИЯ ЗАДАЧ ПО ХИМИИ
СТ. ПРЕПОДАВАТЕЛЬ КАФЕДРЫ НЕОРГАНИЧЕСКОЙ ХИМИИ Цобкало
Ж.А.
Слайд 2ТИПЫ ЗАДАЧ
Связь физико-химических величин (ФХВ) для 1 компонента −
через количество вещества; доли.
Расчеты по стехиометрическим соотношениям связь нескольких объектов
через количества веществСлайд 4 МАТЕМАТИЧЕСКИЕ АСПЕКТЫ РЕШЕНИЯ ЗАДАЧ ПО ХИМИИ -проценты, - дроби, -степени -корни, -пропорции, -уравнения,
-системы,
-логарифмы
-углы
-объемы
Слайд 6P ∙ V = n ∙ R ∙ T (пора
вставать на работу)
- уравнение Клапейрона-Менделеева
101,3 кПа = 1 атм =
760 мм.рт.ст 00С = 273К R= 8,31 кДж/моль∙К
Слайд 7НИ ДНЯ БЕЗ РЕШЁННОЙ ЗАДАЧИ!!!
?2 Какое число атомов содержится в
1 г алмаза?
?3Какая масса молекулы белого фосфора?
?4Какая масса озона может
быть получена из 3,01·1021 молекул кислорода? ?5Какой объем воды (в см3) содержит столько же атомов водорода, сколько и 4,48 дм3 аммиака (н.у.):
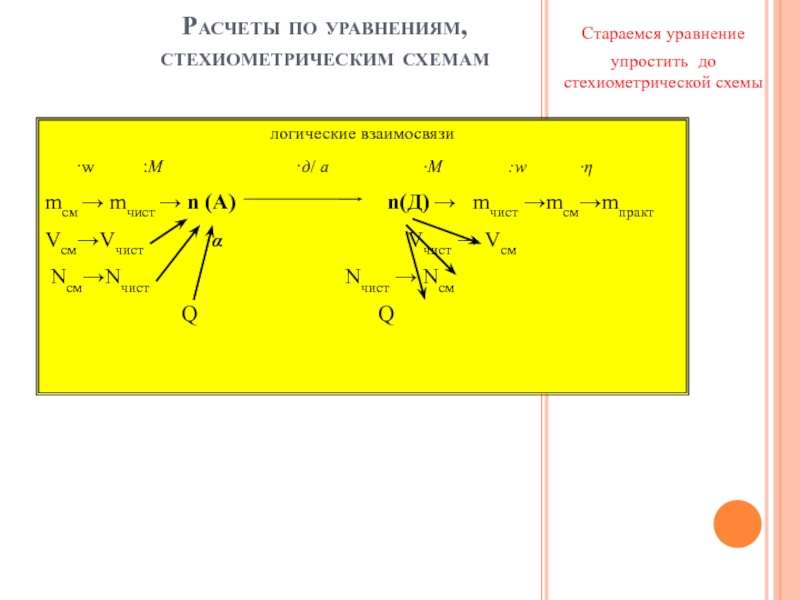
Слайд 8Расчеты по уравнениям,
стехиометрическим схемам
Стараемся уравнение
упростить до стехиометрической схемы
Слайд 9ПЗ 1.Какая масса осадка выпадет при взаимодействии
9,8 г фосфорной
кислоты с гидроксидом стронция?
ПЗ 2. Какой объем аммиака (при
н.у.) можно получить из простых веществ, если объем исходного водорода равен 300 л, а практический выход - 43 %?ПЗ 3. 200 г известняка с массовой долей основного компонента 54% и некарбонатными примесями обработали иодоводородной кислотой, полученное вещество осторожно выпарили. Потери в синтезе составили 5%. Какова масса полученной соли.
Слайд 10ПЗ 4. Молярная теплота сгорания водорода -142,2 КДж/моль. Какой объем
кислорода необходим, чтобы при сжигании водорода получить 2844 кДж тепла,
если потери тепла в этом процессе составят 20%?ПЗ 5. Мольная доля кислорода в воздухе – 0,208. Какой объем воздуха необходим для сгорания 5,6 м3 природного газа с 1% негорючих примесей? Какая теплота при этом может быть получена, если при сгорании 1,6 г основного компонента природного газа выделяется 89,1 кДж?
Слайд 11ПЗ 6. Какова массовая доля серной кислоты, если в процессе
ее полного взаимодействия её с оксидом алюминия массой 14,2 г
было получено 524,2 г раствора?ПЗ 7 Какую массу (т) магнетита с массовой долей основного компонента 87% необходимо взять для получения 1 тонны стали, содержащей 0,5% нежелезных примесей, если выход процесса составляет 75%.
Слайд 12Суббота
Введение в химию 15 сентября в 12-00 (501 ауд)
Органическая химия
15 сентября в 10-00 (507 ауд) Неорганическая химия 15 сентября в
12-00 (507 ауд) Углубленный курс химии 15 сентября в 14-00 (507 ауд)Слайд 14РАСТВОРЫ
приготовление, смешение, выпадение осадка при охлаждении
Сколько воды надо добавить к
50 г 15%-ного раствора хлорида натрия, чтобы получить 10% раствор.
Решение:0,1=(50·0,15)/(50+х) => х=25 г
Слайд 15
Какую массу кристаллической соды необходимо растворить в 200 г воды,
чтобы при добавлении данного раствора в 50 г раствора с
массовой долей карбоната натрия 10% получить 20% раствор?Решение: x∙0,371+ 50 ∙0,1 х=
х+200+50
=0,2
Слайд 16Смешали 300 г 50%-ного раствора гироксида натрия и 500 мл
20%-ного раствора (плотность 1,1 г/см3) Какова массовая доля полученного раствора?
Какие объемы 20 %-ного (ρ=1,15) и
5 %-ного (ρ=1,05) растворов соли необходимо смешать для получения 300 г 8%-ного раствора?
Слайд 17В каком соотношении масс необходимо взять 10%-ный раствор сульфата меди
и медного купороса, чтобы получить 30%-ный раствор?
Решение. Необходимо найти соотношение
Пусть m1= х, а m2=1, тогда
Слайд 18
Определите концентрацию раствора фосфорной кислоты, полученного сливанием
200 мл 0,3-молярного
р-ра и 300 мл 0,6-молярного р-ра. Какая массовая и мольная
доля фосфорной кислоты в полученном растворе?Слайд 19Какая масса осадка образуется при охлаждении 250 г 30%-ного раствора
сульфата калия до 20 C0, если растворимость при данной температуре
соли составляет 21,4 г на 100 г растворителя?Решение:
w20= 21,4/121,4=(250·0,30 – х)/(250–х) => х=
ОХЛАЖДЕНИЕ РАСТВОРОВ
(нагревание р-ров газов, осушение, упаривание растворов)
Слайд 20Приготовили 200 г насыщенного при 60 0С раствора сульфата меди.
Какая масса медного купороса выкристаллизуется из раствора при охлаждении его
до 0 0C? Растворимость сульфата меди при 60 0С равна 39,5 г, а при 0 0C – 14,3 г на 100 г воды.Какая масса КГ выпадет, если перед охлаждением испарить 10% массы воды, находящейся раствора?
Решение:
0,125=(200∙0,283– х∙0,64)/200-х =>х=