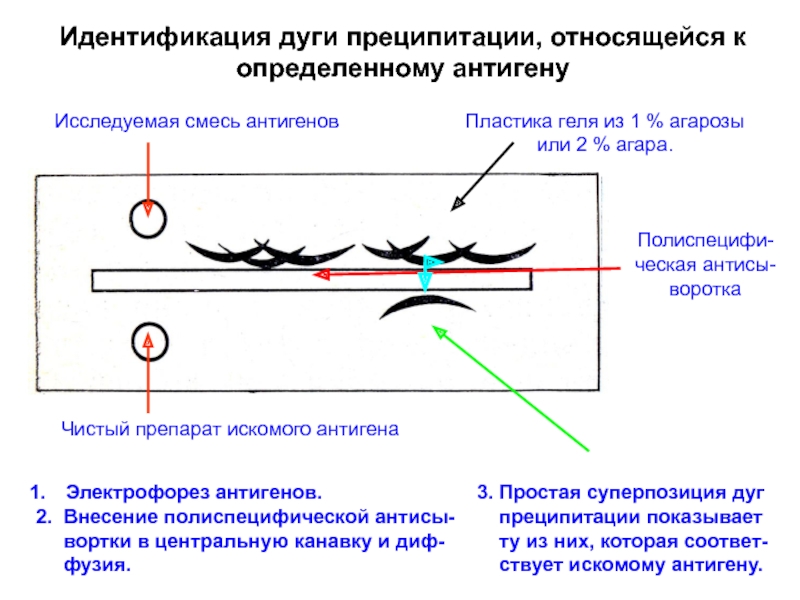
действием сил постоянного электрического поля
Метод был предложен Тизелиусом для разделения
заряженных молекул (1925г.).В 1948 году Тизелиус получил Нобелев-скую премию за разработку методов электрофоретического разделения белков.