Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Электролиз
Содержание
- 1. Электролиз
- 2. ЭлектролизЭлектролиз – окислительно-восстановительный процесс, протекающий на электродах
- 3. Перемещение ионов в электролите под дейст-вием электрического
- 4. Процесс на катодеЕсли в растворе ионы Н+
- 5. Процесс на анодеесли анод растворяется (железо, цинк,
- 6. Если анод не растворяется (его называют инертным
- 7. Анионы бескислородных кислот (кроме F-)Разряжаются до простого
- 8. Закон электролизаЗаконы Фарадея.Масса веществ, выделившегося на электроде
- 9. Применение электролизаДля получения щёлочных, щёлочноземельных металлов, алюминия,
- 10. Конец
- 11. Скачать презентанцию
Слайды и текст этой презентации
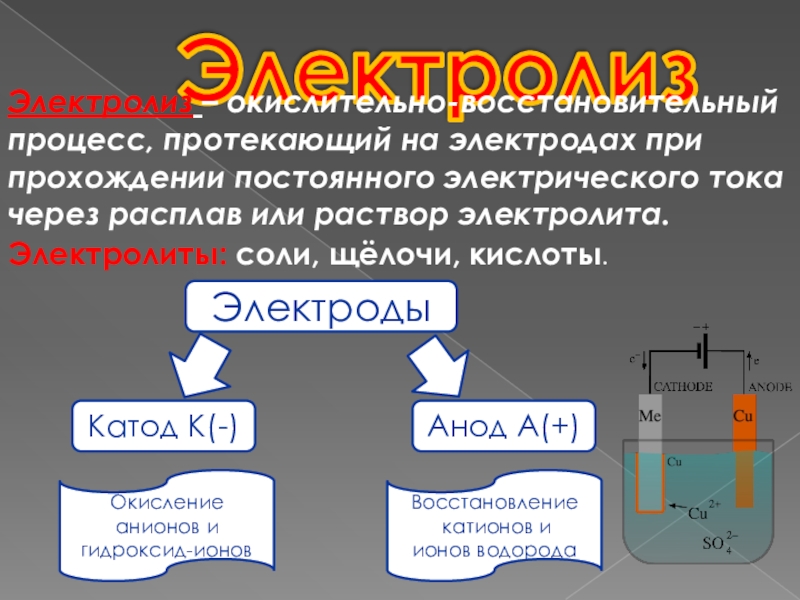
Слайд 2Электролиз
Электролиз – окислительно-восстановительный процесс, протекающий на электродах при прохождении постоянного
электрического тока через расплав или раствор электролита.
Слайд 3Перемещение ионов
в электролите под дейст-
вием электрического поля
Анод – это
положительно- заряженный электрод
Катод -это отрицательно - заряженный электрод
Слайд 4Процесс на катоде
Если в растворе ионы Н+ - они разряжаются
до Н2
Металлы правее Н:
Разряжаются на катоде - Ме
Men+ +
ne- → Me0Металлы от Al до Н :
Идет 2 параллельных процесса:
А) разрядка металла – Мe
Б) разрядка воды – Н2
Men+ + ne- → Me0
2H2O + 2e- → H20↑+ 2OH-
Металлы левее Al
Восстанавливаются молекулы воды – Н2М
2H2O + 2e- → H20↑+ 2OH-
Слайд 5Процесс на аноде
если анод растворяется (железо, цинк, медь, серебро и
все металлы, которые окисляются в процессе электролиза), то окисляется металл
анода, несмотря на природу аниона;Слайд 6Если анод не растворяется (его называют инертным — графит, золото,
платина)
Процесс на аноде
Анионы бескислородных кислот (кроме F-)
Анионы кислородсодержащих кислот и
F-Анионы карбоновых кислот – реакция Кольбе
Слайд 7Анионы бескислородных кислот (кроме F-)
Разряжаются до простого вещества: S2-, I-,
Br-, СI-
2Hal- -2e- → Cl02
Процесс на аноде
Анионы кислородсодержа-щих кислот и
F-Не разряжаются,
идет разрядка воды – О2
2 H2O - 4e- → О20↑ + 4H+
2 H2O - 4e- → О20↑ + 4H+
Анионы карбоновых кислот – реакция Кольбе
Происходит процесс декарбоксилирования и выделяется алкан
2СН3СОО- - 2е- → 2 СО2 + СН3-СН3
Слайд 8Закон электролиза
Законы Фарадея.
Масса веществ, выделившегося на электроде при электролизе, пропорциональна
количеству электричества, прошедшее через электролит. m–масса веществ продуктов электролиза, гр.
Э
– эквивалентная масса вещества, гр.I – сила тока, А.
F – постоянная Фарадея = 96500 Кл.
t – время электролиза, сек.