Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Геосферы планеты Земля и проблемы устойчивого развития
Содержание
- 1. Геосферы планеты Земля и проблемы устойчивого развития
- 2. Слайд 2
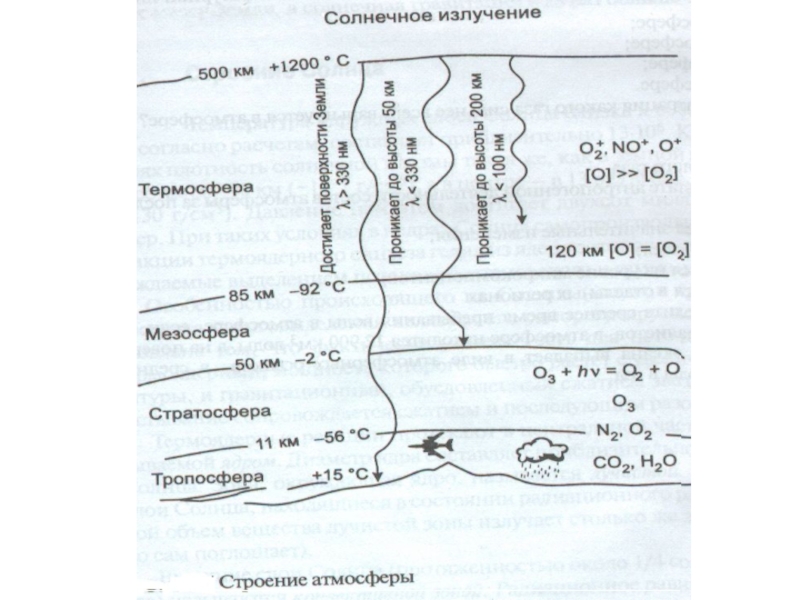
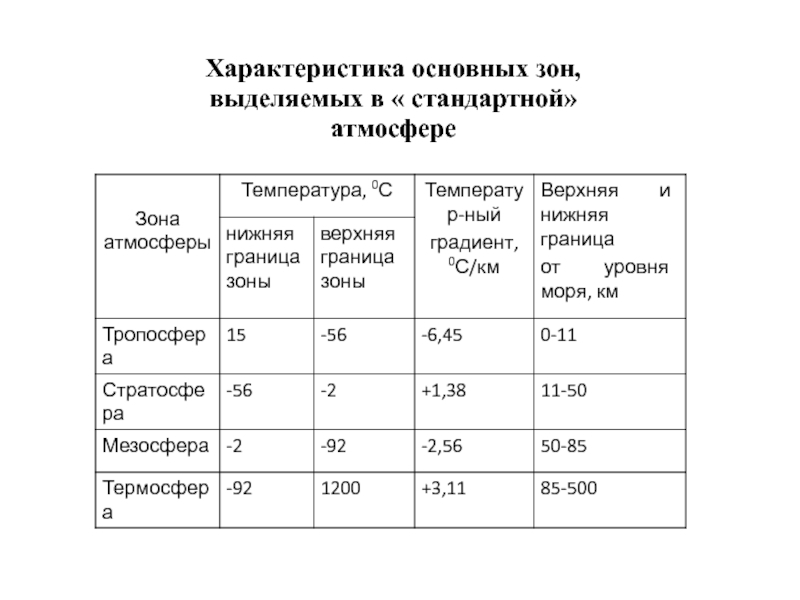
- 3. Характеристика основных зон, выделяемых в « стандартной» атмосфере
- 4. Тропосфера Тропосфера – нижний, непосредственно соприкасающийся с
- 5. Процессы окисления примесей в тропосфере Протекают по
- 6. Концентрация примесей в тропосфере
- 7. Образование гидроксидного радикала в тропосфереO(1D)+Н2О = O(1D)+
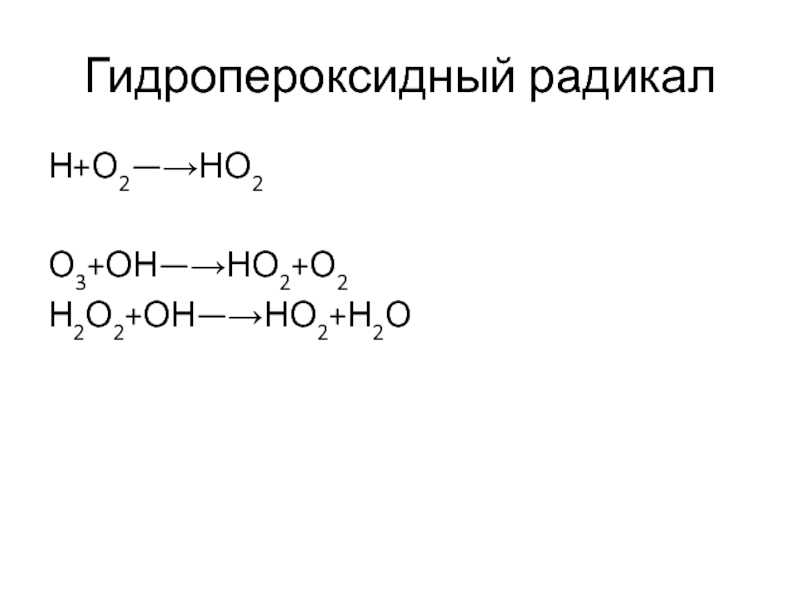
- 8. Гидропероксидный радикалН+О2—→НО2 О3+ОН—→НО2+О2 Н2О2+ОН—→НО2+Н2О
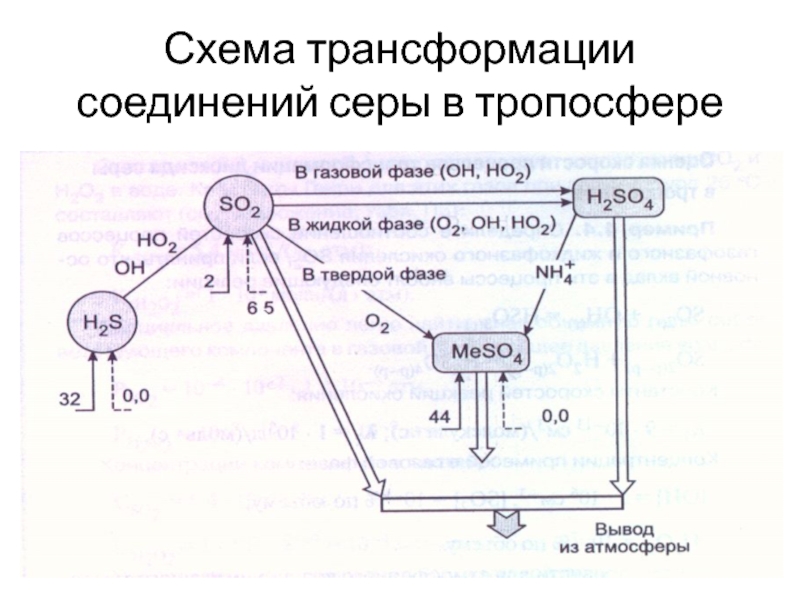
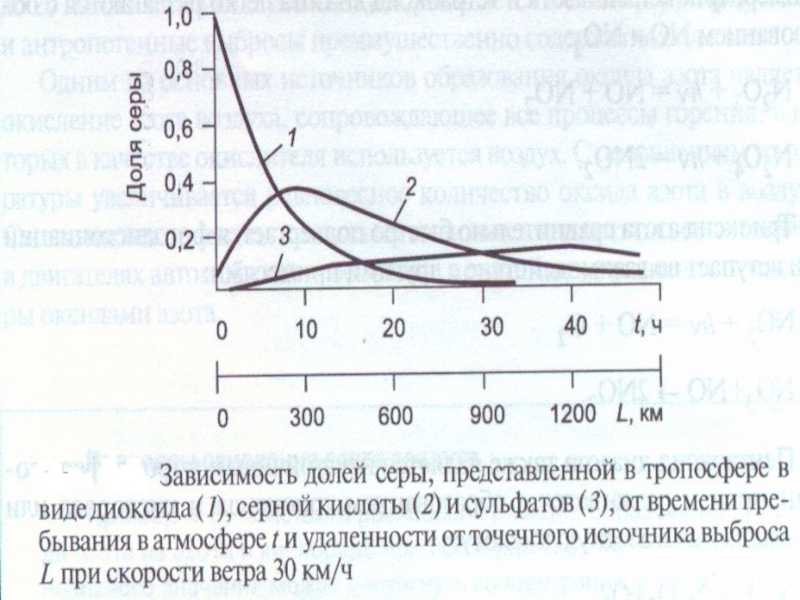
- 9. Схема трансформации соединений серы в тропосфере
- 10. Антропогенные источники серы В природе нет ископаемого
- 11. Антропогенные источники серыСырьем для получения меди, свинца
- 12. Слайд 12
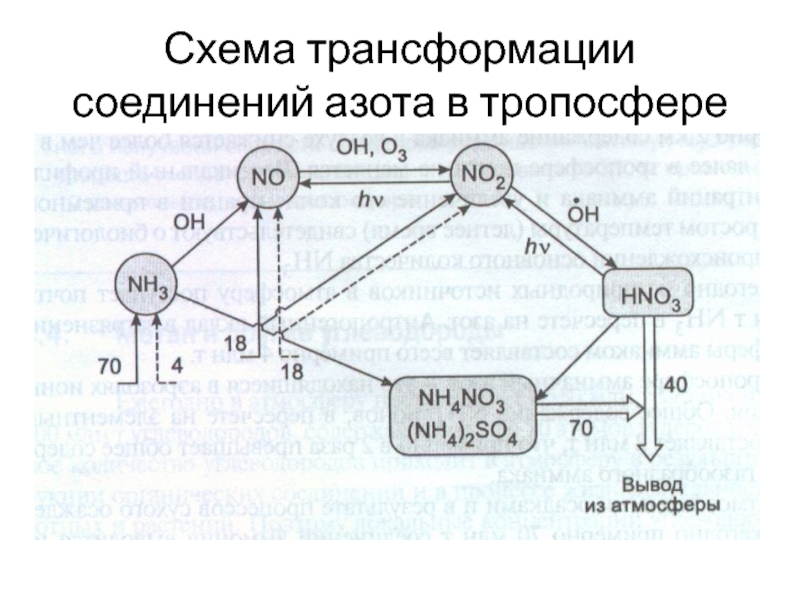
- 13. Схема трансформации соединений азота в тропосфере
- 14. Доля метана, выделяющегося из различных источников, %
- 15. CH4 + OH CH3 +H2 O
- 16. Градиент температуры и устойчивость атмосферы. .____ градиент температуры в окружающем воздухе; ------ адиабатический вертикальный градиент температуры
- 17. Слайд 17
- 18. Слайд 18
- 19. Смог в городской атмосфереПонятие "смог"* впервые было
- 20. Изменение концентрации примесей во времени при облучении разбавленных выхлопных газов автомобилей
- 21. С присутствием органических соединений в воздухе городов
- 22. Высокотоксичные соединения в атмосфере В последние
- 23. Полиядерные ароматические углеводороды нафталин
- 24. Присутствующие в атмосфере в газовой фазе ПАУ
- 25. Галогенсодержащие суперэкотоксиканты Все наиболее опасные из
- 26. Слайд 26
- 27. Диоксины и дибензофураны. К этим хлорорганическим соединениям
- 28. дибензо-п-диоксин
- 29. Тяжелые металлы в атмосфере Поскольку одна
- 30. В целом эта группа суперэкотоксикантов имеет широкий
- 31. Концентрации некоторых тяжелых металлов в природных районах и на урбанизированных территориях Северной Америки и Европы
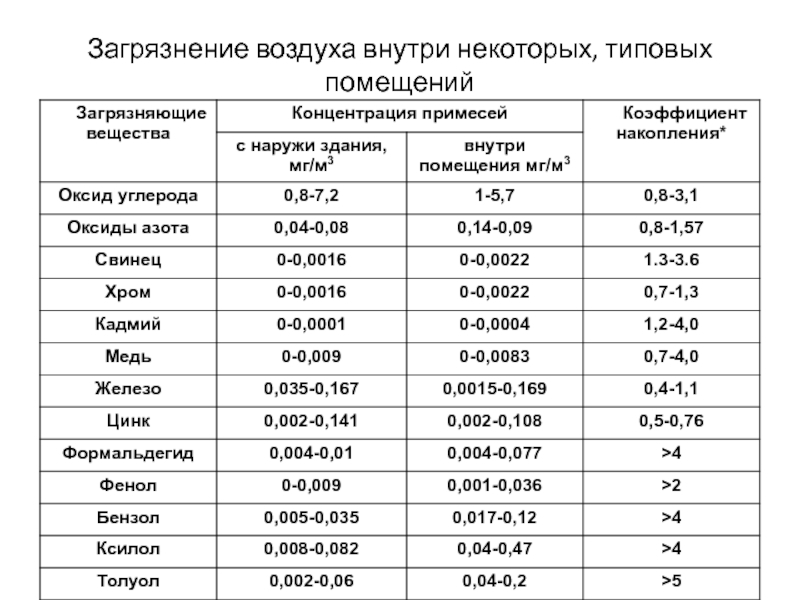
- 32. Загрязнение воздуха внутри некоторых, типовых помещений
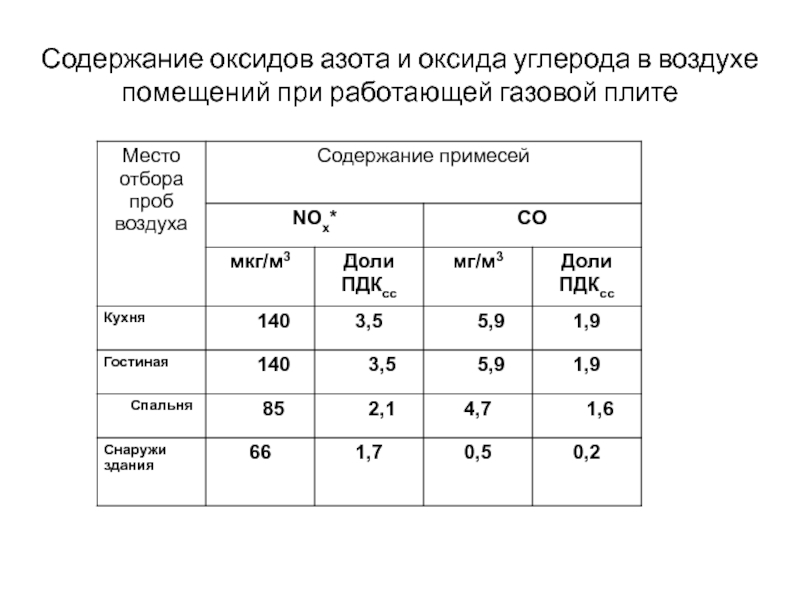
- 33. Содержание оксидов азота и оксида углерода в воздухе помещений при работающей газовой плите
- 34. Аэрозоли в атмосфереАэрозолями называют дисперсные системы, содержащие
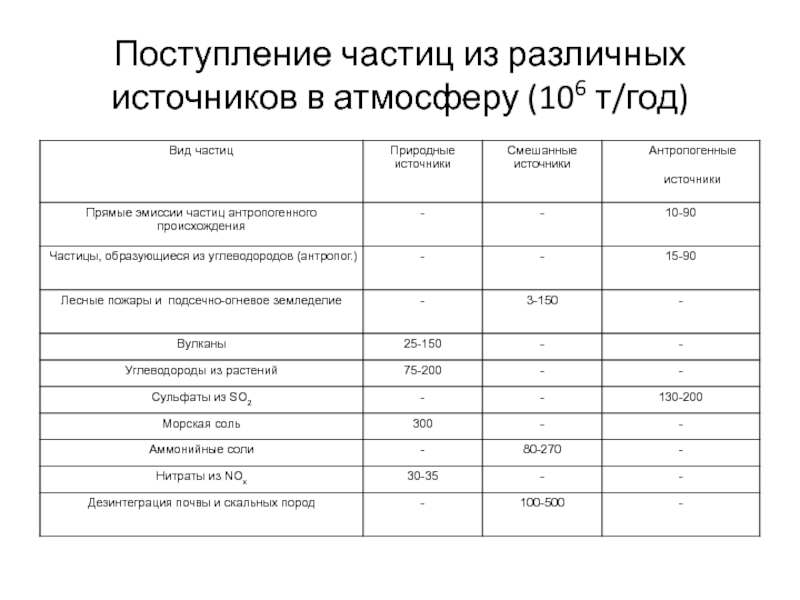
- 35. Поступление частиц из различных источников в атмосферу (106 т/год)
- 36. Критерии устойчивости аэрозольных частицДля существования устойчивого аэрозоля
- 37. Слайд 37
- 38. По типу происхождения и по
- 39. Крупные частицы — больше чем 100 микрон.Быстро
- 40. Средний размер частиц — в пределах до
- 41. Мелкие частицы — менее 1 микронаОтносятся к
- 42. Классификация частиц по размерамЯдра Айткена
- 43. Концентрация аэрозолей (см-3)Антарктида
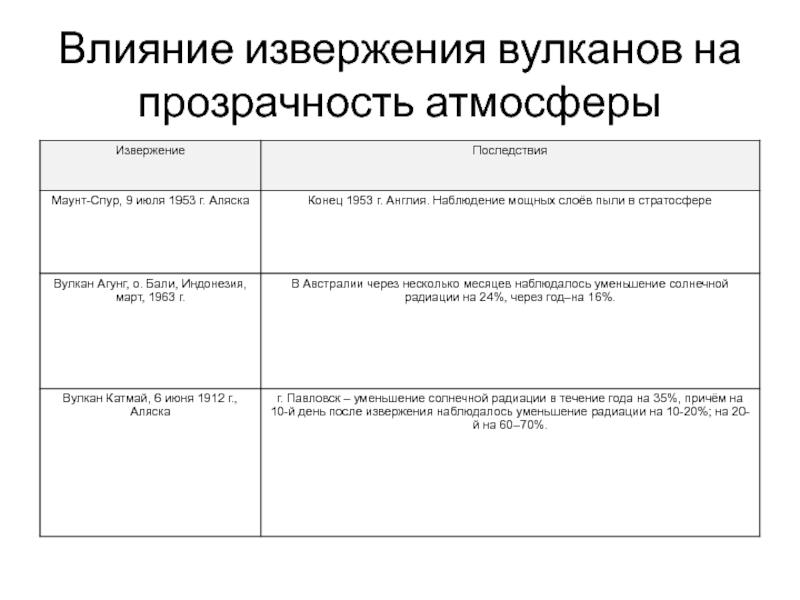
- 44. Влияние извержения вулканов на прозрачность атмосферы
- 45. Радиационный балансQприход = Q расходQприход= I*Sпроекции*(1-А)Q расход= Sземли*σ*Т4Т = [I*(1-A)/4 σ]1/4T = 2520K
- 46. Слайд 46
- 47. Слайд 47
- 48. Парниковый эффектПарниковым может считаться любой газ, поглощающий
- 49. Концентрация СО2 (ppm)180 тыс. лет назад
- 50. Поступления СО2 (млрд.т/год)Природные источники
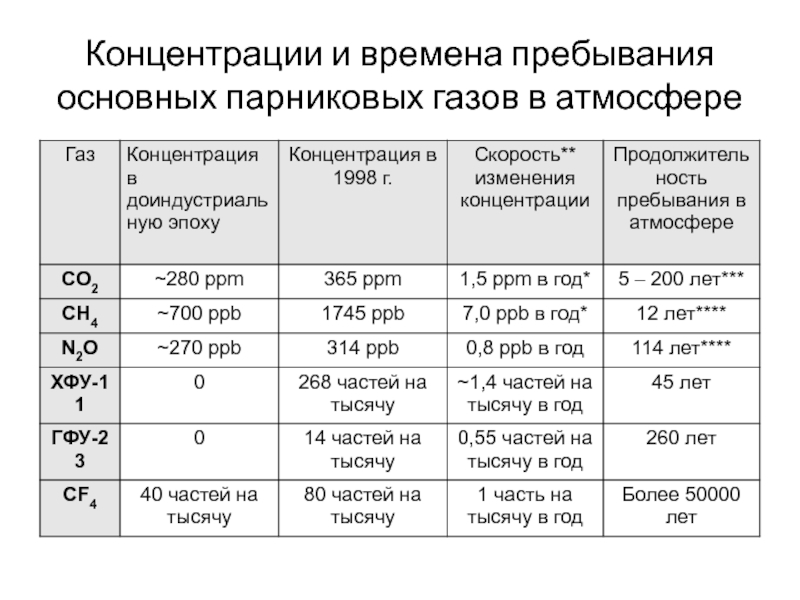
- 51. Концентрации и времена пребывания основных парниковых газов в атмосфере
- 52. Скачать презентанцию
Слайды и текст этой презентации
Слайд 4Тропосфера
Тропосфера – нижний, непосредственно соприкасающийся с земной поверхностью, слой атмосферы.
Слайд 5Процессы окисления примесей в тропосфере
Протекают по различным направлениям:
1) Окисление
непосредственно в газовой фазе;
2) Окислению предшествует абсорбция частицами воды, и
в дальнейшем процесс окисления протекает в растворе;3) Окислению предшествует адсорбция примесей на поверхности твердых частиц, взвешенных в воздухе.
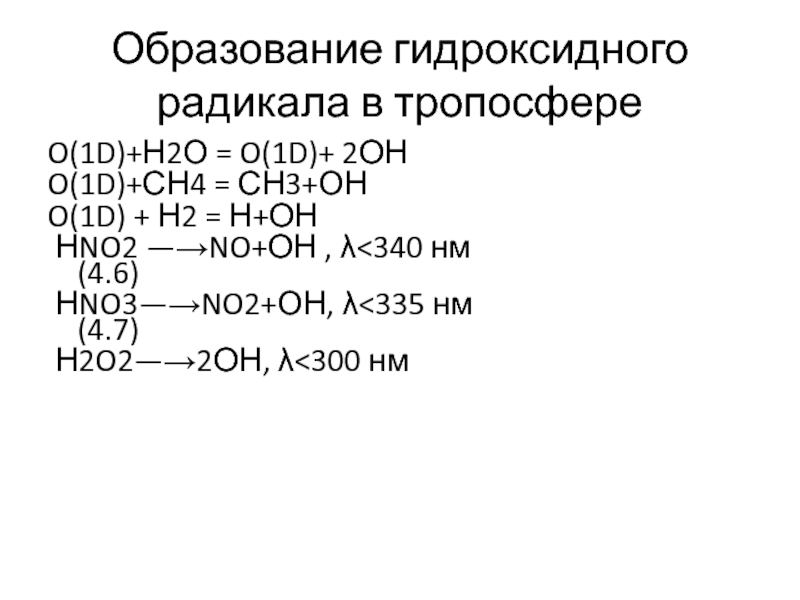
Слайд 7Образование гидроксидного радикала в тропосфере
O(1D)+Н2О = O(1D)+ 2ОН
O(1D)+СН4 = СН3+ОН
O(1D)
+ Н2 = Н+ОН
НNO2 —→NO+ОН , λ
НNO3—→NO2+ОН, λ<335 нм (4.7)Н2O2—→2ОН, λ<300 нм
Слайд 10Антропогенные источники серы
В природе нет ископаемого топлива, которое состояло
бы из одних углеводородов. Всегда имеется примесь других элементов, и
один из них — сера.Даже природный газ содержит по крайней мере следы серы.
В сырой нефти, в зависимости от месторождения, содержится
от 0,1 до 5,5 процента серы;
уголь содержит от
0,2 до 7 процентов серы.
Сжигание топлива дает 80—90 % всего антропогенного сернистого газа,
причем больше всего (70 процентов и более) дает сжигание угля.
10—20 процентов приходятся на выплавку цветных металлов и производство серной кислоты.
Слайд 11Антропогенные источники серы
Сырьем для получения меди, свинца и цинка служат
главным образом руды, содержащие большое количество серы (до 45 процентов).
Эти руды и другие богатые серой минералы служат сырьем для получения серной кислоты.
Слайд 15CH4 + OH CH3 +H2 O
CH3 + O2
CH3 OO
CH3 OO + NO CH3 O
+ NO2 CH3 O + O2 CH2 O + HO2
HO2 + NO NO2 + OH
CH4 + 2O2 CH2 O + H2O + 2O3
CH2 O +OH H2 O + HCO
HCO + O2 HO2 + CO
HO2 + NO NO2 + OH
CH2 O + 2O2 CO +H2O +O3
CO +OH CO2 + H
H + O2 HO2
CO + 2O2 CO2 +O3
HO2 + NO NO2 + OH
4(NO2 + h ) 4(NO+O)
4(O + O2 + M) 4 O3 + 4М*
--------------------------------------------------
Суммируя все реакции, получим:
CH4 + 8 O2 + 4 М = CO2 + 2Н2О + 4М* + 4 O3
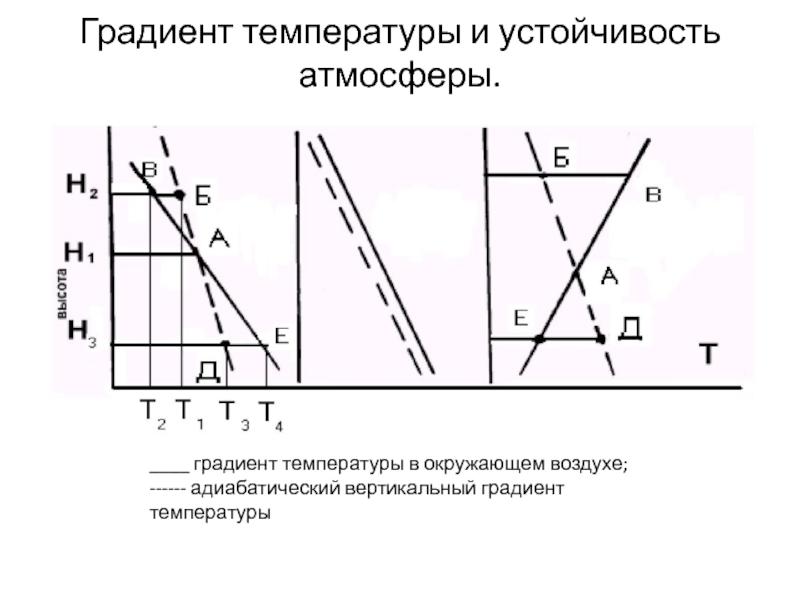
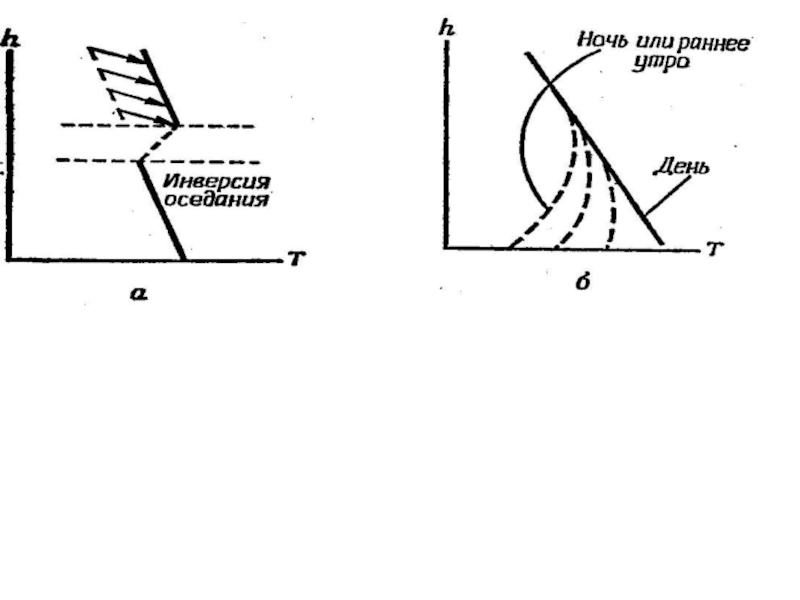
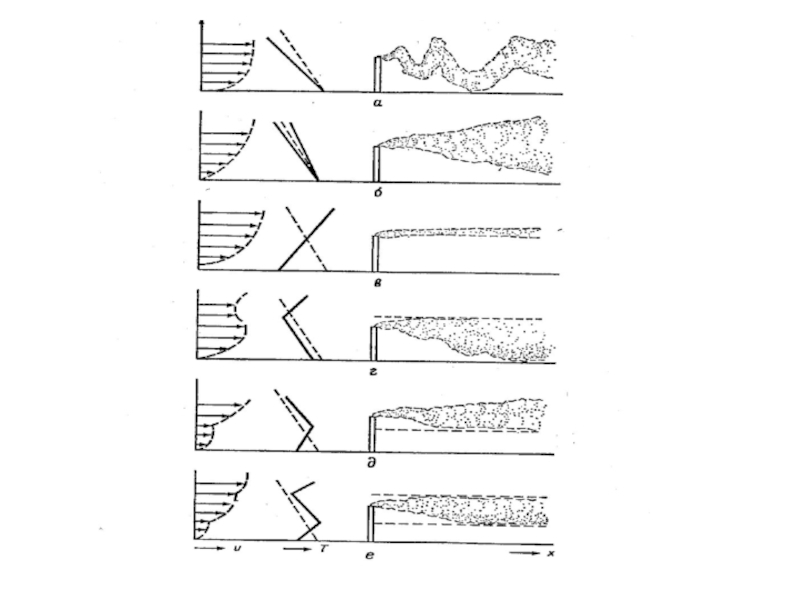
Слайд 16Градиент температуры и устойчивость атмосферы.
.
____ градиент температуры в окружающем воздухе;
------
адиабатический вертикальный градиент температуры
Слайд 19Смог в городской атмосфере
Понятие "смог"* впервые было употреблено около 100
лет назад применительно к смеси дыма и тумана, обычно имевшей
жёлтый цвет и образовывавшейся над Лондоном в периоды температурных инверсийПозже *(smog smoke + fog (англ.), дым + туман) его стали применять для характеристики задымленных или туманных условий, наблюдаемых в атмосфере и других регионов. В настоящее время различают два основных вида смога: смог, связанный с загрязнением атмосферы копотью или дымом, содержащим диоксид серы (лондонский смог), и смог, вызванный загрязнением воздуха выхлопными газами транспорта, содержащими оксиды азота (смог Лос-Анджелеса).
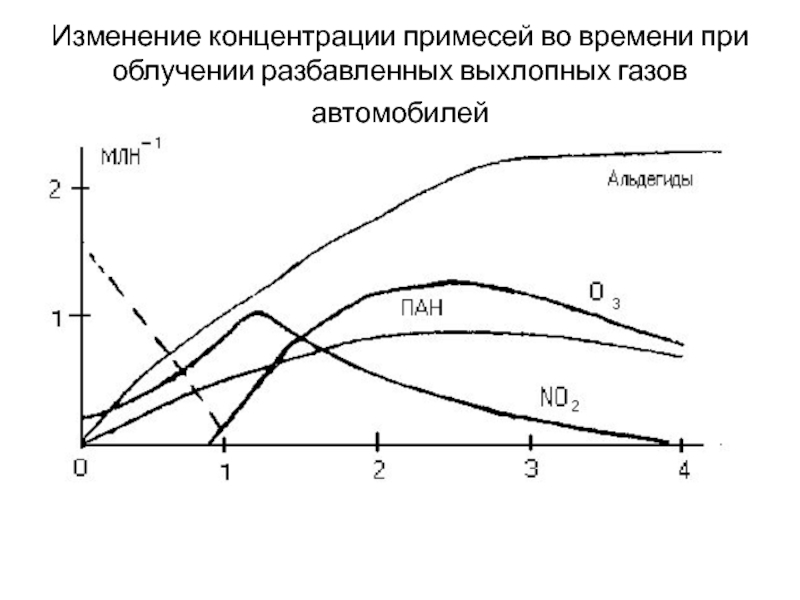
Слайд 20Изменение концентрации примесей во времени при облучении разбавленных выхлопных газов
автомобилей
Слайд 21С присутствием органических соединений в воздухе городов связаны и процессы
образования высокотоксичных пероксидных соединений:
R-С(О)-О-О-NO2
Наиболее распространенным пероксидным соединением, синтезирующимся в атмосфере,
является пероксиацетилнитрат - первый член гомологического ряда, часто сокращенно называемый ПAH, СН3-С(О)-О-О-NO2.
В случае присутствия в воздухе ароматических углеводородов возможно образование ароматических производных.
Так, например, пepoксибензоилнитрат, являющийся сильным слезоточивым газом, был идентифицирован в атмосфере Лос-Анджелеса наряду с пероксиацетилнитратом и его гомологами.
Слайд 22 Высокотоксичные соединения в атмосфере
В последние десятилетия внимание специалистов
в области охраны окружающей среды направлено на изучение химических превращений
и мониторинг высокотоксичных соединений, часто называемых суперэкотоксикантами.Среди суперэкотоксикантов следует особо упомянуть группы наиболее распространенных органических соединений – полиядерные ароматические углеводороды (ПАУ) и галогенсодержащие органические соединения, а также, соединения, содержащие тяжелые металлы.
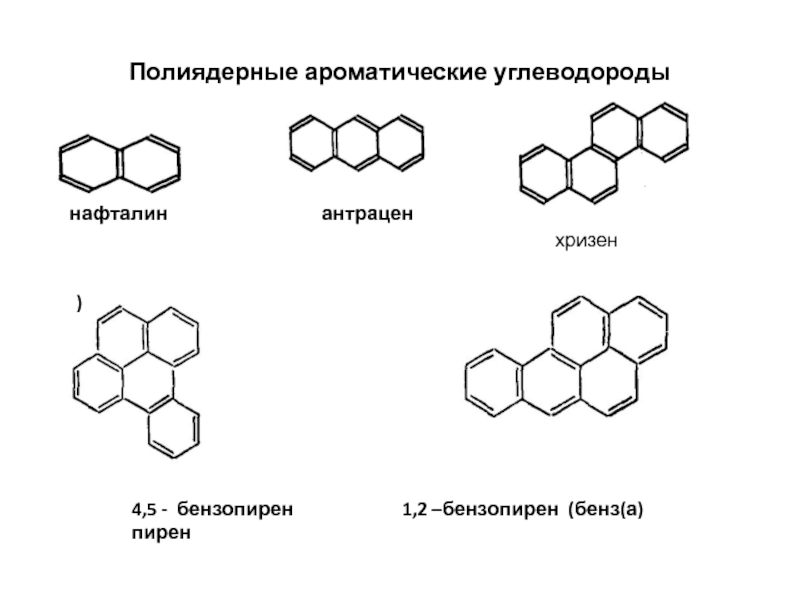
Слайд 23Полиядерные ароматические углеводороды
нафталин
антрацен
хризен
)
4,5 - бензопирен 1,2 –бензопирен (бенз(а)пирен
Слайд 24Присутствующие в атмосфере в газовой фазе ПАУ интенсивно поглощают излучение
длиной волны 320 – 400 нм и сравнительно быстро подвергаются
трансформации с образованием хинонов и карбонильных соединений.Так экспериментально установлено, что в результате 20 - минутного облучения ультрафиолетом (А) происходит разложение более 30% пирена, примерно 80% антрацена и около 50% бенз(а)пирена.
Процессы частичного окисления ПАУ приводят к появлению в отходящих газах разнообразных кислородсодержащих ПАУ (хинонов, спиртов, альдегидов).
В присутствии оксидов азота и озона ПАУ образуют нитро- и кислород содержащие производные.
Так, при взаимодействии с диоксидом азота в воздухе появляются обладающие высокой мутагенной и канцерогенной активностью нитробензпирены, а в присутствии озона образуются полиядерные хиноны и гидроксипроизводные бензпирена.
Слайд 25 Галогенсодержащие суперэкотоксиканты
Все наиболее опасные из этих соединений попадают
в список так называемой «грязной дюжины», в который эксперты UNEP
выделили 12 наиболее опасных стойких органических загрязнителей (СОЗ). В целом к СОЗ (в английском варианте – Persistent organic pollutants (POPs) относятся вещества, которые отвечают следующим требованиям:Являются токсичными;
Являются устойчивыми в окружающей среде;
Способны к биоаккумуляции;
Склонны к трансграничному переносу и к накоплению в окружающей среде;
Являются причиной значительного вредного воздействия на здоровье человека или на окружающую среду вследствие его трансграничного распространения.
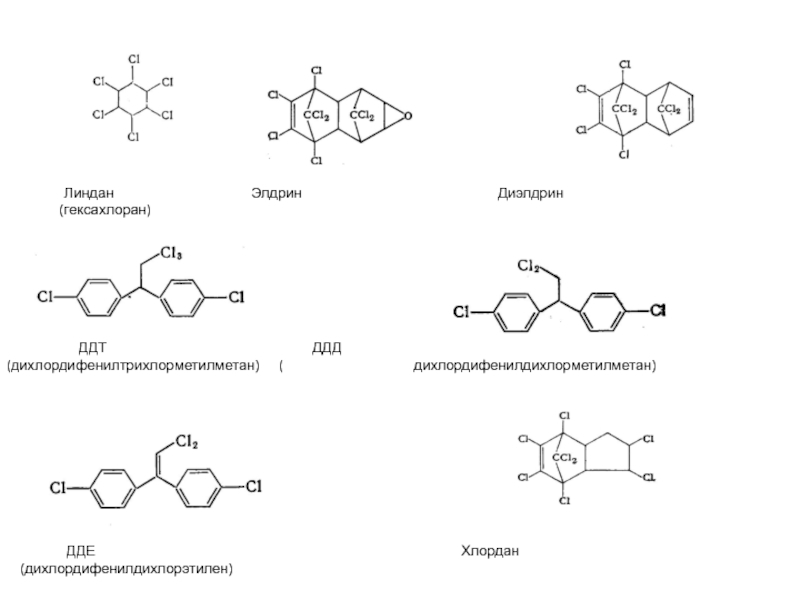
Слайд 26
Линдан
Элдрин Диэлдрин(гексахлоран)
ДДТ ДДД
(дихлордифенилтрихлорметилметан) ( дихлордифенилдихлорметилметан)
ДДЕ Хлордан
(дихлордифенилдихлорэтилен)
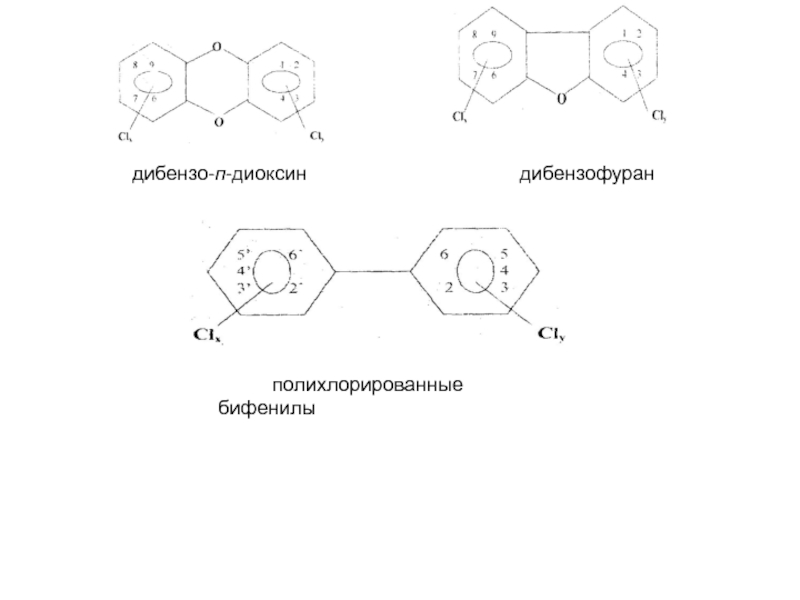
Слайд 27Диоксины и дибензофураны
. К этим хлорорганическим соединениям относится большая группа
гетероциклических полихлорированных соединений, основу которых составляют два ароматических кольца, соединенные,
в случае диоксинов, или правильнее, дибензо-п-диоксинов (ПХДД), двумя кислородными мостиками, и, в случае дибензофуранов (ПХДФ), одним кислородным мостиком, содержащих от одного до 8 атомов хлора.К этой группе хлорорганических соединений часто относят хотя и менее токсичные, но выпускаемые в промышленных масштабах полихлорированные бифенилы (ПХБ), в которых два бензольных кольца непосредственно связаны друг с другом
Слайд 29 Тяжелые металлы в атмосфере
Поскольку одна из важнейших особенностей
элементов, объединяемых в группу «тяжелых металлов» связана с их опасностью
для человека, представляется целесообразным учитывать не только плотность и атомную массу элемента, но и такие характеристики, как –токсичность, стойкость, способность накапливаться в окружающей среде и масштабы использования металлов.
По этим признакам в группу «тяжелых металлов» относят -
свинец, ртуть, кадмий, цинк, висмут, кобальт, никель, медь, олово, сурьму, ванадий, марганец, хром, молибден, мышьяк и, часто, сравнительно легкий алюминий.
Слайд 30В целом эта группа суперэкотоксикантов имеет широкий спектр токсического действия,
в некоторых случаях они проявляют канцерогенные свойства. Хотя у различных
видов живых организмов нет единого порядка чувствительности по отношению к тяжелым металлам, по этому показателю их часто располагают в следующей последовательности:Hg > Cu > Zn > Ni > Pb > Cd > Cr > Sn > Fe > Mn > Al.
Необходимо помнить, что опасность воздействия тяжелых металлов на организмы и их способность мигрировать в окружающей среде во многом зависит от вида соединений в состав, которого они входят. Поэтому при контроле качества тех или иных сред и продуктов нельзя ограничиваться лишь определением их валового содержания. Следует определить и дифференцировать структуры соединений, в которые входят конкретные тяжелые металлы.
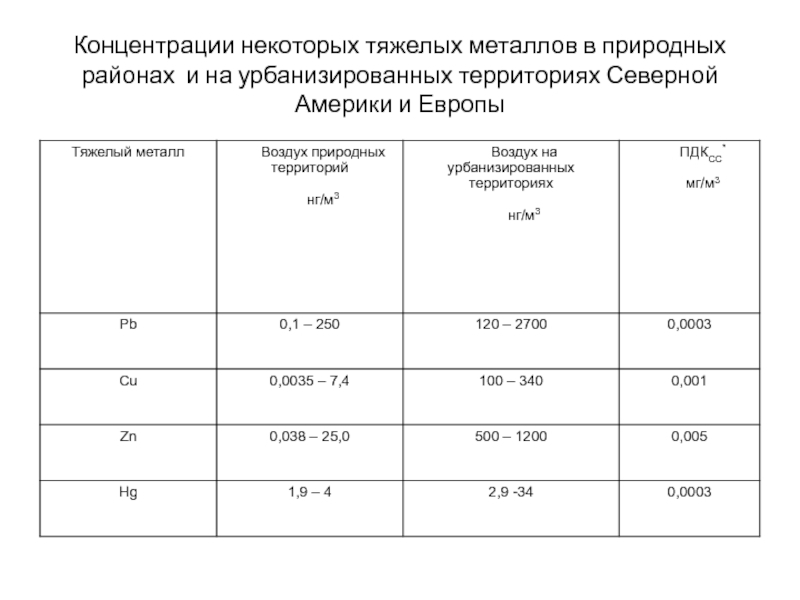
Слайд 31Концентрации некоторых тяжелых металлов в природных районах и на урбанизированных
территориях Северной Америки и Европы
Слайд 34Аэрозоли в атмосфере
Аэрозолями называют дисперсные системы, содержащие твердые или жидкие
частицы, суспендированные в газовой фазе.
Твердая фаза представляет собой
продукты конверсии примесей, либо частицы золы и минеральной пыли. Жидкая фаза состоит из воды, продуктов превращения примесей и растворимых компонентов.
Превращения примесей сопровождаются постоянным взаимодействием между газовой, жидкой и твердой фазами, присутствующими в тропосфере.
Химические реакции, протекающие в этих сложных системах, часто называют гетерогенными химическими реакциями.
Слайд 36Критерии устойчивости аэрозольных частиц
Для существования устойчивого аэрозоля (аэродисперсной системы) необходимы
следующие условия:
1) скорость седиментации частиц мала;
2) силами инерции при
перемещении частиц можно пренебречь (отношение сил инерции к силам вязкости мало);3) броуновское движение частиц весьма эффективно;
4) система характеризуется высокой удельной поверхностью.
Слайд 38 По типу происхождения и по размерам аэрозоли обычно
подразделяют на две большие группы: микро- и макрочастицы.
Микрочастицы радиуса
меньше 0,5 -1,0 мкм образуются в процессах коагуляции и конденсации, тогда как макрочастицы возникают в основном при дезинтеграции поверхности Земли.Слайд 39Крупные частицы — больше чем 100 микрон.
Быстро падают из воздуха
(оседают на пол и горизонтальные поверхности)
включают волосы, снег, грязь от
насекомых, комнатную пыль, скопление сажи, крупный песокМогут попасть в нос и рот в процессе дыхания. Эффективно задерживаются в дыхательных путях и бронхах, не проникая в легкие. Опасны в очень больших концентрациях, увеличивают нагрузку на дыхательные пути, могут вызывать рак, аллергические реакции.
Задерживаются обычными фильтрами грубой очистки.
Слайд 40Средний размер частиц — в пределах до 10 микрон.
Относятся к
PM10 по принятой классификации размеров частиц.
Медленно падают из воздуха (оседают на
пол и горизонтальные поверхности)Это - цветочная пыльца, большие бактерии, частицы золы в воздухе, угольную пыль, мелкий песок, и мелкая пыль
Частицы, которые через дыхательные пути попадают в легкие, но не попадают в зону газообмена и не всасываются в кровь. Зашлаковывают легкие, могут вызывать рак, астму, аллергические реакции.
Задерживаются фильтрами тонкой очистки.
Слайд 41Мелкие частицы — менее 1 микрона
Относятся к PM1 по принятой классификации
размеров частиц.
Очень медленно падают из воздуха (оседают на пол и
горизонтальные поверхности).В спокойной атмосфере процесс оседания может занять от дней до нескольких лет.
В возмущенной атмосфере они могут никогда не осесть.
Включает вирусы, мелкие бактерии, металлургическую копоть, сажу, пары масла, табачный дым, копоть.
Эти частицы проникают в зону легких, отвечающую за газообмен.
Через альвеолы могут всасываться в кровь, вызывая зашлаковывание сердечно-сосудистой системы, аллергические реакции, интоксикацию адсорбированными на поверхности частиц химическими соединениями.
Задерживаются фильтрами высокой эффективности.
Слайд 42Классификация частиц по размерам
Ядра Айткена
менее 0,1 мкм
Большие частицы от
0,1 до 1 мкмГигантские частицы более 1 мкм
Слайд 43Концентрация аэрозолей (см-3)
Антарктида
100 -1000
Природные территории 1000 – 10000
Городской воздух 10 млн.
-------------------------------------------------------------------
Ядра Айткена Большие Гигантские
N (см-3) 105 100 1
N (мкг/м3) 40 20 20
Слайд 45Радиационный баланс
Qприход = Q расход
Qприход= I*Sпроекции*(1-А)
Q расход= Sземли*σ*Т4
Т = [I*(1-A)/4
σ]1/4
T = 2520K
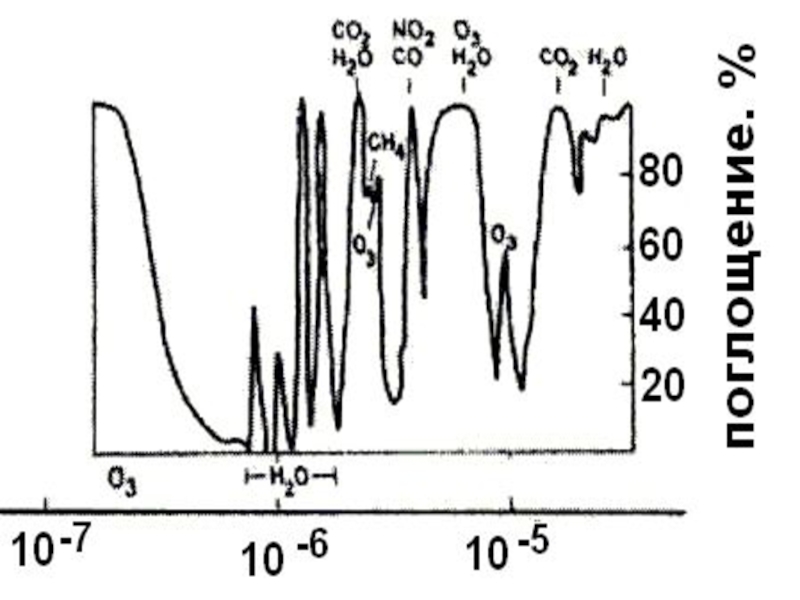
Слайд 48Парниковый эффект
Парниковым может считаться любой газ, поглощающий в ИК-области и
содержащийся в сколь угодно малых количествах в атмосфере.
водяной пар,
находящийся в атмосфереуглекислый газ (диоксид углерода) (СО2),
метан (СН4),
оксиды азота, в особенности N2O
озон (О3)
хлорфторуглероды
Слайд 50Поступления СО2 (млрд.т/год)
Природные источники
100
Антропогенные поступления 5,7
В том
числе (%):Производство энергии 22
Транспорт 22
Промышленность 15
ЖКХ 15
Уничтожение лесов 26

























![Геосферы планеты Земля и проблемы устойчивого развития Радиационный балансQприход = Q расходQприход= I*Sпроекции*(1-А)Q расход= Sземли*σ*Т4Т = [I*(1-A)/4 σ]1/4T = 2520K Радиационный балансQприход = Q расходQприход= I*Sпроекции*(1-А)Q расход= Sземли*σ*Т4Т = [I*(1-A)/4 σ]1/4T = 2520K](/img/thumbs/7ef2bd0b247d478e8e28fe4111ac3ef7-800x.jpg)