Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Гетерогенные равновесия и процессы в растворах электролитов
Содержание
- 1. Гетерогенные равновесия и процессы в растворах электролитов
- 2. Изолированное гетерогенное равновесие …… равновесие, которое устанавливается
- 3. Направление гетерогенного равновесияОпределяется соотношением констант растворимости и произведениями концентраций ионов (Пс).
- 4. Факторы, влияющие на растворимость и образование осадковВведение
- 5. Факторы, влияющие на растворимость и образование осадковКислотность
- 6. Совмещённые гетерогенные равновесияВозможны 2 варианта совмещённых гетерогенных
- 7. Совмещённые гетерогенные равновесияПри невыполнении данного условия выполняется
- 8. Термодинамика остеогенезаОбразование костной ткани происходит при рН
- 9. Термодинамика остеогенезаДалее идёт процесс депротонирования НРО42– иона
- 10. Термодинамика остеогенезаУвеличение концентрации ионов Са2+ в плазме
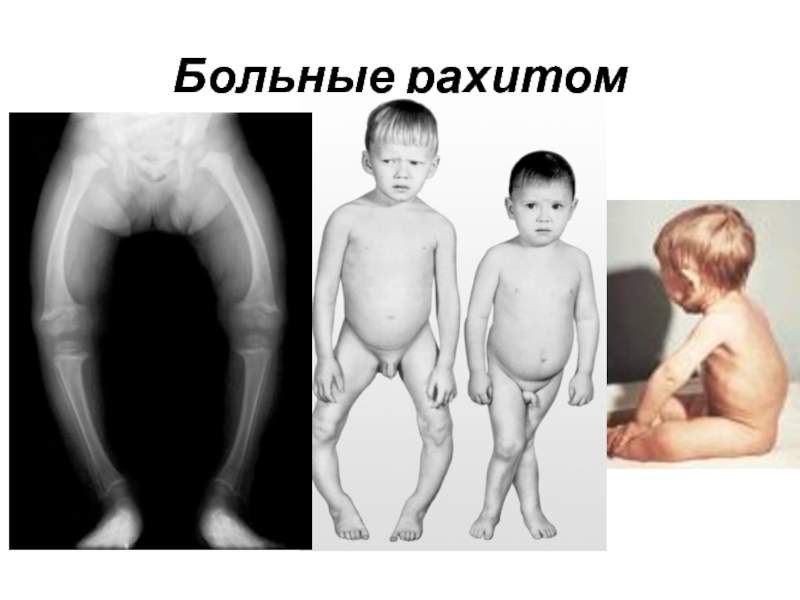
- 11. Больные рахитом
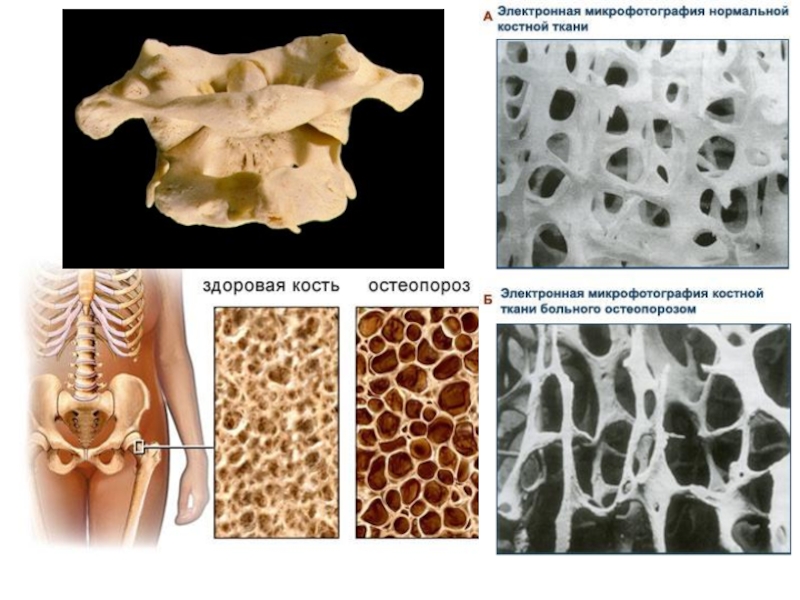
- 12. Слайд 12
- 13. Изоморфизм – …… явление замещения частиц одного
- 14. ИзоморфизмЯвление изоморфизма может оказывать и положительное влияние
- 15. Термодинамика образования конкрементовНа основе совмещённых гетерогенных равновесий
- 16. При этом в организме могут образовываться оксалатные
- 17. Основным принципом лечения мочекаменной болезни является извлечение
- 18. Спасибо за внимание!
- 19. Скачать презентанцию
Слайды и текст этой презентации
Слайд 1Гетерогенные равновесия и процессы в растворах электролитов
Лекция №3
Лектор: к.х.н.,
доцент Иванова Надежда Семёновна
Слайд 2Изолированное гетерогенное равновесие …
… равновесие, которое устанавливается в насыщенном растворе
малорастворимого вещества.
Может быть выражено уравнением:
МеАТ ↔ МеАР ↔ Ме+ +
А–→ растворение осадка;
← образование осадка
По ЗДМ для изолированного гетерогенного равновесия:
Слайд 3Направление гетерогенного равновесия
Определяется соотношением констант растворимости и произведениями концентраций ионов
(Пс).
Слайд 4Факторы, влияющие на растворимость и образование осадков
Введение одноимённого иона по
уравнению
приводит к сдвигу равновесия влево и выпадению осадка.
Влияние постороннего иона.
CaCO3
↔ Ca2+ + CO32– KS = 3,8⋅10–9BaCl2 ↔ 2Cl– + Ba2+ KS(ВаСО3)= 4,0⋅10–10
Вывод: ВаСО3 менее растворим, поэтому СаСО3 в присутствии ВаСl2 будет растворяться.
Правило перехода одного осадка в другой: для перевода одного осадка в другой необходимо, чтобы КS образовавшегося осадка был меньше КS исходного.
Слайд 5Факторы, влияющие на растворимость и образование осадков
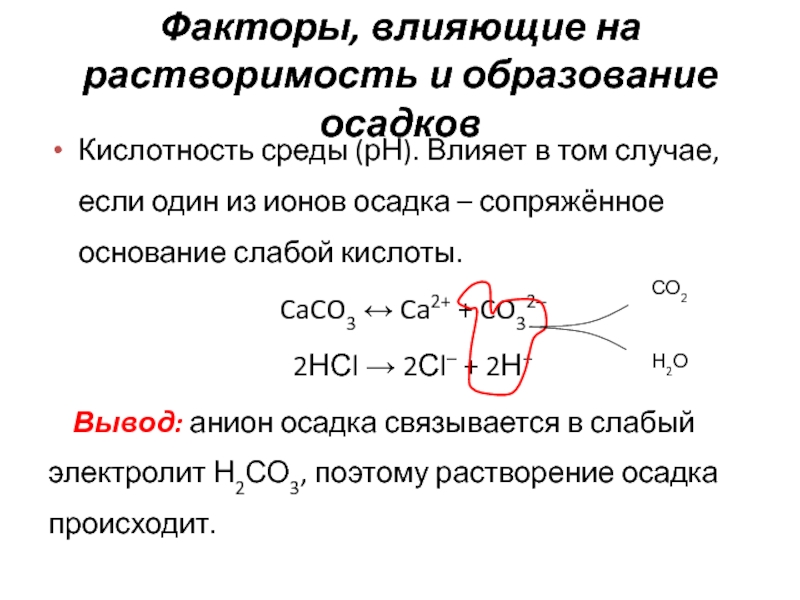
Кислотность среды (рН). Влияет
в том случае, если один из ионов осадка – сопряжённое
основание слабой кислоты.CaCO3 ↔ Ca2+ + CO32–
2НСl → 2Сl– + 2Н+
Вывод: анион осадка связывается в слабый электролит Н2СО3, поэтому растворение осадка происходит.
СО2
Н2О
Слайд 6Совмещённые гетерогенные равновесия
Возможны 2 варианта совмещённых гетерогенных равновесий:
конкуренция катионов за
анион.
Ме1+ Ме2+
А1– А2–А– Ме+
Ме1А Ме2А МеА1 МеА2
KS(Ме1А) < KS(Ме2А) KS(МеА1) < KS(МеА2)
конкуренция анионов за катион.
Вывод: в совмещённом гетерогенном равновесии доминирует тот процесс, в котором образуется осадок с меньшей КS при условии значений концентраций ионов, достаточных для достижения КS.
Слайд 7Совмещённые гетерогенные равновесия
При невыполнении данного условия выполняется правило: 2 иона
будут переходить в осадок одновременно, если отношение их концентраций равно
отношению KS их осадков.SO42– CrO42–
Ba2+
BaSO4 BaCrO4
осадки выпадают одновременно, если [SO42–] в 2 раза меньше [СrO42–]; процесс называется соосаждением осадков;
если [SO42–] / [СrO42–] > 0,5, первым выпадает BaSO4;
если [SO42–] / [СrO42–] < 0,5, первым выпадает BaCrO4.
Слайд 8Термодинамика остеогенеза
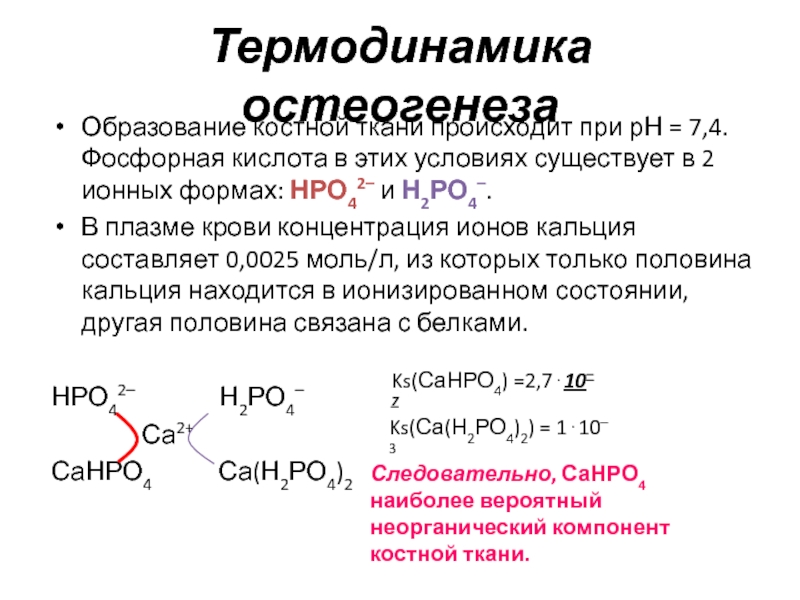
Образование костной ткани происходит при рН = 7,4. Фосфорная
кислота в этих условиях существует в 2 ионных формах: НРО42–
и Н2РО4–.В плазме крови концентрация ионов кальция составляет 0,0025 моль/л, из которых только половина кальция находится в ионизированном состоянии, другая половина связана с белками.
НРО42– Н2РО4–
Са2+
СаНРО4 Са(Н2РО4)2
Ks(СаНРО4) =2,7⋅10– 7
Ks(Са(Н2РО4)2) = 1⋅10– 3
Следовательно, СаНРО4 наиболее вероятный неорганический компонент костной ткани.
Слайд 9Термодинамика остеогенеза
Далее идёт процесс депротонирования НРО42– иона с образованием основной
соли:
3СаНРО4 + 2ОН– + Са2+ → Са4Н(РО4)3 + 2Н2О
Ca4H(PO4)3 +
2OH– + Ca2+ → Ca5(PO4)3OH + H2OРастворимость в ряду CaHPO4 → Ca4H(PO4)3 → Ca5(PO4)3OH понижается, что способствует образованию Ca5(PO4)3OH.
Наряду с гидроксидфосфатом кальция в костную ткань входит аморфный фосфат кальция (Ks(Са3(РО4)2)=2⋅10–29), который считают резервом Са2+ и фосфат-ионов в организме. С возрастом содержание Са3(РО4)2 ↓.
Ks =1,3 ⋅10–47
Ks=1,6 ⋅10–58
Слайд 10Термодинамика остеогенеза
Увеличение концентрации ионов Са2+ в плазме крови приводит к
отложению кальция в костной ткани.
Снижение концентрации ионов Са2+ в
плазме крови вызывает растворение минеральных компонентов костной ткани.Например, при рахите концентрация ионов Са2+ в плазме крови поддерживается постоянной за счет мобилизации (высвобождения) ионов Са2+ из неорганических компонентов костей.
Слайд 13Изоморфизм – …
… явление замещения частиц одного компонента в узлах
кристаллической решётки частицами другого компонента. Замещающие и замещаемые частицы должны
быть близки по кристаллохимическим параметрам.Благодаря изоморфизму вместе с кальциевыми солями могут осаждаться в костной ткани соли и других катионов, близких по своим свойствам иону кальция: бериллия, стронция, бария.
Са2+ Ва2+ Ks°(СаНРО4) =2,7⋅10–7
НРО42– Ks°(ВаНРО4) =9,1⋅10–8
СаНРО4 ВаНРО4
Слайд 14Изоморфизм
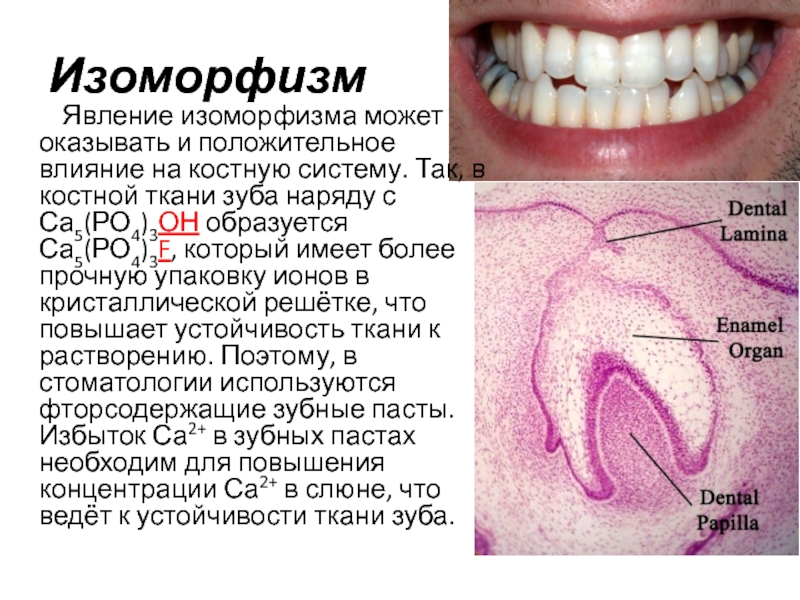
Явление изоморфизма может оказывать и положительное влияние на костную систему.
Так, в костной ткани зуба наряду с Са5(РО4)3ОН образуется Са5(РО4)3F,
который имеет более прочную упаковку ионов в кристаллической решётке, что повышает устойчивость ткани к растворению. Поэтому, в стоматологии используются фторсодержащие зубные пасты. Избыток Са2+ в зубных пастах необходим для повышения концентрации Са2+ в слюне, что ведёт к устойчивости ткани зуба.Слайд 15Термодинамика образования конкрементов
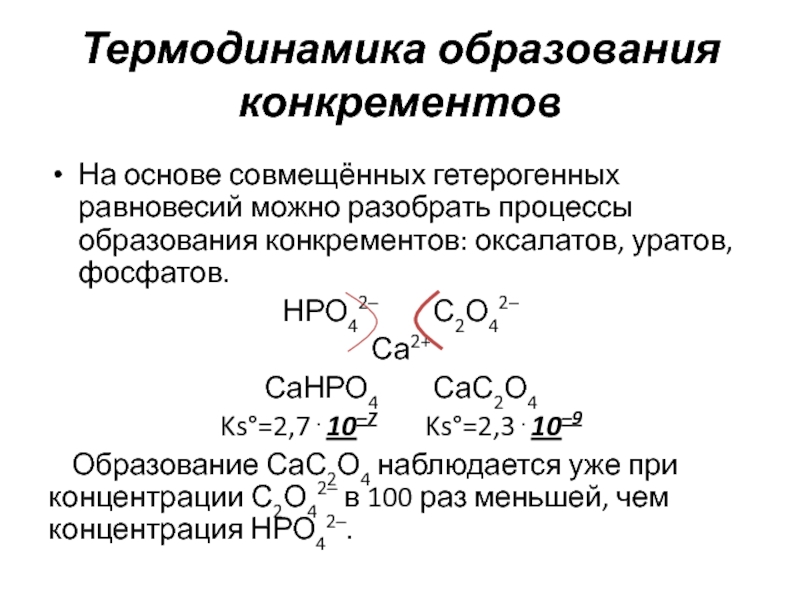
На основе совмещённых гетерогенных равновесий можно разобрать процессы
образования конкрементов: оксалатов, уратов, фосфатов.
НРО42– С2О42–
Са2+
СаНРО4
СаС2О4Ks°=2,7⋅10–7 Ks°=2,3⋅10–9
Образование СаС2О4 наблюдается уже при концентрации С2О42– в 100 раз меньшей, чем концентрация НРО42–.
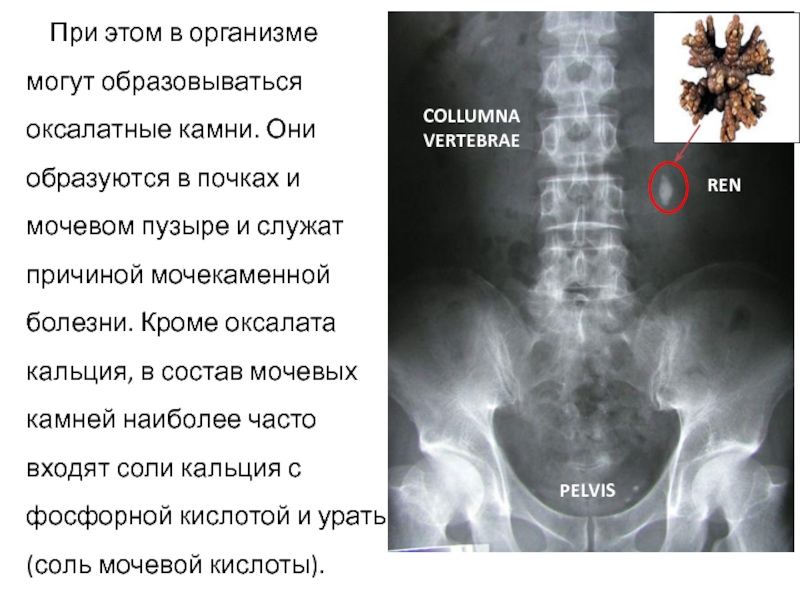
Слайд 16При этом в организме могут образовываться оксалатные камни. Они образуются
в почках и мочевом пузыре и служат причиной мочекаменной болезни.
Кроме оксалата кальция, в состав мочевых камней наиболее часто входят соли кальция с фосфорной кислотой и ураты (соль мочевой кислоты).PELVIS
REN
COLLUMNA VERTEBRAE