Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Государственное бюджетное образовательное учреждение высшего профессионального
Содержание
- 1. Государственное бюджетное образовательное учреждение высшего профессионального
- 2. « Клеточный иммунный ответ. Основные популяции клеток и механизмы их взаимодействия».Практическое занятие № 9
- 3. Вопросы Типы иммунного ответа и факторы, их
- 4. Повторение1.Цитокины антигенпрезентирующих клеток и типы иммунного ответа.
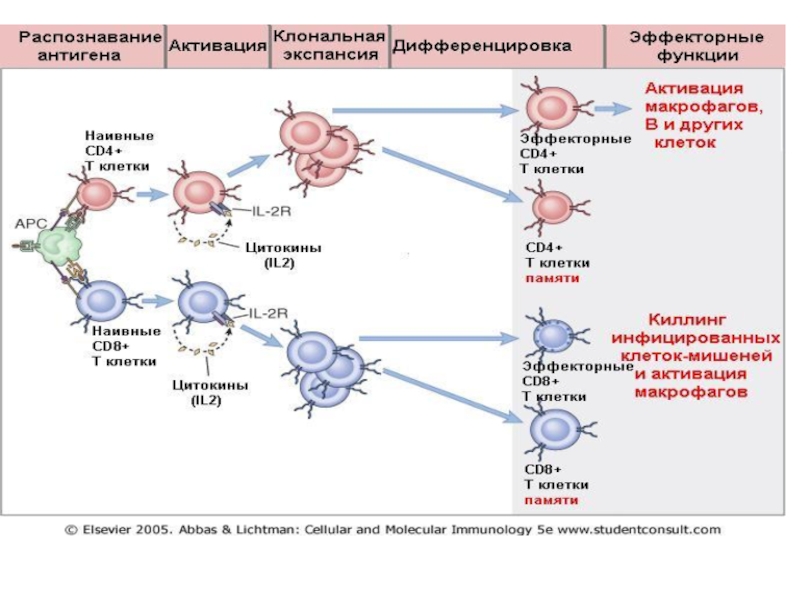
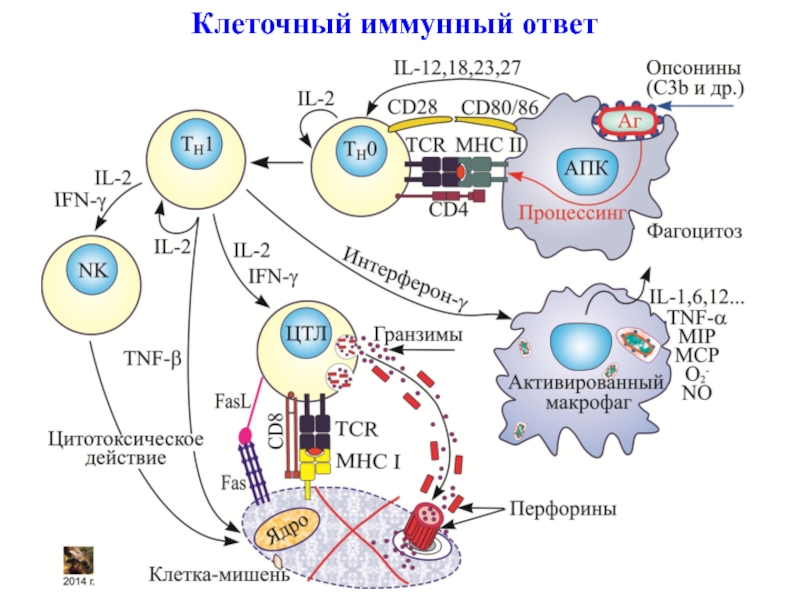
- 5. Клеточный иммунный ответ
- 6. Повторение2. Гуморальный иммунный ответ.
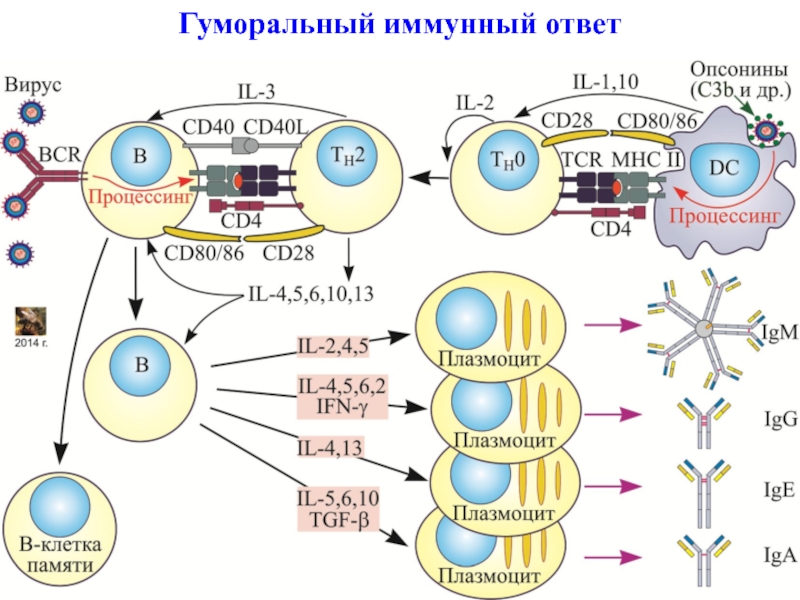
- 7. Гуморальный иммунный ответ
- 8. Повторение3.Формирование Т клеточного рецептора и корецепторов
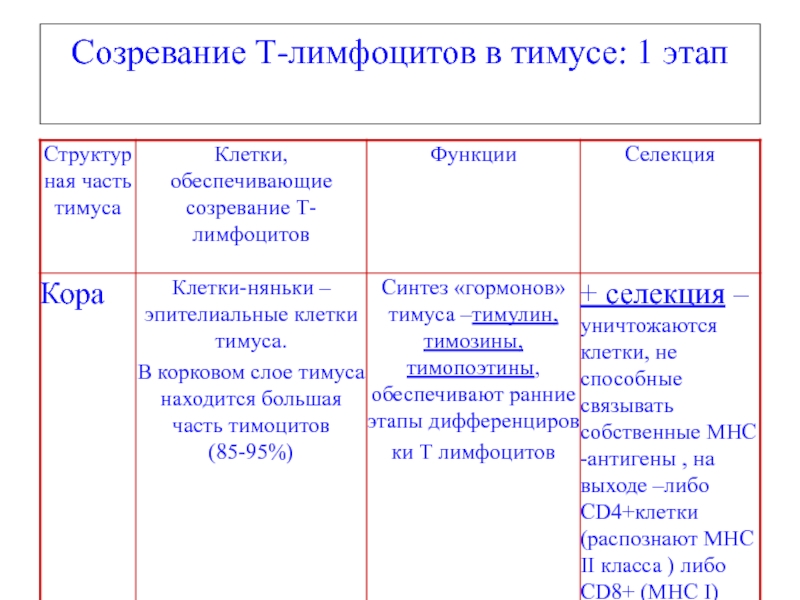
- 9. Созревание Т-лимфоцитов в тимусе: 1 этап
- 10. Созревание Т-лимфоцитов в тимусе: 2 этап
- 11. Процесс созревания тимоцитов: этапы формирования корецепторовКорецепторы: CD4
- 12. Двойное распознавание – «чужое» в «своем»T клетки
- 13. Слайд 13
- 14. Строение Т рецепторовТ клеточный рецептор имеет
- 15. Слайд 15
- 16. Тип иммунного ответа зависит от типа патогенаНа
- 17. Тип презентации антигена зависит от типа патогенаВнеклеточные
- 18. Слайд 18
- 19. Слайд 19
- 20. В любой ядерной клетке антигены после фрагментирования
- 21. Клеточная цитотоксичность - ответ CD8+ Т лимфоцитов
- 22. Слайд 22
- 23. Слайд 23
- 24. Стадии развития цитотоксического (CD8+) иммунного ответа1.Индуктивная стадияДендритные
- 25. Стадии развития цитотоксического (CD8+) иммунного ответаВ Т-зоны
- 26. Строение иммунологического синапса: 3 зоны контактов
- 27. Сигналы 1, 2сигнал1 антиген и рецепторсигнал 2B7
- 28. Строение иммунологического синапса: 3 зоны контактов
- 29. Костимуляция: АПК – Т лимфоцит1. Костимулирующие молекулы-
- 30. Презентация антигена - T клетки костимулированыКостимулирующие молекулы экспрессируются на большинстве АПК
- 31. Механизм костимуляции Т клетокНа покоящихся Т клетках
- 32. экспрессия и цепей IL-2 рецептора,
- 33. сигнал 2активируются AP-1 и NFk-B и повышают
- 34. Анергия (неотвечаемость) развивается при отсутствии сигналов костимуляцииЕсли
- 35. Строение иммунологического синапса: 3 зоны контактов
- 36. Взаимодействие ДК с наивным Т-цитотоксическим лимфоцитом в
- 37. Взаимодействие ДК с наивным Т-хелпером в
- 38. Поляризация ответа
- 39. Akdis M. et al., 2012Цитокины в регуляции функций Т-хелперовBcl-6
- 40. Взаимодействие ДК с наивным Т-хелпером в Т-
- 41. Слайд 41
- 42. Стадии развития цитотоксического (CD8+) иммунного ответа2.Эффекторная фаза:
- 43. Рецептор клеточной гибели. (FADD-Fas-associated death domain)
- 44. Т-киллер убивает клетку, на поверхности которой презентирован
- 45. Заключительный этап цитотоксического (CD8+) иммунного ответаЧерез 7-10
- 46. T h1 –опосредованный ответT h1 –опосредованный воспалительный
- 47. T h1 –опосредованный ответВ очаге инфицирования дендритные
- 48. Характеристика этапов T h1 – опосредованного воспалительного
- 49. Клеточный иммунный ответ
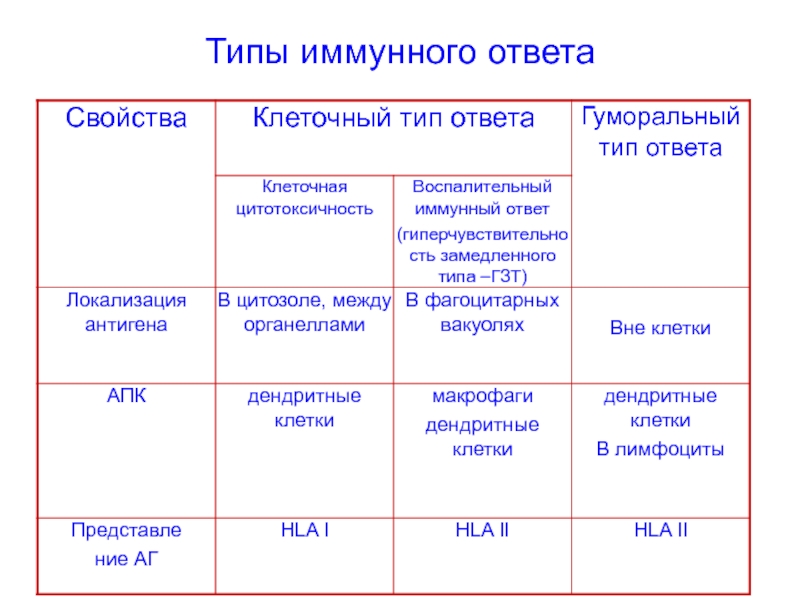
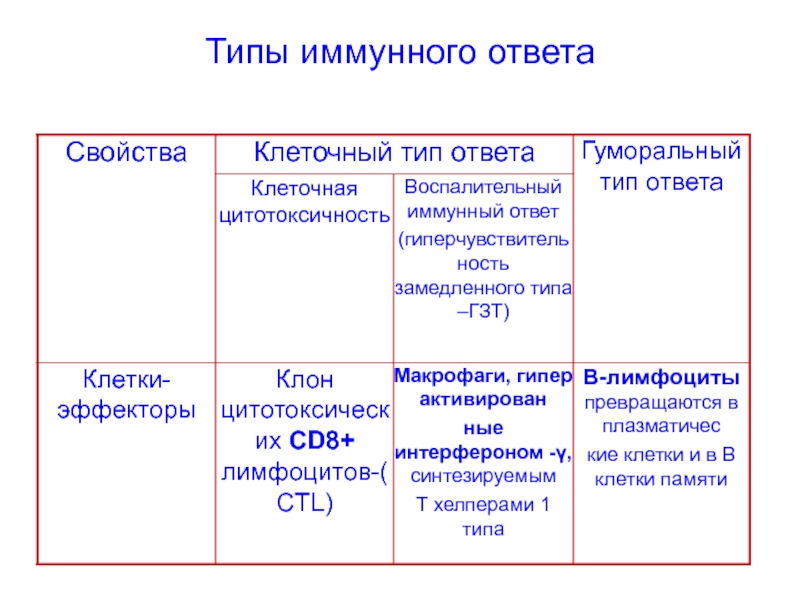
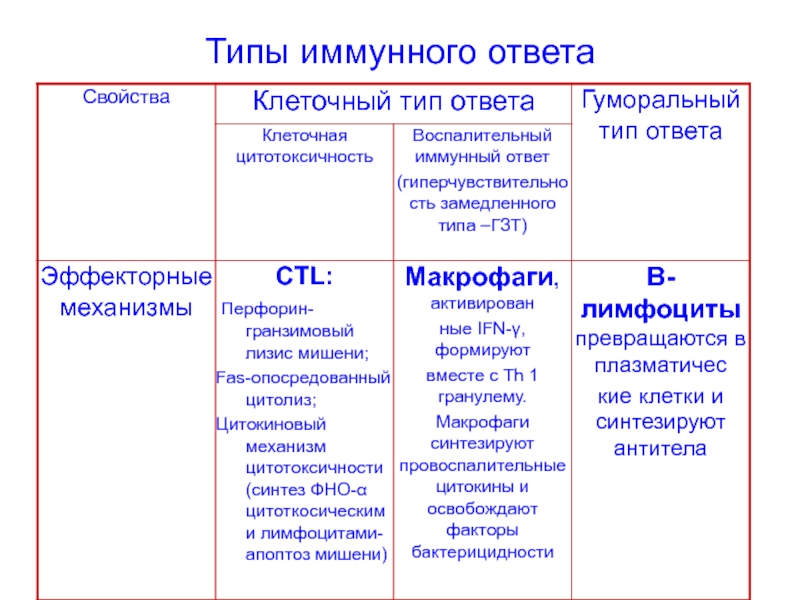
- 50. Типы иммунного ответа
- 51. Типы иммунного ответа
- 52. Типы иммунного ответа
- 53. Типы иммунного ответа
- 54. Типы иммунного ответа
- 55. АПОПТОЗ (краткая характеристика процесса)Апоптоз – физиологическая смерть клеток
- 56. Сигналы, вызывающие запуск апоптозаСуществует несколько типов сигналов,
- 57. Сигналы апоптоза
- 58. Апоптоз –физиологическая смерть клетокFas – рецептор (CD95)-
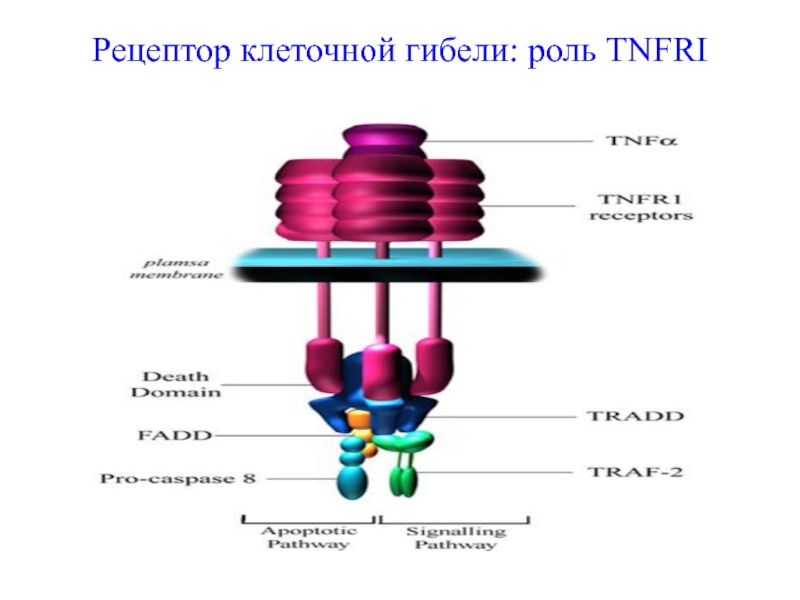
- 59. Рецептор клеточной гибели: роль TNFRI
- 60. Механизмы запуска апоптоза цитотоксическими Т - лимфоцитамиЦитотоксические
- 61. Механизмы запуска апоптозаГранзим B может быть введен
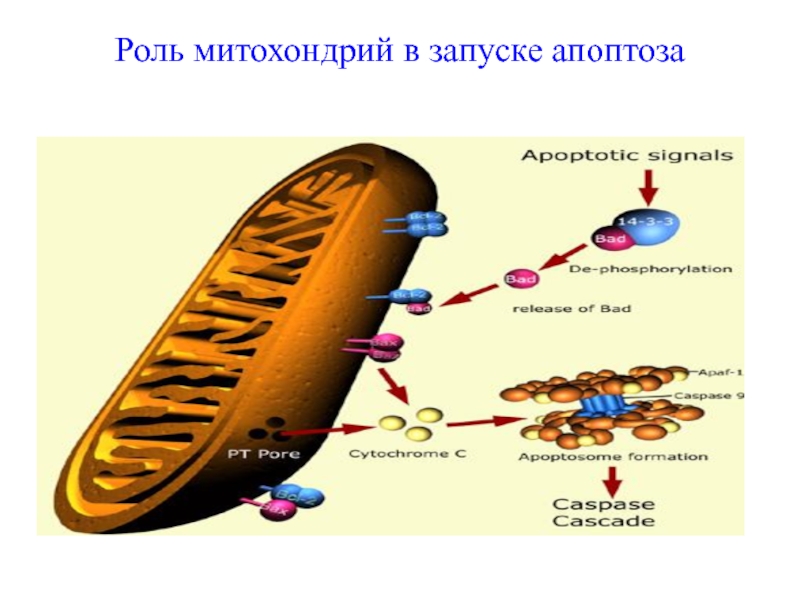
- 62. Роль митохондрий в запуске апоптоза
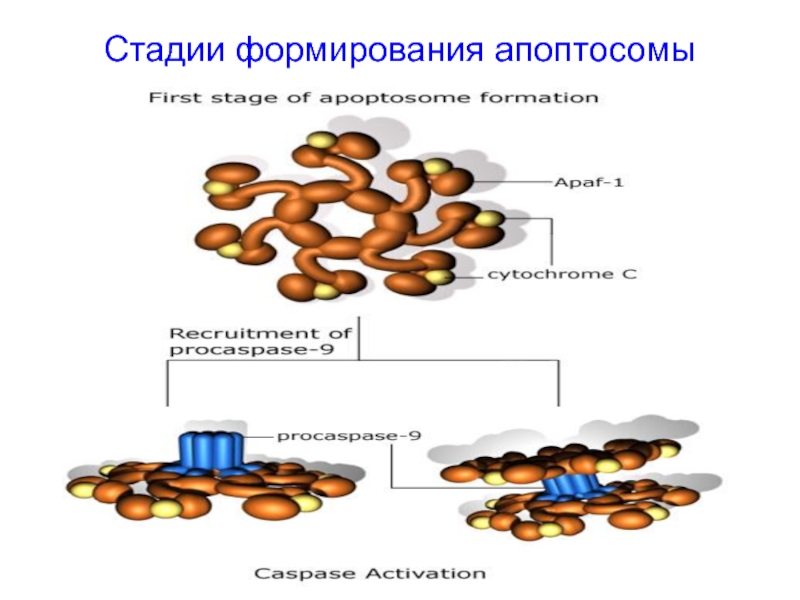
- 63. Стадии формирования апоптосомы
- 64. Каспазы и разрушение хроматина Основной механизм запрограммированной
- 65. Фрагментация хроматина
- 66. 1. Каспазы инактивируют ферменты, участвующие в репарации
- 67. 2. Каспазы разрушают структурные белки ядраЛамины –структурные
- 68. 3. Каспазы вызывают фрагментацию ДНКРадиоизотопные исследования показали,
- 69. Этапы апоптоза(A) Разрыв ламинов (ядерных белков) и
- 70. Этапы апоптоза
- 71. Этапы апоптоза(C) клетка уменьшается в размерах, как
- 72. Этапы апоптоза
- 73. ВопросыТипы иммунного ответа и факторы, их определяющие.Внутриклеточная
- 74. Тестовые вопросыАнтиген в Т-зависимых зонах лимфатических узлов
- 75. Тестовые вопросыЦитотоксические Т-лимфоциты своим корецептором вступают во
- 76. Тестовые вопросыЦитотоксические Т-лимфоциты вызывают гибель клеток-мишеней с
- 77. Тестовые вопросыЦитотоксичность - это:Способность вызывать гибель клеток-мишенейСпособность
- 78. Тестовые вопросыВ индукторной фазе иммунного ответа происходит:
- 79. Скачать презентанцию
« Клеточный иммунный ответ. Основные популяции клеток и механизмы их взаимодействия».Практическое занятие № 9
Слайды и текст этой презентации
Слайд 1 Государственное бюджетное образовательное учреждение высшего профессионального образования «ПЕРВЫЙ САНКТ-ПЕТЕРБУРГСКИЙ ГОСУДАРСТВЕННЫЙ
МЕДИЦИНСКИЙ УНИВЕРСИТЕТ имени академика И.П. Павлова» МИНИСТЕРСТВА ЗДРАВООХРАНЕНИЯ Российской федерАции
иммунологииСлайд 2« Клеточный иммунный ответ. Основные популяции клеток и механизмы их
взаимодействия».
Практическое занятие № 9
Слайд 3Вопросы
Типы иммунного ответа и факторы, их определяющие.
Внутриклеточная локализация патогенна
и тип клеточного иммунного ответа.
Клетки-эффекторы клеточного иммунного ответа.
Роль цитокинов в
реализации клеточного иммунного ответа.Основные различия клеточного и гуморального типов ответов.
Механизмы цитотоксичности CTL.
Роль Т – лимфоцитов – хелперов 1 типа.
Роль активированных макрофагов.
Механизмы действия активированных макрофагов.
Общая характеристика типов иммунных ответов.
Слайд 11Процесс созревания тимоцитов:
этапы формирования корецепторов
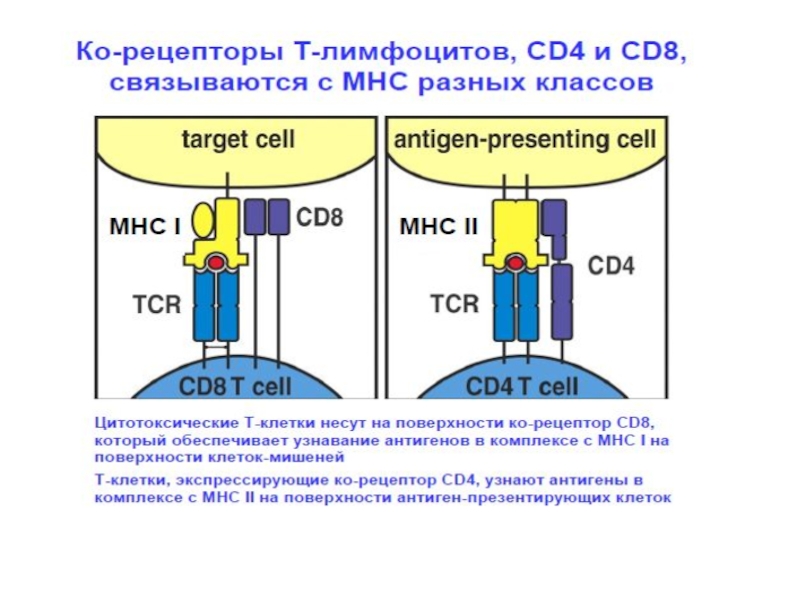
Корецепторы:
CD4 – распознает молекулы МНС
2 класса
CD8 – распознает молекулы МНС 1класса
В коре
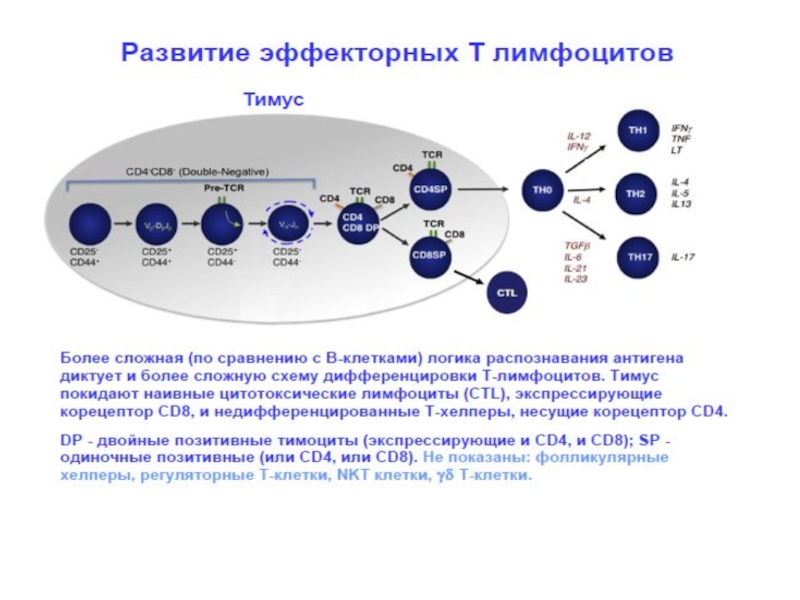
находятся незрелые двойные негативные (CD3/TcR-CD4- 8-) и двойные позитивные тимоциты (CD3/TcR- CD4+ 8+),при переходе в мозговой слой клетки теряют либо CD4, либо CD8 молекулы и становятся однопозитивными:
(CD3+ TcR CD4+) –Т –хелперы
(CD3+ TcR CD8+) –Т –цитотоксические клетки
Слайд 12Двойное распознавание – «чужое» в «своем»
T клетки способны развиваться только
в том случае, если их рецептор (TcR) распознают часть собственных
молекул главного комплекса гистосовместимости (MHC).TcR способны распознавать собственные антигены – (МНС), ассоциированные с фрагментами чужеродных АГ.
MHC молекулы участвуют в активации Т клеток.
Слайд 14Строение Т рецепторов
Т клеточный рецептор имеет и -цепи
(есть альтернативные рецепторы, которые имеют и цепи- обеспечивают
иммунитет слизистых оболочек, первичный ответ при инфекции).Каждая и цепь в составе Т рецептора имеет:
1 наружный вариабельный Vдомен и и 1 наружный константный Cдомен
Трансмембранный сегмент
Цитоплазматический хвостик (короткий)
Слайд 16Тип иммунного ответа зависит от типа патогена
На внутриклеточно-паразитирующие патогены(вирусы и
некоторые бактерии) развивается преимущественно клеточный тип ответа.
На внеклеточные паразиты
(большинство бактерий) развивается гуморальный тип иммунного ответа.Слайд 17Тип презентации антигена зависит от типа патогена
Внеклеточные антигены представляются в
молекулах MHC I I класса, которые распознаются CD4+Т хелперами
(внеклеточный
АГ - MHC I I - CD4 + гуморальный тип ответа).Внутриклеточные антигены представляются в молекулах MHC I класса, которые распознаются CD8+цитотоксическими Т –лимфоцитами
(внутриклеточный АГ - MHC I - CD8+ клеточный тип ответа).
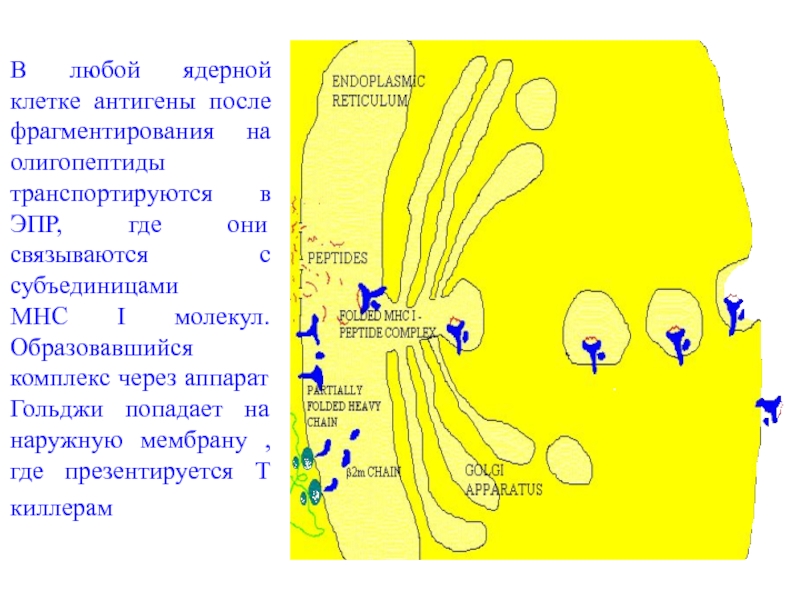
Слайд 20В любой ядерной клетке антигены после фрагментирования на олигопептиды транспортируются
в ЭПР, где они связываются с субъединицами МНС I молекул.
Образовавшийся комплекс через аппарат Гольджи попадает на наружную мембрану , где презентируется Т киллерамСлайд 21Клеточная цитотоксичность - ответ CD8+ Т лимфоцитов на внутриклеточные патогены
Клеточная
цитотоксичность развивается в ответ на внутриклеточные патогены, локализованные в цитозоле
клетки: вирусы, бактерии, микоплазмы.Эффекторы цитотоксического ответа - CD8+ цитотоксические Т лимфоциты.
CD8+ Т цитотоксические лимфоциты распознают своим Т клеточным рецептором антигенные фрагменты, представляемые антигенпрезентирующими клетками в молекуле MHC I класса, при этом корецептор CD8+ Т- цитотоксического лимфоцита распознает молекулу MHC I класса.
Слайд 24Стадии развития цитотоксического (CD8+) иммунного ответа
1.Индуктивная стадия
Дендритные клетки (ДК) после
взаимодействия с патогеном мигрируют в лимфу, по пути превращаются в
вуалевые клетки, одновременно осуществляя процесинг антигена и его предоставление в молекулах MHC I класса.ДК с током афферентной лимфы попадают в Т-зависимые зоны лимфатических узлов.
В лимфатическом узле ДК созревают и превращаются в интердигитальные дендритные клетки.
Слайд 25Стадии развития цитотоксического (CD8+) иммунного ответа
В Т-зоны лимфатического узла с
током крови прибывают постоянно рециркулирующие пока еще «наивные»(т.е. еще не
встретившие «свой антиген») Т-лимфоциты –хелперы (CD4 +) и Т-цитотоксические (CD8 +).Между ДК и Т-лимфоцитами, узнавшими «свой антиген» в молекулах MHC I или MHCII классов на поверхности ДК, формируется иммунологический синапс.
Слайд 26Строение иммунологического синапса: 3 зоны контактов между АПК и Т
лимфоцитами
Группа молекул, обеспечивающих распознавание антигена Т-цитотоксическим лимфоцитом:
Со стороны Т-цитотоксического
лимфоцита: TcR (T-клеточный рецептор) в комплексе с молекулой CD 3 и корецептором CD 8.
Со стороны дендритной клетки – фрагмент антигена, упакованный в молекулу MHC I класса.
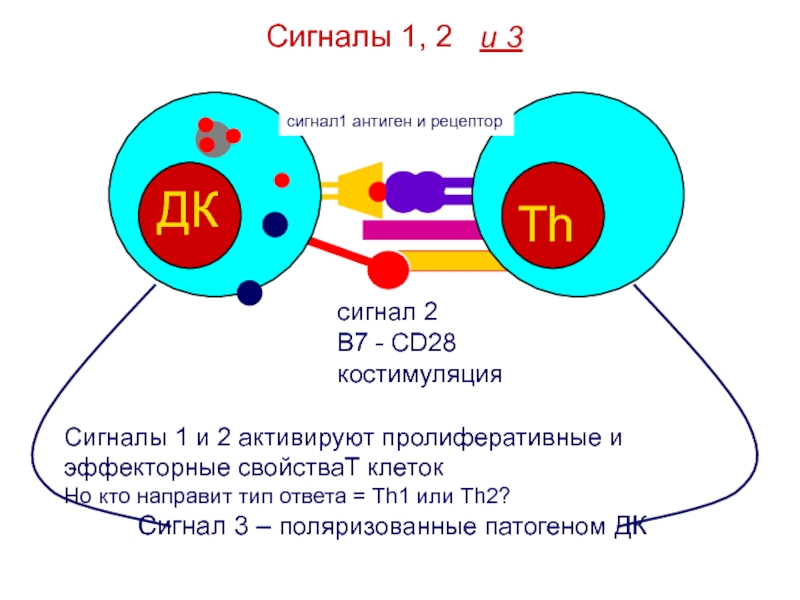
Слайд 27Сигналы 1, 2
сигнал1 антиген и рецептор
сигнал 2
B7 - CD28
костимуляция
и 3
Сигналы
1 и 2 активируют пролиферативные и эффекторные свойстваT клеток
Но кто
направит тип ответа = Th1 или Th2?Слайд 28Строение иммунологического синапса: 3 зоны контактов между АПК и Т
лимфоцитами
2.Костимулирующие взаимодействия:
Взаимодействие молекулы CD 28 на Т-лимфоците и CD 80
или CD 86 на дендритной клетке способствует активации Т- лимфоцита, запуску экспрессии генов ИЛ-2 и α цепи ИЛ-2 рецептора.Взаимодействие ИЛ-2 с ИЛ-2 рецептором на поверхности Т-лимфоцитов приводит к
к пролиферации Т-лимфоцитов с последующей их дифференцировкой либо в эффекторные клетки, либо в клетки памяти.
Взаимодействие CD 40L на Т-лимфоците и CD 40 на дендритной клетке направлено на активацию ДК –и синтезу ИЛ-12, который активирует Т лимфоциты.
Слайд 29Костимуляция: АПК – Т лимфоцит
1. Костимулирующие молекулы- члены семейства B7
(CD80 и CD86) экспрессируются на большинстве АПК, включая, клетки Лангерганса,
моноциты/макрофаги, В клетки и др. , но не экспрессируются клетками, которые не обладают функциями иммунорегуляции – такими, как мышечные, нервные клетки, гепатоциты, эпителиальные клетки и др.2. Молекулы семейства B7 (CD80 и CD86) на АПК связываются с молекулой CD 28 на поверхности Т клетки.
Слайд 30Презентация антигена - T клетки костимулированы
Костимулирующие молекулы экспрессируются на большинстве
АПК
Слайд 31Механизм костимуляции Т клеток
На покоящихся Т клетках экспрессируются низкоаффинные рецепторы
к интерлейкину -2 (IL 2 R) – его и
цепи, но не -цепь.После стимуляции Т лимфоцита, активируются гены, кодирующие -цепь.
Экспрессия -цепи IL 2 R превращает IL 2 рецептор в высокоаффинную форму.
Костимулирующие сигналы активируют ядерные факторы транскрипции , это приводит к повышению продукции интерлейкина -2 более, чем в 100 раз.
Связывание IL 2 R с IL 2 запускает процесс пролиферации Т лимфоцитов, т.е. клональную экспансию.
Слайд 32экспрессия
и цепей IL-2 рецептора, но не a
цепи
Механизм костимуляции Т клеток
сигнал 1
NFAT связывается с промотором
гена a цепи
IL-2 рецептора.a цепь превращает IL-2R
в высокоаффинную форму
Покоящаяся Т клетка
Низкоаффинный IL-2 рецептор
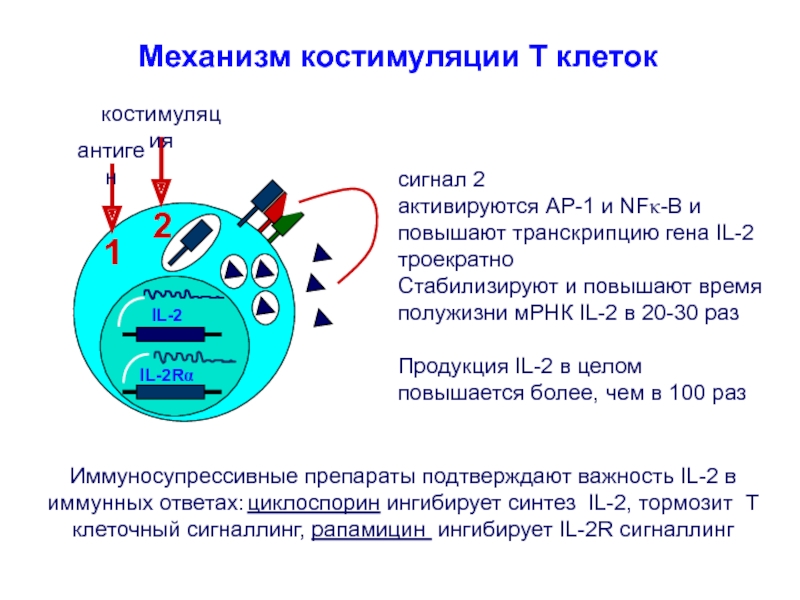
Слайд 33сигнал 2
активируются AP-1 и NFk-B и повышают транскрипцию гена IL-2
троекратно
Стабилизируют и повышают время полужизни мРНК IL-2 в 20-30 раз
Продукция
IL-2 в целом повышается более, чем в 100 разМеханизм костимуляции Т клеток
Иммуносупрессивные препараты подтверждают важность IL-2 в иммунных ответах: циклоспорин ингибирует синтез IL-2, тормозит Т клеточный сигналлинг, рапамицин ингибирует IL-2R сигналлинг
Слайд 34Анергия (неотвечаемость) развивается при отсутствии сигналов костимуляции
Если Т клетка получает
только 1 сигнал –антиген+МНС, который распознается Т клеточным рецептором, но
при этом не получает костимулирующих сигналов, она не способна к активации.В этом случае Т-клетка не способна продуцировать IL-2 и поэтому не способна пролиферировать и подвергаться клональной селекции.
Слайд 35Строение иммунологического синапса: 3 зоны контактов между АПК и Т
лимфоцитами
3. Адгезионные взаимодействия между Т-лимфоцитами и дендритными клетками обеспечивают более
тесный контакт между клетками и стабилизируют иммунный синапс:Молекулы LFA-1 и ICAM-1 - на Т-лимфоците
и комплементарные им молекулы CD2 и CD 58 на поверхности дендритной клетки.
Слайд 36Взаимодействие ДК с наивным Т-цитотоксическим лимфоцитом в Т-клеточной зоне лимфоузла
Комплекс
MHC I- антигенный пептид на поверхности дендритной клетки взаимодействует с
корецептором CD8 и с комплексом TcR/CD3 на поверхности Т-цитотоксического лимфоцита.Это приводит к активации Т- цитотоксического лимфоцита, экспрессии на его мембране адгезионных молекул, экспрессии α –цепи рецептора к ИЛ 2, синтезу ИЛ-2, связывании ИЛ-2 с его рецептором на поверхности Т-лимфоцита, к пролиферации цитотоксического Т-лимфоцита (клональной экспансии).
Слайд 37Взаимодействие ДК с наивным
Т-хелпером в Т-клеточной зоне лимфоузла
Комплекс MHC
I I - антигенный пептид на поверхности дендритной клетки взаимодействует
с корецептором CD4 и с комплексом TcR/CD3 на поверхности наивногоТлимфоцита-хелпера (Th 0).ДК начинают синтезировать ИЛ-12,ИЛ-18 и ИЛ-27, которые вместе с ИФН-γ способствуют дифференцировке наивного Т хелпера в Т хелпер 1 типа (Th 0 в Th 1).
Th 1 начинают продуцировать ИЛ-2, который действует на CD8+ лимфоциты и способствует тх дифференцировке в зрелые цитотоксические Т лимфоциты(CTL).
Слайд 40Взаимодействие ДК с наивным Т-хелпером в Т- клеточной зоне лимфоузла
Комплекс
MHC I I - антигенный пептид на поверхности дендритной клетки
взаимодействует с TcR/CD3 комплексом и CD8 –корецептором на поверхности Т-цитотоксического лимфоцита.Это приводит к активации Т- цитотоксического лимфоцита, экспрессии адгезионных молекул, α –цепи рецептора к ИЛ 2, синтезу ИЛ-2, связыванию ИЛ-2 с его рецептором на поверхности Т-лимфоцита, к пролиферации цитотоксического Т-лимфоцита (клональной экспансии).
Слайд 42Стадии развития цитотоксического (CD8+) иммунного ответа
2.Эффекторная фаза: ЦИТОЛИЗ ИНФИЦИРОВАННЫХ ВНУТРИКЛЕТОЧНЫМИ
ПАТОГЕНАМИ КЛЕТОК зрелыми цитотоксическими Т лимфоцитами (CTL) происходит посредством 3
механизмов:Перфорин-гранзимовый механизм цитотоксичности.
Перфорин –белок, который после дугрануляции встраивается в мембрану клетки-мишени и образует канал. Через канал в клетку-мишень проникают протеазы (ферменты) –гранзимы, запускающие апоптоз клетки- мишени.
Fas –опосредованный апоптоз.
На мембране клетке-мишени эксперссируется рецептор «готовности к смерти» - FasR. Цитотоксический Т лимфоцит экспрессирует Fas-лиганд. При связывании FasR с Fas-лигандом в клетку-мишень идет сигнал, активирующий каспазы, что приводит к апоптозу клетки -мишени.
Цитокиновый механизм цитотоксичности:
взаимодействие ФНО-α , синтезируемого цитотоксическими Т-лимфоцитами, с рецепторами к ФНО-α на клетке- мишени.Сигнал передается через домен смерти. Приводит к активации каспаз и к апоптозу клетки-мишени.
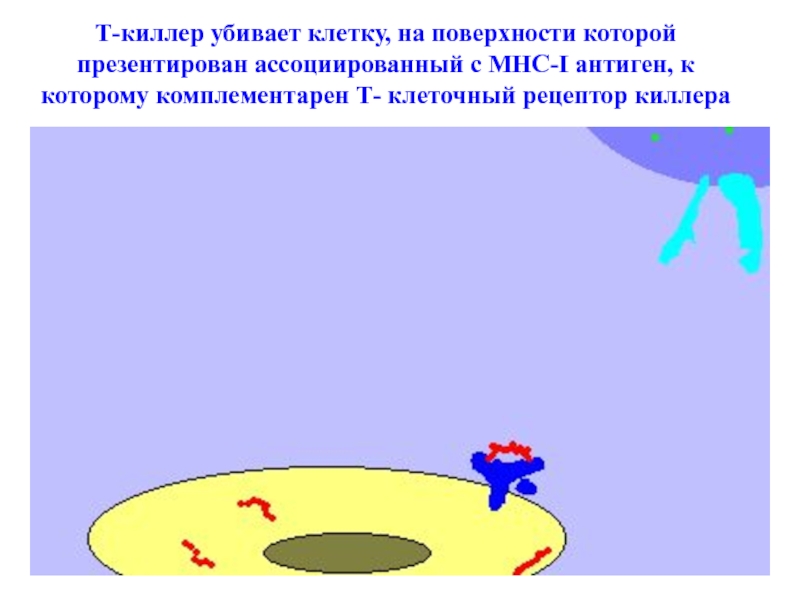
Слайд 44Т-киллер убивает клетку, на поверхности которой презентирован ассоциированный с MHC-I
антиген, к которому комплементарен Т- клеточный рецептор киллера
Слайд 45Заключительный этап цитотоксического (CD8+) иммунного ответа
Через 7-10 дней после распознавания
антигена CTL подвергаются апоптозу.
Остается популяция клеток памяти, способных при повторном
введении антигена становиться цитотоксическими т лимфоцитами. Слайд 46T h1 –опосредованный ответ
T h1 –опосредованный воспалительный ответ осуществляет защиту
от внутриклеточных патогенов, локализованных в гранулах фагоцитов (микобактерии, простейшие, грибы).
Слайд 47T h1 –опосредованный ответ
В очаге инфицирования дендритные клетки поглощают патоген
и или его фрагмент и транспортируют его в регионарный лимфоузел
–в Т-зависимые зоны.В Т-зависимые зоны ЛУ мигрируют Тh 0 (наивные).
ДК презентируют им антигенный пептид в молекулах MHC II класса.
Под влиянием цитокинов (ИЛ-12, 18,23,27 и ИФН-γ) Тh 0 (наивные) дифференцируются в Тh 1 типа.
Тh 1 типа вступают во взаимодействие с макрофагами. Несущими на своей поверхности молекулы MHC II с антигенными пептидами.
Тh 1 типа активируются и начинают синтезировать ИФН-γ и ФНО-α, активирующие макрофаги.
В макрофагах активируются гены, ответственные за активацию окислительного метаболизма.
Макрофаги выделяют кислородные радикалы (оксид азота и др.); цитокины (ФНО-α, ИЛ-6, ИЛ-1,ИФН- α ).
Происходит уничтожение внутриклеточных патогенов (а также возможна деструкция собственных тканей).
Слайд 48Характеристика этапов T h1 – опосредованного воспалительного ответа (краткая)
Презентация дендритными
клетками антигена CD 4+Т –лимфоцитам, приводящая к активации CD 4+Т
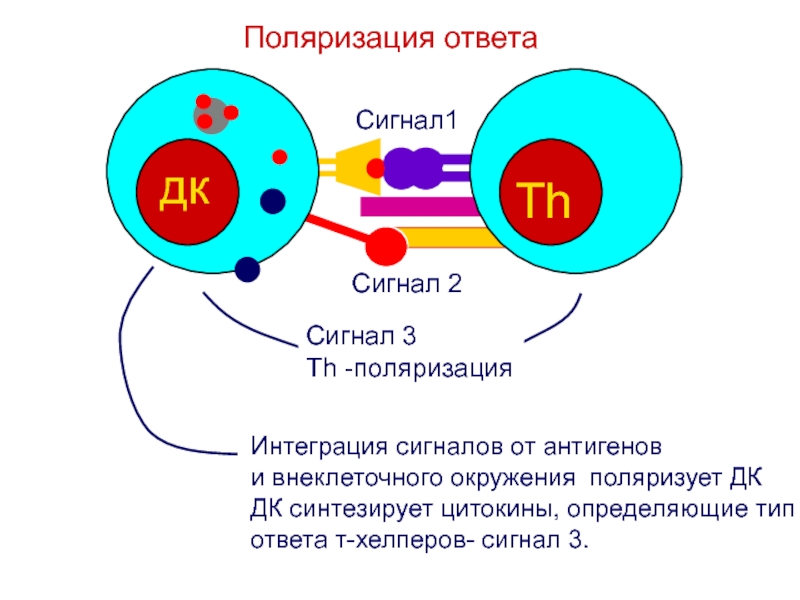
–лимфоцитов.Поляризация ответа по пути T h1 в регионарных лимфоузлах.
Взаимодействие T h1 с макрофагами, презентирующими антиген T h1 – лимфоцитам; взаимная активация T h1 и макрофагов.
Активация цитолиза в фагосомах макрофагов.
Уничтожение микроорганизмов, паразитирующих в фагосомах.
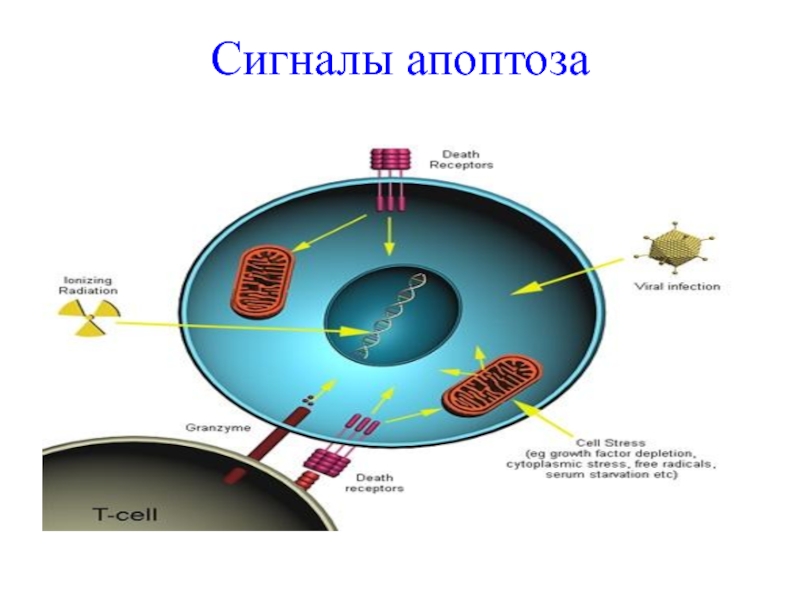
Слайд 56Сигналы, вызывающие запуск апоптоза
Существует несколько типов сигналов, запускающих апоптоз.
Чувствительность клетки
к таким сигналам зависит от многих факторов :
От экспрессии про-
и противоапоптических протеинов (семейства Bcl-2 ).От выраженности (силы) апоптозных стимулов.
От стадии клеточного цикла.
Слайд 58Апоптоз –физиологическая смерть клеток
Fas – рецептор (CD95)- рецептор готовности клетки
к апоптозу
Fas L или CD95L –лиганды Fas - рецептора.
Лигандами для
таких рецепторов могут служить либо растворимые факторы, либо молекулы, экспрессирующиеся на поверхности клеток –таких, как цитотоксические Т лимфоциты.При связывании Fas – рецептора Fas –лигандом, происходит запуск программируемой гибели клеток организма.
Слайд 60Механизмы запуска апоптоза цитотоксическими Т - лимфоцитами
Цитотоксические Т лимфоциты распознают
поврежденные , вирустрансформированные или малигнизированные клетки организма –хозяина и запускают
в них программу апоптоза.Цитотоксические Т лимфоциты также могут вызывать апоптоз клеток –мишеней с помощью специальных ферментов –гранзимов, которые они впрыскивают в отверстия клеточной мембраны клетки –мишени, созданные перфоринами –полимеризующимися в мембране мишени протеинами.
Слайд 61Механизмы запуска апоптоза
Гранзим B может быть введен в клетку-мишень цитотоксическим
Т лимфоцитом с помощью отверстий в мембране мишени, созданных перфоринами.
Гранзим B способен прямо активировать каспазы 3, 7,8 и 10.Митохондрия – также является ключевым регулятором каспазного каскада и апоптоза:
Освобождение цитохрома C из митохондрии прямо активирует сначала каспазу 9, потом каспазу 3.
Слайд 64Каспазы и разрушение хроматина
Основной механизм запрограммированной гибели клеток –
разрушение хромосомальной ДНК до нуклеосом.
Каспазы (ферменты с каскадным принципом действия)
играют основную роль в этом процессе:Активируют ДНКазы
Ингибируют ферменты, участвующие в репарации ДНК
Разрушают структурные протеины ядра
Слайд 661. Каспазы инактивируют ферменты, участвующие в репарации ДНК
Фермент поли (AДФ-рибоза)-
полимераза, или PARP, один из первых белков, обнаруженных в качестве
субстрата для каспаз.PARP участвует в репарации структуры и восстановлении функций ДНК, так как осуществляет катализирование синтеза поли (AДФ-рибозы) , а также связывается с местами повреждений в ДНК и с измененными нуклеопротеинами.
Эта способность PARP к репарации поврежденной ДНК предотвращается ферментативным разрывом молекулы PARP каспазой 3.
Слайд 672. Каспазы разрушают структурные белки ядра
Ламины –структурные ядерные белки, которые
поддерживают форму ядра и обеспечивают взаимодействие между хроматином и мембраной
ядра.Разрушения ламинов каспазой 6 приводит к конденсации хроматина и фрагментации ядра, что и является отличительной особенностью клеток, вошедших в апоптоз.
Слайд 683. Каспазы вызывают фрагментацию ДНК
Радиоизотопные исследования показали, что процесс фрагментации
ДНК до нуклеосом обеспечивается ферментом CAD ( каспазой активированная ДНКаза).
В норме CAD существует в виде неактивного комплекса с ингибитором- ICAD (ингибитор CAD).
Во время апоптоза, ICAD отрывается каспазой 3, и CAD освобождается из комплекса.
Вслед за этим происходит быстрая фрагментация ядра
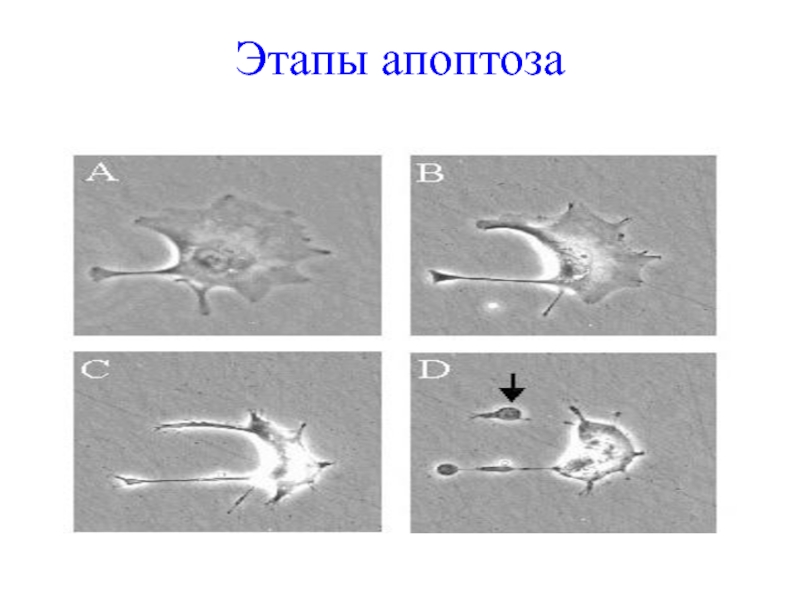
Слайд 69Этапы апоптоза
(A) Разрыв ламинов (ядерных белков) и актинов – белков
цитоскелета.
(B) Повреждение хроматина в ядре , конденсация хроматина. Ядро как
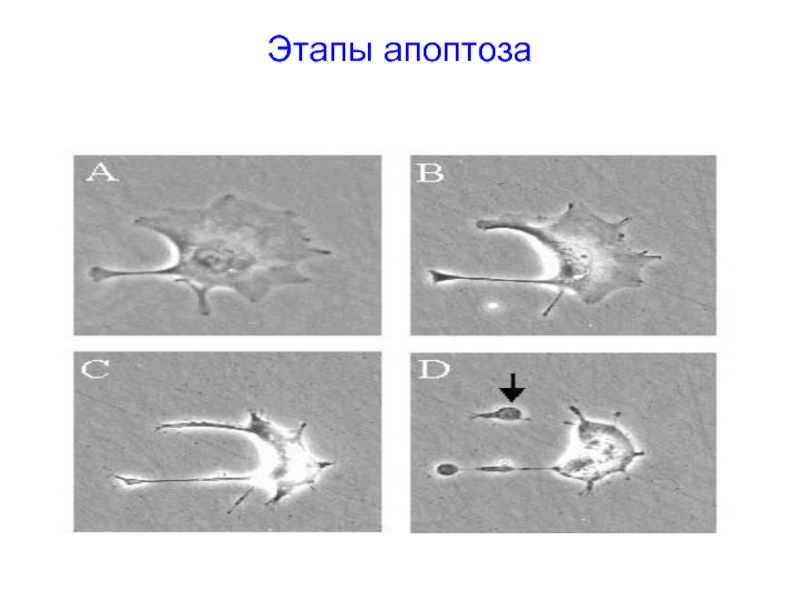
бы «сморщивается». Слайд 71Этапы апоптоза
(C) клетка уменьшается в размерах, как бы упаковывается в
форму, удобную для ее поглощения макрофагом.
Макрофаги ответственны за клиренс апоптозных
клеток из организма, причем при физиологической смерти клеток , в отличие от патологической гибели клеток путем некроза, воспаление не развивается вообще.Слайд 73Вопросы
Типы иммунного ответа и факторы, их определяющие.
Внутриклеточная локализация патогенна и
тип клеточного иммунного ответа.
Клетки-эффекторы клеточного иммунного ответа.
Роль цитокинов в реализации
клеточного иммунного ответа.Основные различия клеточного и гуморального типов ответов.
Механизмы цитотоксичности CTL.
Роль Т – лимфоцитов – хелперов 1 типа.
Роль активированных макрофагов.
Механизмы действия активированных макрофагов.
Общая характеристика типов иммунных ответов.
Слайд 74Тестовые вопросы
Антиген в Т-зависимых зонах лимфатических узлов Т-лимфоцитам представляют:
Плазматические клетки
Дендритные
клетки
Эозинофилы
Нейтрофилы
Эпителиальные клетки
Биологический смысл рециркуляции Т-лимфоцитов:
Завершенный фагоцитоз
Повышение проницаемости мембран клеток
Встреча
со «своим» антигеномАктивация цитотоксичности
Осуществление процессинга антигена
Слайд 75Тестовые вопросы
Цитотоксические Т-лимфоциты своим корецептором вступают во взаимодействие с:
Молекулами MHC
I класса
Молекулами MHC I I класса
Рецепторами компонентов системы комплемента
Высокоаффинными IgE
–рецепторамиРецепторами естественных киллеров
Молекулами MHC I класса экспрессируются на:
Всех ядросодержащих клетках (кроме клеток трофобласта)
Макрофагах
Эпителии
Эритроцитах
Только на Т- и В- лимфоцитах
Слайд 76Тестовые вопросы
Цитотоксические Т-лимфоциты вызывают гибель клеток-мишеней с помощью:
Перфоринов и
гранзимов
Fas-опосредованного апоптоза
Цитокинового механизма цитотоксичности (ФНО-α)
Фагоцитоза
Оксидативного взрыва
Т-лимфоциты-хелперы 1 типа активируют макрофаги
с помощью:Интерферона-гамма
Фактора некроза опухолей – альфа
Простагландина Е
Интерлейкина 5
Эотаксина
Слайд 77Тестовые вопросы
Цитотоксичность - это:
Способность вызывать гибель клеток-мишеней
Способность к переключению изотипов
иммуноглобулинов
Многократное повышение афинности антител
Синтез иммуноглобулинов класса Е
Повышение сосудистой проницаемости
Клеточный тип
ответа формируется преимущественно на: Внеклеточные патогенны
На внутриклеточные патогены
На аллергены
На пищевые добавки
На бактериальные токсины
Слайд 78Тестовые вопросы
В индукторной фазе иммунного ответа происходит:
Процессинг антигена антигенпредставляющими
клетками (АПК)
Презентация антигена антигенпредставляющими клетками (АПК)
Распознавание антигена при взаимодействии
АПК и Т-лимфоцитаАктивация и пролиферация специфического клона Т-лимфоцитов
Дифференцировка лимфоцитов в направлении эффекторов и клеток памяти
Костимулирующие взаимодействия:
Взаимодействие молекулы CD 28 на поверхности Т-лимфоцита и молекул CD80 или CD86 на поверхности АПК
Приводят к экспрессии гена ИЛ-2
Приводят к экспрессии α –цепи ИЛ-2-рецептора
Приводят к пролиферации Т-лимфоцитов
Приводят к дифференцировке Т-лимфоцитов в эффекторные клетки и клетки памяти