Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Химическая связь и строение молекул
Содержание
- 1. Химическая связь и строение молекул
- 2. Химическая связь
- 3. Потенциальная кривая
- 4. Слайд 4
- 5. Атомная орбитальОдноцентровая волновая функция описывающая состояние электрона
- 6. Спин – орбиталь электрона.I = (r,
- 7. Полная волновая функция атома и молекулы. Состояние
- 8. Метод валентных схем (МВС)Рассмотрим молекулу
- 9. Метод молекулярных орбиталей (ММО)
- 10. Метод молекулярных орбиталей
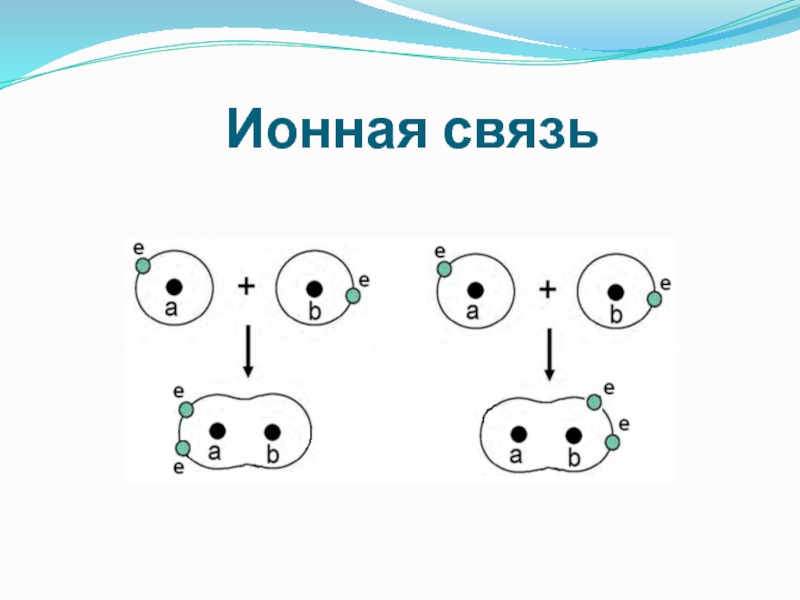
- 11. Ионная связь
- 12. Слайд 12
- 13. Метод валентных схем (МВС)
- 14. Гипервалентность и гибридизация ОА
- 15. Донорно-акцепторное взаимодействие
- 16. Слайд 16
- 17. Метод молекулярных орбиталейH = Te1 +Te2
- 18. Точное решение уравнения Шредингера Точное решение
- 19. Решение для Н2+ H =
- 20. Цилиндрические координаты
- 21. Анализ решения Для молекулы квантовые числа
- 22. Обозначение МО для двухатом-ных молекул
- 23. Осевое квантовое число Квантовое число
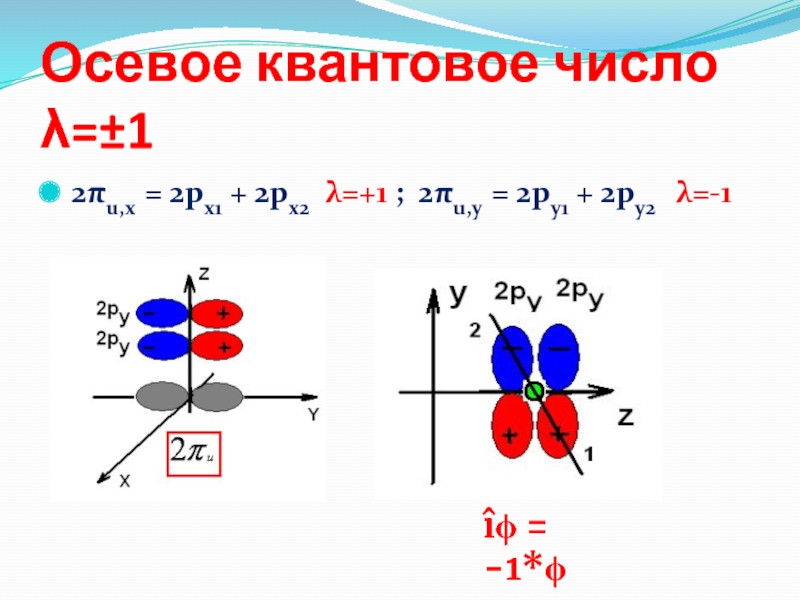
- 24. Осевое квантовое число =12u,x = 2px1 +
- 25. Скачать презентанцию
Химическая связь
Слайды и текст этой презентации
Слайд 5Атомная орбиталь
Одноцентровая волновая функция описывающая состояние электрона в атоме и
зависящая от трех квантовых чисел
Слайд 6 Спин – орбиталь электрона.
I = (r, , )*
(i)= f(n,l,m,ms)
() ms = +1/2 а.е.
()
ms = -1/2 а.е.Пример
1 = 1so* () 1so(1)
В общем случае 1 (1)
Слайд 7Полная волновая функция атома и молекулы.
Состояние системы содержащей несколько
электронов описывается
полной волновой функцией, учитывающей квантовые состояния для
всех электронов, т.е. совокуп-ностью спин-орбиталей I .ат = П I ; мол = П I
Слайд 8 Метод валентных схем (МВС)
Рассмотрим молекулу Н2, которую построим
из двух АО атомов Н.
AO для Н1 – 1s0 и
1 = 1s0,a*(1)= 1s0,a(1)= H,a (1)для Н2 – 1s0 и 2 = 1s0,b *(2)= 1s0,b(2) = H,b (2)
Слайд 12
МВС
Связь образуется между атомами, имеющими неспаренные электроны с
антипараллельными спинами. Образование химической связи обусловлено повышенной электронной плотностью между ядрами. Возникает ковалентная двухэлектрон-ная двухцентровая связь, которую наглядно можно изобразить в виде черточки валентности Н-Н.
Прочность химической связи в большой степени определяется перекрыванием электронных облаков взаимодействующих атомов, или АО.
Слайд 17 Метод молекулярных орбиталей
H = Te1 +Te2 +Uaei + Ue1e2
+ Uab
H = -1/2∇2е1-1/2∇2е2 - Za/ri + 1/r12 + Z2/R
в а.е.Слайд 18 Точное решение уравнения Шредингера
Точное решение уравнения Шредингера для
многоэлектронной молекулы решить невозможно
Причина:Потенциальная энергия взаимо-действия между электронами е1 и е2
Ueiej = 1/rij
Слайд 19 Решение для Н2+
H = -1/2∇2е1- (Za/r1 +
Zb/r2 ) +Z2/R (в а.е.)
Общий подход к решению молекулярных структур
М
= R(r)()() = Z()H()() = f(n,l,) Сферические Цилиндрические
координаты коoрдинаты
ĤМ(r, ,) = E М(r, ,)
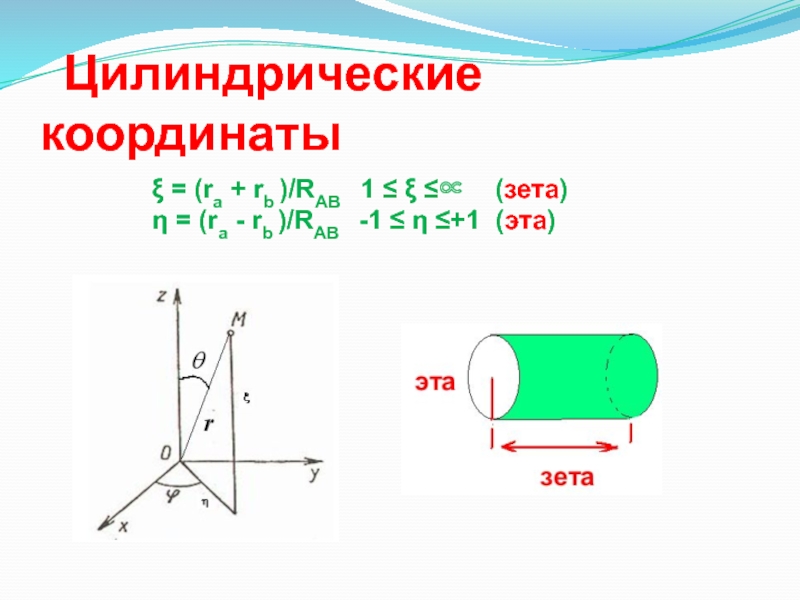
Слайд 20 Цилиндрические координаты
=
(ra + rb )/RAB 1
(зета) = (ra - rb )/RAB -1 +1 (эта)
Слайд 21 Анализ решения
Для молекулы квантовые числа n и l
не имеют физического смысла и не постоянные.
Квантовое число
является решением () = Аexp(i) и называется осевым квантовым числом || = 0, 1, 2, 3Слайд 22Обозначение МО для двухатом-ных молекул
||
0 1 2
3МО
МО = N
где N – номер МО по мере возрастания энергии.
- индекс указывающий симметрию относительно операции инверсии î. Возможны два случая:
î = +1* ( g – четная) или
î = -1* (u – нечетная) функция
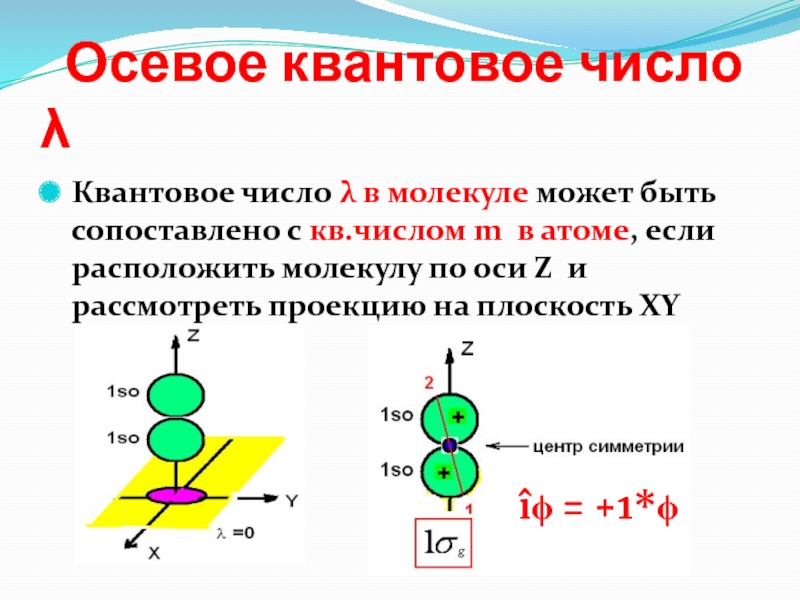
Слайд 23 Осевое квантовое число
Квантовое число в молекуле может
быть сопоставлено с кв.числом m в атоме, если расположить молекулу
по оси Z и рассмотреть проекцию на плоскость XY î = +1*