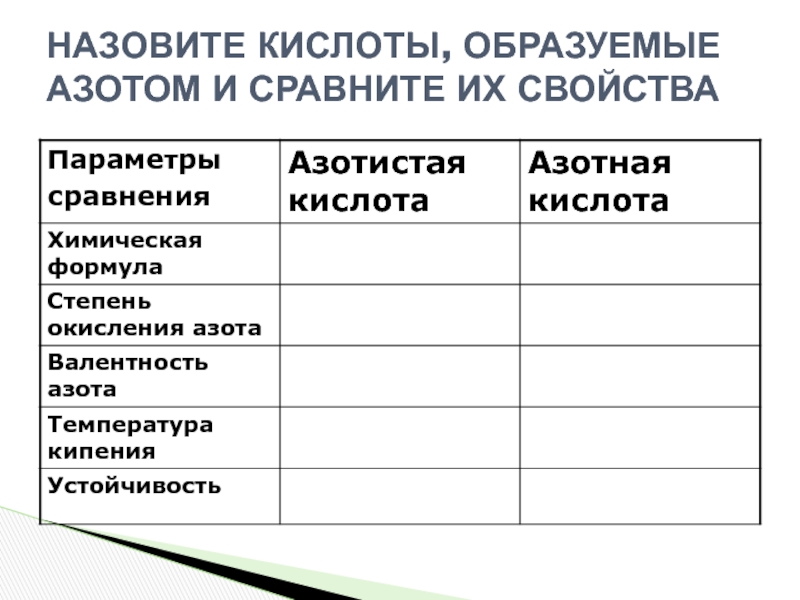
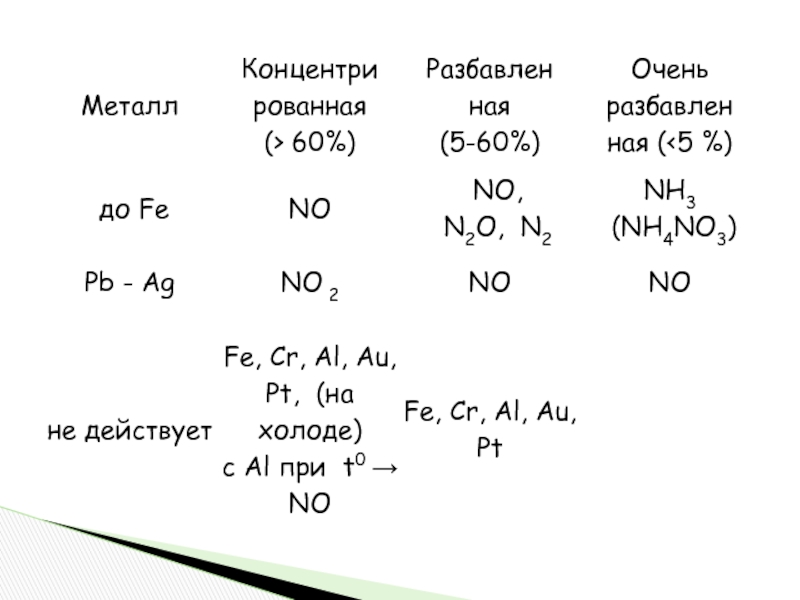
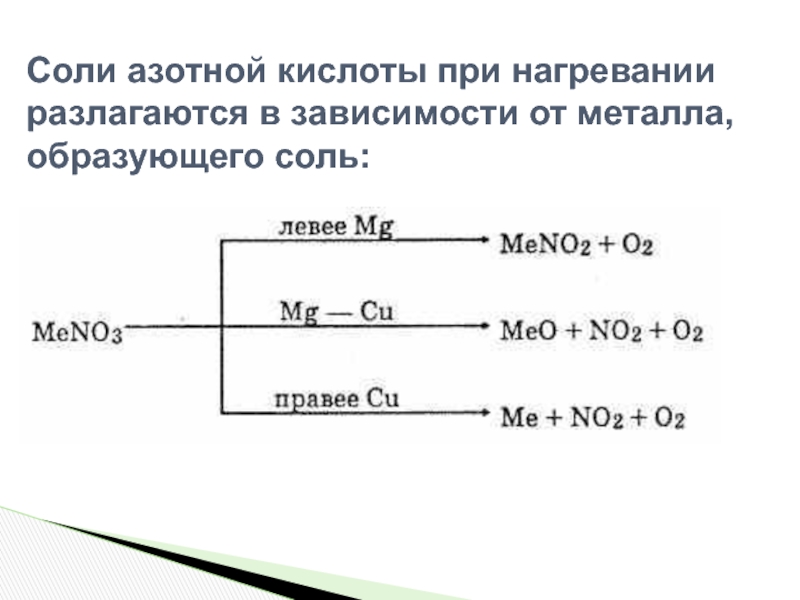
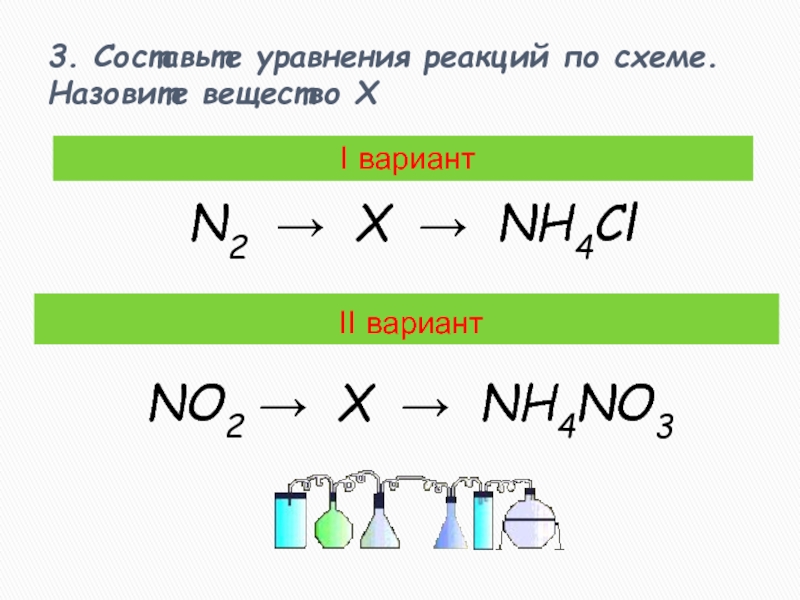
возбуждающе действует на нервную систему человека, используют в медицине как
анестезирующее средство. Физические свойства: газ, без цвета и запаха. Проявляет окислительные свойства, легко разлагается. Несолеобразующий оксид.2N2O=2N2+O2 (баланс)
N2O + Сu= N2 + СuO (баланс)
Оксид азота (I) N2O