Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Кислоты
Содержание
- 1. Кислоты
- 2. «Ум заключается
- 3. День прожит не зря, если ты узнал что-то новое
- 4. Н.Н.Семёнов – советский физико-химик
- 5. Слайд 5
- 6. Слайд 6
- 7. СаО, Ba(ОН)2, СuО, НСl, Н2О, Сl2О7, Fе(ОН)2, НNО3, NаОН, Н2SО4, H3PO4, Н2S
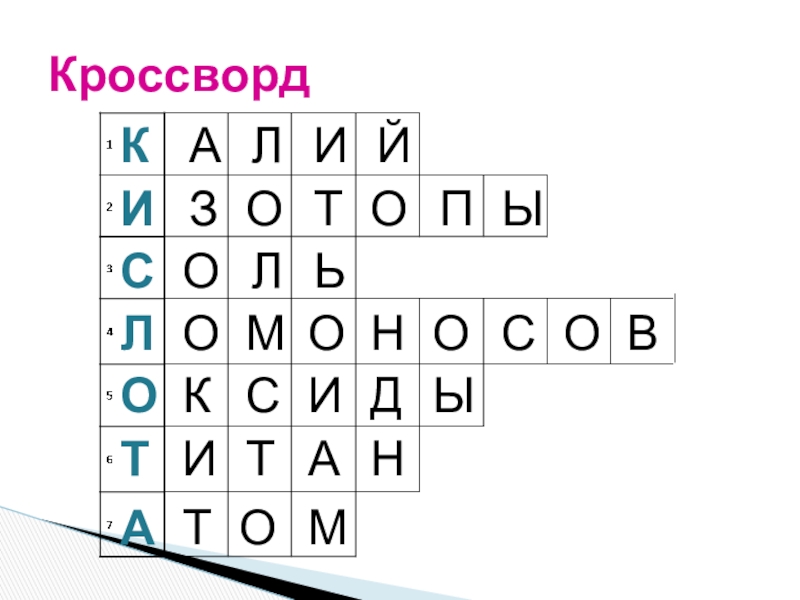
- 8. Кроссворд
- 9. КроссвордКАЛИЙ
- 10. КроссвордКАЛИЙИЗОТОПЫ
- 11. КроссвордКАЛИЙИЗОТОПЫСОЛЬ
- 12. КроссвордКАЛИЙИЗОТОПЫСОЛЬЛОМОНОСОВ
- 13. КроссвордКАЛИЙИЗОТОПЫСОЛЬЛОМОНОСОВОКСИДЫ
- 14. КроссвордКАЛИЙИЗОТОПЫСОЛЬЛОМОНОСОВОКСИДЫТИТАН
- 15. КроссвордКАЛИЙИЗОТОПЫСОЛЬЛОМОНОСОВОКСИДЫТИТАНАТОМ
- 16. Слайд 16
- 17. Что такое кислоты?Какие виды кислот бывают?Как распознать
- 18. Знать определение класса кислот;Уметь составлять формулы кислот;Знать
- 19. что такое кислоты, какие они бывают, как
- 20. СоставНоменклатураКлассификацияРаспознавание кислотПравила техники безопасности при работе с кислотами План изучения кислот:
- 21. Состав кислотН СlН2 SО4Н3 РО4 Атомыводорода КислотныйостатокКислоты
- 22. Номенклатура кислотHFHCLHBrHIH2SH2SO3H2SO4HNO2HNO3H3PO4H2CO3H2SiO3Хлороводородная (соляная)Фтороводородная (плавиковая)БромоводороднаяЙодоводороднаяСероводороднаяСернистаяСернаяАзотистаяАзотнаяФосфорнаяУгольнаяКремниевая
- 23. По какому признаку кислоты разделены на группы?
- 24. Бескислородные Кислородсодержащие
- 25. По какому признаку кислоты разделены на группы??HF
- 26. КИСЛОТЫ2. По числу атомов водородаСl INО3SО4SSiО3РО4одно-основныедвух-основныетрехосновныеН2Н2Н2НННН3Число атомов водорода в кислоте называют основностью.
- 27. Кислоты 3. По растворимости в водеРастворимые Нерастворимые SiО3Н2
- 28. ПРАВИЛА БЕЗОПАСНОСТИЕдкое вещество—кислота! Разрушает и раздражает кожу,
- 29. Слайд 29
- 30. Определите оксиды, соответствующие кислотам:H2SO3
- 31. Кислоты – это сложные вещества, молекулы которых
- 32. а) H3PO4б) кислородсодержащая в) трёхосновнаяг) растворимая в
- 33. 1. л а к м у с
- 34. Слайд 34
- 35. День прожит не зря, если ты узнал что-то новое
- 36. «Знание только тогда знание, когда оно приобретено усилиями своей мысли, а не памятью»Лев Николаевич Толстой
- 37. Параграф 21Упражнения 2-4Домашнее задание:Презентации «Кислоты в домашней аптечке»,»Кислоты в продуктах питания»-по желанию.
- 38. Спасибо за урок!
- 39. Скачать презентанцию
Слайды и текст этой презентации
Слайд 1Кислоты
Муниципальное бюджетное общеобразовательное учреждение «Средняя многопрофильная школа №65 „Спектр‟» г.Липецка
2018
год
Слайд 4 Н.Н.Семёнов – советский физико-химик
“Всё мы
связываем с химической наукой: дальнейший прогресс окружающего нас мира, новые
методы преобразования и усовершенствования. И не может быть в наши дни специалиста, который сумел бы обойтись без знаний химии” .Слайд 17Что такое кислоты?
Какие виды кислот бывают?
Как распознать кислоты среди других
веществ?
Определите степени окисления элементов в кислотах (смотри приложение №2).
Попробуйте ответить
на вопросы:Слайд 18Знать определение класса кислот;
Уметь составлять формулы кислот;
Знать номенклатуру кислот;
Знать классификацию
кислот;
Уметь распознавать кислоты;
Знать правила техники безопасности при работе с кислотами.
Цели
урокаСлайд 19что такое кислоты, какие они бывают, как их классифицируют;
формулы некоторых
неорганических кислот;
правила техники безопасности при работе с кис- лотами;
Что
нам нужно узнать?Чему мы должны научиться?
распознавать кислоты среди других соединений;
определять заряды ионов кислотных остатков;
определять степени окисления атомов химических элементов , образующих кислоты.
Слайд 20Состав
Номенклатура
Классификация
Распознавание кислот
Правила техники безопасности при работе с кислотами
План изучения
кислот:
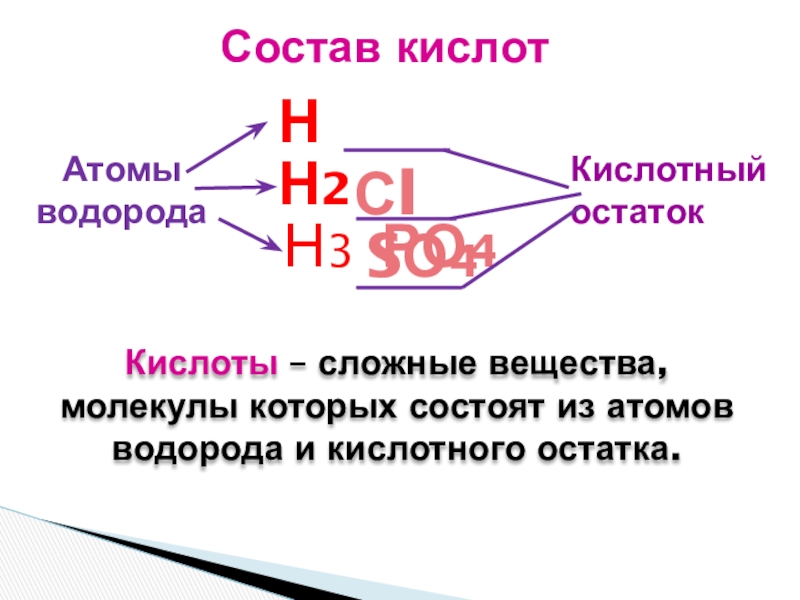
Слайд 21Состав кислот
Н
Сl
Н2
SО4
Н3
РО4
Атомы
водорода
Кислотный
остаток
Кислоты – сложные вещества,
молекулы которых состоят из атомов водорода и кислотного остатка.
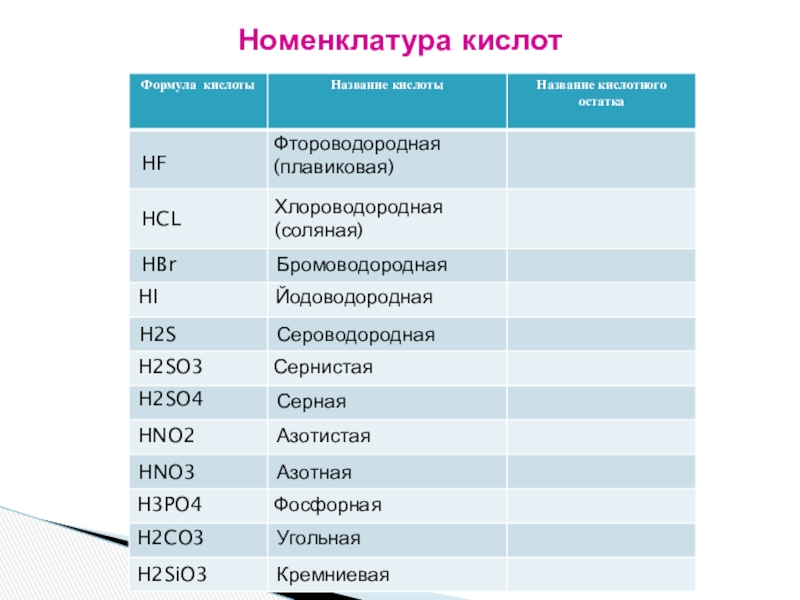
Слайд 22Номенклатура кислот
HF
HCL
HBr
HI
H2S
H2SO3
H2SO4
HNO2
HNO3
H3PO4
H2CO3
H2SiO3
Хлороводородная (соляная)
Фтороводородная (плавиковая)
Бромоводородная
Йодоводородная
Сероводородная
Сернистая
Серная
Азотистая
Азотная
Фосфорная
Угольная
Кремниевая
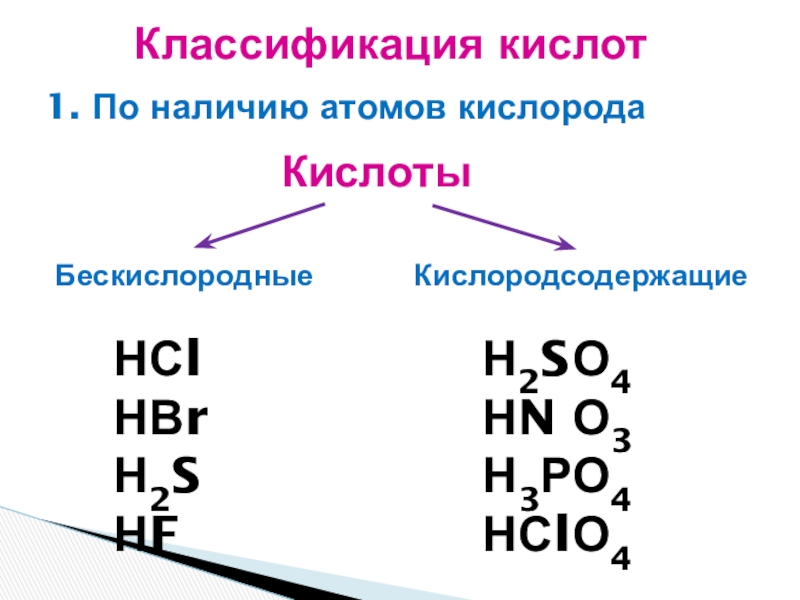
Слайд 24Бескислородные Кислородсодержащие
Кислоты
НСl
НВr
Н2S
НF
Н2S НN Н3Р НСl
Классификация
кислот 1. По наличию атомов кислорода
О4
О3
О4
О4
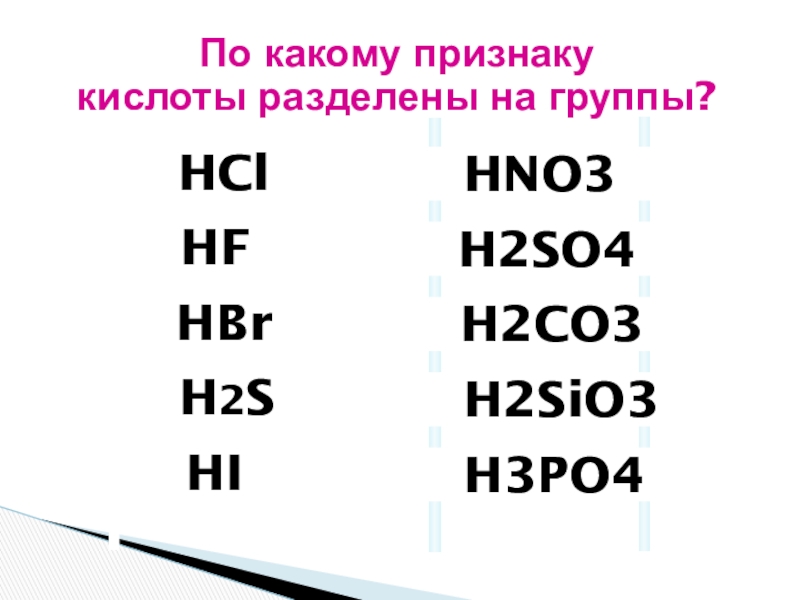
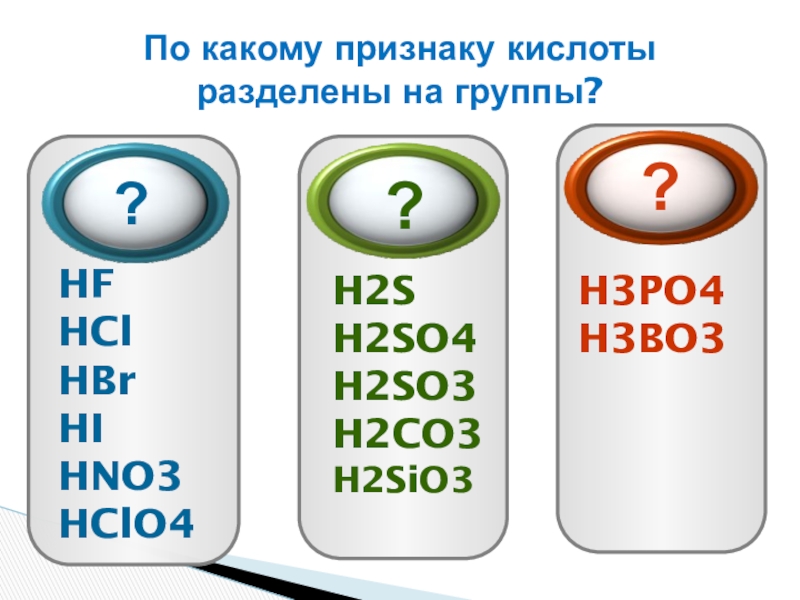
Слайд 25По какому признаку кислоты разделены на группы?
?
HF
HCl
HBr
HI
HNO3
HClO4
?
H2S
H2SO4
H2SO3
H2CO3
H2SiO3
?
H3PO4
H3BO3
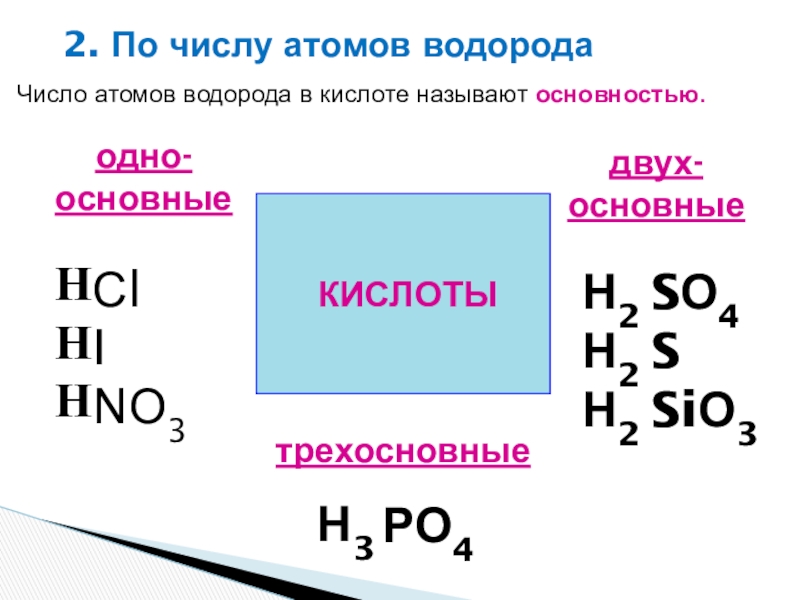
Слайд 26КИСЛОТЫ
2. По числу атомов водорода
Сl
I
NО3
SО4
S
SiО3
РО4
одно-
основные
двух-
основные
трехосновные
Н2
Н2
Н2
Н
Н
Н
Н3
Число атомов водорода в кислоте
называют основностью.
Слайд 28ПРАВИЛА БЕЗОПАСНОСТИ
Едкое вещество—кислота! Разрушает и раздражает кожу, слизистые оболочки.
Попавшие на
кожу капли раствора кислоты немедленно смойте сильной струей холодной воды,
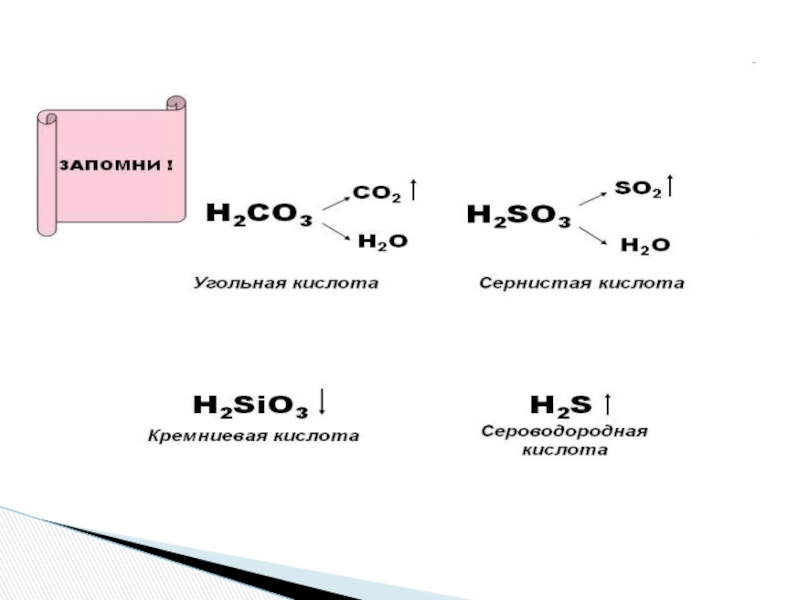
а затем обработайте поврежденную поверхность 2%-м раствором питьевой соды.Слайд 30Определите оксиды, соответствующие кислотам:
H2SO3
→
Сернистая кислота
HNO2
→ Азотистая кислота
SO2
N2O3
Слайд 31Кислоты – это сложные вещества, молекулы которых состоят из атомов
водорода и кислотного остатка.
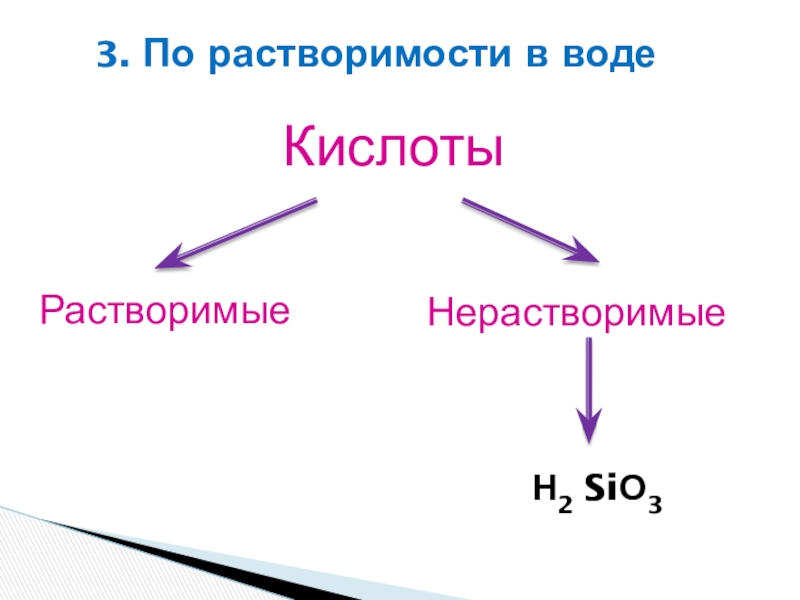
Классификация кислот – бескислородные и кислородсодержащие; одноосновные,
двухосновные и многоосновные; растворимые и нерастворимые. Кислоты изменяют окраску индикаторов: лакмуса из фиолетового в красный, метилового оранжевого из оранжевого в красный.
Индикаторы – вещества, изменяющие свой цвет в растворах кислот.
Слайд 32а) H3PO4
б) кислородсодержащая
в) трёхосновная
г) растворимая в воде
д) +1
+5 -2
H3PO4
е) H3+PO43-
ж) P2+5O5-2
Проверим:
Слайд 331. л а к м у с
2. а) HCl,
так как бескислородная кислота
б) H3PO4 , так
как трехосновная кислотаПроверим: