Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Коррозия металлов
Содержание
- 1. Коррозия металлов
- 2. Коррозия Корро́зия (от лат. corrosio — разъедание)
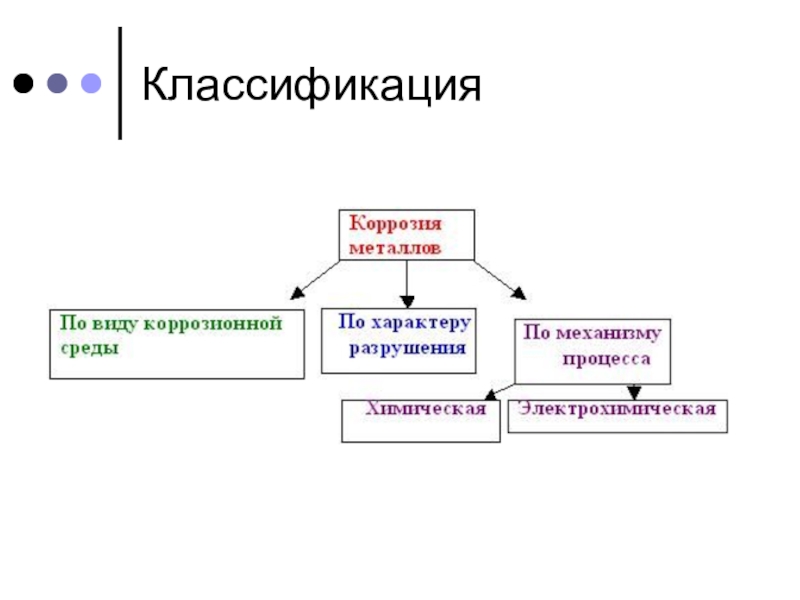
- 3. Классификация
- 4. «Ржа ест железо» - гласит русская народная
- 5. По характеру разрушения металла различаюткоррозию сплошную и
- 6. Химическая коррозия металлов — это разрушение
- 7. Электрохимическая коррозия— это разрушение металлов, которое сопровождается
- 8. Слайд 8
- 9. Слайд 9
- 10. Способы защиты от коррозии 1. легирование металлов2.
- 11. 1. легирование металлов1. легирование металлов, т.е. получение
- 12. 2. нанесение на поверхность металлов защитных пленок:2.
- 13. Слайд 13
- 14. 3. введение ингибиторов (замедлителей коррозии)3. введение ингибиторов
- 15. 4. протекторный метод защиты от коррозии
- 16. 4. протекторный метод защиты от коррозии Если
- 17. Закрепление Требуется скрепить железные детали. Какими заклепками
- 18. Скачать презентанцию
Коррозия Корро́зия (от лат. corrosio — разъедание) — это самопроизвольное разрушение металлов в результате химического или физико-химического взаимодействия с окружающей средой
Слайды и текст этой презентации
Слайд 4«Ржа ест железо» - гласит русская народная поговорка. Ржавчина, которая
появляется на поверхности стальных и чугунных изделий, - это яркий
пример коррозии.Ржавлением называют только коррозию железа и его сплавов. Другие металлы коррозируют, но не ржавеют.
Слайд 5По характеру разрушения металла различают
коррозию сплошную и местную.
Сплошная коррозия
распределяется равномерно по всей поверхности металла или сплава (например,процесс ржавления
сплавов железа на воздухе или их взаимодействие с сильными кислотами).При местной коррозии ее очаги распределяются неравномерно — в виде коррозионных пятен или точек, что особенно опасно для промышленной химической аппаратуры.
Слайд 6Химическая коррозия металлов
— это разрушение металлов в результате их
химического взаимодействия с веществами окружающей среды.
Наиболее распространенным видом химической
коррозии является газовая коррозия,проистекающая в сухих газах при полном отсутствии влаги. Газообразное вещество окружающей среды реагирует с металлом на поверхности металлического изделия и образует с ним соединения. Слайд 7Электрохимическая коррозия
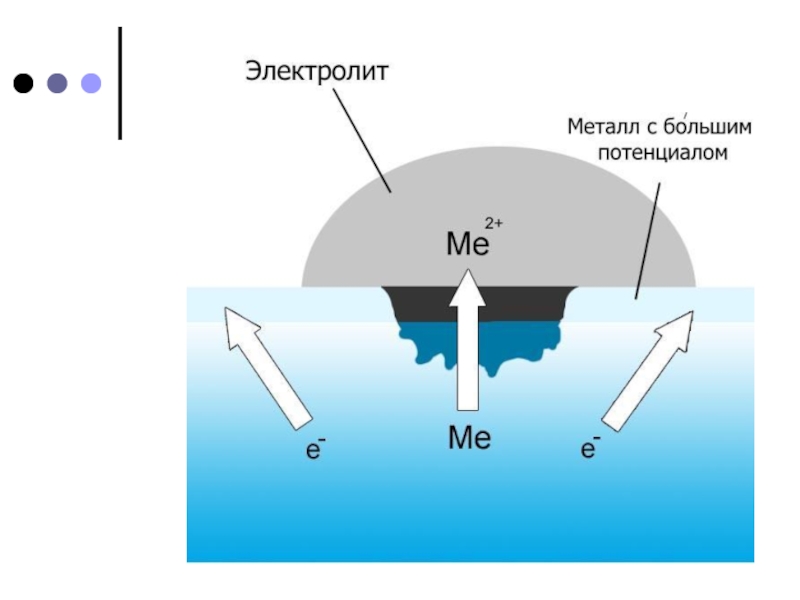
— это разрушение металлов, которое сопровождается возникновением электрического тока.
Это такая коррозия, в результате которой наряду с химическими процессами
(отдача электронов атомами коррозируемого металла — процесс окисления)протекают электрические (перенос электронов от одного участка изделия к другому).Слайд 10Способы защиты от коррозии
1. легирование металлов
2. нанесение на поверхность металлов
защитных пленок
3. введение ингибиторов (замедлителей коррозии)
4. протекторный метод защиты
от коррозииСлайд 111. легирование металлов
1. легирование металлов, т.е. получение сплавов. Например, в
настоящее время создано большое число нержавеющих сталей путем присадок к
железу никеля, хрома, кобальта и др. Такие стали, действительно, не покрываются ржавчинойСлайд 122. нанесение на поверхность металлов защитных пленок:
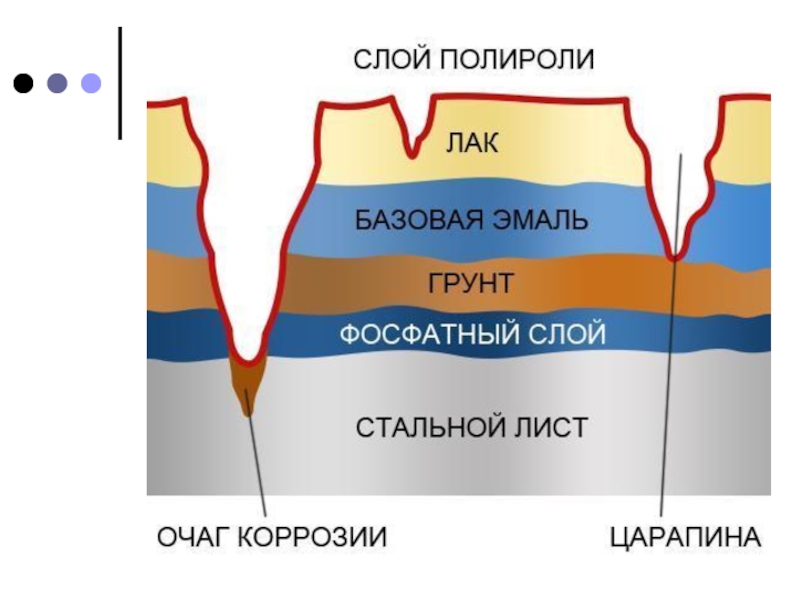
2. нанесение на поверхность
металлов защитных пленок: лака, краски, эмали, других металлов.
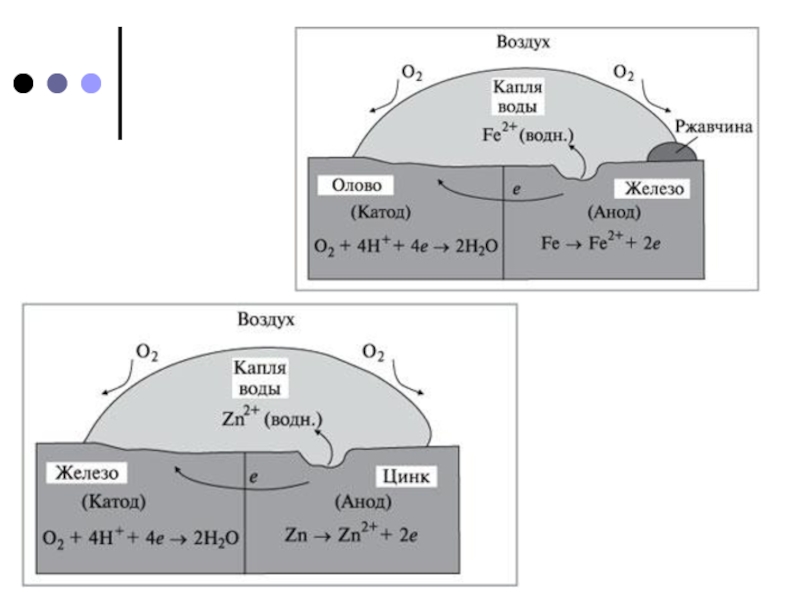
Листовое железо,
покрытое цинком, называют оцинкованным железом, а покрытое оловом – белой жестью. Первое в больших количествах идет на кровли домов, а из второго изготавливают консервные банки. И то и другое получают главным образом протягиванием листа железа через расплав соответствующего металла.Покрытия из цинка и олова (так же, как и других металлов) защищают железо от коррозии при сохранении сплошности. При нарушении покрывающего слоя (трещины, царапины) коррозия изделия протекает даже более интенсивно, чем без покрытия. Это объясняется «работой» гальванического элемента железо – цинк и железо – олово.
Слайд 143. введение ингибиторов (замедлителей коррозии)
3. введение ингибиторов (замедлителей коррозии)
Проведение
эксперимента. В пробирку на 1/5 объема налили разбавленную серную кислоту,
затем поместили в нее железные стружки. Довели до кипения. Наблюдали выделение пузырьков газа водорода.Затем в эту же пробирку добавили ингибитор уротропин (1 измельченную таблетку). Уротропин можно заменить тиомочевиной или сухим горючим. Реакция с кислотой прекратилась.
Слайд 164. протекторный метод защиты от коррозии
Если это не учитывать!
Один из
американских миллионеров, не жалея денег,решил построить самую шикарную яхту. Ее
днище было обшито дорогим металлом (сплав 70% никеля и 30%меди), а киль, форштевень и раму руля изготовили из стали. В морской воде в подводной части яхты образовался гальванический элемент с катодом из металла, а анодом из стали. Он настолько энергично работал, что яхта еще до завершения отделочных работ вышла из строя, ни разу не побывав в море.Слайд 17Закрепление
Требуется скрепить железные детали. Какими заклепками следует пользоваться медными или
цинковыми, чтобы замедлить коррозию железа? Ответ обоснуйте.
Как называются вещества, замедляющие
коррозию?Введение каких элементов в сталь повышает ее коррозионную стойкость?
К стальному днищу машины была предложена протекторная защита. Какой металл для этого лучше применить: Zn, Cu или Ni?
Почему многие детали быстрее корродируют вблизи предприятий?
Лист железа, покрытый цинком, и лист железа, покрытый оловом, процарапали до железа. Будет ли подвергаться коррозии железо в обоих случаях?