Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Коррозия металлов
Содержание
- 1. Коррозия металлов
- 2. Слово коррозия происходит от латинского «corrodere», что
- 3. Ущерб, наносимый коррозиейМировая потеря 20 млн. тонн металла в годЕще более значимы косвенные потери
- 4. В III до нашей эры на острове
- 5. Что является символом Парижа? –Эйфелева башня. Она
- 6. Хотя коррозию чаще всего связывают с металлами,
- 7. Таким образом, коррозия - самопроизвольный процесс разрушения
- 8. Виды коррозии
- 9. КоррозияПо виду коррозионной средыПо характеруразрушенияПо процессамГазоваяЖидкостная Атмосферная Почвенная Сплошная Местная Химическая Электрохимическая Межкристаллитная Блуждающими токами
- 10. По виду коррозионной среды
- 11. Газовая Атмосферная Жидкостная Почвенная Блуждающими токами
- 12. По характеру разрушений
- 13. Сплошная коррозияРавномерная Неравномерная
- 14. Местная коррозияЯзвенная Точечная Пятнами
- 15. Причины возникновения местной коррозииСоль на дорогахМорская водаМежкристаллитная коррозия
- 16. По процессам
- 17. Химическая коррозияХимическая коррозия – самопроизвольное разрушение металлов
- 18. Химическая коррозия не сопровождается возникновением электрического тока.
- 19. Электрохимическая коррозияЭлектрохимическая коррозия металлов – самопроизвольный процесс
- 20. Закономерности коррозии: 1. Если соединены два разных
- 21. 2. Скорость коррозии тем больше, чем
- 22. Разрушение железа, покрытого медью в кислой среде
- 23. Строго отделить химическую коррозию от электрохимической трудно,
- 24. Защита металлов от коррозии
- 25. Нанесение защитных покрытийПластмасса Краска ЛакГрунтовкаСмолаЭмаль Масло
- 26. Позолота Покрытие антикоррозионным металломЛужение Покрытие алюминиемПокрывающие металлы
- 27. Покрытие антикоррозионным металломХромирование Никелирование Оцинковка
- 28. Создание сплавов с антикоррозионными свойствами. Для этого
- 29. Протекторная защита анодFeО2О2Zn - 2е- → Zn2+катодZn
- 30. ЭлектрозащитаЭлектрический ток пропускают в направлении, противоположном тому, который возникает в процессе коррозии.
- 31. Усиление коррозии SnанодкатодFe - 2е-
- 32. Применение ингибиторовИнгибиторы - это вещества, способные замедлять
- 33. Известно, что дамасские мастера для снятия окалины
- 34. Задача 1Сантехника попросили поставить водопроводный кран, на
- 35. Задача 2Человек поставил на зуб золотую коронку,
- 36. СПАСИБО ЗА ВНИМАНИЕ!
- 37. Скачать презентанцию
Слайды и текст этой презентации
Слайд 3Ущерб, наносимый коррозией
Мировая потеря 20 млн. тонн металла в год
Еще
более значимы косвенные потери
Слайд 4В III до нашей эры на острове Родос был построен
маяк в виде огромной статуи Гелиоса.
Колосс Родосский
считался одним из семи чудес света, однако просуществовал всего 66 лет и рухнул во время землетрясения. У Колосса Родосского бронзовая оболочка была смонтирована на железном
каркасе.
Под действием влажного,
насыщенного солями
средиземноморского воздуха
железный каркас разрушился.
Слайд 5 Что является символом Парижа? –Эйфелева башня.
Она неизлечима больна, ржавеет
и разрушается, и только постоянная химиотерапия помогает бороться с этим
смертельным недугом:её красили 18 раз, отчего её масса 9000 т каждый раз увеличивается на 70 т.
Слайд 6 Хотя коррозию чаще всего связывают с металлами, но ей подвергаются
также камни, пластмассы и другие полимерные материалы и дерево.
Например,
в настоящее время мы являемся свидетелями большого беспокойства широких слоев людей в связи с тем, что от кислотных дождей катастрофически страдают памятники (здания и скульптуры), выполненные из известняка или мрамора.Слайд 7Таким образом,
коррозия - самопроизвольный процесс разрушения материалов и изделий
из них под химическим воздействием окружающей среды.
Коррозия– это процесс
перехода металла в то природное, естественное состояние, в котором мы встречаем его в земной коре. Процессы физического разрушения к коррозии не относят, хотя
часто они наносят
не меньший вред
памятникам культуры.
Их называют
истиранием,
износом, эрозией
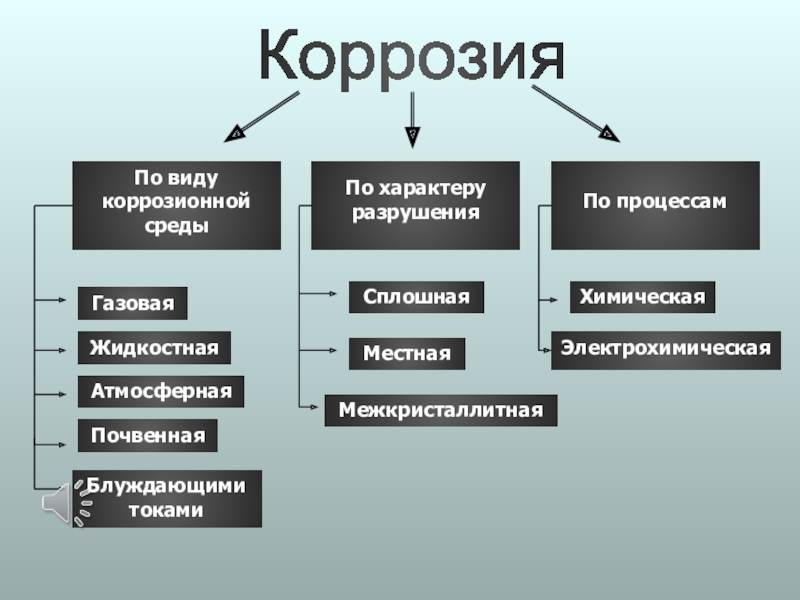
Слайд 9Коррозия
По виду
коррозионной среды
По характеру
разрушения
По процессам
Газовая
Жидкостная
Атмосферная
Почвенная
Сплошная
Местная
Химическая
Электрохимическая
Межкристаллитная
Блуждающими токами
Слайд 17Химическая коррозия
Химическая коррозия – самопроизвольное разрушение металлов
в среде окислительного
газа (кислорода, галогенов и т.д.) при
повышенных температурах или в
жидких не электролитах.2Fe + 3Cl2 = 2FeCl3
4Fe + 3О2 = 2Fe2 О3
Газовая
В жидких
не электролитах
В нефти
В сере
В органических веществах
Cu + S = CuS
2 Ag + S = Ag2S
2Al + 6ССl4 = 3C2Cl6 + 3AlCl3
Слайд 18Химическая коррозия не сопровождается возникновением электрического тока. Она основана
на реакции
между металлом и агрессивным реагентом.
Этот вид коррозии протекает в
основном равномерно по всей поверхности металла. В связи с этимхимическая коррозия менее опасна, чем электрохимическая.
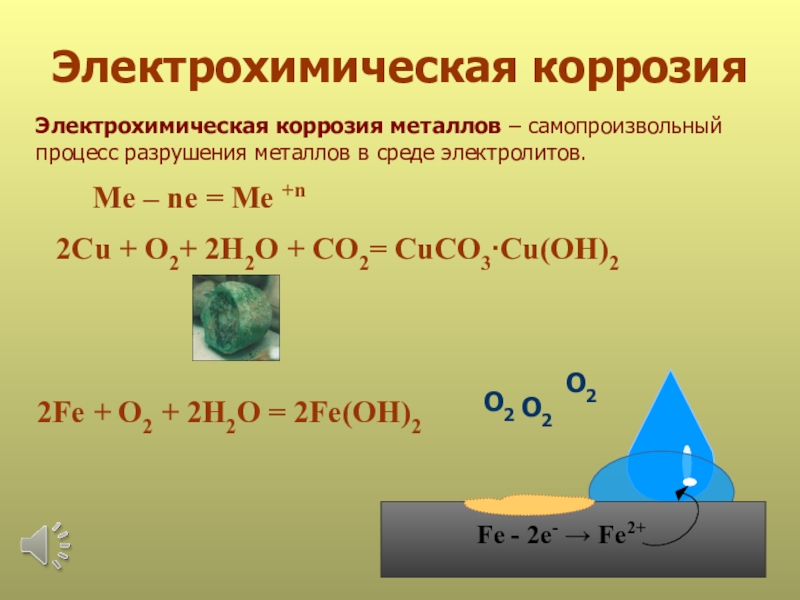
Слайд 19Электрохимическая коррозия
Электрохимическая коррозия металлов – самопроизвольный
процесс разрушения металлов в
среде электролитов.
2Fe + O2 + 2H2O = 2Fe(OH)2
Me –
ne = Me +nFe - 2е- → Fe2+
О2
О2
2Сu + O2+ 2H2O + CO2= CuCO3∙Cu(OH)2
О2
Слайд 20Закономерности коррозии:
1. Если соединены два разных металла, то
коррозии подвергается только более активный, и пока он полностью не
разрушится, менее активный защищён.Слайд 21 2. Скорость коррозии тем больше, чем дальше друг от
друга в ряду напряжений расположены соединённые металлы.
Закономерности коррозии:
Слайд 23Строго отделить химическую коррозию от электрохимической трудно, а иногда и
невозможно. Дело в том, что электрохимическая коррозия часто связана с
наличием в металле случайных примесей или специально введенных легирующих добавок.Слайд 26Позолота
Покрытие антикоррозионным металлом
Лужение
Покрытие
алюминием
Покрывающие металлы сами корродируют с
малой скоростью, так как покрываются плотной оксидной пленкой.
Слайд 28Создание сплавов с антикоррозионными свойствами.
Для этого в основной металл
добавляют до 12% хрома, никеля, кобальта или меди
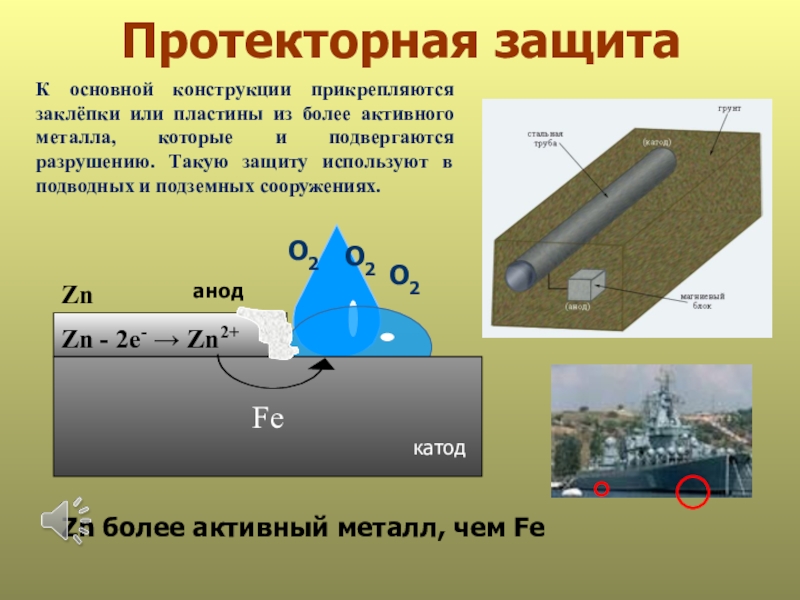
Слайд 29Протекторная защита
анод
Fe
О2
О2
Zn - 2е- → Zn2+
катод
Zn более активный металл,
чем Fe
Zn
О2
К основной конструкции прикрепляются заклёпки или пластины из более
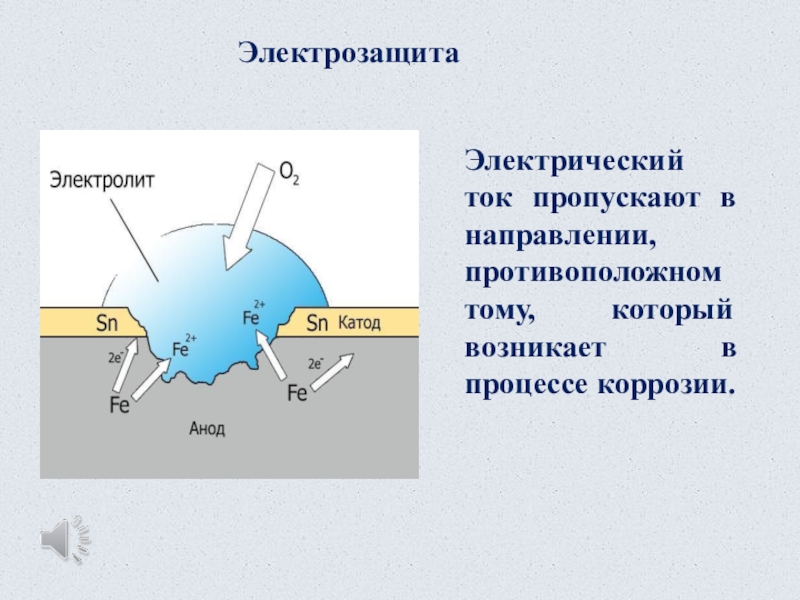
активного металла, которые и подвергаются разрушению. Такую защиту используют в подводных и подземных сооружениях.Слайд 30Электрозащита
Электрический ток пропускают в направлении, противоположном тому, который возникает в
процессе коррозии.
Слайд 31
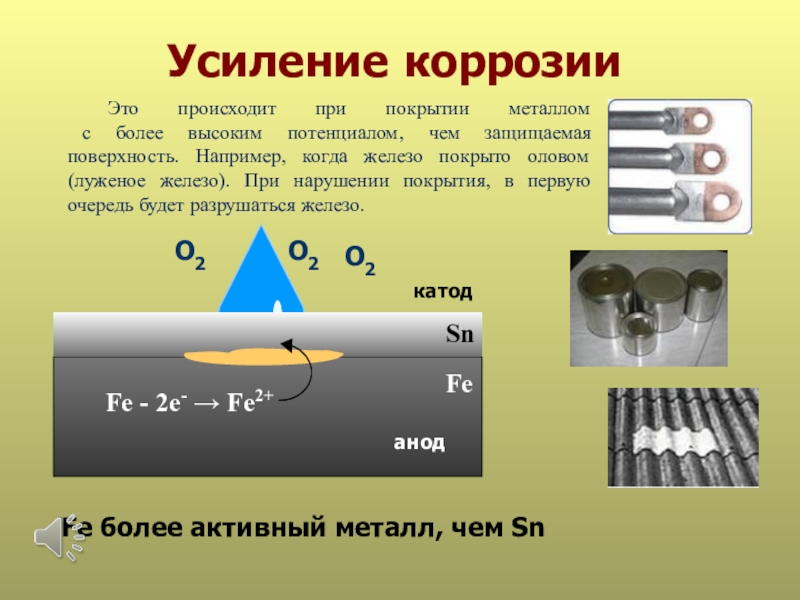
Усиление коррозии
Sn
анод
катод
Fe - 2е- → Fe2+
Fe
Fe более активный металл,
чем Sn
О2
О2
О2
Это происходит при покрытии металлом
с более высоким
потенциалом, чем защищаемая поверхность. Например, когда железо покрыто оловом (луженое железо). При нарушении покрытия, в первую очередь будет разрушаться железо.Слайд 32Применение ингибиторов
Ингибиторы - это вещества, способные замедлять протекание химических процессов
или останавливать их.
Известно более 5 тысяч
Применение ингибиторов – один
из эффективных способов борьбы с коррозией металлов в различных агрессивных средах (в атмосферных, в морской воде, в охлаждающих жидкостях и солевых растворах, в окислительных условиях и т.д.). Слайд 33Известно, что дамасские мастера для снятия окалины и ржавчины пользовались
растворами серной кислоты с добавками пивных дрожжей, муки, крахмала. Эти
примеси были одними из первых ингибиторов. Они не позволяли кислоте действовать на оружейный металл, в результате чего растворялись лишь окалина и ржавчина.Слайд 34Задача 1
Сантехника попросили поставить водопроводный кран,
на стальную трубу. В
наличии оказались хромированный и медный краны. Какой кран лучше выбрать?
Аргументируйте ответ.Слайд 35Задача 2
Человек поставил на зуб золотую коронку, по истечении
некоторого
времени возникла необходимость в еще одной
коронке, но средств на коронку
у него нет. Возможен ли вариант, чтобы поставить на зуб
стальную коронку?
Что Вы можете предложить в решении данной проблемы?