Слайд 1Ксенобиотики
Микросомальное окисление
Автор – доцент Е.А. Рыскина
Слайд 2Ксенобиотики (чужеродные вещества) – вещества, поступающие из окружающей среды и
не используемые в организме
1. Продукты хозяйственной деятельности человека (промышленность, сельское
хозяйство и др.)
2. Вещества бытовой химии (моющие средства, пестициды, парфюмерия и др.)
3. Вулканы и природные
выбросы
4. Большинство лекарств
Слайд 3Детоксикация или обезвреживание ксенобиотиков.
Гидрофильные ксенобиотики выводятся с мочой в неизменном
виде.
Гидрофобные ксенобиотики могут задерживаться в тканях и застревать в
мембранах клеток.
Для удаления ненужных для
организма веществ в процессе
эволюции выработались
механизмы их детоксикации.
Слайд 4Механизмы обезвреживание ксенобиотиков.
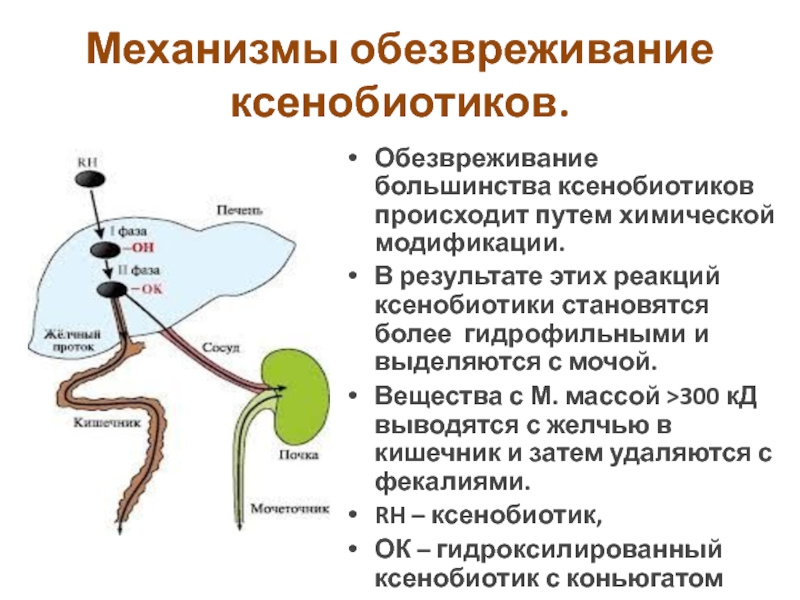
Обезвреживание большинства ксенобиотиков происходит путем химической модификации.
В
результате этих реакций ксенобиотики становятся более гидрофильными и выделяются с
мочой.
Вещества с М. массой >300 кД выводятся с желчью в кишечник и затем удаляются с фекалиями.
RH – ксенобиотик,
ОК – гидроксилированный ксенобиотик с коньюгатом
Слайд 5Система обезвреживания
состоит из 2 фаз:
Химическая модификация ксенобиотика включает:
1
фаза - Повышение растворимости ксенобиотика.
Можно ввести ОН – группу. Это
осуществляется на цитохроме Р-450 и называется микросомальное окисление. Большинство ксенобиотиков обезвреживаются таким образом.
2 фаза - Образование коньюгатов .
Коньюгаты образуются с глюкуроновой кислотой, глицином, глутатионом. Далее они выводятся из клетки и организма.
Слайд 6Система обезвреживания включает множество микросомальных ферментов, под действием которых практически
любой ксенобиотик может быть модифицирован. Микросомальные ферменты катализируют реакции (R
– ксенобиотик):
Гидроксилирование RH → ROH
Окислительное дезаминирование
RNH2 → R=O + NH3
Дезалкилирование по азоту, кислороду, сере:
RNHCH3 → RNH2 + H2C=O
ROCH3 → ROH + H2CO
RSCH3 → RSH + H2CO
Окисление по атому серы (сульфоокисление) и др.
Слайд 7Микросомальное окисление
Микросомальное окисление - совокупность реакций первой фазы биотрансформации
ксенобиотиков и эндогенных соединений, катализирующихся ферментными системами мембран эндоплазматического ретикулума
гепатоцитов при участии цитохрома Р-450.
При центрифугировании эндоплазматический ретикулум оказывается в микросомальной фракции, поэтому эти реакции получили название микросомальных, а соответствующие ферменты - микросомальных оксигеназ.
Слайд 8Семейство цитохромов Р-450
Цитохром Р450-зависимые монооксигеназы катализируют расщепление различных веществ с
участием донора электрона НАДФН и молекулярного кислорода.
Ферменты семейства Р450
могут также катализировать реакции гидроксилирования алифатических соединений, N-окисление, окислительное дезаминирование, реакции восстановления нитросоединений.
Семейство цитохромов – Р – 450 включает более 100 изоформ.
Цитохром Р-450 содержит в качестве кофермента железосодержащий гем, имеет участки связывания с кислородом и ксенобиотиком.
Слайд 9Микросомальная система окисления состоит из 2 электронтранспортных цепей (внемитохондриальные ЦПЭ)
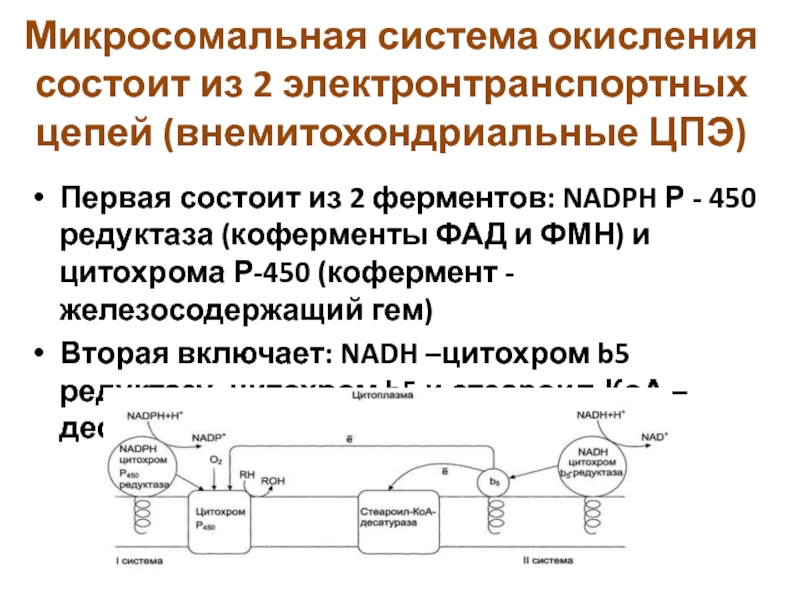
Первая
состоит из 2 ферментов: NADPH Р - 450 редуктаза (коферменты
ФАД и ФМН) и цитохрома Р-450 (кофермент - железосодержащий гем)
Вторая включает: NADH –цитохром b5 редуктазу, цитохром b5 и стеароил-КоА –десатуразу.
Слайд 10Функционирование первой ЦПЭ
Мультиферментный комплекс формирует цепь переноса электронов и протонов,
в конце ее происходит активация кислорода. Активированный кислород присоединяется к
активному центру цитохрома Р450, и на него переносятся электроны, а затем этот кислород включается в молекулу субстрата (ксенобиотика).
Слайд 11Функционирование второй ЦПЭ
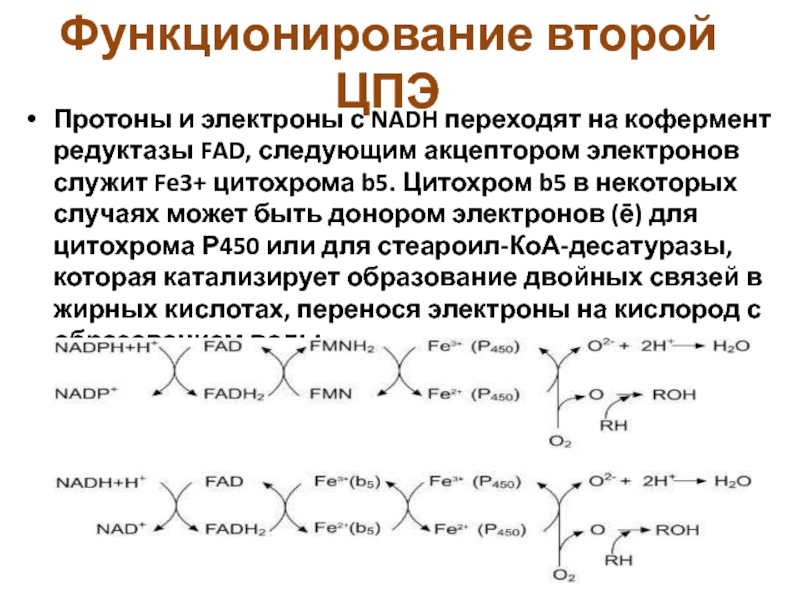
Протоны и электроны с NADH переходят на кофермент
редуктазы FAD, следующим акцептором электронов служит Fe3+ цитохрома b5. Цитохром
b5 в некоторых случаях может быть донором электронов (ē) для цитохрома Р450 или для стеароил-КоА-десатуразы, которая катализирует образование двойных связей в жирных кислотах, перенося электроны на кислород с образованием воды.
Слайд 12Реакции гидроксилирования на цитохроме Р450
Суть реакций заключается в гидроксилировании вещества
типа R-H с использованием одного атома молекулы кислорода О2, второй
атом соединяется с протонами водорода H+ с образованием воды. Донором протонов водорода является восстановленный NADPH(H+). Таким образом, меняется структура исходного вещества.
Уравнение реакции:
RH + O2 + NADPH(H+) → ROH + H2O + NADP+
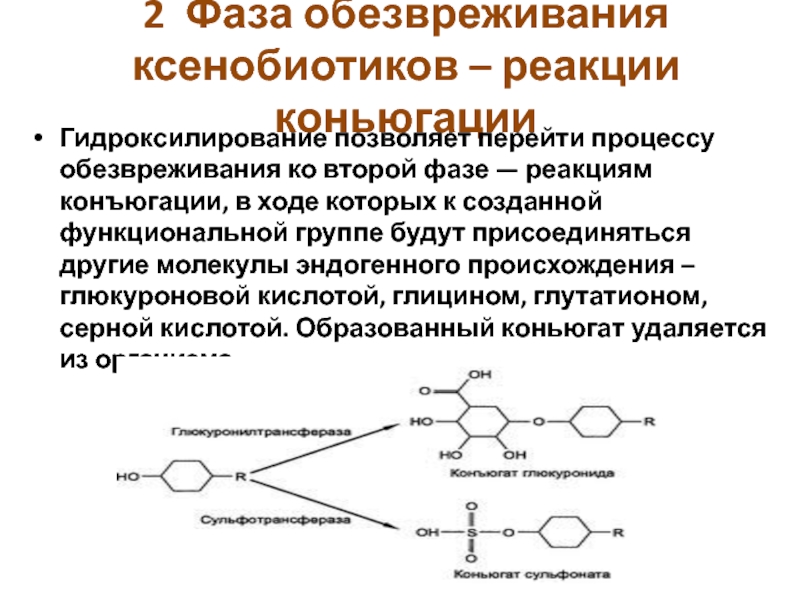
Слайд 132 Фаза обезвреживания ксенобиотиков – реакции коньюгации
Гидроксилирование позволяет перейти процессу
обезвреживания ко второй фазе — реакциям конъюгации, в ходе которых
к созданной функциональной группе будут присоединяться другие молекулы эндогенного происхождения – глюкуроновой кислотой, глицином, глутатионом, серной кислотой. Образованный коньюгат удаляется из организма.
Слайд 14Все ферменты, функционирующие во второй фазе обезвреживания ксенобиотиков, относят к
классу трансфераз. Они характеризуются широкой субстратной специфичностью.
Слайд 15Свойства системы микросомального окисления - широкая субстратная специфичность, которая позволяет
обезвреживать самые разнообразные по строению вещества и ксенобиотики.