Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
КУЛЬТИВИРОВАНИЕ ВИРУСОВ
Содержание
- 1. КУЛЬТИВИРОВАНИЕ ВИРУСОВ
- 2. Способы культивирования вирусовкуриный эмбрионкультура клетокорганизм лабораторного животногообнаружение наличия вируса(индикация)определение типа вируса(идентификация)
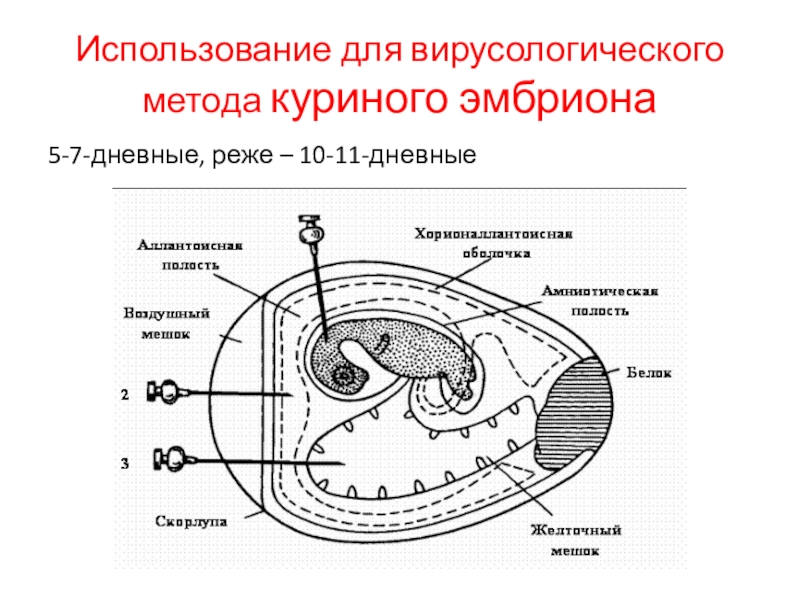
- 3. Использование для вирусологического метода куриного эмбриона5-7-дневные, реже – 10-11-дневные
- 4. Основные способы заражения куриных эмбрионовна хорион-аллантоисную оболочкув хорион-аллантоисную полостьв полость желточного мешкав полость амнионав тело эмбриона
- 5. Обнаружение вирусов в курином эмбрионеиндикация:гибель эмбрионаморфологические изменения
- 6. Использование культур клетокКультуры клеток = соматические или
- 7. Первичные культуры клетокполучают из тканей (эмбриональных или
- 8. Перевиваемые культуры клетокПеревиваемые = стабильные = готовят
- 9. Полуперевиваемые культуры клеток– диплоидные клетки различных тканей
- 10. Преимущества перевиваемых культур клеток перед первичными:продолжительность
- 11. Использование культур клетокЧаще – перевиваемые монослойныеиндикация:ЦПД (цитопатическое
- 12. Условия культивирования клеток: Питательные среды сложного
- 13. Условия культивирования клеток: Питательные среды сложного
- 14. Обнаружение = индикация вирусов в культуре
- 15. ЦПД = видимые под микроскопом морфологические
- 16. Виды ЦПДокругление и сморщивание клеток – пикорнавирусы,нарастающая
- 17. ЦПД вирусов
- 18. Включения= скопление вирионов или отдельных их компонентов
- 19. Тельца Бабеша-Негри
- 20. Бляшки, или “негативные” колонии= ограниченные участки разрушенных
- 21. Реакция гемагглютинации (РГА)основана на способности некоторых вирусов
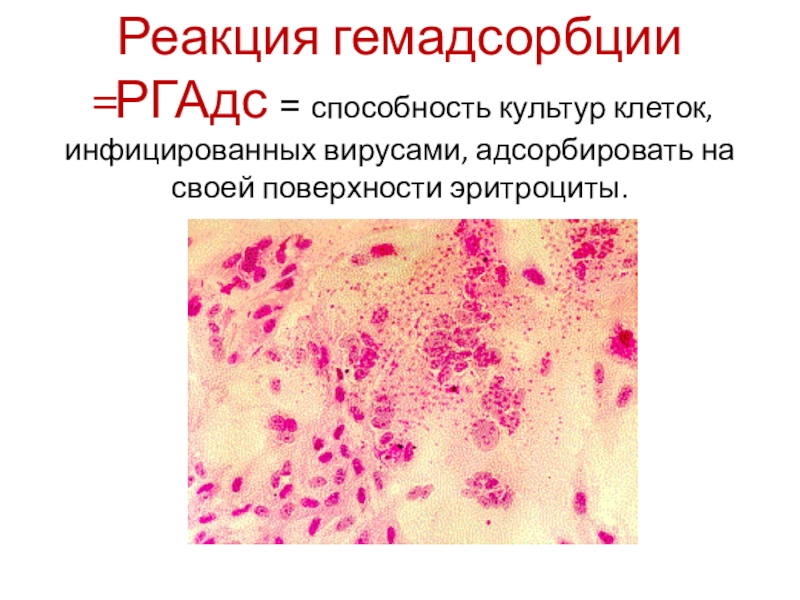
- 22. Реакция гемадсорбции =РГАдс = способность культур
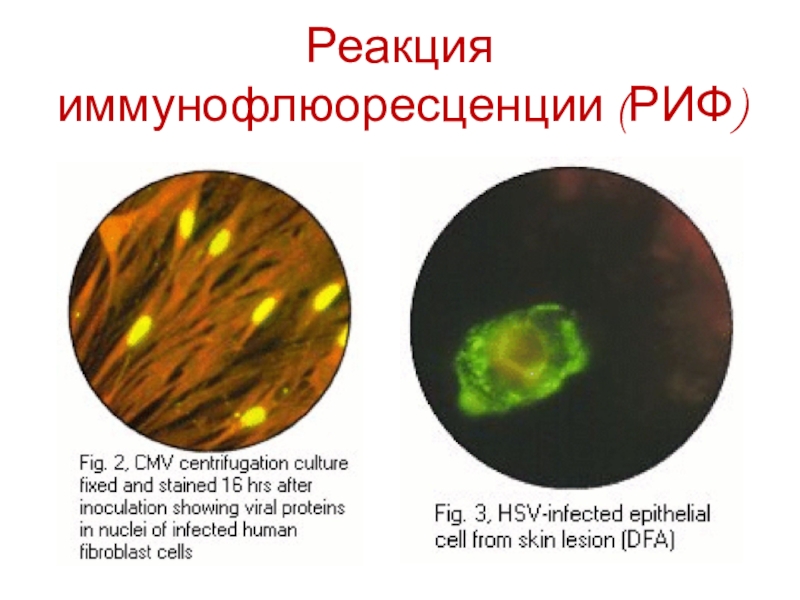
- 23. Реакция иммунофлюоресценции (РИФ)
- 24. Использование лабораторных животныхвзрослые или новорожденные белые мыши,
- 25. Способы заражения лабораторных животныхинтраназально, подкожно, внутримышечно, внутрибрюшинно, интрацеребрально,
- 26. Обнаружение вируса при заражении лабораторных животныхобнаруживают вирус
- 27. Прионы – белковые молекулы, способные вызывать разрушение
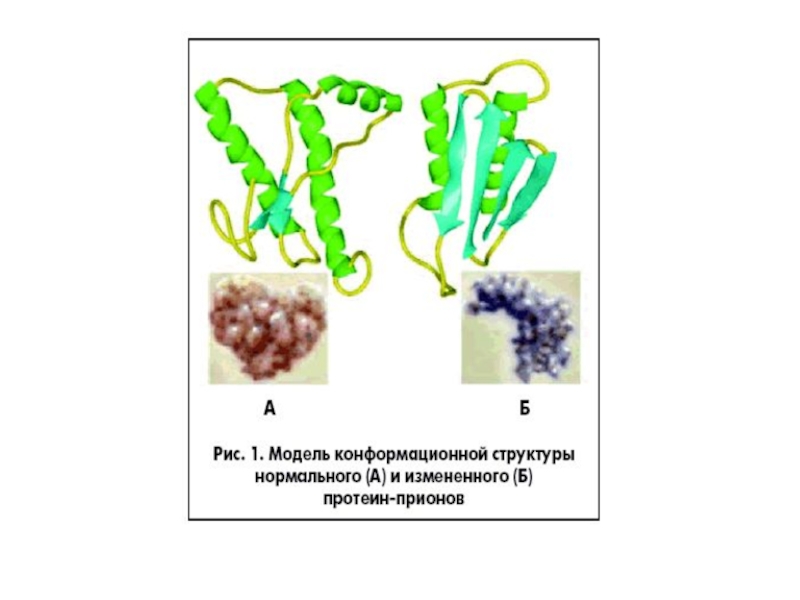
- 28. Прионы Прионный белок может существовать в двух
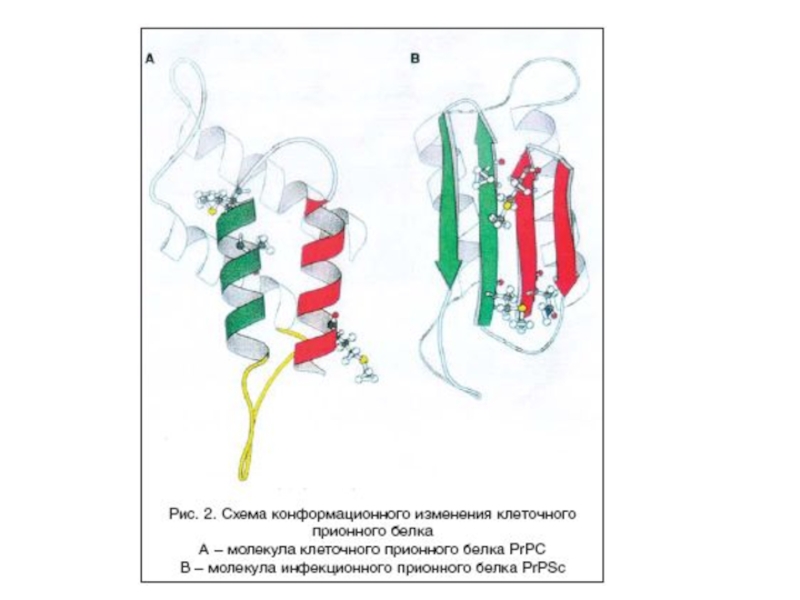
- 29. Прионы инфекционная форма (PrPs) – характеризуется:измененной вторичной
- 30. Слайд 30
- 31. Слайд 31
- 32. Слайд 32
- 33. Слайд 33
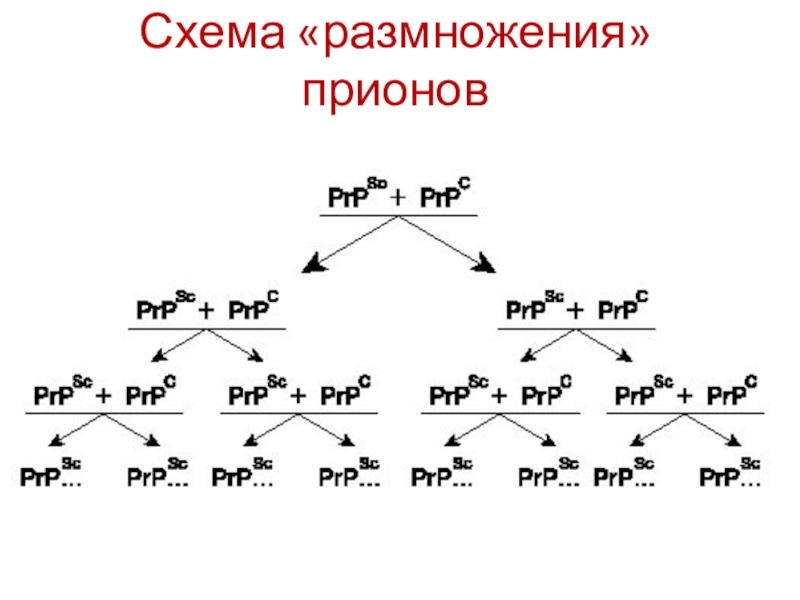
- 34. Схема «размножения» прионов
- 35. БАКТЕРИОФАГИвирусы бактерий
- 36. БАКТЕРИОФАГИ«пожирающий бактерии» (от бактерия + греч. phagos
- 37. Слайд 37
- 38. Слайд 38
- 39. Строение бактериофаговикосаэдрическая головка,хвостовой отросток: внутри – полый
- 40. Слайд 40
- 41. Нуклеиновая кислота фагаБактериофаги (фаги) содержат ДНК или
- 42. В состав головки входит: полипептид, состоящий
- 43. В состав сокращающегося чехла входит:
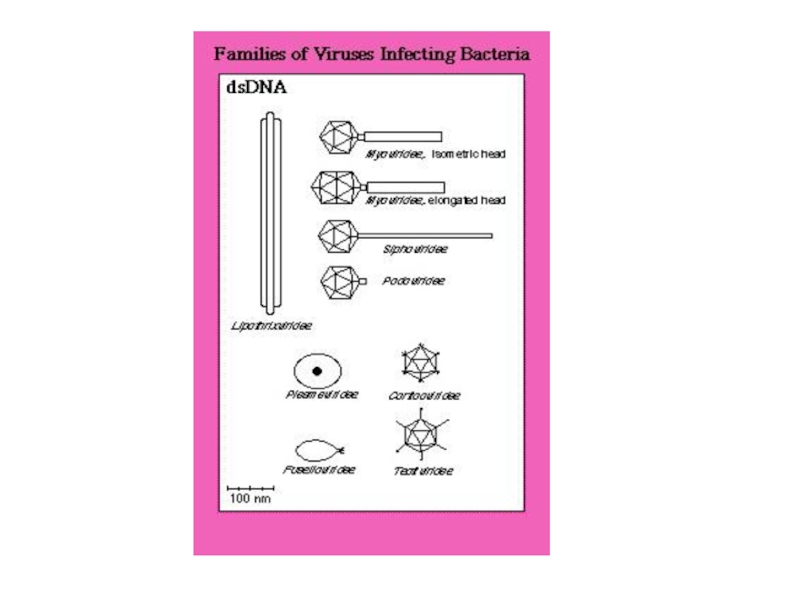
- 44. Морфологические типы бактериофаговI тип (нитчатые)без головки (только
- 45. Слайд 45
- 46. Классификация бактериофагов по спектру действияполифагипоражают несколько видовмонофаги (видовые)поражают один видтиповые фагипоражают часть вида (фаговар)
- 47. Классификация фагов в зависимости от эффекта действия на бактериальную клеткувирулентныеумеренные
- 48. Классификация фагов в зависимости от эффекта действия
- 49. Классификация фагов в зависимости от эффекта действия
- 50. Взаимодействие фагов с бактериямиможет происходить:- по продуктивному
- 51. Вирулентные бактериофагипопав в бактерию, реплицируются, формируя 200-300
- 52. Взаимодействие вирулентного фага с бактериальной клеткойадсорбция фага
- 53. Этапы взаимодействия вирулентного фага с бактериальной клеткой
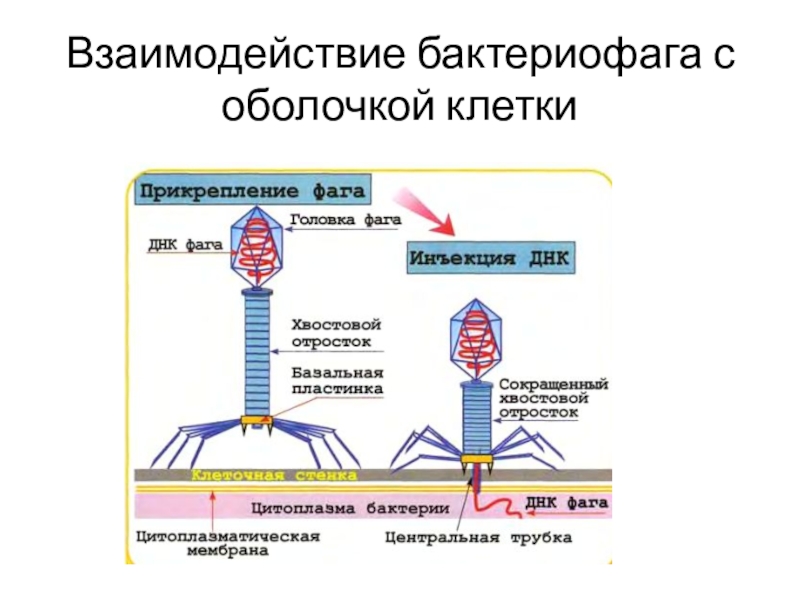
- 54. Взаимодействие бактериофага с оболочкой клетки
- 55. Этапы взаимодействия вирулентного фага с бактериальной клеткой
- 56. Этапы взаимодействия вирулентного фага с бактериальной клеткой
- 57. Взаимодействие умеренного фага с бактериальной клеткойадсорбция фага
- 58. Взаимодействие умеренного фага с бактериальной клеткойУмеренные бактериофаги
- 59. Взаимодействие умеренного фага с бактериальной клеткойПри интегративном
- 60. Взаимодействие умеренного фага с бактериальной клеткойДНК фага,
- 61. Взаимодействие умеренного фага с бактериальной клеткойПри лизогении
- 62. Взаимодействие умеренного фага с бактериальной клеткойПрофаг придает
- 63. Применение фагов для профилактики, для
- 64. Практическое применение бактериофаговФагопрофилактикабрюшной тифдизентерия
- 65. Практическое применение бактериофаговФаготерапияФаг применяется в том случае, когда антибиотики применять нельзя,Чаще всего местно
- 66. Практическое применение бактериофаговФагодиагностикаВыявление определённого вида бактерий в патологическом материалереакция нарастания титра фагаИдентификация чистой культурыопределение видафагоиндикацияопределение фаговарафаготипирование
- 67. Выделение бактериофагаматериалобъект внешней средыбактериальная культурабактериальный фильтрфильтратМПБ +
- 68. Определение активности бактериофагов = фагоиндикация
- 69. Определение активности бактериофагов = фагоиндикация Качественный
- 70. Метод фагоиндикации = «стекающая капля» = «стерильная
- 71. Определение активности бактериофагов = фагоиндикация Количественные
- 72. Титрование фага по ГрациаМПА + разведение фагосодержащего
- 73. Слайд 73
- 74. Определение активности бактериофагов = фагоиндикация Количественные
- 75. Титрование фага по Аппельману
- 76. Фаготипирование бактерийзасев газоном на чашку с питательным
- 77. Слайд 77
- 78. Фаготипирование стафилококков
- 79. Определение спектра литического действия фага Чашку
- 80. Скачать презентанцию
Способы культивирования вирусовкуриный эмбрионкультура клетокорганизм лабораторного животногообнаружение наличия вируса(индикация)определение типа вируса(идентификация)
Слайды и текст этой презентации
Слайд 2Способы культивирования вирусов
куриный эмбрион
культура клеток
организм лабораторного животного
обнаружение наличия вируса
(индикация)
определение типа
вируса
Слайд 3Использование для вирусологического метода куриного эмбриона
5-7-дневные, реже – 10-11-дневные
Слайд 4Основные способы заражения куриных эмбрионов
на хорион-аллантоисную оболочку
в хорион-аллантоисную полость
в полость
желточного мешка
в полость амниона
в тело эмбриона
Слайд 5Обнаружение вирусов в курином эмбрионе
индикация:
гибель эмбриона
морфологические изменения эмбриона/оболочек
РГА с жидкостью
из полостей куриного эмбриона
идентификация:
РН (в т.ч. РТГА)
РСК
Слайд 6Использование культур клеток
Культуры клеток = соматические или эмбриональные клетки человека
или животных, культивируемые в лабораторных условиях.
Подразделяют по числу жизнеспособных генераций
на:- первичные,
- перевиваемые,
- полуперевиваемые.
Слайд 7Первичные культуры клеток
получают из тканей (эмбриональных или нормальных) многоклеточных организмов.
Такие клетки не способны к делению – используются однократно.
В основе
получения лежит обработка протеолитическими ферментами (трипсином) = первично-трипсинизированные. Н-р, эмбриональная ткань человека, почечная ткань эмбрионов человека и обезьян.
Слайд 8Перевиваемые культуры клеток
Перевиваемые = стабильные = готовят из опухолевых клеток,
способных длительно размножаться in vitro не меняя своих свойств.
Н-р,HeLa
– выделены из карциномы шейки матки,Hep-2 – из карциномы гортани,
Hep-3 – лимфокарцинома,
KB – эпидермоидная карцинома полости рта,
Детройт-6 – костный мозг больного раком легкого.
Слайд 9Полуперевиваемые культуры клеток
– диплоидные клетки различных тканей и органов, способные
к ограниченному размножению in vitro.
Они сохраняют свои свойства в
течение 20-50 пассажей (пересевов) = до года. При культивировании не претерпевают злокачественного перерождения – преимущество перед перевиваемыми → могут использоваться в производстве вакцин.
Слайд 10 Преимущества перевиваемых культур клеток перед первичными:
продолжительность культивирования – десятки
лет,
высокая скорость размножения,
меньшая трудоемкость,
сохраняют свои свойства в замороженном состоянии много
лет,возможность использования международных линий культур.
Но: злокачественный характер и возможность мутаций ограничивает применение для производства вакцин.
Слайд 11Использование культур клеток
Чаще – перевиваемые монослойные
индикация:
ЦПД (цитопатическое действие вирусов –
любое изменение клеток монослоя, включая бляшкообразование и цветную пробу)
гемадсорбирующая активность
монослоя (РГАдс)РИФ (= идентификация)
идентификация:
РН (в т.ч. РТГАдс)
РСК
РИФ
Слайд 12
Условия культивирования клеток:
Питательные среды сложного состава (среда 199, Игла), сод-т
источники энергии (глюкозу), минеральные вещества, аминокислоты, витамины, сыворотку крови, факторы
роста.Клетки чувствительны к изменениям рН – для контроля рН добавляют индикатор и буферные растворы.
Соблюдение правил асептики.
Использование лабораторной посуды из нейтрального стекла – пробирки, флаконы, матрасы (=флакон 4-х гранной формы)
Добавление антибиотиков к питательной среде для подавления роста бактерий
Соблюдение оптимальной температуры культивирования (36-38,5о).
Слайд 13
Условия культивирования клеток:
Питательные среды сложного состава (среда 199, Игла), сод-т
источники энергии (глюкозу), минеральные вещества, аминокислоты, витамины, сыворотку крови, факторы
роста.Клетки чувствительны к изменениям рН – для контроля рН добавляют индикатор и буферные растворы.
Соблюдение правил асептики.
Использование лабораторной посуды из нейтрального стекла – пробирки, флаконы, матрасы (=флакон 4-х гранной формы)
Добавление антибиотиков к питательной среде для подавления роста бактерий
Соблюдение оптимальной температуры культивирования (36-38,5о).
Слайд 14 Обнаружение = индикация вирусов в культуре клеток
проводят на основе
следующих феноменов:
- цитопатогенного действия (ЦПД) вирусов или
цитопатического эффекта, - образования внутриклеточных включений,
- образования “бляшек”,
- реакции гемагглютинации, гемадсорбции или “цветной” реакции.
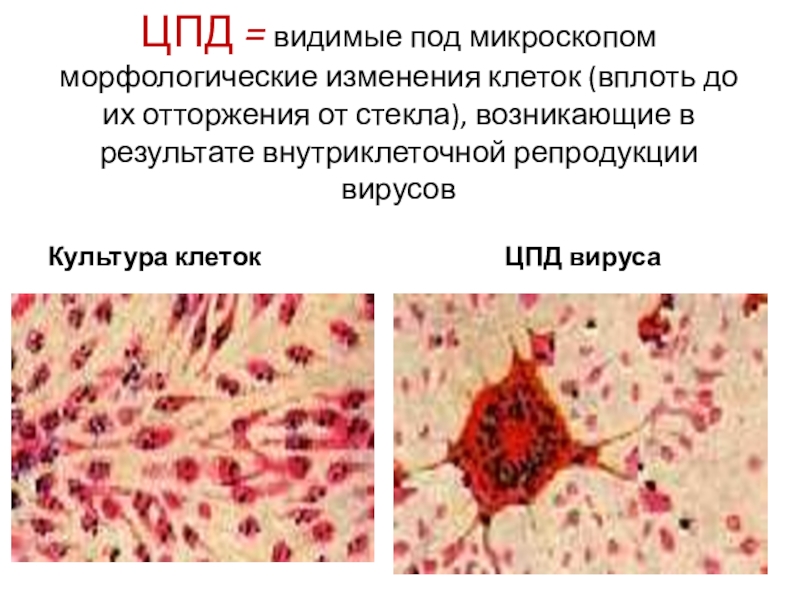
Слайд 15 ЦПД = видимые под микроскопом морфологические изменения клеток (вплоть до
их отторжения от стекла), возникающие в результате внутриклеточной репродукции вирусов
Культура
клетокЦПД вируса
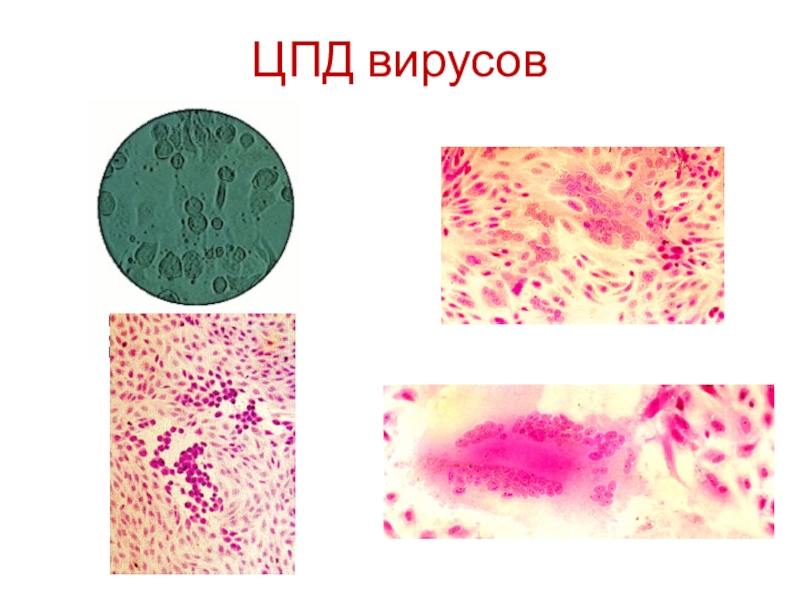
Слайд 16Виды ЦПД
округление и сморщивание клеток – пикорнавирусы,
нарастающая деструкция – герпесвирусы,
пролиферация
(образование дырок) – поксвирусы,
образование гигантских многоядерных клеток = симпласты –
парамиксовирусы.Слайд 18Включения
= скопление вирионов или отдельных их компонентов в цитоплазме или
ядре клеток, выявляемые под микроскопом при специальном окрашивании.
Н-р, вирус
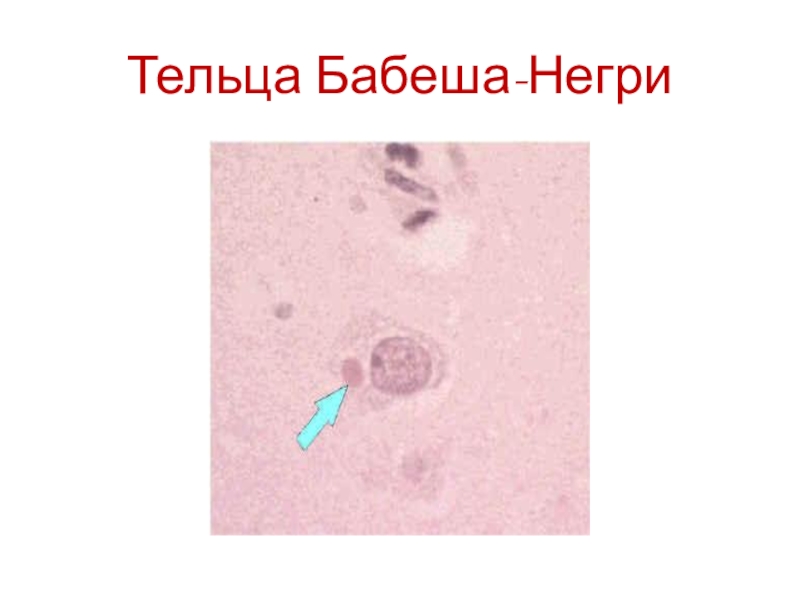
натуральной оспы образует цитоплазматические включения - тельца Гварниери;вирус бешенства в цитоплазме образует тельца Бабеша-Негри,
вирусы герпеса и аденовирусы - внутриядерные включения.
Слайд 20Бляшки, или “негативные” колонии
= ограниченные участки разрушенных вирусами клеток, культивируемых
на питательной среде под агаровым покрытием, видимые как светлые пятна
на фоне окрашенных живых клеток.Один вирион образует потомство в виде одной бляшки.
“Негативные” колонии разных вирусов отличаются по размеру, форме, поэтому метод бляшек используют для дифференциации вирусов, а также для определения их концентрации.
Слайд 21Реакция гемагглютинации (РГА)
основана на способности некоторых вирусов вызывать агглютинацию (склеивание)
эритроцитов за счет вирусных гликопротеиновых шипов – гемагглютининов.
Слайд 22 Реакция гемадсорбции =РГАдс = способность культур клеток, инфицированных вирусами, адсорбировать
на своей поверхности эритроциты.
Слайд 24Использование лабораторных животных
взрослые или новорожденные белые мыши, хомяки, кролики, обезьяны
применяется
для выделения тех вирусов, которые плохо репродуцируются в культуре клеток
или курином эмбрионе,Вид и способ заражения – от вируса
индикация:
заболевание животного
его гибель
идентификация:
РН
Слайд 25Способы заражения лабораторных животных
интраназально,
подкожно,
внутримышечно,
внутрибрюшинно,
интрацеребрально,
Слайд 26Обнаружение вируса при заражении лабораторных животных
обнаруживают вирус по:
- развитию
видимых клинических проявлений – параличи – рабдовирусы,
-патоморфологическим изменениям органов
и тканей – пикорна-, тогавирусы- в реакции гемагглютинации с суспензией из органов,
недостаток:
- высокая вероятность контаминации организма животных посторонними микробами,
- необходимость заражения культуры клеток для выделения чистой культуры вируса.
Слайд 27Прионы
– белковые молекулы, способные вызывать разрушение клеток организма человека
и животных.
Они характеризуются устойчивостью:
к высоким температурам,
ионизирующей радиации,
ультрафиолету.
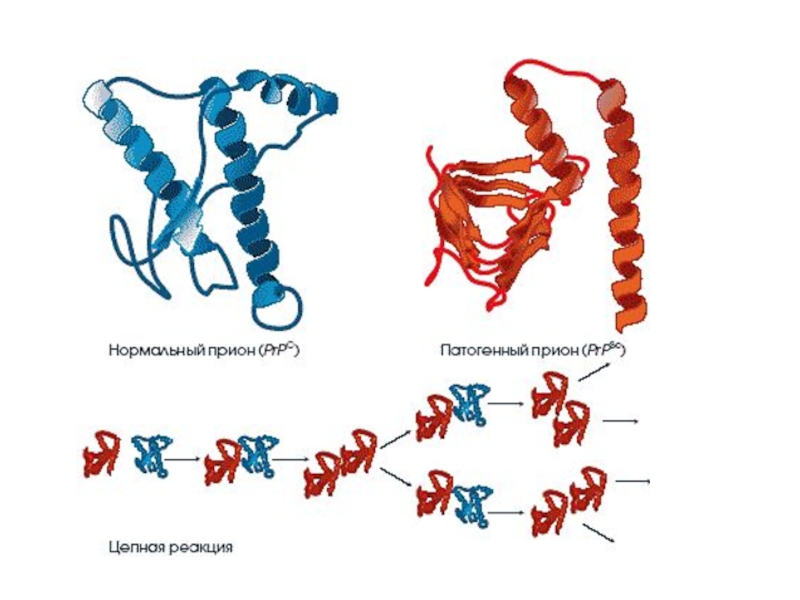
Слайд 28Прионы
Прионный белок может существовать в двух формах:
нормальная клеточная форма(РrPc)
- обнаруживается в организме всех млекопитающих.
Ген, кодирующий этот белок,
расположен в коротком плече 20 хромосомы. РrPc участвует в передаче нервных импульсов, в поддержании циркадных ритмов клетки,
Слайд 29Прионы
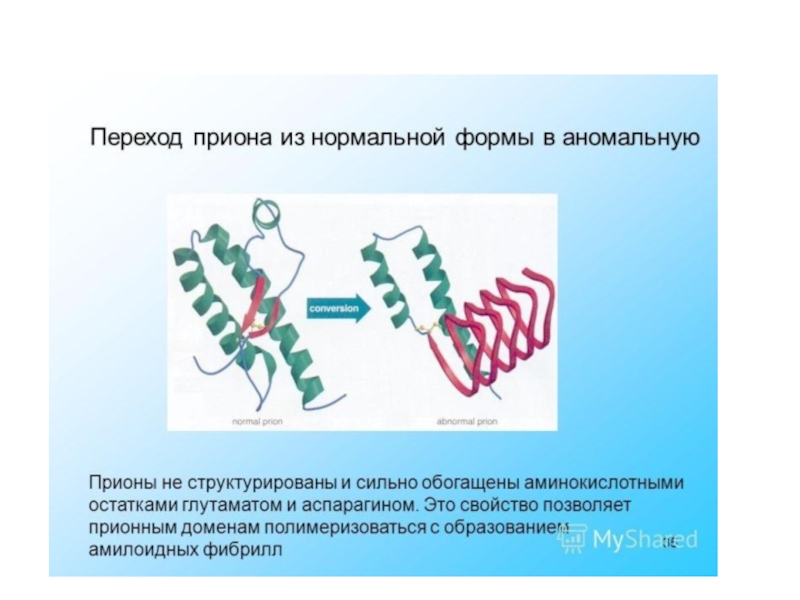
инфекционная форма (PrPs) – характеризуется:
измененной вторичной и третичной структурой
молекулы,
высокой устойчивостью к нагреванию, ультрафиолетовому свету, проникающей радиации и
переваривающему действию протеаз.Слайд 36БАКТЕРИОФАГИ
«пожирающий бактерии» (от бактерия + греч. phagos – пожирающий)
вирусы бактерий,
специфически проникающие в бактериальные клетки и поражающие их.
Для обозначения используют:
название
м/о, из которых они выделены: колифаги, стафилофаги,буквы латинского алфавита
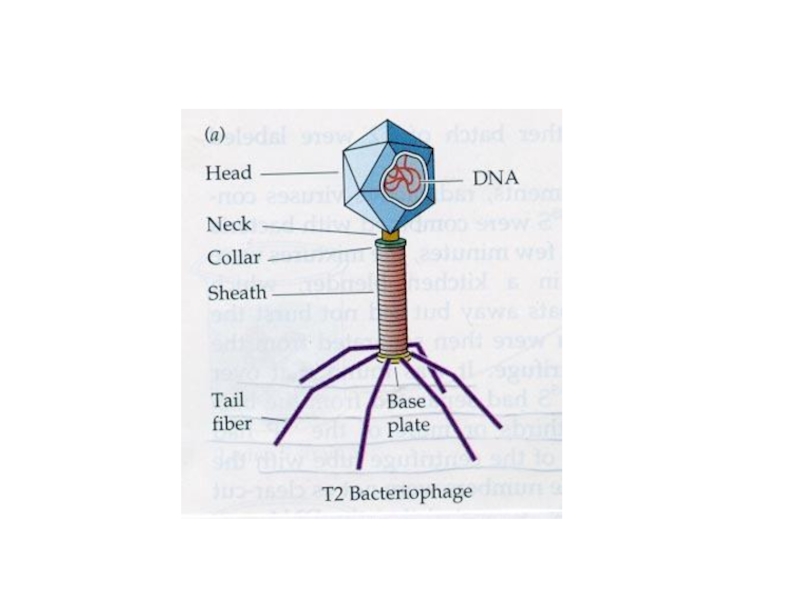
Слайд 39Строение бактериофагов
икосаэдрическая головка,
хвостовой отросток: внутри – полый цилиндрический стержень, сообщающийся
с головкой, а снаружи - чехол отростка, заканчивающийся шестиугольной базальной
пластинкой с шипами, от которых отходят фибриллы (нити),капсид головки и чехол хвостового отростка бактериофага состоят из полипептидных субъединиц, уложенных по икосаэдрическому (головка) или спиральному (отросток) типу симметрии.
Слайд 41Нуклеиновая кислота фага
Бактериофаги (фаги) содержат ДНК или РНК:
- двунитевые
-
однонитевые
линейные,
-кольцевые.
Большинство – двунитевую ДНК, замкнутую в кольцо
Слайд 42
В состав головки входит:
полипептид, состоящий из аспарагиновой, глутаминовой кислот и
лизина,
- у некоторых – гистоноподобный белок → суперспирализация ДНК.
Слайд 43
В состав сокращающегося чехла входит:
у некоторых фагов входит АТФ
и ионы кальция.
В дистальной части отростка – лизоцим.
Слайд 44Морфологические типы бактериофагов
I тип (нитчатые)
без головки (только отросток)
II тип
без отростка
(только головка)
III тип
головка и отросток, короткий без чехла
IV тип
головка и
отросток, длинный с чехлом, не сократительныйV тип
головка и отросток, длинный с чехлом, сократительный
Слайд 46Классификация бактериофагов по спектру действия
полифаги
поражают несколько видов
монофаги (видовые)
поражают один вид
типовые
фаги
поражают часть вида (фаговар)
Слайд 47Классификация фагов в зависимости от эффекта действия на бактериальную клетку
вирулентные
умеренные
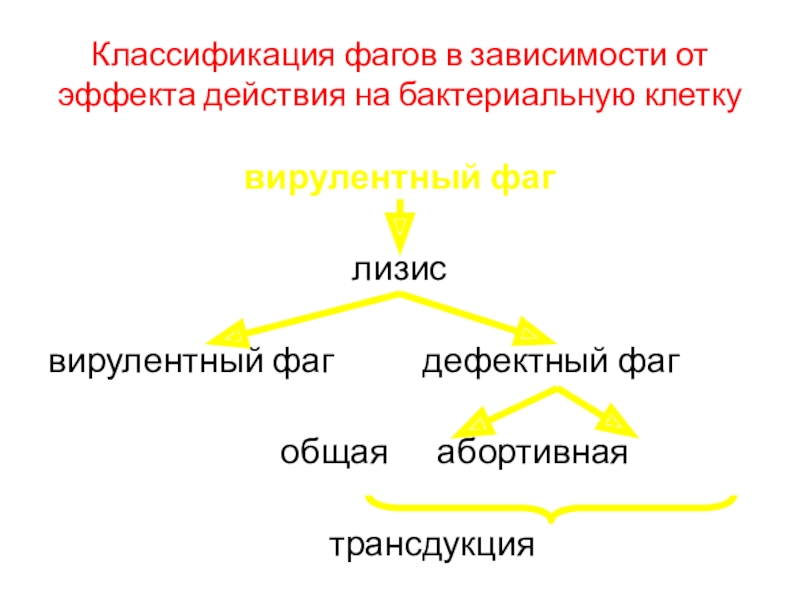
Слайд 48Классификация фагов в зависимости от эффекта действия на бактериальную клетку
вирулентный
фаг
лизис
вирулентный фаг дефектный фаг
общая абортивнаятрансдукция
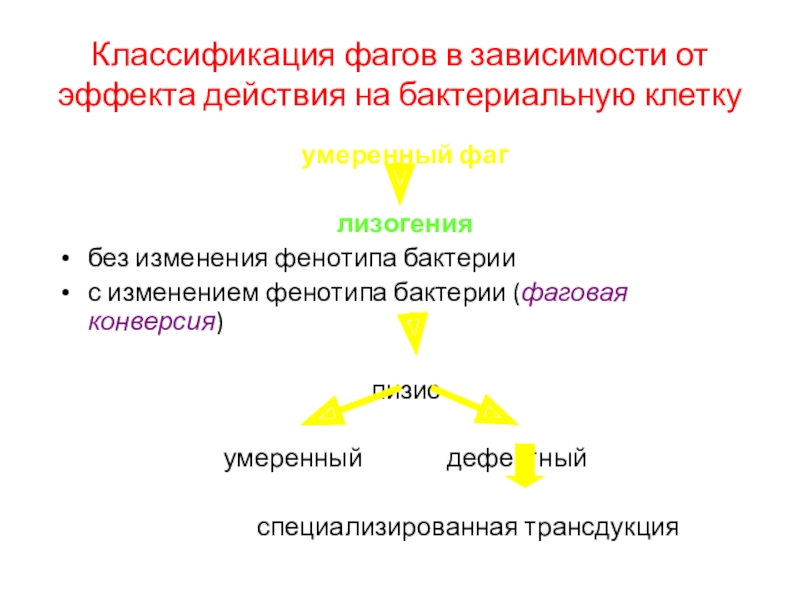
Слайд 49Классификация фагов в зависимости от эффекта действия на бактериальную клетку
умеренный
фаг
лизогения
без изменения фенотипа бактерии
с изменением фенотипа бактерии (фаговая конверсия)
лизис
умеренный
дефектныйспециализированная трансдукция
Слайд 50Взаимодействие фагов с бактериями
может происходить:
- по продуктивному типу – вирулентные
фаги→фаговое потомство, бактерии лизируются
- интегративному – умеренные →встраиваются в геном
клетки и сосуществуют с ней,- абортивному типу →фаговое потомство не образуется, бактерии сохраняют свою жизнедеятельность
Слайд 51Вирулентные бактериофаги
попав в бактерию, реплицируются, формируя 200-300 фаговых частиц, и
вызывают гибель (лизис) бактерии = это продуктивный тип взаимодействия
Слайд 52Взаимодействие вирулентного фага с бактериальной клеткой
адсорбция фага на специальных рецепторах
КС
(на протопластах не происходит)
проникновение НК
(депротеинизация)
репликация фаговой НК и синтез
фаговых белковсборка фаговых частиц
выход зрелых фагов
лизис бактерии бактерия не погибает
(«взрыв») (некоторые нитчатые фаги)
ПРОДУКТИВНАЯ ИНФЕКЦИЯ
Слайд 53Этапы взаимодействия вирулентного фага с бактериальной клеткой =продуктивный тип взаимодействия
1.
Бактериофаги с сокращающимся чехлом адсорбируются на клеточной стенке с помощью
фибрилл хвостового отростка.2. Чехол хвостового отростка сокращается, и стержень с помощью ферментов (лизоцима) просверливает оболочку клетки.
3. Через канал стержня бактериофага нуклеиновая кислота инъецируется из головки в бактериальную клетку, а капсид бактериофага остается снаружи бактерии.
Слайд 55Этапы взаимодействия вирулентного фага с бактериальной клеткой =продуктивный тип взаимодействия
4. Инъецированная внутрь клетки нуклеиновая кислота подавляет биосинтез компонентов клетки,
заставляя ее синтезировать нуклеиновую кислоту и белки бактериофага:происходит полный распад ДНК бактерии и ее утилизация.
если ДНК бактерии не хватает для образования фаговой ДНК – она синтезируется из компонентов среды.
Слайд 56Этапы взаимодействия вирулентного фага с бактериальной клеткой =продуктивный тип взаимодействия
5.
Образовавшиеся в разных частях клетки компоненты бактериофага собираются в фаговые
частицы путем заполнения фаговой нуклеиновой кислотой пустотелых капсидов головки6. Сформированная головка соединяется с хвостовой частью, образуя новый фаг.
Затем в результате лизиса клетки бактериофаги выходят из нее.
Слайд 57Взаимодействие умеренного фага с бактериальной клеткой
адсорбция фага на специальных рецепторах
КС
(на протопластах не происходит)
проникновение НК
(депротеинизация)
интеграция фаговой НК в геном
бактериипрофаг
(фаговый репрессор блокирует транскрипцию)
лизогенная культура
Л И З О Г Е Н И З А Ц И Я
в дальнейшем – может
индукция профага
продуктивная инфекция
Слайд 58Взаимодействие умеренного фага с бактериальной клеткой
Умеренные бактериофаги взаимодействуют с бактериями:
- либо по продуктивному,
либо по интегративному типу.
Продуктивный цикл
умеренного фага идет как и у вирулентных фагов, и заканчивается лизисом бактерий. Слайд 59Взаимодействие умеренного фага с бактериальной клеткой
При интегративном типе ДНК умеренного
фага встраивается в хромосому бактерии:
- приобретает форму кольца,
- интегрируется в
гомологичную область,- реплицируется синхронно с геномом бактерии, не вызывая ее лизиса (передается при делении бактерии).
Слайд 60Взаимодействие умеренного фага с бактериальной клеткой
ДНК фага, встроенная в хромосому
бактерии, называется профагом,
культура бактерий — лизогенной;
сам процесс – лизогенией
(от греч. lysis – разложение, genea – происхождение).Слайд 61Взаимодействие умеренного фага с бактериальной клеткой
При лизогении фаги не образуются
в результате “выключения“ фаговых генов репрессором (=низкомолекулярный белок), кодируемым одним
геном фага.Профаги могут спонтанно или под действием индуцирующих агентов (УФ-лучи, митомицин С и др.) дерепрессироваться, исключаться из хромосомы. Этот процесс заканчивается продукцией фагов (индукция профага) и лизисом бактерий.
Слайд 62Взаимодействие умеренного фага с бактериальной клеткой
Профаг придает бактерии новые свойства,
что получило название фаговой конверсии (лат. conversio – превращение).
Конвертироваться
могут:морфологические,
культуральные,
биохимические,
антигенные и другие свойства бактерий.
Например, наличие профага в дифтерийной палочке обусловливает ее способность продуцировать дифтерийный экзотоксин.
Слайд 63
Применение фагов
для профилактики,
для лечения инфекций,
в
генной инженерии в качестве векторов для получения рекомбинантной ДНК,
для
диагностики (например, для фаготипирования с целью выявления источника инфекции или внутривидовой идентификации).Слайд 65Практическое применение бактериофагов
Фаготерапия
Фаг применяется в том случае, когда антибиотики применять
нельзя,
Чаще всего местно
Слайд 66Практическое применение бактериофагов
Фагодиагностика
Выявление определённого вида бактерий в патологическом материале
реакция нарастания
титра фага
Идентификация чистой культуры
определение вида
фагоиндикация
определение фаговара
фаготипирование
Слайд 67Выделение бактериофага
материал
объект внешней среды
бактериальная культура
бактериальный фильтр
фильтрат
МПБ + чувствительная бактерия
Инкубация 24
час
роста нет – фаг присутствует (очищают фильтрованием)
рост есть – фаг
отсутствуетСлайд 68
Определение активности бактериофагов = фагоиндикация
Качественный метод:
метод «стерильной дорожки»
Количественные методы:
А) Метод
Грациа
Б) Метод Аппельмана
Слайд 69
Определение активности бактериофагов = фагоиндикация
Качественный метод:
На чашку газоном засевают культуру
микроорганизмов, наносят каплю бактериофага и дают ей стечь. Чашки инкубируют
при 37 градусах 24 час и учитывают результат:там, где стекал бактериофаг, образовалась «стерильная дорожка»
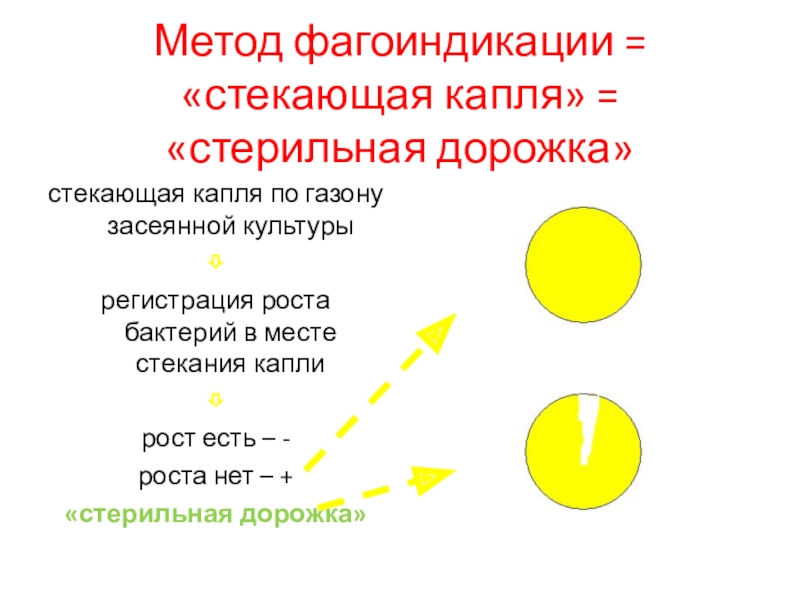
Слайд 70Метод фагоиндикации = «стекающая капля» = «стерильная дорожка»
стекающая капля по
газону засеянной культуры
регистрация роста бактерий в месте стекания капли
рост есть
– -роста нет – +
«стерильная дорожка»
Слайд 71
Определение активности бактериофагов = фагоиндикация
Количественные методы:
А) Метод Грациа: готовят десятикратные
разведения фага в хлориде натрия от 10-2 до 10-7
Затем
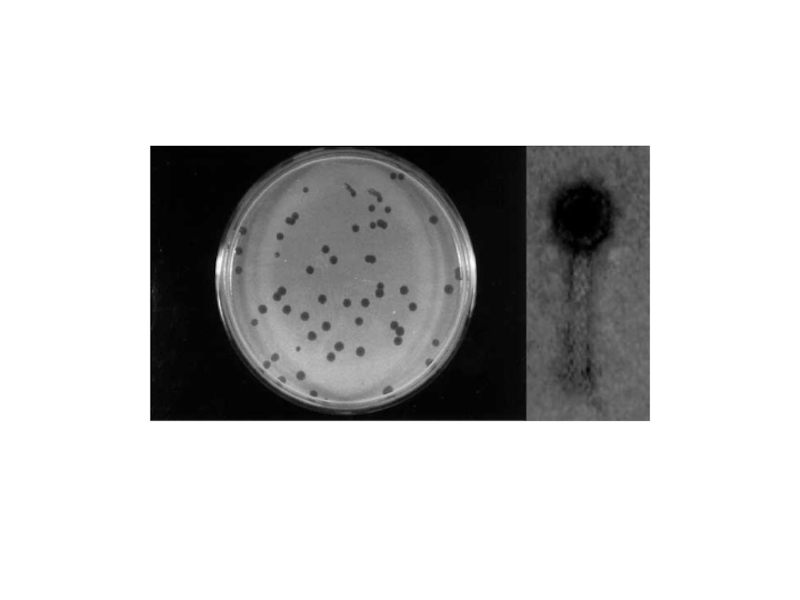
по 0,5 мл из каждого разведения смешивают с таким же объемом бульонной культуры и 4 мл расплавленного и остуженного до 45 град. агара и выливают на чашки Петри. Когда агар застынет чашки помещают в термостат при 37 градусах на 24 часа и затем учитывают результаты:
-одна фаговая частица образует одно «стерильное пятно»
- Величина, показывающая концентрацию фага называется титром.
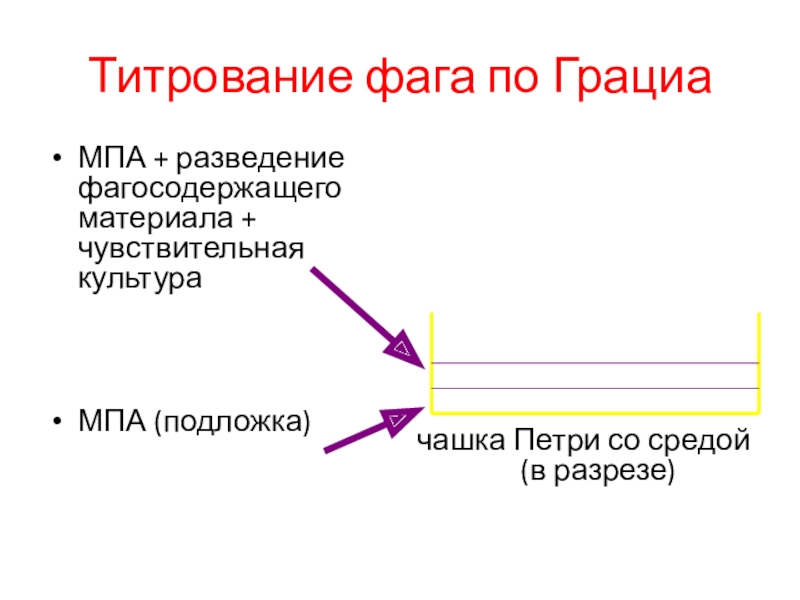
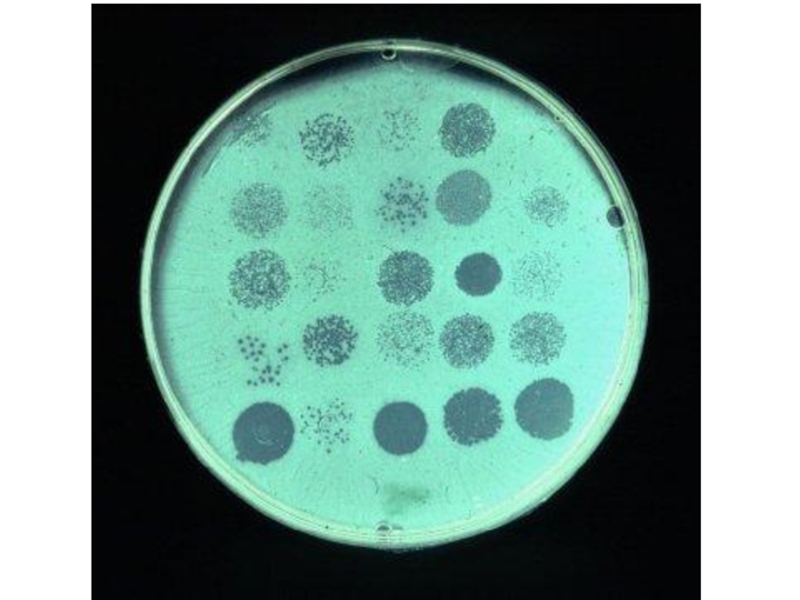
Слайд 72Титрование фага по Грациа
МПА + разведение фагосодержащего материала + чувствительная
культура
МПА (подложка)
чашка Петри со средой (в разрезе)
Слайд 74
Определение активности бактериофагов = фагоиндикация
Количественные методы:
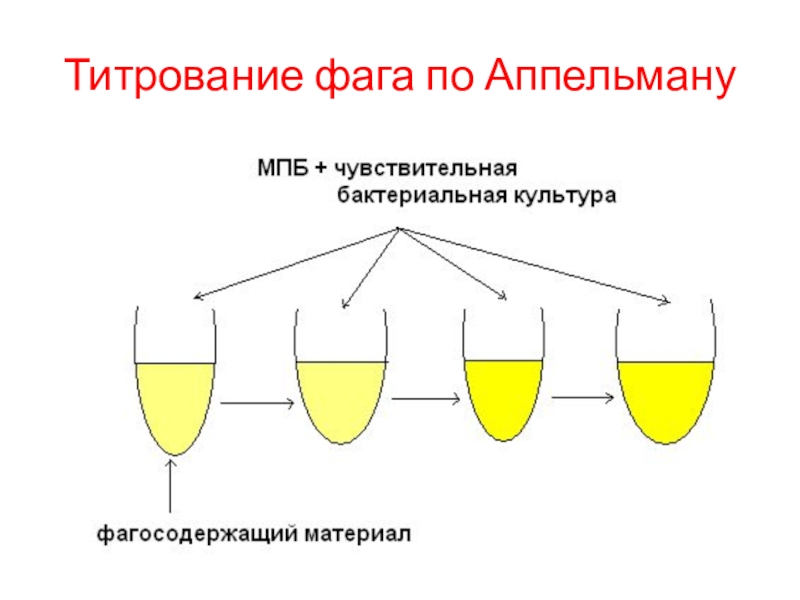
Б) Метод Аппельмана: готовят десятикратные
разведения фага в питательном бульоне
от 10-2 до
10-8. Затем в каждую пробирку добавляют по 0,2мл бульонной культуры и ряды ставят в термостат.
После инкубации в термостате учитывают результаты:
= в положительном случае наблюдается просветление среды.
Разведение в последней пробирке, где произошел полный лизис культуры, называется титром фага.
Слайд 76Фаготипирование бактерий
засев газоном на чашку с питательным агаром изучаемого штамма
чашку
делят на квадратики и на каждый наносят бактериофаг
инкубация
регистрация «стерильных
пятен» («бляшек»)фаготип (фаговар) = перечень типовых фагов, лизирующих данный вариант
Слайд 79
Определение спектра литического действия фага
Чашку делят на квадратики и на
каждый газоном засевают испытуемые штаммы,
затем на каждый квадратик петлей
или пипеткой наносят каплю фага после инкубации в термостате в течение 24 час определяют наличие «стерильных пятен».
Количество культур, которые лизирует бактериофаг – спектр его литического действия.