Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Курс Биология опухолевой клетки (201 9 г. ) Лекция 2 Нарушения регуляции
Содержание
- 1. Курс Биология опухолевой клетки (201 9 г. ) Лекция 2 Нарушения регуляции
- 2. Злокачественные новообразования возникают в результате нарушений в
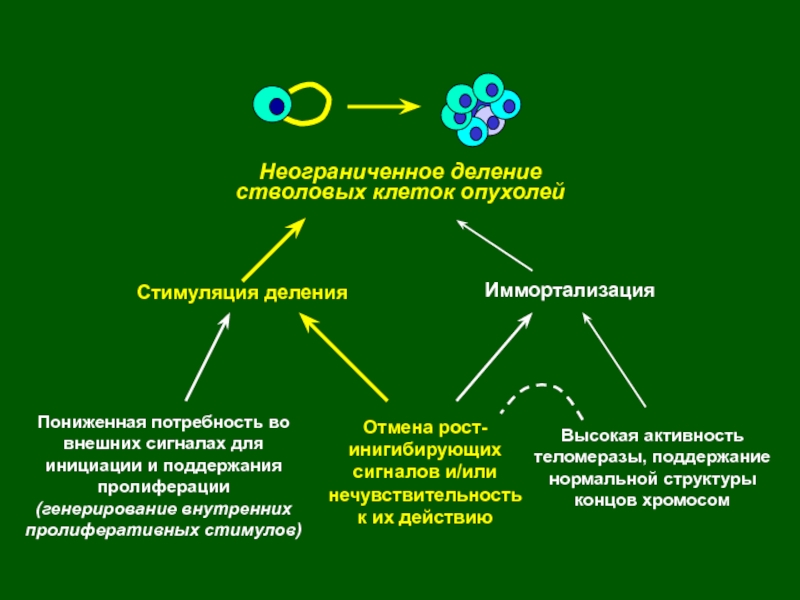
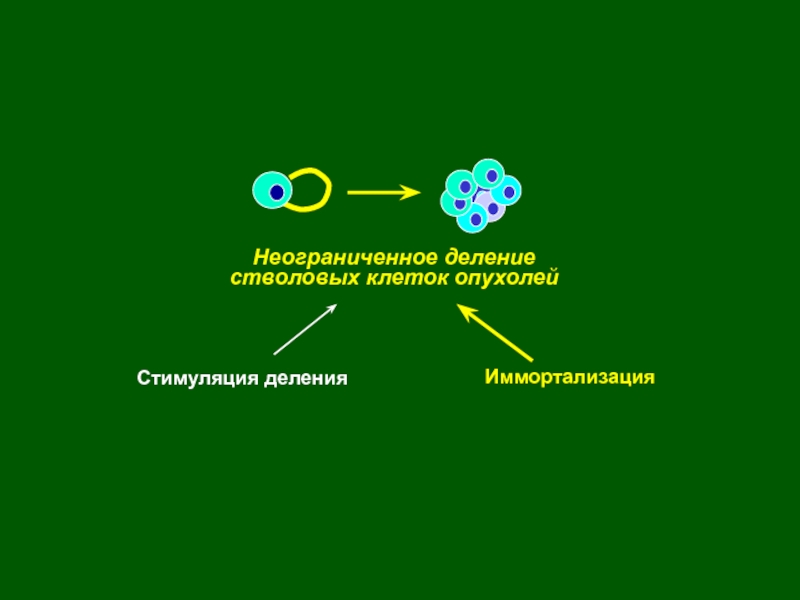
- 3. Неограниченное делениестволовых клеток опухолейСтимуляция деленияИммортализацияОтмена рост-инигибирующихсигналов и/илинечувствительность
- 4. “Мотором” клеточного цикла служат активности последовательно сменяющих
- 5. RbP HDACRbPPЦиклин A-Cdk2, ДГФР, ТК и др.PP
- 6. Фосфорилирование pRb включает петли позитивной регуляции комплексов
- 7. G0G1МитозSG2 Циклин BCdc2(Cdk1)Циклины D1-D3
- 8. .Транскрипционные факторыВнешние
- 9. Рецепторные тирозинкиназыЦитокины/ГормоныВнеклеточный матриксТранскрипционные факторыЦиклинзависимые
- 10. Онкогены - клеточные или вирусные гены, экспрессиякоторых
- 11. Онкогены - клеточные или вирусные гены, экспрессиякоторых
- 12. Критерии принадлежности к онкогенам/опухолевым супрессорам: Закономерные изменения
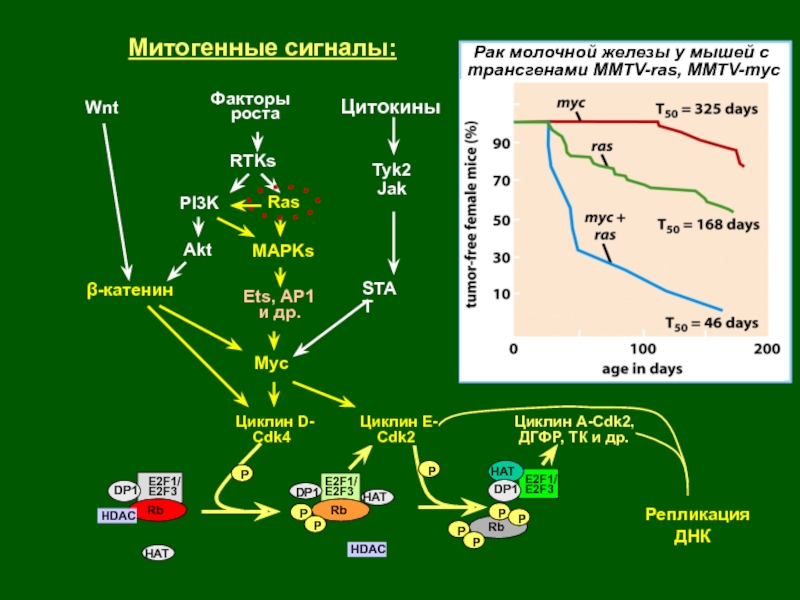
- 13. Факторы ростаЦитокиныWnt МАРKsSTATβ-катенинMyc Митогенные сигналы:
- 14. Репликация ДНКRbP HDACE2F1/E2F3Rb HDACRbPPЦиклин A-Cdk2,
- 15. Транскрипционные комплексы Myc (Myc-Max, Myc-Miz1) стимулируют деление
- 16. Rothenberg et al. “The Myc connection: ES
- 17. Bui and Mendell, “Myc: Maestro of MicroRNAs”,
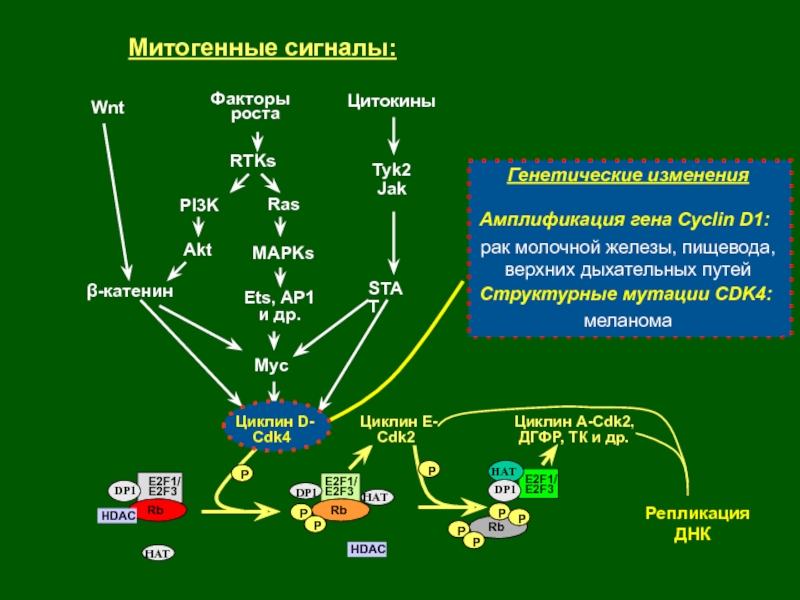
- 18. Изменения генов Myc в неопластических клетках: 1)
- 19. Репликация ДНКRbP HDACE2F1/E2F3Rb HDACRbPPЦиклин A-Cdk2,
- 20. Алгоритм функционирования β-катенина синтезApcAxin
- 21. Генетические изменения в новообразованиях человека, активирующие сигнальный
- 22. Свидетельства происхождения рака из полипов1. Опухоли содержат
- 23. Репликация ДНКRbP HDACE2F1/E2F3Rb HDACRbPPЦиклин A-Cdk2,
- 24. Сигнальный путь PI3K-PIP3-Akt в регуляции деления клетокмембрана
- 25. Репликация ДНКRbP HDACE2F1/E2F3Rb HDACRbPPЦиклин A-Cdk2,
- 26. Активирующие мутации B-Raf: меланома (70%) рак
- 27. Репликация ДНКRbP HDACE2F1/E2F3Rb HDACRbPPЦиклин A-Cdk2,
- 28. Спектр мутаций генов семейства RAS в
- 29. Репликация ДНКRbP HDACE2F1/E2F3Rb HDACRbPPЦиклин A-Cdk2,
- 30. Репликация ДНКRbP HDACE2F1/E2F3Rb HDACRbPPЦиклин A-Cdk2,
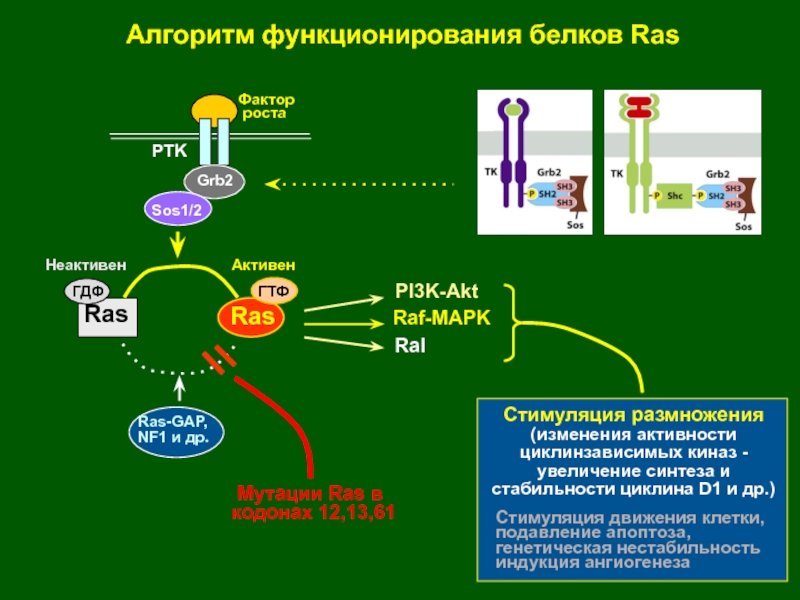
- 31. RasRasГДФГТФНеактивенАктивенSos1/2Алгоритм функционирования белков RasRas-GAP,NF1 и др.
- 32. RasRasГДФГТФНеактивенАктивенАлгоритм функционирования белков RasRas-GAP,NF1 и др.
- 33. Raf-MAPKPI3K-AktRalНейрофиброматоз 1(болезнь Реклингаузена),(из шванновских клеток)Алгоритм функционирования белков RasRas-GAP,NF1 и др. герминальныеинактивирующиемутации NF1кожа спинырадужка глазаRasRasГДФГТФНеактивенАктивен
- 34. Репликация ДНКRbP HDACE2F1/E2F3Rb HDACRbPPЦиклин A-Cdk2,
- 35. Пути активации рецепторов факторов ростаГибридные белки
- 36. Характерные для опухолей человекаизменения рецепторов факторов роста
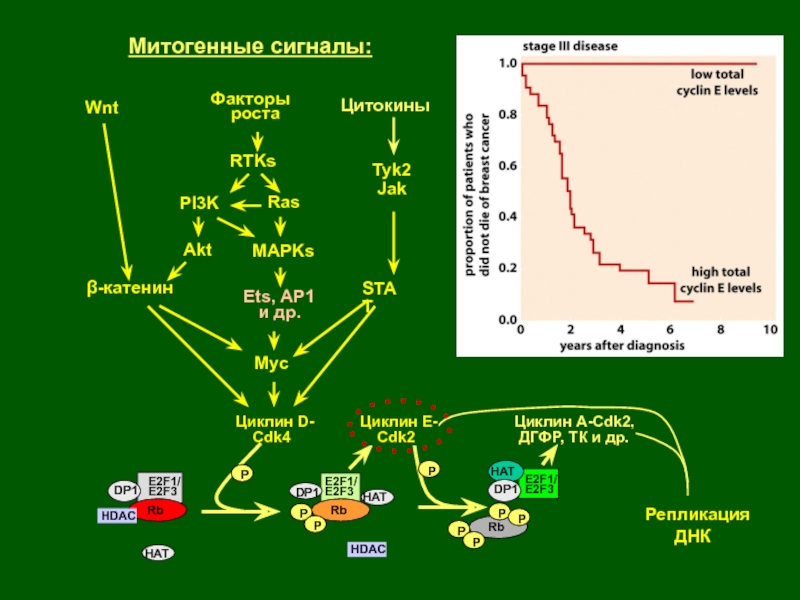
- 37. безрецидивная выживаемость(доля пациентов)месяцы после постановки диагнозаАмплификация и/или
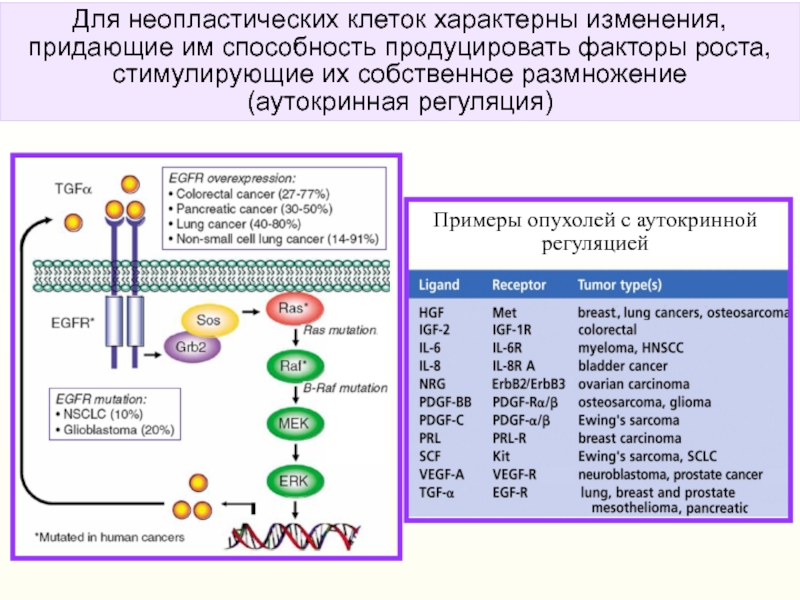
- 38. Для неопластических клеток характерны изменения, придающие им
- 39. Репликация ДНКRbP HDACE2F1/E2F3Rb HDACRbPPЦиклин A-Cdk2,
- 40. Сигнальный путь Jak-STATв регуляции деления клеток
- 41. Репликация ДНКRbP HDACE2F1/E2F3Rb HDACRbPPЦиклин A-Cdk2,
- 42. Примеры изменений различных протоонкогенов, контролирующих вход в
- 43. Неограниченное делениестволовых клеток опухолейСтимуляция деленияИммортализацияОтмена рост-инигибирующихсигналов и/илинечувствительность
- 44. Нечувствительность к рост-супрессирующим сигналам1. Отсутствие “контактного торможения”
- 45. G1SG2МитозЦитокин TGFbНарушенияструктурыДНКМежклеточные контактыОтсутствиеконтактов с матриксомГипоксияНарушенияверетена деленияp16Ink4ap53Различные рост-ингибирующие воздействия вызывают активацию чекпойнтов и остановку клеточного циклаp15Ink4bp27Kip1p21Cip1CycD1-D3 Cdk4,6CycECdk2CycACdk2CycBCdc2pRbE2FChfr,Bub1,BubR1,Mad1/2Cdc25A,C
- 46. G1SG2МитозЦитокин TGFbНарушенияструктурыДНКМежклеточные контактыОтсутствиеконтактов с матриксомГипоксияНарушенияверетена деленияp16Ink4ap53p27Kip1p21Cip1CycD1-D3 Cdk4,6CycECdk2CycACdk2CycBCdc2pRbE2FКомпоненты
- 47. Adapted from A.Knudson, Proc.Natl.Acad.Sci. USA, 1971, 68:820-823;
- 48. Схема развития семейных и спорадических ретинобластом
- 49. Последствия мутаций генов RbЧеловек Герминальные мутации Соматические
- 50. Почему при инактивации pRb возникают
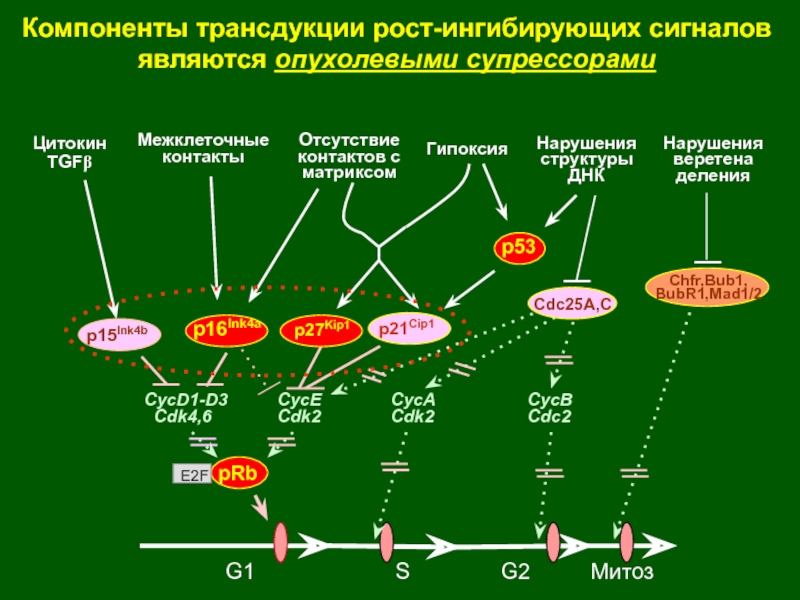
- 51. Компоненты трансдукции рост-ингибирующих сигналов являются опухолевыми супрессорамиG1SG2МитозЦитокин TGFbНарушенияструктурыДНКМежклеточные контактыОтсутствиеконтактов с матриксомГипоксияНарушенияверетена деленияp16Ink4ap53p15Ink4bp27Kip1p21Cip1CycD1-D3 Cdk4,6CycECdk2CycACdk2CycBCdc2pRbE2FCdc25A,CChfr,Bub1,BubR1,Mad1/2
- 52. Последствия мутаций генов Rb и CKIsЧеловек Герминальные
- 53. Подавление антипролиферативной функции p27Kip1в новообразованиях человекаГерминальные и
- 54. Компоненты передачи рост-ингибирующих сигналов являются опухолевыми супрессорамиG1SG2МитозЦитокин TGFbНарушенияструктурыДНКМежклеточные контактыОтсутствиеконтактов с матриксомГипоксияНарушенияверетена деленияp16Ink4ap53p27Kip1p21Cip1CycD1-D3 Cdk4,6CycECdk2CycACdk2CycBCdc2pRbE2FChfr,Bub1,BubR1,Mad1/2Cdc25A,Cp15Ink4b
- 55. Инактивация опухолевого супрессора р53 (мутации
- 56. Неограниченное делениестволовых клеток опухолейСтимуляция деленияИммортализация
- 57. Курс «Биология опухолевой клетки»(2019 г.)Лекция 3Иммортализация (неограниченный репликативныйпотенциал) стволовых клеток опухолиН.Л. Лазаревич
- 58. Скачать презентанцию
Слайды и текст этой презентации
Слайд 1Курс «Биология опухолевой клетки»
(2019 г.)
Лекция 2
Нарушения регуляции клеточного цикла в
неопластических клетках: роль онкогенов и опухолевых супрессоров
Слайд 2Злокачественные новообразования возникают в результате нарушений в системах, обеспечивающих естественный
процесс обновления тканей, когда вследствие мутаций и
эпигенетических изменений в
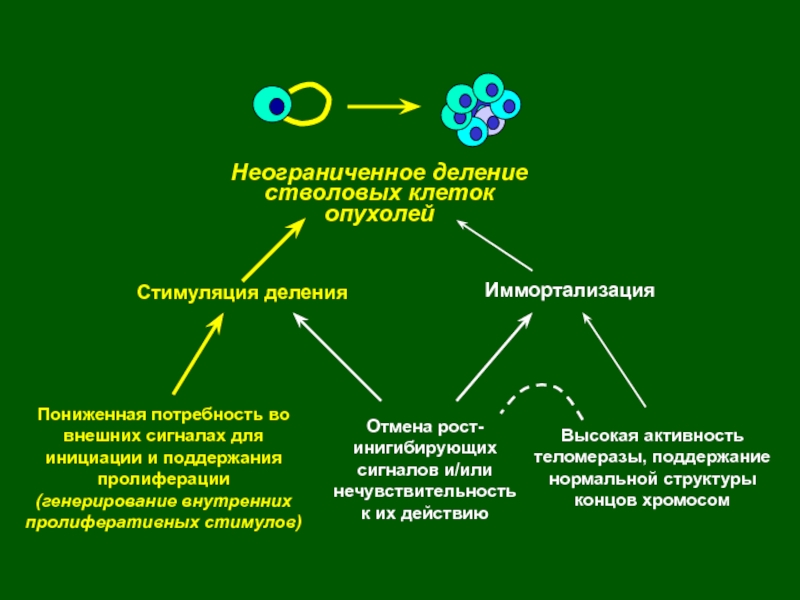
стволовых клетках или их незрелых потомках образуются т.н. «стволовые клетки опухолей», способные к неограниченному размножению, выходу за пределы собственной ткани и росту на территориях других тканей. Слайд 3Неограниченное деление
стволовых клеток опухолей
Стимуляция деления
Иммортализация
Отмена рост-инигибирующих
сигналов и/или
нечувствительность
к их действию
Пониженная
потребность во внешних сигналах для инициации и поддержания пролиферации
(генерирование
внутренних пролиферативных стимулов) Высокая активность теломеразы, поддержание
нормальной структуры
концов хромосом
Пониженная потребность во внешних сигналах для инициации и поддержания пролиферации
(генерирование внутренних пролиферативных стимулов)
Слайд 4“Мотором” клеточного цикла служат активности последовательно сменяющих друг друга циклин-зависимых
киназ (Cdks)
Какие белки являются мишенями Cdks?
Слайд 5Rb
P
HDAC
Rb
P
P
Циклин A-Cdk2,
ДГФР, ТК и др.
P
P
Циклин E-
Cdk2
Активация
точек начала
репликации
(вход в S),
дупликация центросом
Репликация
ДНК Циклин D-
Cdk4
E2F1/
E2F3
E2F1/
E2F3
HAT
DP1
DP1
HAT
P
P
P
Транскрипционные
факторы
Митогенные
стимулы
Важнейшей мишенью киназ Cdk4/6 и Cdk2 является белок pRb, регулирующий вход в S-фазу и репликацию ДНК
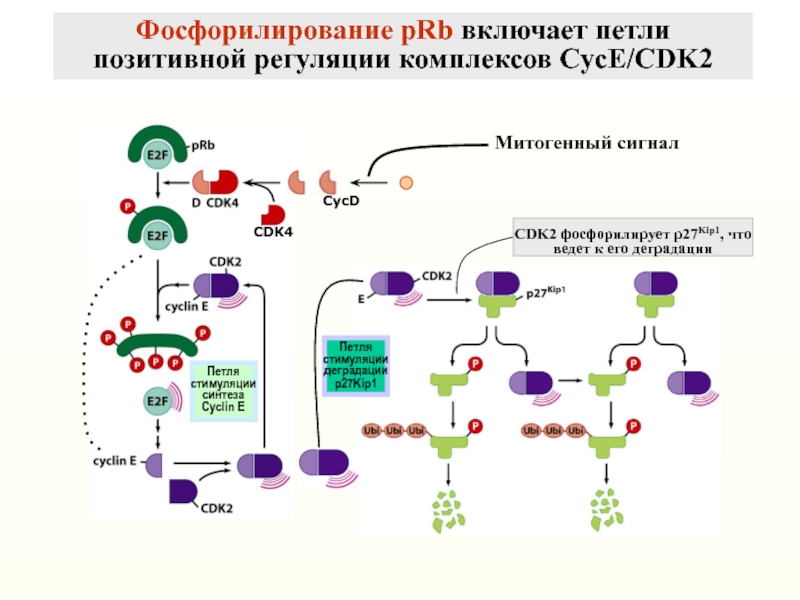
Слайд 6Фосфорилирование pRb включает петли позитивной регуляции комплексов CycE/CDK2
Петля
стимуляции
синтеза Cyclin E
Петля
стимуляции
деградации
p27Kip1
CDK2
фосфорилирует p27Kip1, что ведет к его деградации
Слайд 7G0
G1
Митоз
S
G2
Циклин B
Cdc2(Cdk1)
Циклины D1-D3
Cdk4,6
Циклин E
Cdk2
Циклин A
Cdk2
Циклин A
Cdc2(Cdk1)
Циклины D1-D3
Cdk4,6
В
норме митогенная сигнализация имеет квантовый характерСлайд 8.
Транскрипционные
факторы
Внешние митогенные стимулы
G1
Митоз
S
G2
Циклин
B
Cdc2(Cdk1)
Циклин E
Cdk2
Циклин A
Cdk2
Циклин B
Cdk2
Циклины
D1-D3Cdk4,6
G0
.
Основополагающее свойство неопластических клеток – пониженная потребность во внешних сигналах для инициации и поддержания пролиферации. Оно возникает вследствие различных генетических изменений, обеспечивающих способность генерировать внутри себя митогенные сигналы, в норме исходящие от внешних стимулов
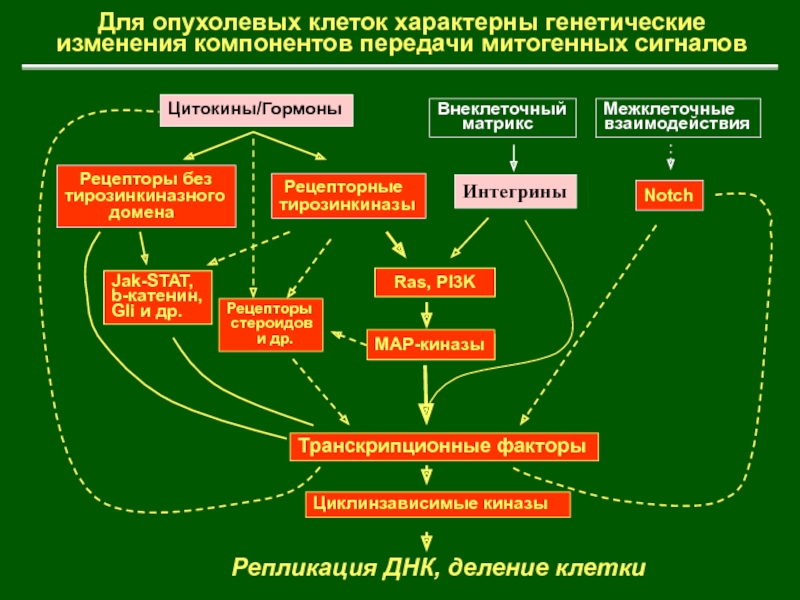
Слайд 9 Рецепторные
тирозинкиназы
Цитокины/Гормоны
Внеклеточный
матрикс
Транскрипционные факторы
Циклинзависимые киназы
Репликация ДНК, деление
клетки
Notch
Межклеточные
взаимодействия
Jak-STAT,
b-катенин,
Gli и др.
Ras, PI3K
Рецепторы без
тирозинкиназного
доменаРецепторы
стероидов
и др.
МАР-киназы
Интегрины
Для опухолевых клеток характерны генетические
изменения компонентов передачи митогенных сигналов
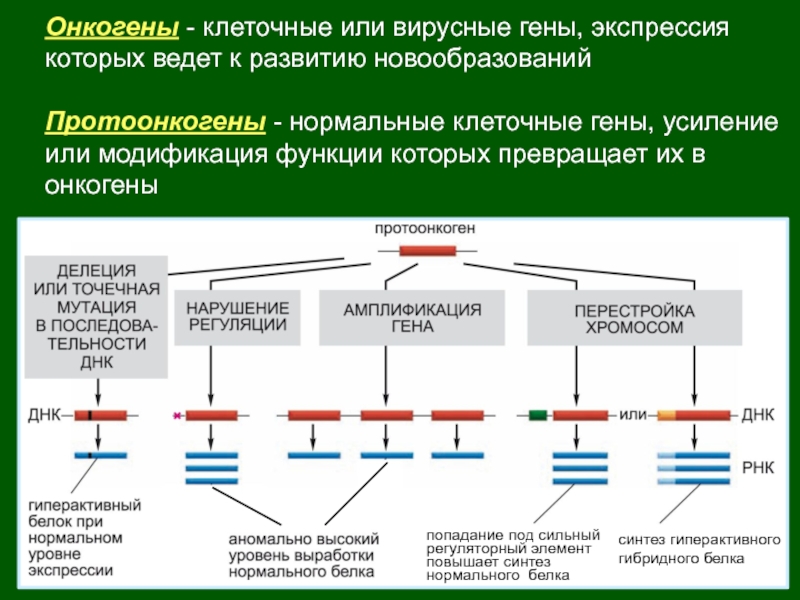
Слайд 10Онкогены - клеточные или вирусные гены, экспрессия
которых ведет к развитию
новообразований
Протоонкогены - нормальные клеточные гены, усиление
или модификация функции которых превращает
их вонкогены
Слайд 11Онкогены - клеточные или вирусные гены, экспрессия
которых ведет к развитию
новообразований.
Протоонкогены - нормальные клеточные гены, усиление
или модификация функции которых превращает
их вонкогены.
Опухолевые супрессоры (антионкогены, рецессивные
опухолевые гены) - клеточные гены, инактивация которых
резко увеличивает вероятность развития новообразований,
а восстановление функции, наоборот, может подавить рост
опухолевых клеток.
Механизмы инактивации
1 ) Генетические (мутации, делеции, потеря хромосом, митотическая рекомбинация, конверсия гена)
2) Эпигенетические (метилирование промотора, микроРНК и др.).
Слайд 12Критерии принадлежности
к онкогенам/опухолевым супрессорам:
Закономерные изменения структуры и/или экспрессии
данного
гена в клетках новообразований
Возникновение определенных форм опухолей
у индивидов с передающимися по наследству герминальными (т.е. произошед-
шими в половой клетке) мутациями данного гена
Резкое повышение частоты появления опухолей у трансгенных
животных, экспрессирующих активированную (онкогены) или
инактивированную (опухолевые супрессоры) формы данного
гена
Способность вызывать в культивируемых in vitro клетках морфо-
логическую трансформацию и неограниченный рост (онкогены),
или подавление роста и выраженности признаков трансформации
(опухолевые супрессоры)
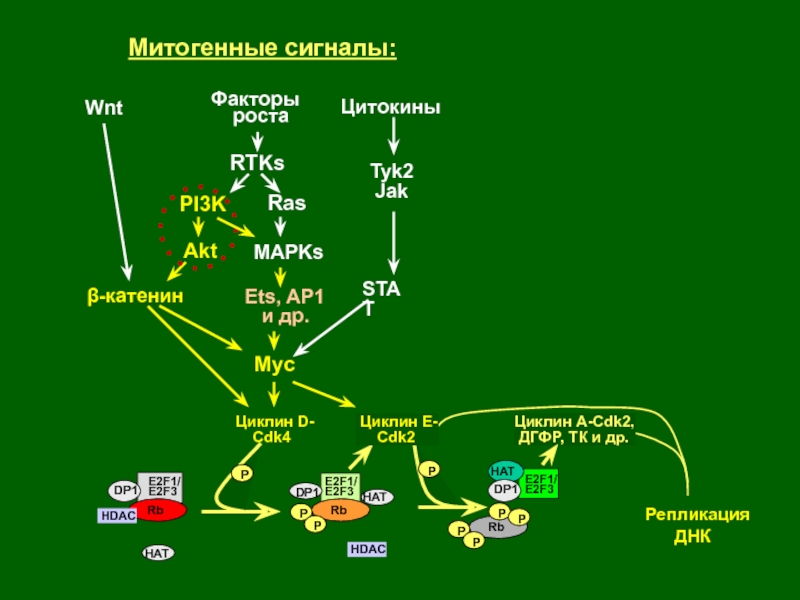
Слайд 13Факторы
роста
Цитокины
Wnt
МАРKs
STAT
β-катенин
Myc
Митогенные сигналы:
Ets, AP1
и др.
Ras
Репликация
ДНК
Rb
P
HDAC
E2F1/
E2F3
Rb
HDAC
Rb
P
P
Циклин A-Cdk2,
ДГФР, ТК и др.P
P
Циклин E-
Cdk2
E2F1/
E2F3
E2F1/
E2F3
HAT
HAT
DP1
DP1
DP1
HAT
P
P
P
Циклин D-
Cdk4
Tyk2
Jak
PI3K
Akt
RTKs
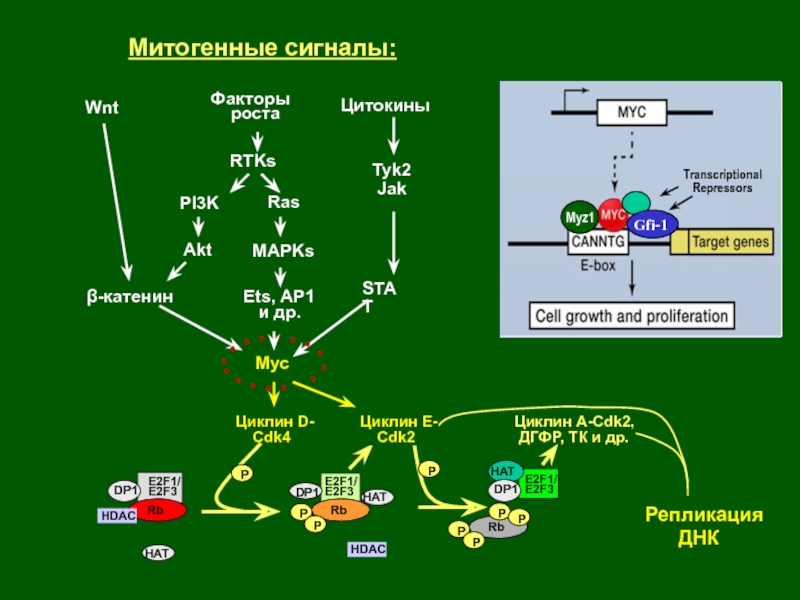
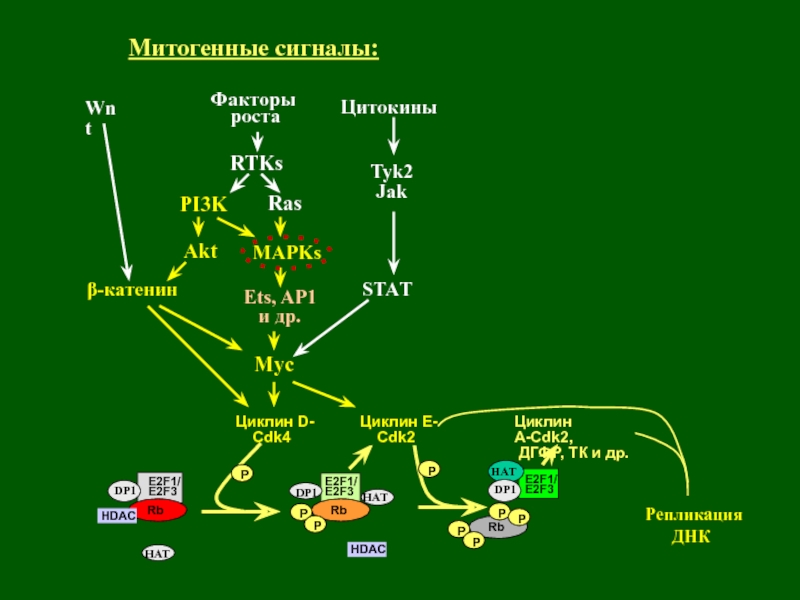
Слайд 14Репликация
ДНК
Rb
P
HDAC
E2F1/
E2F3
Rb
HDAC
Rb
P
P
Циклин A-Cdk2,
ДГФР, ТК и
др.
P
P
Циклин E-
Cdk2
Циклин D-
Cdk4E2F1/
E2F3
E2F1/
E2F3
HAT
HAT
DP1
DP1
DP1
HAT
P
P
P
Факторы
роста
Цитокины
Wnt
МАРKs
STAT
β-катенин
Митогенные сигналы:
Ets, AP1
и др.
Ras
Tyk2
Jak
PI3K
Akt
RTKs
Myc
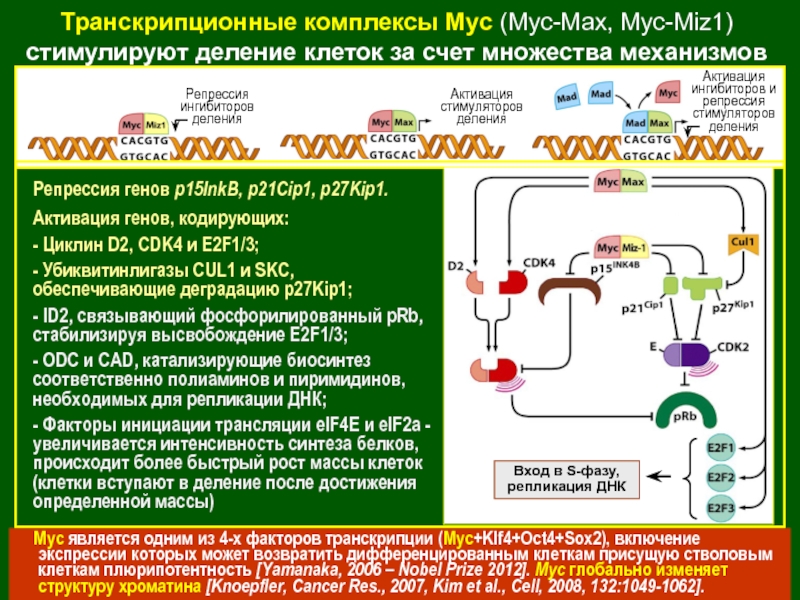
Слайд 15Транскрипционные комплексы Myc (Myc-Max, Myc-Miz1) стимулируют деление клеток за счет
множества механизмов
Myc является одним из 4-х факторов транскрипции
(Myc+Klf4+Oct4+Sox2), включение экспрессии которых может возвратить дифференцированным клеткам присущую стволовым
клеткам плюрипотентность [Yamanaka, 2006 – Nobel Prize 2012]. Myc глобально изменяет
структуру хроматина [Knoepfler, Cancer Res., 2007, Kim et al., Cell, 2008, 132:1049-1062].
Активация стимуляторов деления
Репрессия
ингибиторов деления
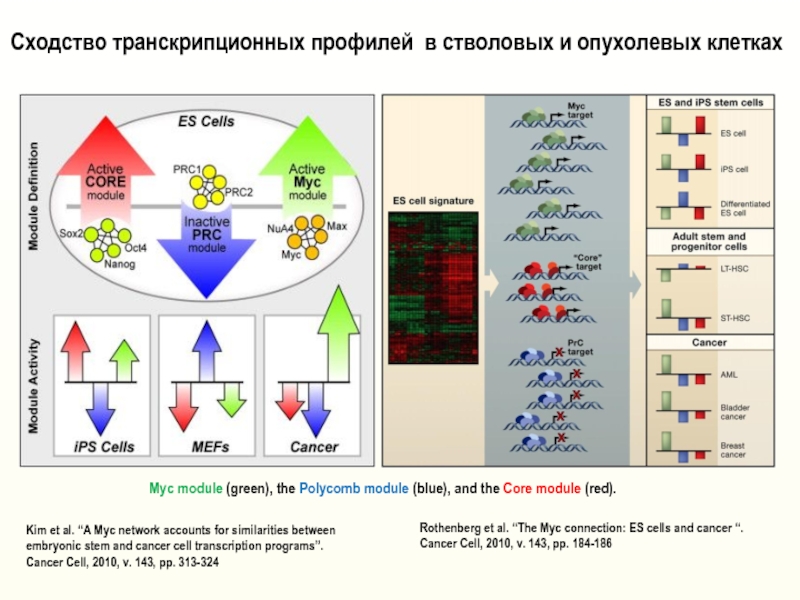
Слайд 16Rothenberg et al. “The Myc connection: ES cells and cancer
“. Cancer Cell, 2010, v. 143, pp. 184-186
Kim et al.
“A Myc network accounts for similarities between embryonic stem and cancer cell transcription programs”. Cancer Cell, 2010, v. 143, pp. 313-324Myc module (green), the Polycomb module (blue), and the Core module (red).
Сходство транскрипционных профилей в стволовых и опухолевых клетках
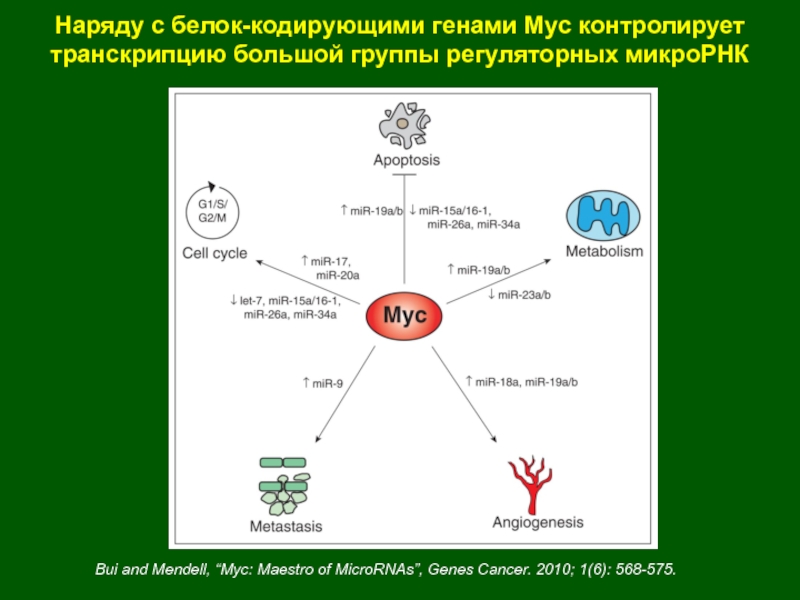
Слайд 17Bui and Mendell, “Myc: Maestro of MicroRNAs”, Genes Cancer. 2010;
1(6): 568-575.
Наряду с белок-кодирующими генами Myc контролирует транскрипцию большой группы
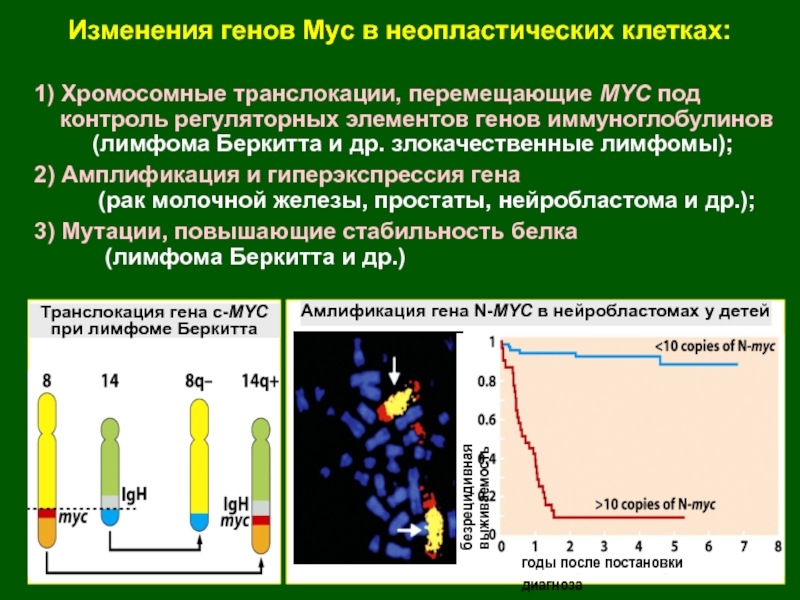
регуляторных микроРНКСлайд 18Изменения генов Myc в неопластических клетках:
1) Хромосомные транслокации, перемещающие
MYC под
контроль регуляторных элементов генов иммуноглобулинов
(лимфома Беркитта и др. злокачественные лимфомы);2) Амплификация и гиперэкспрессия гена
(рак молочной железы, простаты, нейробластома и др.);
3) Мутации, повышающие стабильность белка
(лимфома Беркитта и др.)
Слайд 19Репликация
ДНК
Rb
P
HDAC
E2F1/
E2F3
Rb
HDAC
Rb
P
P
Циклин A-Cdk2,
ДГФР, ТК и
др.
P
P
Циклин E-
Cdk2
Циклин D-
Cdk4E2F1/
E2F3
E2F1/
E2F3
HAT
HAT
DP1
DP1
DP1
HAT
P
P
P
Факторы
роста
Цитокины
Wnt
МАРKs
STAT
b-катенин
Myc
Митогенные сигналы:
Ets, AP1
и др.
Ras
Tyk2
Jak
PI3K
Akt
RTKs
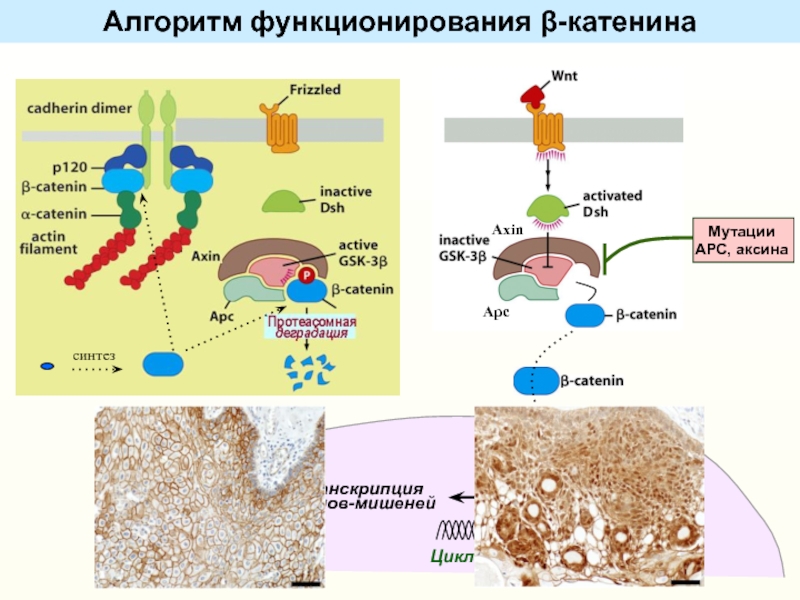
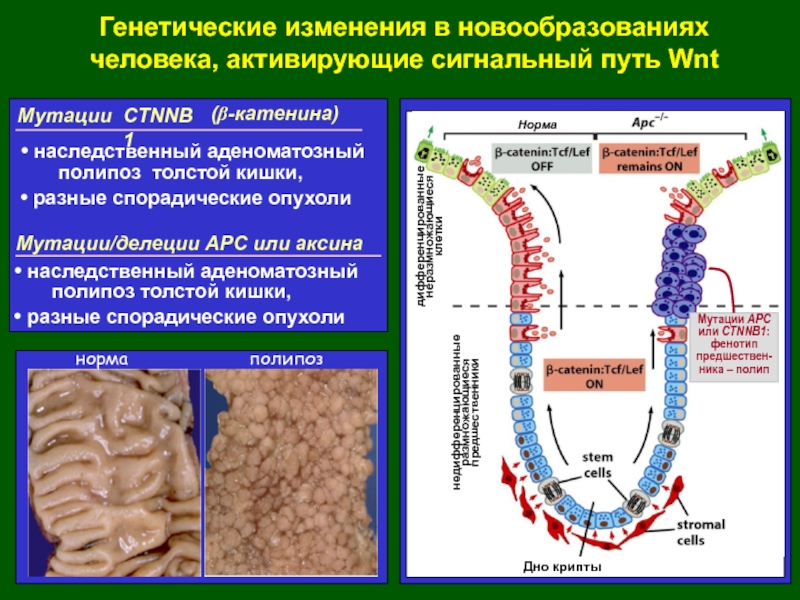
Слайд 21Генетические изменения в новообразованиях человека, активирующие сигнальный путь Wnt
Мутации/делеции
АРС или аксина
наследственный аденоматозный
полипоз толстой кишки,
разные спорадические опухолинорма
полипоз
наследственный аденоматозный
полипоз толстой кишки,
разные спорадические опухоли
Слайд 22Свидетельства происхождения рака из полипов
1. Опухоли содержат (сохраняют) участки доброкачественных
аденом
2. Удаление полипов при колоноскопии снижает частоту ненаследственного рака кишки
Adapted
from R. Weinberg, The Biology of Cancer (© Garland Science 2007, 2013)Слайд 23Репликация
ДНК
Rb
P
HDAC
E2F1/
E2F3
Rb
HDAC
Rb
P
P
Циклин A-Cdk2,
ДГФР, ТК и
др.
P
P
Циклин E-
Cdk2
Циклин D-
Cdk4E2F1/
E2F3
E2F1/
E2F3
HAT
HAT
DP1
DP1
DP1
HAT
P
P
P
Факторы
роста
Цитокины
Wnt
МАРKs
STAT
β-катенин
Myc
Митогенные сигналы:
Ets, AP1
и др.
Ras
Tyk2
Jak
PI3K
Akt
RTKs
Слайд 25Репликация
ДНК
Rb
P
HDAC
E2F1/
E2F3
Rb
HDAC
Rb
P
P
Циклин A-Cdk2,
ДГФР, ТК и
др.
P
P
Циклин E-
Cdk2
Циклин D-
Cdk4E2F1/
E2F3
E2F1/
E2F3
HAT
HAT
DP1
DP1
DP1
HAT
P
P
P
Факторы
роста
Цитокины
Wnt
МАРKs
STAT
b-катенин
Myc
Митогенные сигналы:
Ets, AP1
и др.
Ras
Tyk2
Jak
PI3K
Akt
RTKs
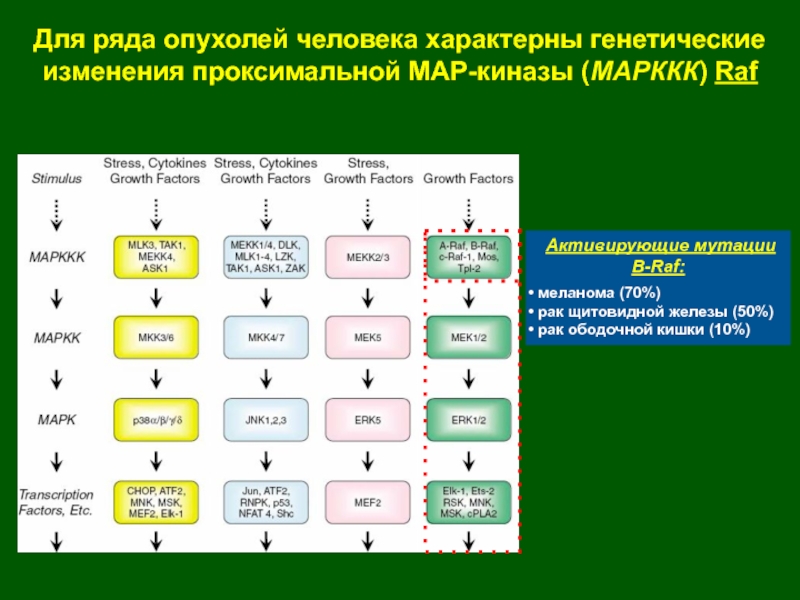
Слайд 26 Активирующие мутации B-Raf:
меланома (70%)
рак щитовидной железы (50%)
рак ободочной кишки (10%)
Для ряда опухолей человека характерны генетические изменения
проксимальной МАР-киназы (МАРККК) RafСлайд 27Репликация
ДНК
Rb
P
HDAC
E2F1/
E2F3
Rb
HDAC
Rb
P
P
Циклин A-Cdk2,
ДГФР, ТК и
др.
P
P
Циклин E-
Cdk2
Циклин D-
Cdk4E2F1/
E2F3
E2F1/
E2F3
HAT
HAT
DP1
DP1
DP1
HAT
P
P
P
Факторы
роста
Цитокины
Wnt
МАРKs
STAT
β-катенин
Myc
Митогенные сигналы:
Ets, AP1
и др.
Ras
Tyk2
Jak
PI3K
Akt
RTKs
Активирующие мутации Ras
(K-, H-, N-):
рак поджелудочной железы (95% , K-)
рак ободочной кишки (50%, K-)
множественная миелома (40%, K- + N-)
рак легкого (30%, K-)
меланома (30%, N-)
многие другие опухоли (20-25%)
Слайд 28Спектр мутаций генов семейства RAS
в разных типах опухолей
Cox AD
et al., Drugging the undruggable RAS: Mission possible? Nat Rev
Drug Discov. 2014;13(11):828-51Слайд 29Репликация
ДНК
Rb
P
HDAC
E2F1/
E2F3
Rb
HDAC
Rb
P
P
Циклин A-Cdk2,
ДГФР, ТК и
др.
P
P
Циклин E-
Cdk2
Циклин D-
Cdk4E2F1/
E2F3
E2F1/
E2F3
HAT
HAT
DP1
DP1
DP1
HAT
P
P
P
Факторы
роста
Цитокины
Wnt
МАРKs
STAT
β-катенин
Myc
Митогенные сигналы:
Ets, AP1
и др.
Ras
Tyk2
Jak
PI3K
Akt
RTKs
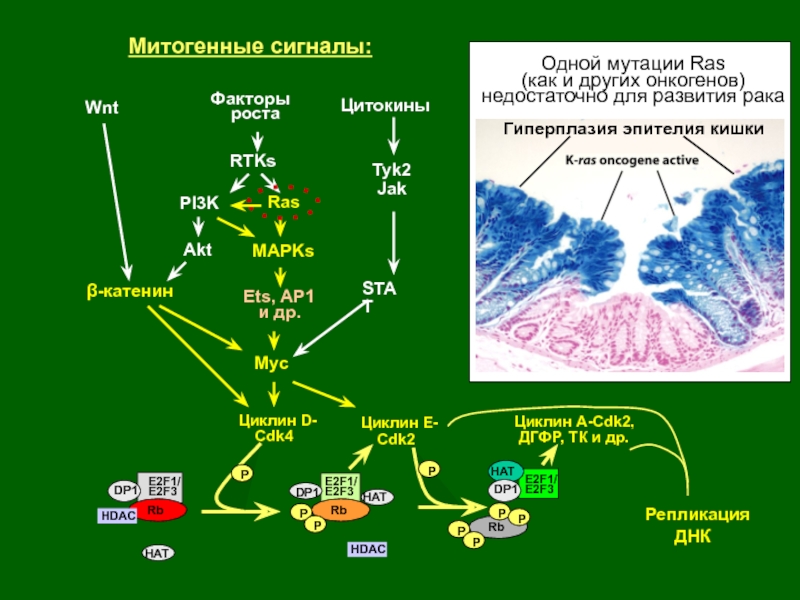
Одной мутации Ras
(как и других онкогенов)
недостаточно для развития рака
Гиперплазия эпителия кишки
Слайд 30Репликация
ДНК
Rb
P
HDAC
E2F1/
E2F3
Rb
HDAC
Rb
P
P
Циклин A-Cdk2,
ДГФР, ТК и
др.
P
P
Циклин E-
Cdk2
Циклин D-
Cdk4E2F1/
E2F3
E2F1/
E2F3
HAT
HAT
DP1
DP1
DP1
HAT
P
P
P
Факторы
роста
Цитокины
Wnt
МАРKs
STAT
β-катенин
Myc
Митогенные сигналы:
Ets, AP1
и др.
Ras
Tyk2
Jak
PI3K
Akt
RTKs
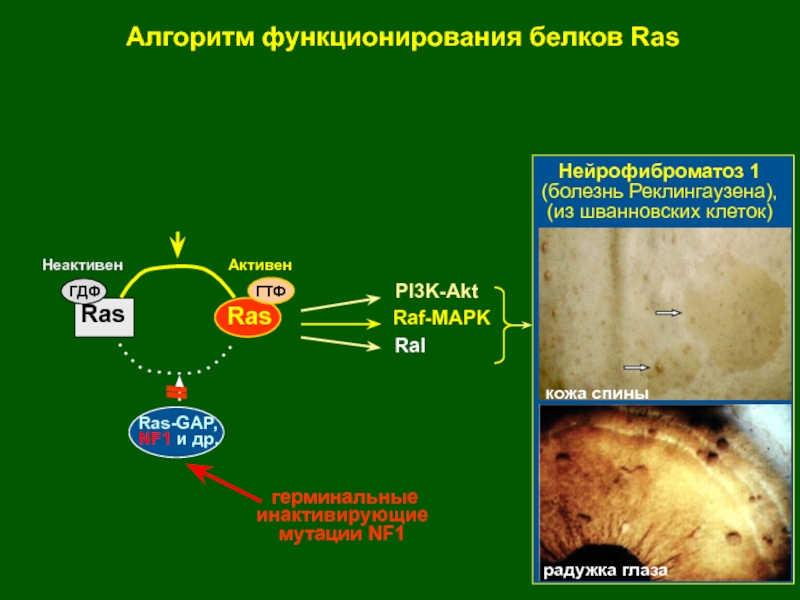
Слайд 33Raf-MAPK
PI3K-Akt
Ral
Нейрофиброматоз 1
(болезнь Реклингаузена),
(из шванновских клеток)
Алгоритм функционирования белков Ras
Ras-GAP,
NF1 и др.
герминальные
инактивирующие
мутации NF1
кожа спины
радужка глаза
Ras
Ras
ГДФ
ГТФ
Неактивен
Активен
Слайд 34Репликация
ДНК
Rb
P
HDAC
E2F1/
E2F3
Rb
HDAC
Rb
P
P
Циклин A-Cdk2,
ДГФР, ТК и
др.
P
P
Циклин E-
Cdk2
Циклин D-
Cdk4E2F1/
E2F3
E2F1/
E2F3
HAT
HAT
DP1
DP1
DP1
HAT
P
P
P
Факторы
роста
Цитокины
Wnt
МАРKs
STAT
β-катенин
Myc
Митогенные сигналы:
Ets, AP1
и др.
Ras
Tyk2
Jak
PI3K
Akt
RTKs
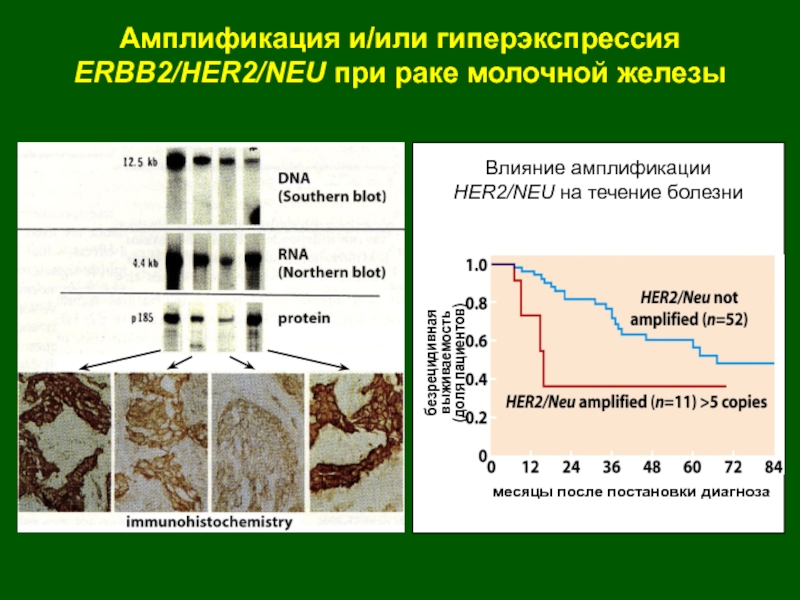
Слайд 37безрецидивная выживаемость
(доля пациентов)
месяцы после постановки диагноза
Амплификация и/или гиперэкспрессия
ERBB2/HER2/NEU при
раке молочной железы
Влияние амплификации
HER2/NEU на течение болезни
Слайд 38Для неопластических клеток характерны изменения, придающие им способность продуцировать факторы
роста, стимулирующие их собственное размножение
(аутокринная регуляция)
Примеры опухолей с аутокринной
регуляциейСлайд 39Репликация
ДНК
Rb
P
HDAC
E2F1/
E2F3
Rb
HDAC
Rb
P
P
Циклин A-Cdk2,
ДГФР, ТК и
др.
P
P
Циклин E-
Cdk2
Циклин D-
Cdk4E2F1/
E2F3
E2F1/
E2F3
HAT
HAT
DP1
DP1
DP1
HAT
P
P
P
Факторы
роста
Цитокины
Wnt
МАРKs
STAT
β-катенин
Myc
Митогенные сигналы:
Ets, AP1
и др.
Ras
Tyk2
Jak
PI3K
Akt
RTKs
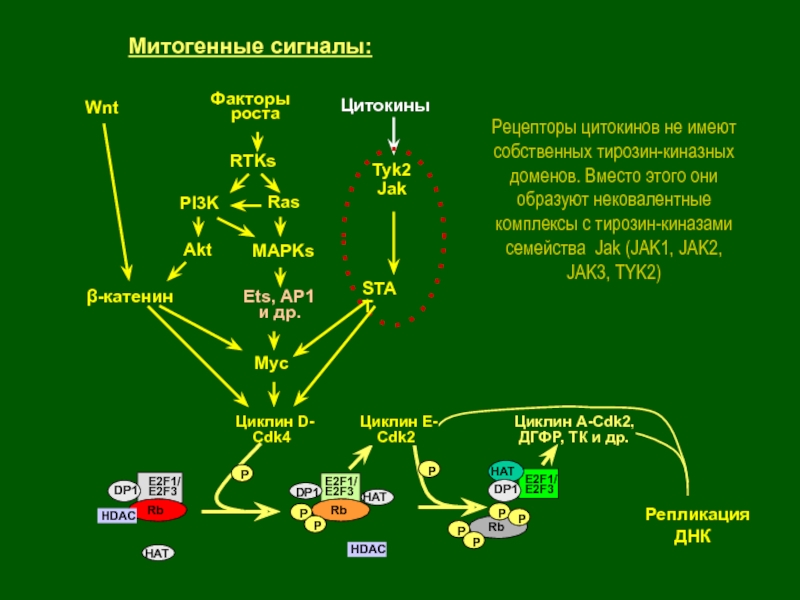
Рецепторы цитокинов не имеют собственных тирозин-киназных доменов. Вместо этого они образуют нековалентные комплексы с тирозин-киназами семейства Jak (JAK1, JAK2, JAK3, TYK2)
Слайд 41Репликация
ДНК
Rb
P
HDAC
E2F1/
E2F3
Rb
HDAC
Rb
P
P
Циклин A-Cdk2,
ДГФР, ТК и
др.
P
P
Циклин E-
Cdk2
Циклин D-
Cdk4E2F1/
E2F3
E2F1/
E2F3
HAT
HAT
DP1
DP1
DP1
HAT
P
P
P
Факторы
роста
Цитокины
Wnt
МАРKs
STAT
β-катенин
Myc
Митогенные сигналы:
Ets, AP1
и др.
Ras
Tyk2
Jak
PI3K
Akt
RTKs
Слайд 42Примеры изменений различных протоонкогенов, контролирующих вход в S-фазу, в новообразованиях
человека
Рецепторные
тирозинкиназы:
мутации, инверсии
RET
/
GDNF-R
амплификация
ERBB2/HER2
транслокации
PDGF
-
R
b
G-
белки семейства Ras:
мутации
K-RAS,
N-RAS, H-RASПодмембранные
киназы:
мутации, амплификация
PIK3CA
Компоненты
STAT-
путей:
хромосом.
транслокации
JAK2
Факторы транскрипции:
транслокации, амплификация
MYC
мутации
CTNNB1
(
β
-катенина
)
хром.
транслокации
FLI1
Циклинзависимые
киназы:
амплификация Р
RAD1/
циклин
D1
Рак щитовидной железы
Рак молочной железы
Острый и
хрон.
миелолейкозы
Многие новообразования
Рак желудка, ободочной кишки и др.
Острый
лимфолейкоз
Лимфомы, рак молочной жел. и др.
Опухоли толстого кишечника
Саркома
Юинга
Рак молочной железы, кожи,
пищевода, печени и др. опухоли
хромосом. транслокации BCR/ABL
Хронический миелоидный лейкоз
мутации
SRC
Рак ободочной кишки
мутации
GLI
Глиобластомы, рак кожи
циклина Е
Слайд 43Неограниченное деление
стволовых клеток опухолей
Стимуляция деления
Иммортализация
Отмена рост-инигибирующих
сигналов и/или
нечувствительность
к их действию
Высокая
активность теломеразы, поддержание
нормальной структуры
концов хромосом
Пониженная потребность во
внешних сигналах для инициации и поддержания пролиферации (генерирование внутренних пролиферативных стимулов)
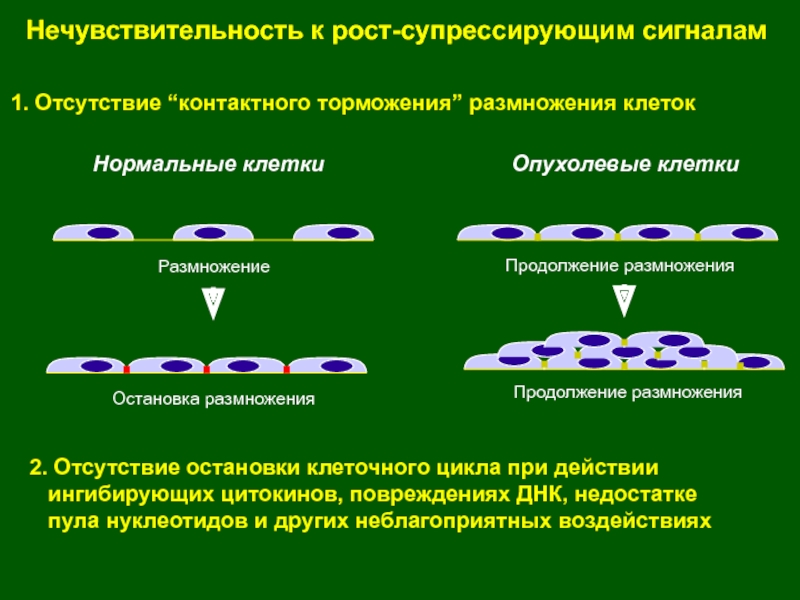
Слайд 44Нечувствительность к рост-супрессирующим сигналам
1. Отсутствие “контактного торможения” размножения клеток
2. Отсутствие
остановки клеточного цикла при действии
ингибирующих цитокинов, повреждениях
ДНК, недостатке пула нуклеотидов и других неблагоприятных воздействиях
Остановка размножения
Продолжение размножения
Нормальные клетки
Опухолевые клетки
Размножение
Продолжение размножения
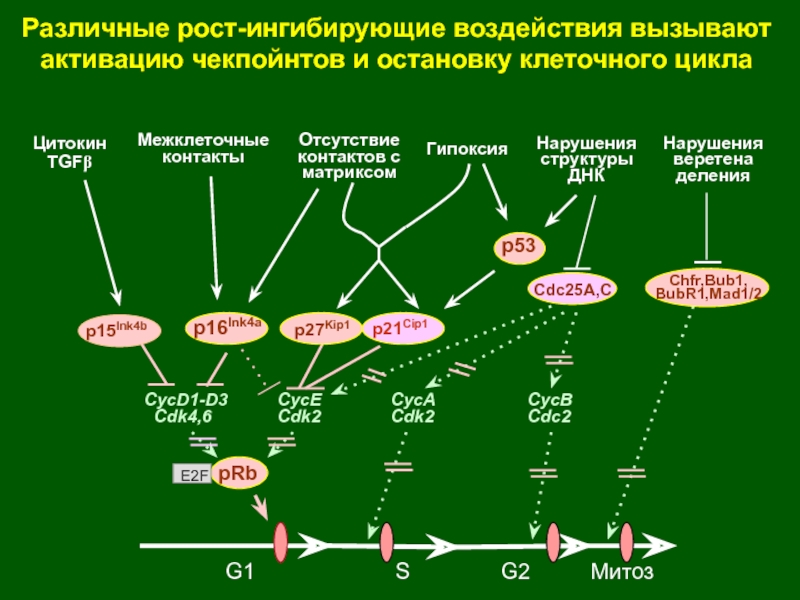
Слайд 45G1
S
G2
Митоз
Цитокин TGFb
Нарушения
структуры
ДНК
Межклеточные контакты
Отсутствие
контактов с матриксом
Гипоксия
Нарушения
веретена деления
p16Ink4a
p53
Различные рост-ингибирующие воздействия вызывают активацию
чекпойнтов и остановку клеточного цикла
p15Ink4b
p27Kip1
p21Cip1
CycD1-D3
Cdk4,6
CycE
Cdk2
CycA
Cdk2
CycB
Cdc2
pRb
E2F
Chfr,Bub1,
BubR1,Mad1/2
Cdc25A,C
Слайд 46G1
S
G2
Митоз
Цитокин TGFb
Нарушения
структуры
ДНК
Межклеточные контакты
Отсутствие
контактов с матриксом
Гипоксия
Нарушения
веретена деления
p16Ink4a
p53
p27Kip1
p21Cip1
CycD1-D3
Cdk4,6
CycE
Cdk2
CycA
Cdk2
CycB
Cdc2
pRb
E2F
Компоненты трансдукции рост-ингибирующих сигналов
являются опухолевыми супрессорами
Cdc25A,C
Chfr,Bub1,
BubR1,Mad1/2
p15Ink4b
Мишени E2F: циклины А и E, Cdc2, Cdc25C
(дефосфори-лирование Cdc2/Cdk1), p21 - т.е. блокируются все фазы клеточного цикла после ранней G1
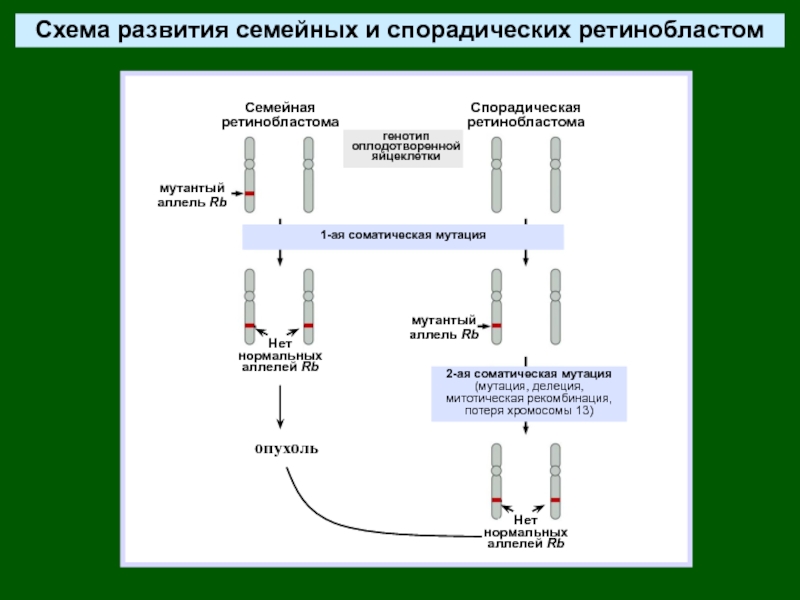
Слайд 47Adapted from A.Knudson, Proc.Natl.Acad.Sci. USA, 1971, 68:820-823; and R.Weinberg, The
Biology of Cancer (© Garland Science 2007)
Ретинобластома – опухоль из
предшественников клеток сетчатки - имеет две формы: спорадическую (односторонняя) и семейную (часто двусторонняя)Прорастание
опухоли, сужение
оптического нерва
Ретинобластома
Дисплазия ретины
Семья с наследственной ретинобластомой
Слайд 49Последствия мутаций генов Rb
Человек
Герминальные мутации
Соматические мутации, метилирование (оба
аллеля)
RB +/- Ретинобластома, остеосаркома
Различные новообразованияНокаут у мышей
RB +/- Аденома гипофиза
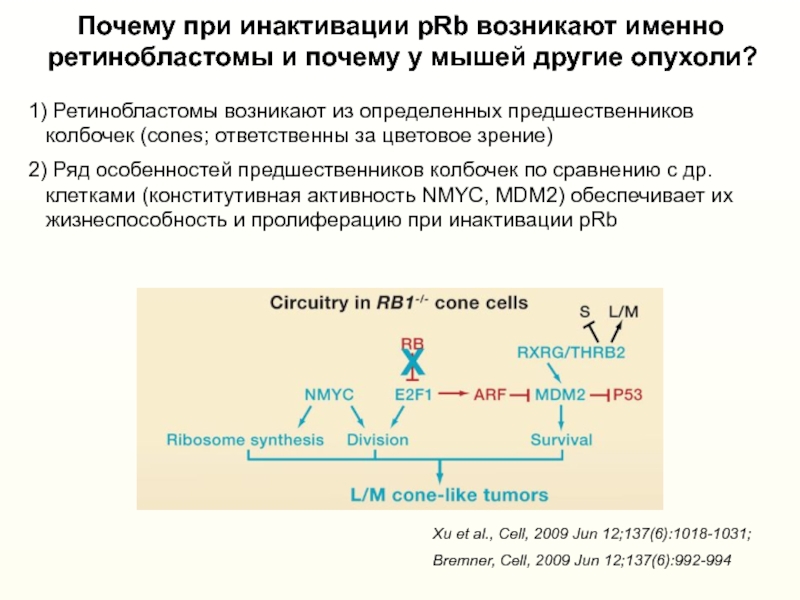
Слайд 50 Почему при инактивации pRb возникают именно
ретинобластомы и
почему у мышей другие опухоли?
1) Ретинобластомы возникают из определенных предшественников
колбочек (cones; ответственны за цветовое зрение)2) Ряд особенностей предшественников колбочек по сравнению с др.
клетками (конститутивная активность NMYC, MDM2) обеспечивает их
жизнеспособность и пролиферацию при инактивации pRb
Xu et al., Cell, 2009 Jun 12;137(6):1018-1031;
Bremner, Cell, 2009 Jun 12;137(6):992-994
Слайд 51Компоненты трансдукции рост-ингибирующих сигналов являются опухолевыми супрессорами
G1
S
G2
Митоз
Цитокин TGFb
Нарушения
структуры
ДНК
Межклеточные контакты
Отсутствие
контактов с
матриксом
Гипоксия
Нарушения
веретена деления
p16Ink4a
p53
p15Ink4b
p27Kip1
p21Cip1
CycD1-D3
Cdk4,6
CycE
Cdk2
CycA
Cdk2
CycB
Cdc2
pRb
E2F
Cdc25A,C
Chfr,Bub1,
BubR1,Mad1/2
Слайд 52Последствия мутаций генов Rb и CKIs
Человек
Герминальные мутации
Соматические мутации,
метилирование и др.
RB +/-
Ретинобластома, остеосаркомаp16INK4A +/- Меланома
p27KIP1 +/- Эндокринные опухоли (вариант синдрома MEN1)
RB Различные новообразования
Нокаут у мышей
RB +/- Аденомы гипофиза
р16INK4A Различные новообразования
р15INK4В +/- Частота опухолей не повышается
р27KIP1 Различные новообразования
р16INK4A +/- Фибросаркома, лимфомы и др.
р27KIP1 +/- Аденомы гипофиза
р21СIP1 +/- Частота опухолей не повышается
Слайд 53Подавление антипролиферативной функции p27Kip1
в новообразованиях человека
Герминальные и соматические мутации (MEN1,
редко)
Подавление транскрипции вследствие нарушений
регулирующих
ген р27 транскрипционных факторов MYC, MЕNIN, FOX-O, PML (многие раки)
Подавление трансляции вследствие гиперэкспрессии
miR 221/222 (многие раки);
Усиленная деградация вследствие амплификации или
гиперэкспрессии гена SKP2 и др. механизмов
(многие раки);
Подавление связывания с Сdk4/6 и секвестрации от Cdk2 из-за фосфорилирования онкобелками сем. Src,
Аbl (лейкозы, рак ободочной кишки и др.);
Транслокация из ядра в цитоплазму вследствие
фосфорилирования онкобелком Akt/PKB и др.,
где р27 функционирует как онкобелок, стимулируя
миграцию клеток за счет регуляции RhoA (лекция 5)
(многие раки)
Слайд 54Компоненты передачи рост-ингибирующих сигналов являются опухолевыми супрессорами
G1
S
G2
Митоз
Цитокин TGFb
Нарушения
структуры
ДНК
Межклеточные контакты
Отсутствие
контактов с
матриксом
Гипоксия
Нарушения
веретена деления
p16Ink4a
p53
p27Kip1
p21Cip1
CycD1-D3
Cdk4,6
CycE
Cdk2
CycA
Cdk2
CycB
Cdc2
pRb
E2F
Chfr,Bub1,
BubR1,Mad1/2
Cdc25A,C
p15Ink4b
Слайд 55 Инактивация опухолевого супрессора р53 (мутации и др. аномалии)
– наиболее универсальное молекулярное изменение в опухолях человека. Она характерна
для большинства новообразований 50 разных типов. Врожденные мутации р53 в половых клетках
ведут к синдрому Ли-Фраумени – наследственной
предрасположенности к развитию в молодом
возрасте сарком, рака молочной железы, опухолей
мозга, лимфолейкозов, и других новообразований.
Подробно об инактивации р53 – в лекции 8