Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Лекция 6
Содержание
- 1. Лекция 6
- 2. Люминесценция – свечение атомов, молекул, ионов и
- 3. Основное состояние электроновS1 возбужденное состояниеS2 возбужденное состояниеAbsorbance energyФлуоресцения =10-9 sПоглощение=10-15 sБезызлучательная релаксацияПоглощение света и люминесценция
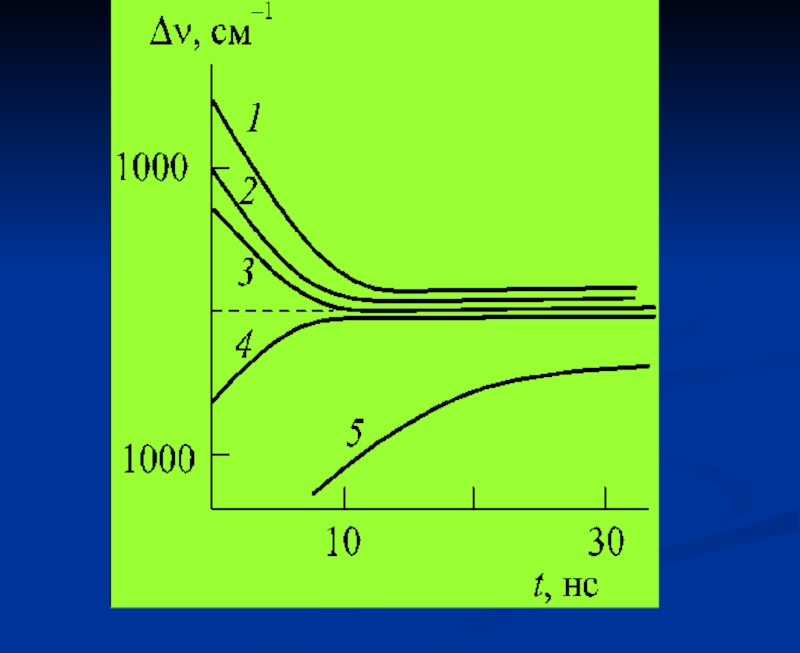
- 4. Законы затухания люминесценции
- 5. Законы затухания люминесценции
- 6. Слайд 6
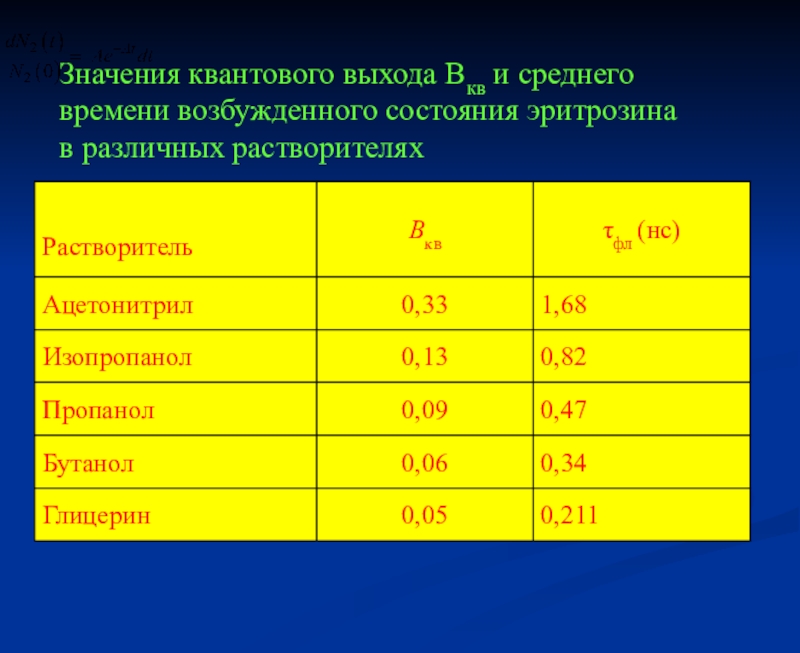
- 7. Значения квантового выхода Вкв и среднего времени возбужденного состояния эритрозина в различных растворителях
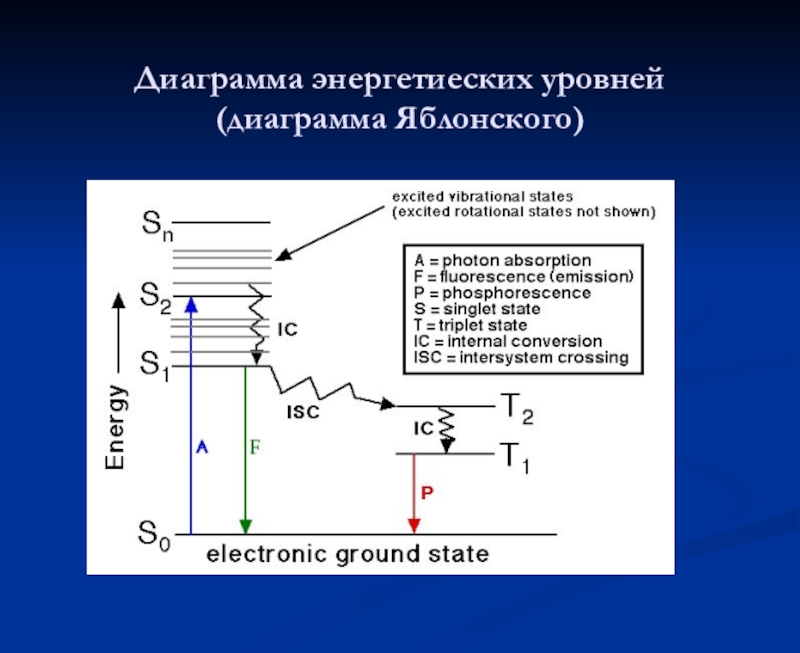
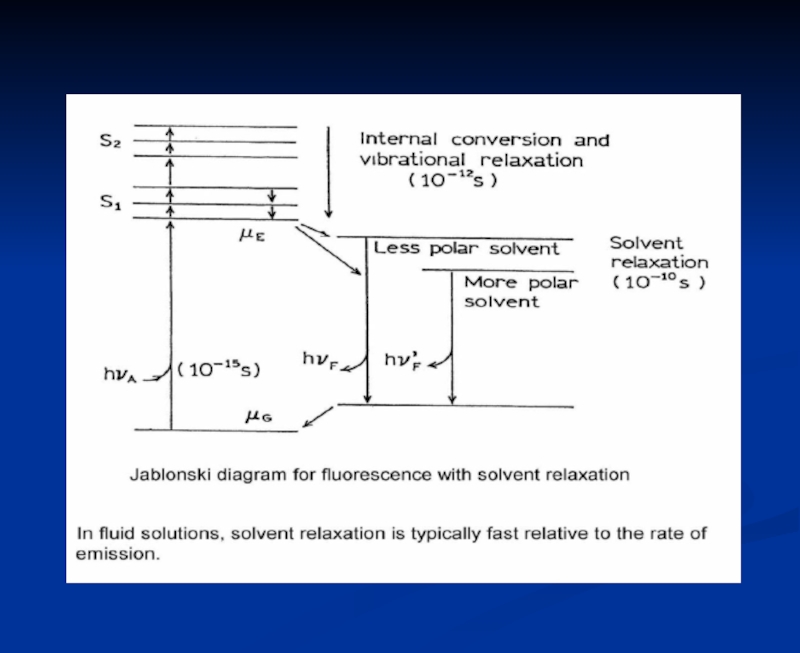
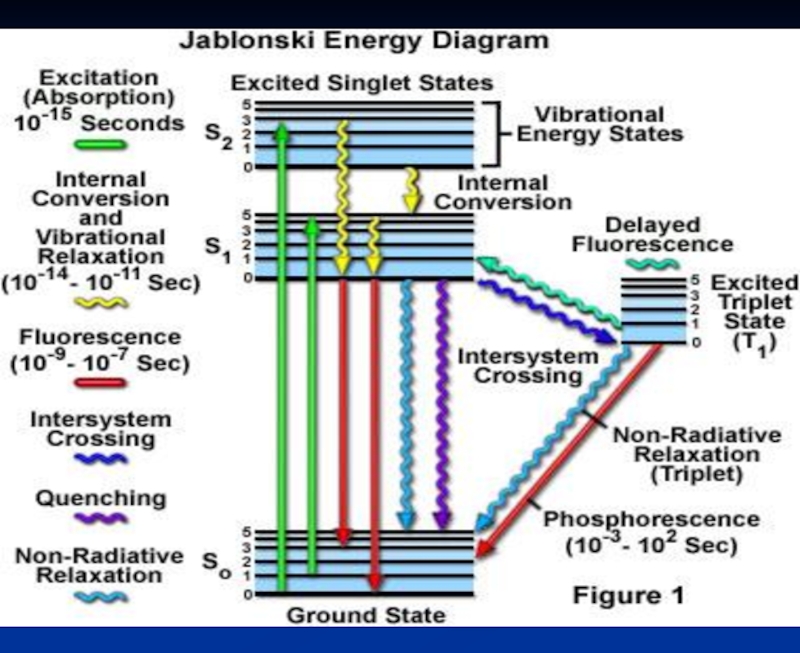
- 8. Диаграмма энергетиеских уровней (диаграмма Яблонского)
- 9. Фосфоресценция .Внутренняя и интекомбинационная конверсияДлительные процессы свечения
- 10. Фосфоресценция
- 11. Слайд 11
- 12. Слайд 12
- 13. kF = излучение(S1 S0)kic = внутренняя
- 14. a) Колебательная релаксация: столкновение растворителя - l излучения
- 15. d) Интеркомбинационные переходы: -Спин электрона «переворачивается»- Изменение
- 16. Влияние внутри и межмолекулярных взаимодействий на люминесценцию
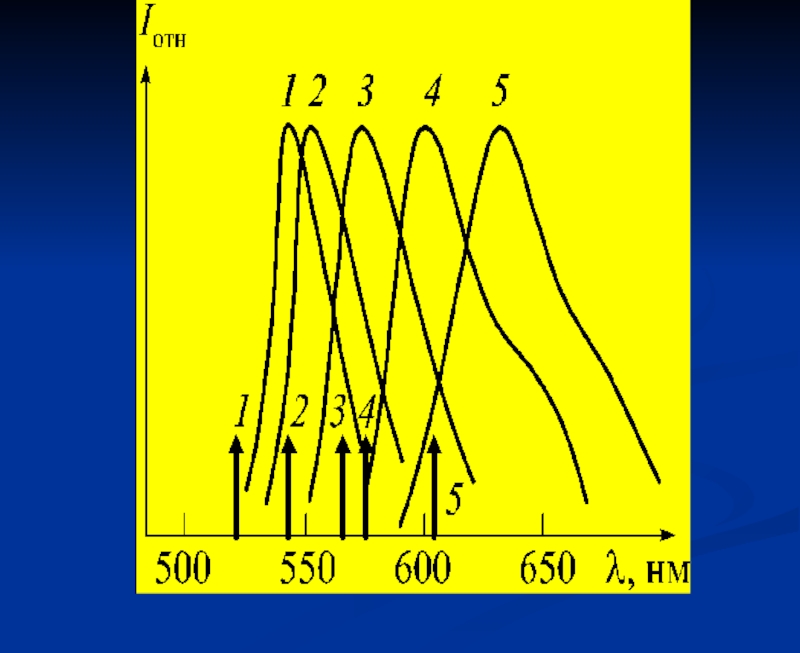
- 17. Эффекты растворителя и окружающей среды на спектры
- 18. Слайд 18
- 19. Молекулярные процессы в конденсированной фазеДиффузияРелаксацияСольватацияПеренос заряда (электрон
- 20. Слайд 20
- 21. Слайд 21
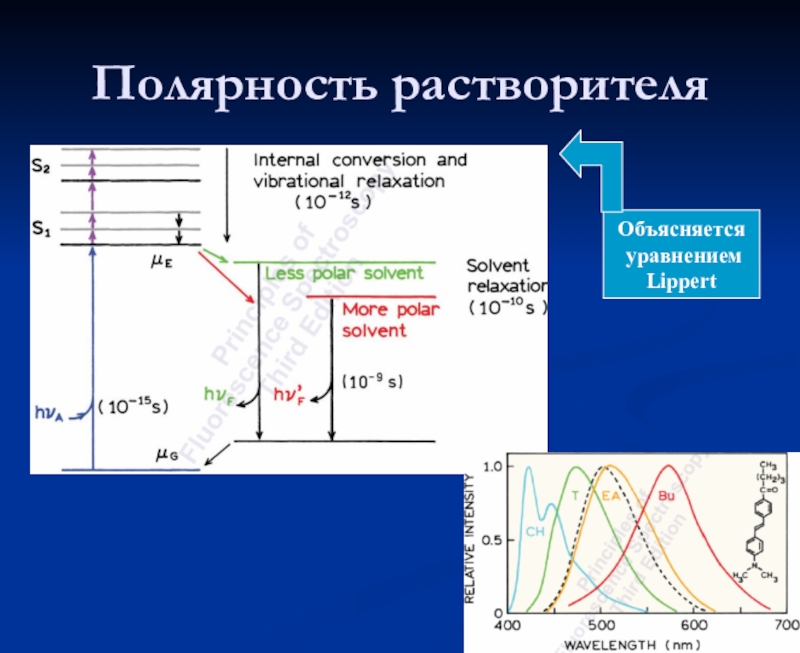
- 22. Полярность растворителя
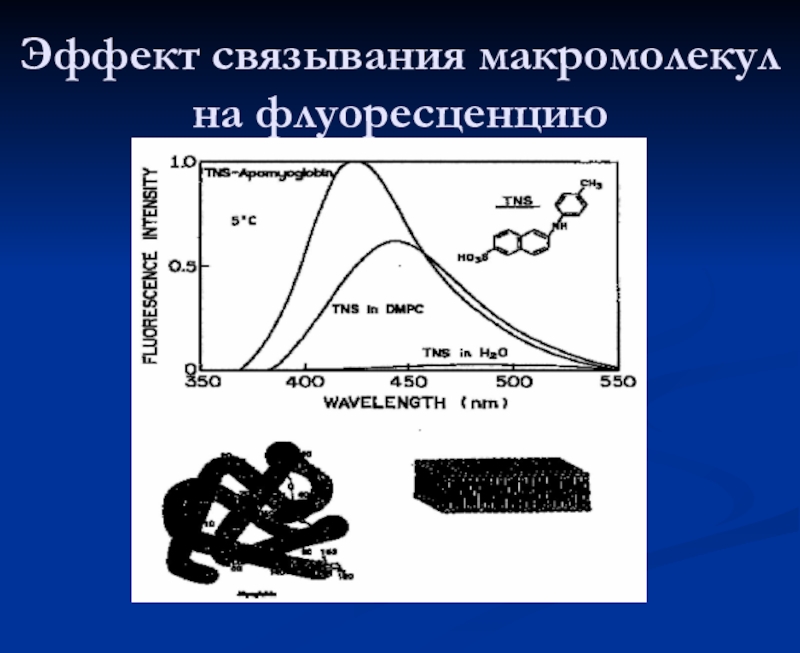
- 23. Эффект связывания макромолекул на флуоресценцию
- 24. Слайд 24
- 25. Диэлектрическая сольватацияФлуоресценция Кумарина 153 0, 0.05, 0.1,
- 26. Ориентационные ИндукционныеДисперсионные где r – расстояние между
- 27. Полярность растворителя Объясняется уравнениемLippert
- 28. Уравнение LippertaОриентационная поляризуемость Энергия диполя в электрическом полеR- электрическое поле (реактивное)индуцированное диполемf- поляризуемость растворителяa- радиус полости
- 29. Поляризуемость растворителя: подвижность электронов растворителя и дипольного
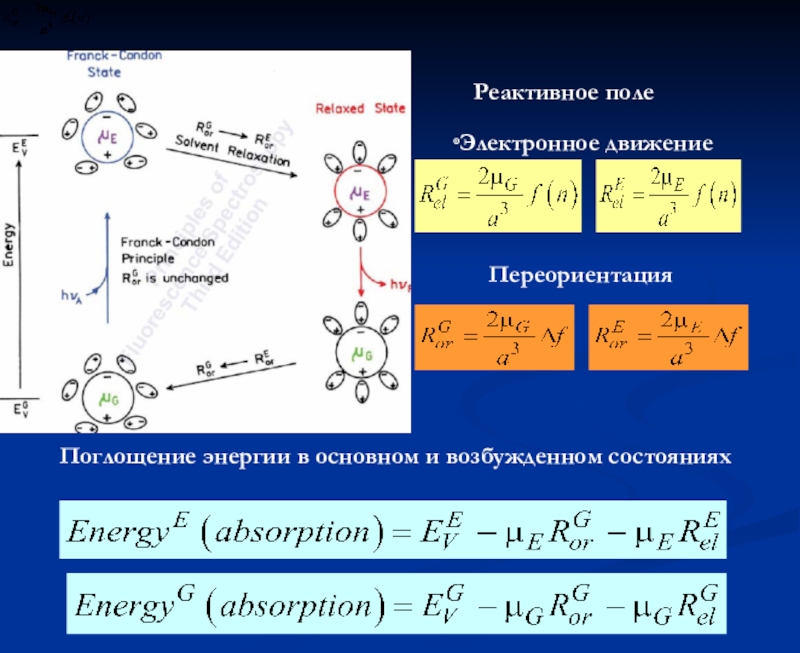
- 30. Реактивное полеЭлектронное движениеПереориентация Поглощение энергии в основном и возбужденном состояниях
- 31. Энергия поглощенияЭнергии двух уровней для излученияЭнергия излучения
- 32. Уравнение Липперта
- 33. Слайд 33
- 34. Специфические взаимодействия
- 35. Слайд 35
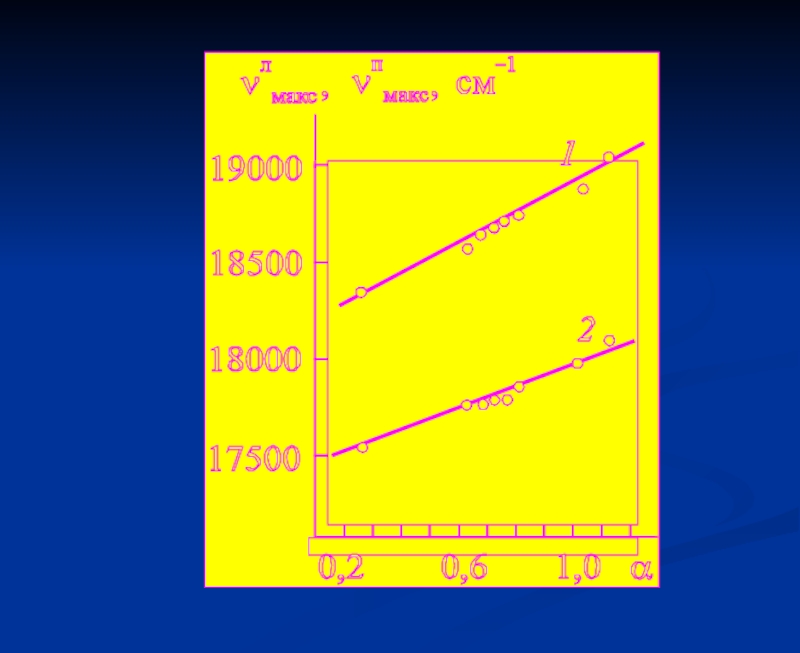
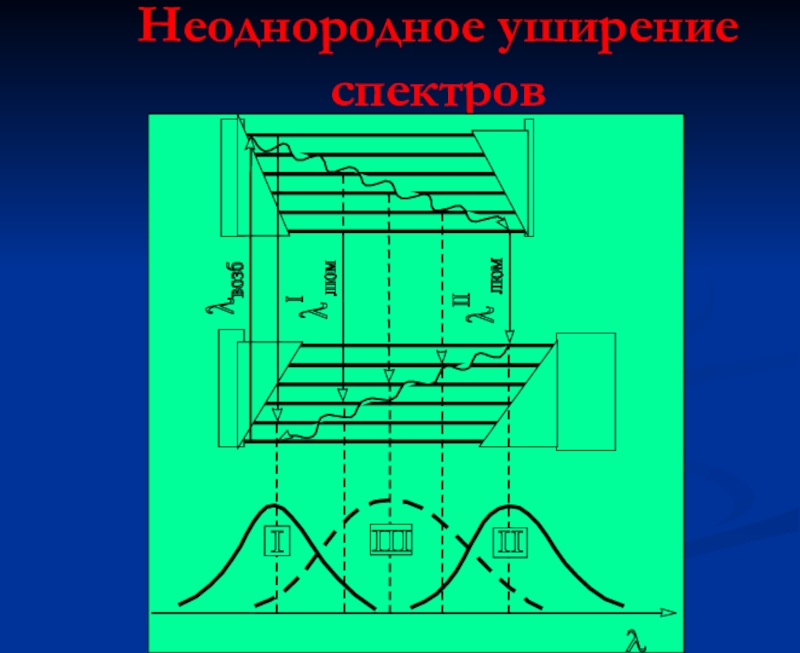
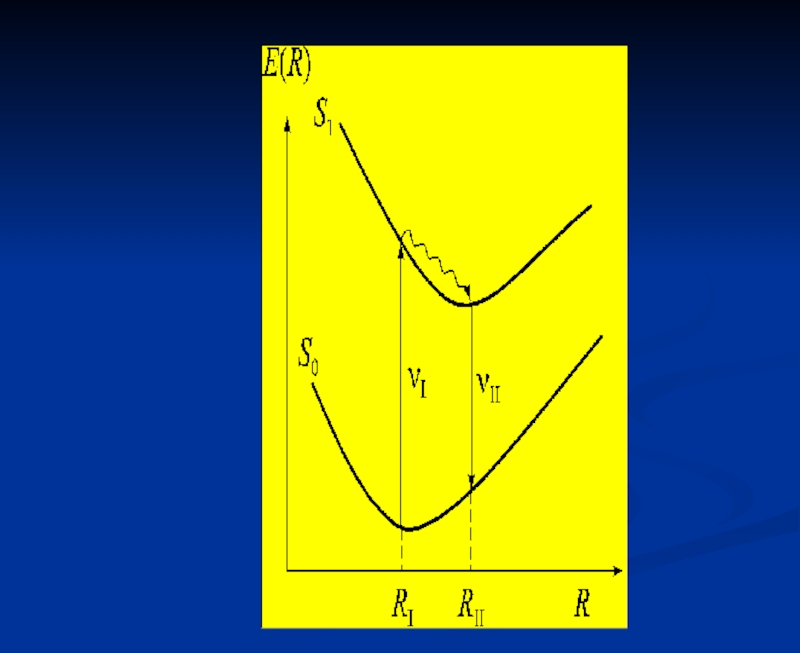
- 36. Неоднородное уширение спектров
- 37. Слайд 37
- 38. Слайд 38
- 39. Слайд 39
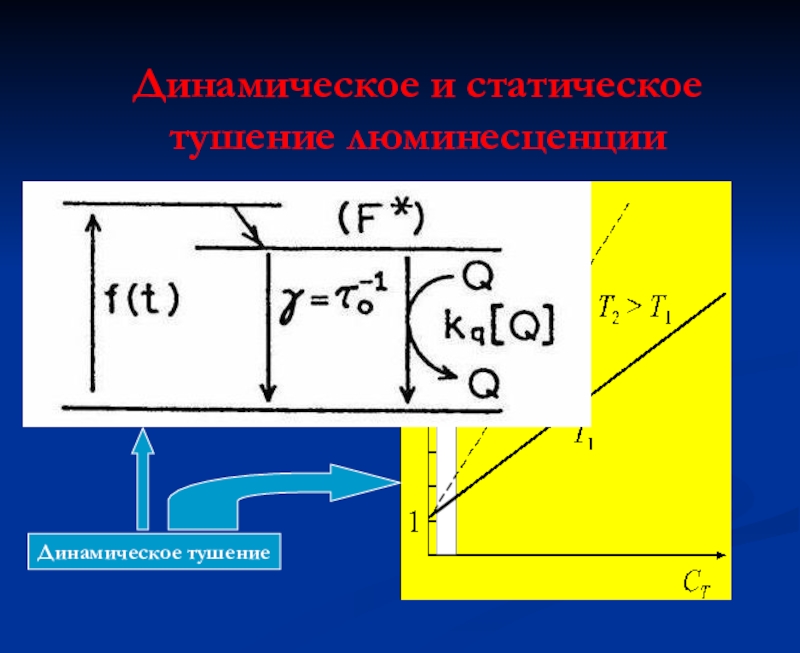
- 40. Динамическое и статическое тушение люминесценцииДинамическое тушение
- 41. Динамическое тушение
- 42. Динамическое и статическое тушение люминесценцииСтатическое тушение
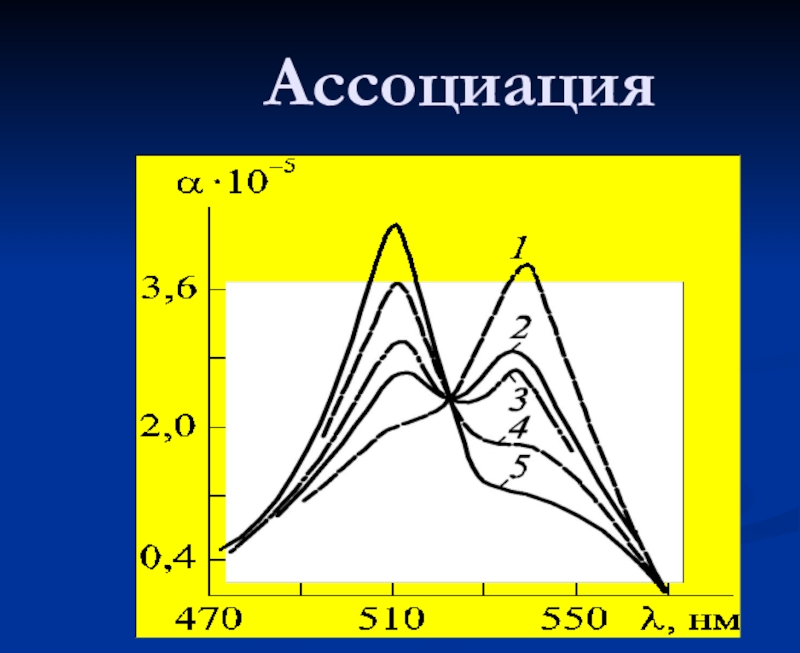
- 43. Ассоциация
- 44. Сравнение динамического и статического тушенияДля динамического и
- 45. ФлуоресценцияМолекулы могут излучать свет большей длны волны,
- 46. Квантовый выход Q Отношение числа
- 47. ПРОЦЕССЫ ПЕРЕНОСА ЭНЕРГИИ ЭЛЕКТРОННОГО ВОЗБУЖДЕНИЯ
- 48. Слайд 48
- 49. ФлуоресценцияМолекулы могут излучать свет большей длны волны,
- 50. Квантовый выход Q Отношение числа
- 51. ДонорАкцептор(ы)
- 52. ПЭЭВ
- 53. НАЗВАНИЕ?Флуоресцентный резонансный перенос энергии илиФерстеровский резонансный перенос
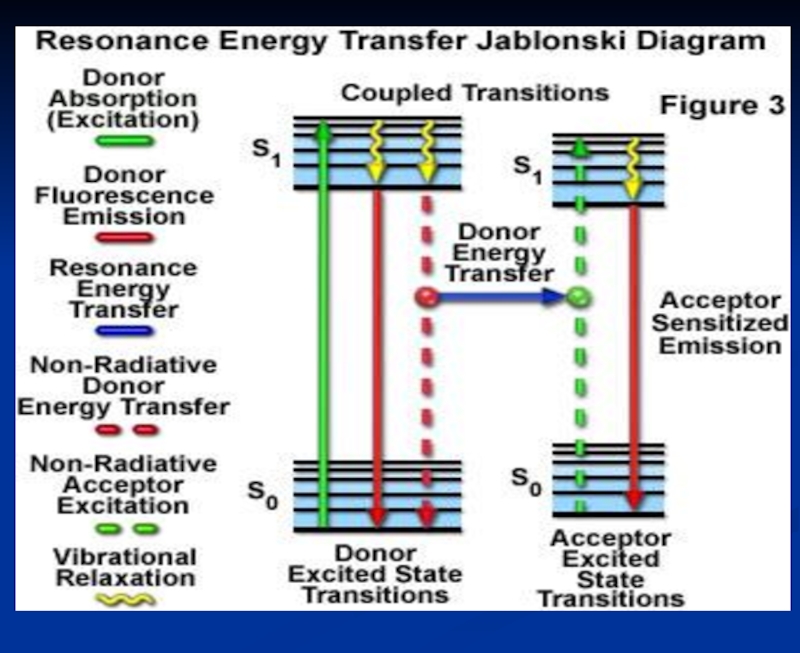
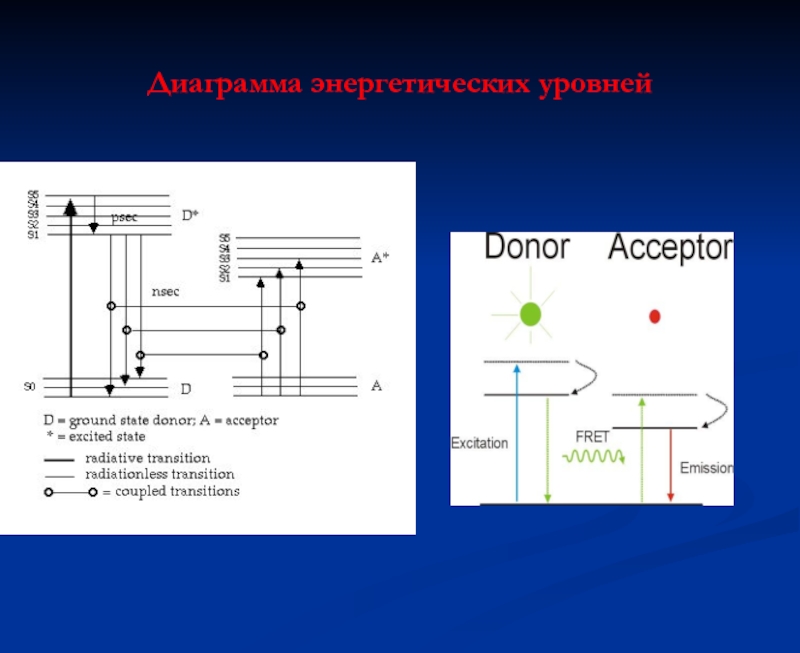
- 54. Диаграмма энергетических уровней
- 55. Реакционная схемаD- донор A- акцепторhv
- 56. Квантовый выход донора в присутствии акцептора QКвантовый
- 57. Эффективность ПЭЭВ EгдеИзмерение интенсивности флуоресценции донора с
- 58. ПЭЭВ –динамический процесс с константой скорости kT:Энергия
- 59. Fritz LondonVan der Waals interactionQuantum Theory: London, 1930; London, 19372nd order perturbation theoryFluctuating Induced-Dipole-Induced-Dipole
- 60. Радиус ФерстераСоотношение между эффективностью передачи и расстоянием между донором и акцептором (R) Ro : Радиус Ферстера
- 61. Ro может быть вычислен Qd : квантовый
- 62. Слайд 62
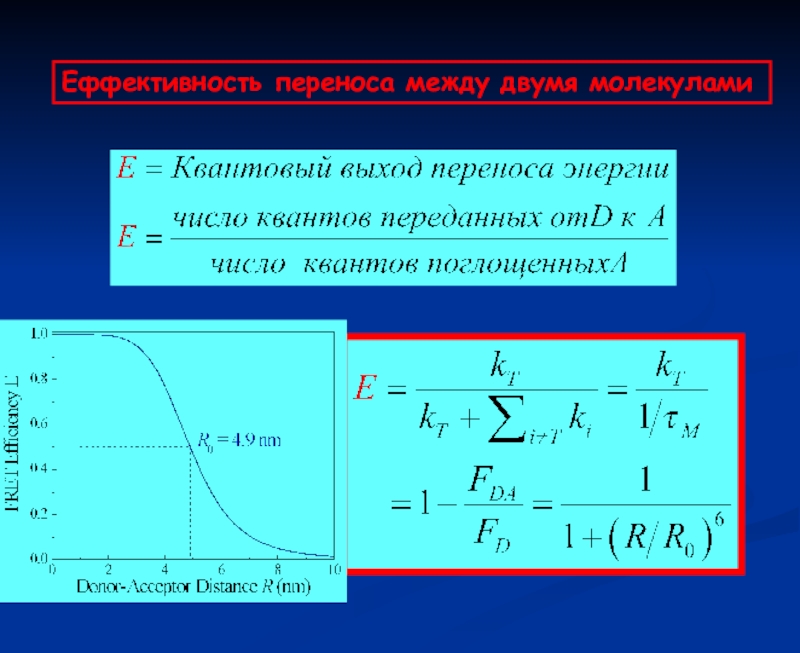
- 63. Eффективность переноса между двумя молекулами
- 64. Безызлучательный перенос имеет местоВ ближнем поле осциллятораБлижнее
- 65. • Энергия взаимодейстия,
- 66. Ориентационный фактор:
- 67. Слайд 67
- 68. Скачать презентанцию
Слайды и текст этой презентации
Слайд 3Основное
состояние
электронов
S1 возбужденное состояние
S2 возбужденное состояние
Absorbance energy
Флуоресцения =10-9 s
Поглощение=10-15
s
Безызлучательная
релаксация
Поглощение света и люминесценция
Слайд 7Значения квантового выхода Вкв и среднего
времени возбужденного состояния эритрозина
в различных растворителях
Слайд 13kF = излучение(S1 S0)
kic = внутренняя конверсия
(S1
S0)
kisc = интеркомбинационная конверсия (S1 T1)
kpd = предиссоциация
kd =
диссоциацияКвантовый выход флуоресценции
Слайд 14
a) Колебательная релаксация: столкновение растворителя
- l излучения > l возбуждения
(Стоксов сдвиг)
- колебательная релаксация эффективна и идет на нижние колебательные
уровни электронного состояния с 10-12s или меньше.- значительно короткое время жизни чем электронного возбужденного состояния
- флуоресценция происходит с низжнего колебательного уровня электронного возбужденного состояния, но может происходить на верхние колебательные уровни основного состояния.
b) Внутренняя конверсия:
- пересечение e- с нижним электронным состоянием.
- переход S1 на S0
- эффективный,поэтому многие вещества не флуоресцирует
- -особенно вероятный, если колебательные уровни двух электронных состояний пересекаются, может привести к предиссоциации или диссоциации.
диссоциация: прямое возбуждение (поглощение) колебательного состояния с достаточной энергии для разрыва связи
-предиссоциация: релаксация колебательного состояния to vibrational state of низшего электронного состояния с достаточным количеством энергии разорвать связь
Диактивациоонные процессы:
Слайд 15d) Интеркомбинационные переходы:
-Спин электрона «переворачивается»
- Изменение мультиплетности в молекуле
(синглет на триплет)
- увеличиваются, если колебательные уровни перекрываются
- вероятен, если
молекула содержит тяжелые атомы (I, Br)e) Фосфоресценция:
переход с триплетного электронного состояния в основное с излучением фотона
c)Внешняя конверсия:
Дизактивация благодаря столкновению с растворителем (столкновительное тушение)
Уменьшение столкновений увеличивается флуоресценция или фосфоресценции
Уменьшается температура и /или увеличивается вязкость
Уменьшается концентрация тушителя
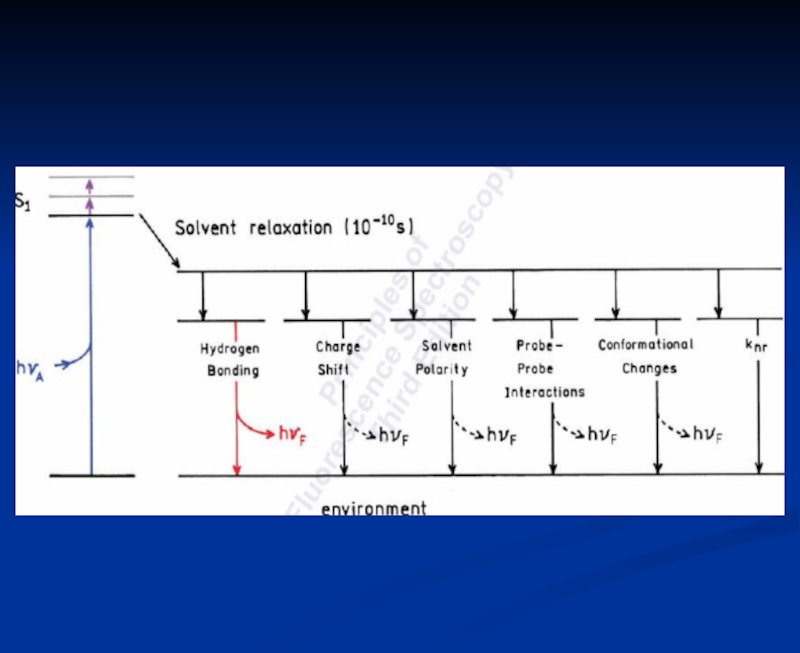
Слайд 17Эффекты растворителя и окружающей среды на спектры флуоресценции
Скорость релаксации
растворителя
Полярность и вязкость растворителя
Конформационные изменения в молекуле-активаторе
Жесткость локального окружения
Внутренний перенос
зарядаПеренос протона и реакции в возбужденном состоянии
Взаимодействие между молекулами-активатора
Изменение скоростей излучательного и
безызлучательного переходов
Слайд 19Молекулярные процессы в конденсированной фазе
Диффузия
Релаксация
Сольватация
Перенос заряда (электрон и протон)
Растворитель:
активный участник – энергия, трение, сольватация
Молекулярная временная шкала
Диффузия D~10-5cm2/s
Электронные 10-16-10-15s
Колебания
10-14sКолебательная релаксация 1-10-12s
Химические реакции xxxxxxxxx1012-10-12s
Вращения 10-12s
Время столкновения 10-12s
Слайд 25Диэлектрическая сольватация
Флуоресценция Кумарина 153 0, 0.05, 0.1, 0.2, 0.5, 1,
2, 5, and 50 ps
Сольватная энергия (по Бору)
Слайд 26
Ориентационные
Индукционные
Дисперсионные
где r – расстояние между молекулами активатора и растворителя,
a - поляризуемость молекул растворителя,
– потенциал ионизации
молекул активатора (растворителя).
Существует три вида ван-дер-ваальсовых (универсальных) взаимодействий:
Слайд 28Уравнение Lipperta
Ориентационная поляризуемость
Энергия диполя в электрическом поле
R- электрическое поле
(реактивное)
индуцированное диполем
f- поляризуемость растворителя
a- радиус полости
Слайд 29Поляризуемость растворителя:
подвижность электронов растворителя
и дипольного моменте молекул растворителя
Высокочастотная поляризуемость
-
перераспределения электронов растворителя
Низкочастотная поляризуемость
-переориентация диполей растворителя
Ориентационная поляризуемость
Слайд 30Реактивное поле
Электронное движение
Переориентация
Поглощение энергии в основном и возбужденном состояниях
Слайд 44Сравнение динамического и статического тушения
Для динамического и статического тушения флуоресценции
наблюдается одинаковая зависимость от концентрации тушителя !!!
Слайд 45Флуоресценция
Молекулы могут излучать свет большей длны волны, чем длина волны
возбуждающего света
D + hv E
D*
D + hv F
k f
k i
D
Слайд 46Квантовый выход Q
Отношение числа фотонов излучающих к
числу фотонов поглощенных
Время жизни
Среднее время между
временем возбуждения и временем возвращения в основное состояниеСлайд 49Флуоресценция
Молекулы могут излучать свет большей длны волны, чем длина волны
возбуждающего света
D + hv E
D*
D + hv F
k f
k i
D
Слайд 50Квантовый выход Q
Отношение числа фотонов излучающих к
числу фотонов поглощенных
Время жизни
Среднее время между
временем возбуждения и временем возвращения в основное состояниеСлайд 53НАЗВАНИЕ?
Флуоресцентный резонансный перенос энергии
или
Ферстеровский резонансный перенос энергии E (FRET
-ПЭЭВ)
?? is it resonance ??
Fluorescence Energy Transfer (FET)
or
Förster Energy Transfer
(FET)(D*,A)—>(D,A*)
-----------------------------------------------------------------
Слайд 55 Реакционная схема
D- донор A- акцептор
hv e,d,f – энергия
фотона для процессов
K di,ai – безызлучательные константы затухания
K d –
излучательная константа затухания для донора в отсуствии акцептораK a – излучательная константа затухания для акцептора
K t – скорость передачи энергии
Слайд 56Квантовый выход донора в присутствии акцептора Q
Квантовый выход донора Q
в присуствии (Qda) и отсутствии акцептора and (Qd)
Слайд 57Эффективность ПЭЭВ E
где
Измерение интенсивности флуоресценции донора с акцептором (Qda) и
без него (Qd).
Используя время жизни донора в присутствии акцептора
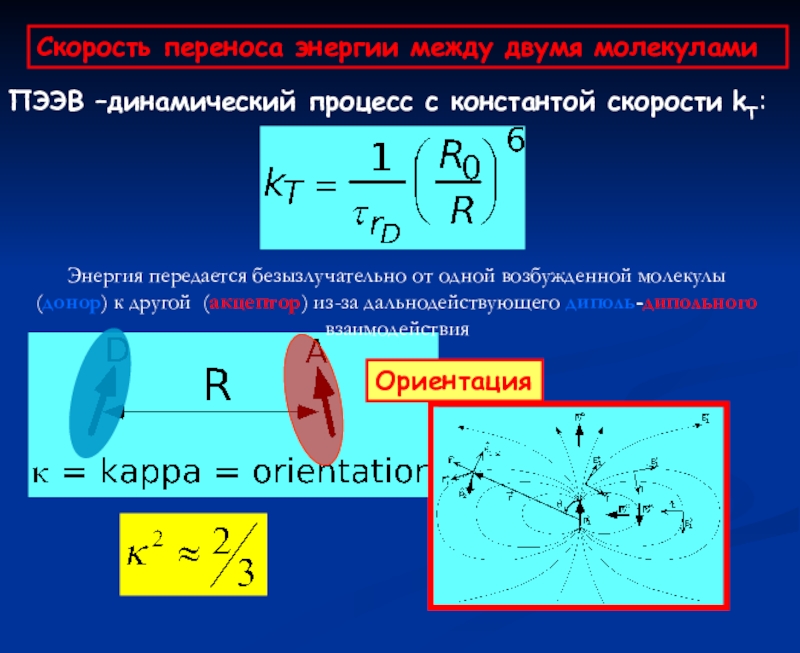
(Tda) и отсуствии акцептора (Td) Слайд 58ПЭЭВ –динамический процесс с константой скорости kT:
Энергия передается безызлучательно от
одной возбужденной молекулы (донор) к другой (акцептор) из-за дальнодействующего диполь-дипольного
взаимодействияOриентация
Скорость переноса энергии между двумя молекулами
Слайд 59Fritz London
Van der Waals interaction
Quantum Theory: London, 1930; London, 1937
2nd
order perturbation theory
Fluctuating Induced-Dipole-Induced-Dipole
Слайд 60Радиус Ферстера
Соотношение между эффективностью передачи и расстоянием между донором и
акцептором (R)
Ro : Радиус Ферстера
Слайд 61Ro может быть вычислен
Qd : квантовый выход донора,
n :
коэффициент преломления среды
Nav : число Авагадро (Nav= 6.02 x 1023
per mole)Kappa2 : ориентационный фактор
J : интеграл перекрытия
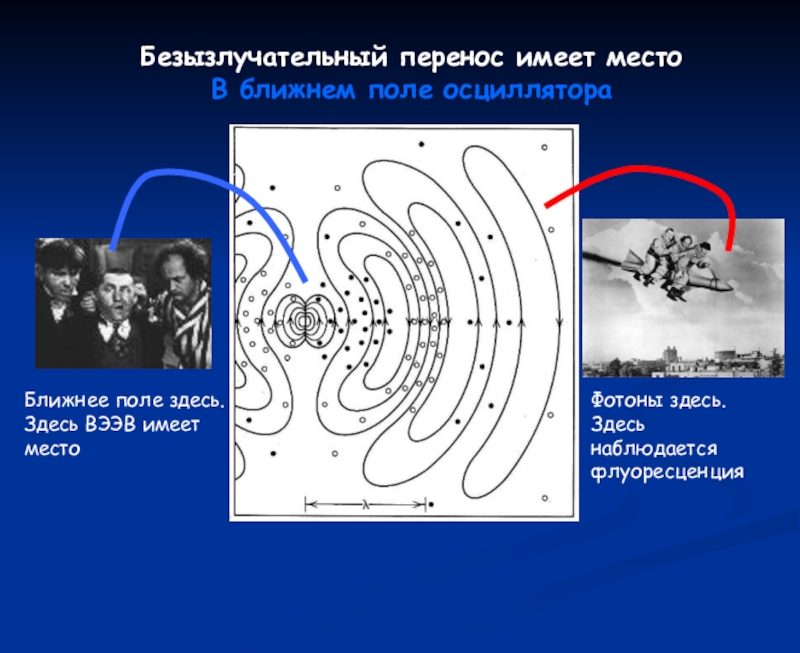
Слайд 64Безызлучательный перенос имеет место
В ближнем поле осциллятора
Ближнее поле здесь. Здесь
ВЭЭВ имеет место
Фотоны здесь. Здесь наблюдается флуоресценция
Слайд 65• Энергия взаимодейстия, , между двумя
идентичными диполями is (|ближнее поле осциллирующего диполя| = поле неподвижного
диполя):
Два
оссцилирующих
диполя
Kappa!